文档内容
微专题 11 钠盐的图象及相关计算
碳酸钠、碳酸氢钠与酸反应的定量关系及反应历程是近年高考的重点,通过滴加顺序不
同,反应现象不同,结合图象进行问题分析,考查了学生对知识的灵活运用及归纳、分
析、推理能力,进而考查了学生的思维品质和学科素养。
一、反应原理
1、碳酸钠与盐酸反应
(1)把盐酸逐滴滴加到碳酸钠溶液中
(2)化学反应方程式
NaCO+HCl=NaHCO +NaCl‥‥‥①,NaHCO +HCl=NaCl+H O+CO↑ ‥‥‥②
2 3 3 3 2 2
第一阶段反应①:NaCO 与盐酸反应刚好完全转化为NaHCO 所消耗的盐酸的体积为
2 3 3
V,
1
第二阶段反应②:NaHCO 与盐酸刚好完全反应生成氯化钠、水和CO 所消耗的盐酸的体
3 2
积为V,则V=V,二者消耗的盐酸的体积相等;
2 1 2
(3)试验现象:开始没有气泡出现,随着盐酸的滴加,溶液中开始有气体放出,随着盐
酸的滴加,气体越来越多,直至完全反应,没有气体放出为止。
(4)解释:碳酸钠先和盐酸反映生成氯化钠和碳酸氢钠,等全部转化为碳酸氢钠后,生
成的碳酸氢钠又和多的盐酸反应,生成氯化钠和水和二氧化碳。 加热会加快气体的放
出。
(5)把碳酸钠溶液逐滴滴加到盐酸中,马上就有气体放出,直至完全反应为止。
(6)反应方程式
NaCO+2HCl=2NaCl+H O+CO↑
2 3 2 2
规律总结:通过滴加顺序不同,反应现象不同,可以来鉴别碳酸钠溶液和盐酸。
2.碳酸氢钠与盐酸反应
(1)化学反应方程式
NaHCO +HCl=NaCl+H O+CO↑
3 2 2
(2)试验现象:NaHCO 与稀盐酸的反应要比NaCO 与稀盐酸的反应剧烈的多,直接生
3 2 3
成大量气体(CO)。
2二、碳酸钠、碳酸氢钠与盐酸反应的基本图像的归纳总结:
1.向NaCO 中逐滴加入盐酸,消耗HCl的体积与产生CO 的体积的关系如图1所示;
2 3 2
反应在a点所消耗的盐酸的体积V,从a点到b点所消耗的盐酸的体积V,则V=V,二
1 2 1 2
者消耗的盐酸的体积相等;
2.向NaHCO 中逐滴加入盐酸,消耗HCl的体积与产生CO 的体积的关系如图2所示;
3 2
3.当NaCO 溶液中含有NaOH时,向溶液中滴加盐酸时,盐酸先与NaOH溶液反应生
2 3
成氯化钠和水,氢氧根离子反应完全后,盐酸再与碳酸钠反应;所以在第一阶段a点所消
耗的盐酸的体积V(包含与NaOH反应所消耗盐酸的体积),大于第二阶段a点到b点所
1
消耗盐酸的体积V,即V>V;
2 1 2
向NaOH、NaCO 的混合物中逐滴加入盐酸,消耗HCl的体积与产生CO 的体积的关系
2 3 2
如图3所示(设NaOH、NaCO 的物质的量之比x∶y=1∶1,则V=2V,其他比例时的
2 3 1 2
图像略);
4.当NaCO 中含有NaHCO 时,向NaCO、NaHCO 的混合物中逐滴加入盐酸,第一阶
2 3 3 2 3 3
段是NaCO 与盐酸反应生成NaHCO ,即到a点所消耗的盐酸的体积为V,第二阶段是
2 3 3 1
NaHCO (包含原来的NaHCO )与盐酸反应生成氯化钠、水和CO,即a点到b点所消
3 3 2
耗HCl的体积为V,则VV(ab)(即0a段消耗盐酸的体积大于ab段消耗盐酸的体积),溶液中的溶质为
NaCO 和NaOH;
2 3
4.若V(0a)AB,则下
列分析与判断一定正确的是(不计CO 的溶解)
2
A.(1)图显示M中只有一种溶质且为NaCO
2 3
B.(3)图显示M中有两种溶质且为NaCO、NaOH
2 3
C.(2)图显示M中有两种溶质且为NaCO、NaHCO
2 3 3
D.(4)图显示M中c(NaCO)=c(NaHCO )
2 3 3
【答案】C
【解析】
A.(1)图显示加入盐酸之后,开始就有气体放出,其成分为NaHCO ,A错误;
3
B.(3)图显示两段消耗盐酸的量相等,其成分为NaCO,B错误;
2 3C.(2)图显示第一段消耗盐酸的体积小于第二段消耗盐酸的体积,其成分应为
NaCO、NaHCO ,C正确;
2 3 3
D.(4)图显示第一段消耗盐酸的体积大于第二段消耗盐酸的体积,其成分应为
NaCO、NaOH,D错误;
2 3
故选C。
2.向100 mL NaOH溶液中通入一定量的CO 气体,充分反应后,再向所得溶液中逐滴加
2
入2.0 mol/L的盐酸,产生CO 的体积与所加盐酸体积之间关系如图所示。回答下列问题:
2
(1)图1中通入CO 后所得溶液的溶质成分为___________;
2
(2)图3中通入CO 后所得溶液的溶质成分为___________。
2
【答案】NaCO NaOH、NaCO
2 3 2 3
【分析】
向NaOH溶液中通入一定量的CO,可能发生的反应有:2NaOH+CO ═Na CO+H O或
2 2 2 3 2
NaOH+CO ═NaHCO ,假设反应后溶液中溶质只有NaCO,再向溶液中滴加盐酸,先发
2 3 2 3
生反应:NaCO+HCl=NaHCO +NaCl,没有气体产生,后发生反应:
2 3 3
NaHCO +HCl=NaCl+CO ↑+H O,产生气体,前后2个阶段消耗盐酸的体积相等。假设反
3 2 2
应后溶液中溶质只有NaHCO ,再向溶液中滴加盐酸,立即发生反应:
3
NaHCO +HCl=NaCl+CO ↑+H O,产生气体。
3 2 2
【解析】
(1)图1中加入盐酸,开始没有气体生成,加入一定条件的盐酸后生成气体,且前后2阶
段消耗盐酸体积相等,故通入CO 后所得溶液的溶质成分为:NaCO,故答案为:
2 2 3
NaCO;
2 3
(2)图3中加入盐酸,开始没有气体生成,加入一定条件的盐酸后生成气体,且前后2阶
段消耗盐酸体积之比为2:1,故通入CO 后所得溶液的溶质成分为:NaOH、NaCO,故
2 2 3答案为:NaOH、NaCO。
2 3
五、专题训练
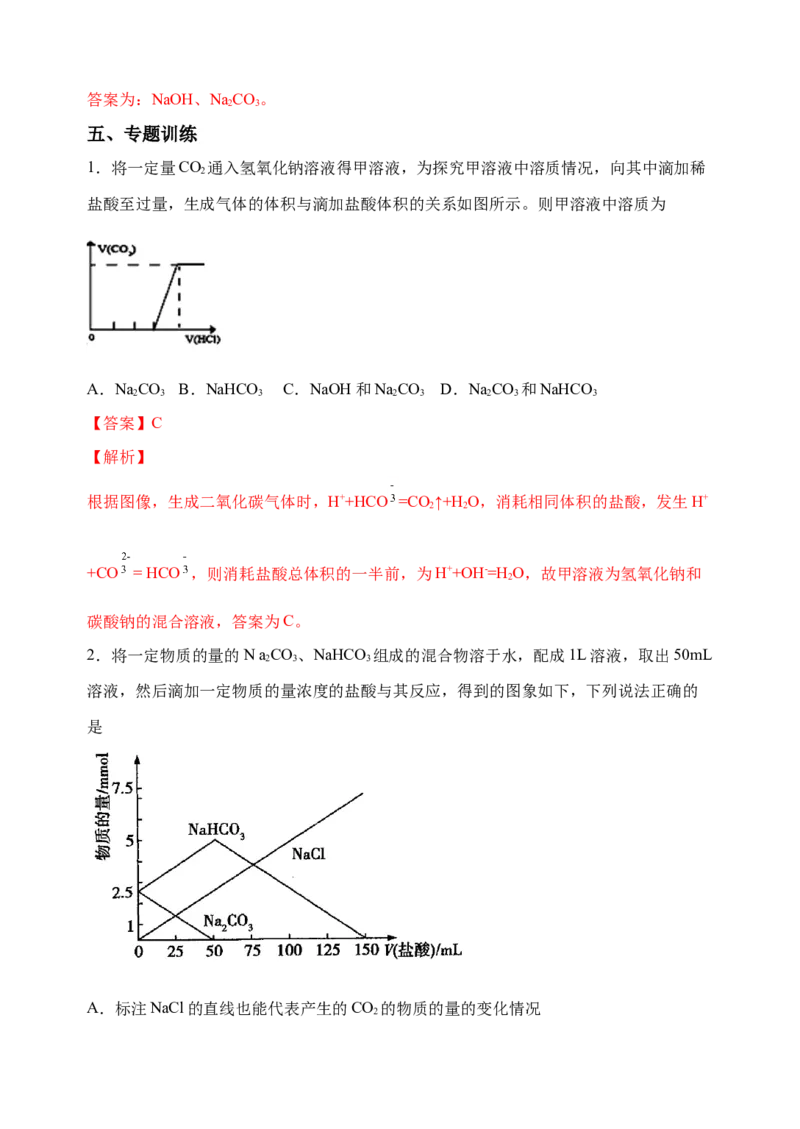
1.将一定量CO 通入氢氧化钠溶液得甲溶液,为探究甲溶液中溶质情况,向其中滴加稀
2
盐酸至过量,生成气体的体积与滴加盐酸体积的关系如图所示。则甲溶液中溶质为
A.NaCO B.NaHCO C.NaOH和NaCO D.NaCO 和NaHCO
2 3 3 2 3 2 3 3
【答案】C
【解析】
根据图像,生成二氧化碳气体时,H++HCO =CO ↑+H O,消耗相同体积的盐酸,发生H+
2 2
+CO = HCO ,则消耗盐酸总体积的一半前,为H++OH-=H O,故甲溶液为氢氧化钠和
2
碳酸钠的混合溶液,答案为C。
2.将一定物质的量的N aCO、NaHCO 组成的混合物溶于水,配成1L溶液,取出50mL
2 3 3
溶液,然后滴加一定物质的量浓度的盐酸与其反应,得到的图象如下,下列说法正确的
是
A.标注NaCl的直线也能代表产生的CO 的物质的量的变化情况
2B.原混合物中NaCO 与NaHCO 的物质的量之比为2:1
2 3 3
C.盐酸的浓度是
D.加入的盐酸为150mL时,放出CO 气体 (标准状况下)
2
【答案】C
【分析】
由图可知,0mL~50mL,发生反应为:NaCO+HCl=NaCl+NaHCO ,50mL~150mL,发
2 3 3
生反应为:NaHCO +HCl=NaCl+H O+CO↑,以此解答。
3 2 2
【解析】
A.由图0mL~50mL,发生反应为:NaCO+HCl=NaCl+NaHCO ,没有CO 产生,故A
2 3 3 2
错误;
B.从图(0,2.5)看出,原混合物中NaCO 与NaHCO 的物质的量之比为1:1,故B错误;
2 3 3
C.由图可知,50mL溶液中碳酸钠完全转化成碳酸氢钠和氯化钠时,消耗的盐酸的体积
为50mL,由NaCO+HCl=NaCl+NaHCO 可知,n(Na CO)= n(HCl)=0.0025mol,c(HCl)=
2 3 3 2 3
= ,故C正确;
D.由图50mL~150mL,发生反应为:NaHCO +HCl=NaCl+H O+CO↑,可知
3 2 2
n(CO)=n(HCl)=100×10-3×0.05=5×10-3mol,V(CO )=5×10-3mol×22.4mol/L=0.112L=112mL,
2 2
故D错误;
故选C。
3.向某NaOH溶液中通入CO 气体后得溶液M,因CO 通入量的不同,溶液M的组成也
2 2
不同。若向M中逐滴加入0.1mol•L-1盐酸,标准状况下,产生的气体体积V(CO )与加入
2
盐酸的体积V(HCl)的关系如图所示,下列有关说法不正确的是A.溶液M中的溶质是NaOH和NaCO
2 3
B.A点对应的盐酸的体积为0.3L
C.AB段反应的离子方程式只有H++HCO =H O+CO↑
2 2
D.原溶液中NaOH的物质的量为0.01mol
【答案】D
【解析】
A、由于消耗的盐酸的体积:OA段大于AB段,所以溶液M中的溶质是NaOH和
,A项正确;
B、由于 ,所以AB段消耗盐酸的物质的量为0.01mol,A点对应的盐
酸的体积为0.3L,故B正确;
C、OA段发生的反应为: 、 ,AB段发生的
反应为: ,故C正确;
D、当消耗0.4L盐酸时,B点溶质的成分为NaCl,据钠元素守恒,知原溶液中NaOH的
物质的量为0.04mol,D项错误;
答案选D。
4.向200mL的NaOH和NaCO 混合溶液中滴加0.1 mol/L稀盐酸,CO 的生成量与加入
2 3 2
盐酸的体积的关系如图所示。下列判断正确的是
A.0~a段只发生中和反应
B.原混合液中NaOH 的物质的量浓度为 0.1mol/LC.a=0.2
D.原混合溶液中 NaOH与 NaCO 的物质的量之比为1∶2
2 3
【答案】B
【分析】
向混合液中滴加HCl,首先发生反应:NaOH+HCl=NaCl,接着发生反应:
NaCO+HCl=NaHCO +NaCl,最后发生反应:NaHCO +HCl=NaCl+CO ↑+H O。前两步反
2 3 3 3 2 2
应没有CO 生成,对应图像横坐标0~a段;第三步反应生成CO 气体,对应图像横坐标
2 2
a~0.4段。
【解析】
A.由分析知,0~a段发生反应:NaOH+HCl=NaCl和NaCO+HCl=NaHCO +NaCl,A错
2 3 3
误;
B.当NaOH与NaCO 恰好与HCl完全反应后,溶液中溶质为NaCl,根据Na、Cl元素
2 3
守恒得:n(NaOH)+2n(Na CO)=n(NaCl)=n(HCl)=0.1 mol/L ×0.4 L=0.04 mol,由图像知,生
2 3
成CO 为0.01 mol,由C元素守恒知n(Na CO)=n(CO )=0.01 mol,故n(NaOH)=0.02 mol,
2 2 3 2
则原溶液中c(NaOH)= ,B正确;
C.由B选项知n(NaOH)=0.02 mol ,n(Na CO)=n(CO )=0.01 mol,故0~a段消耗HCl:
2 3 2
n(HCl)=n(NaOH)+ n(Na CO)=0.03 mol,故a= ,C错误;
2 3
D.由B选项知n(NaOH)=0.02 mol ,n(Na CO)=n(CO )=0.01 mol,故两者物质的量之比
2 3 2
为2:1,D错误;
故答案选B。
5.将一定物质的量的NaCO、NaHCO 的混合物溶于水,配成1L溶液,取50mL溶液,
2 3 3
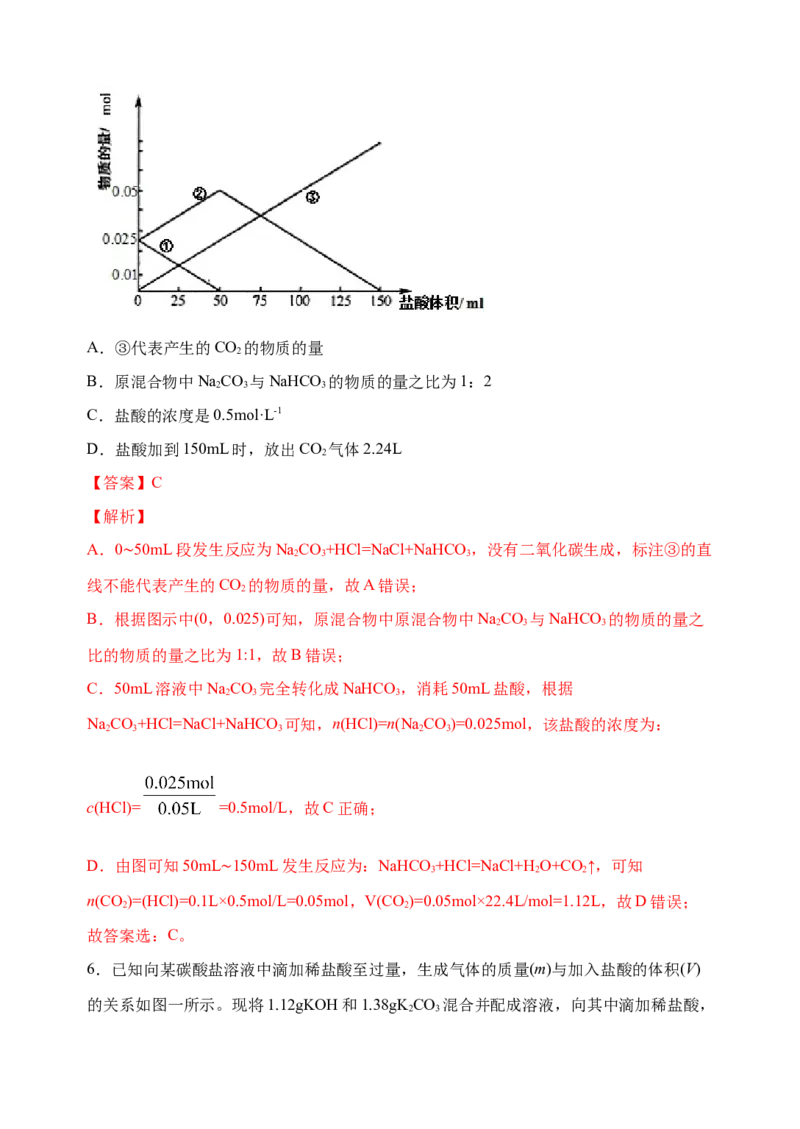
滴加一定物质的量浓度的盐酸与它反应,得到的图像如下,下列说法正确的是A.③代表产生的CO 的物质的量
2
B.原混合物中NaCO 与NaHCO 的物质的量之比为1:2
2 3 3
C.盐酸的浓度是0.5mol·L-1
D.盐酸加到150mL时,放出CO 气体2.24L
2
【答案】C
【解析】
A.0 50mL段发生反应为NaCO+HCl=NaCl+NaHCO ,没有二氧化碳生成,标注③的直
2 3 3
线不能∼代表产生的CO 的物质的量,故A错误;
2
B.根据图示中(0,0.025)可知,原混合物中原混合物中NaCO 与NaHCO 的物质的量之
2 3 3
比的物质的量之比为1:1,故B错误;
C.50mL溶液中NaCO 完全转化成NaHCO ,消耗50mL盐酸,根据
2 3 3
NaCO+HCl=NaCl+NaHCO 可知,n(HCl)=n(Na CO)=0.025mol,该盐酸的浓度为:
2 3 3 2 3
c(HCl)= =0.5mol/L,故C正确;
D.由图可知50mL 150mL发生反应为:NaHCO +HCl=NaCl+H O+CO↑,可知
3 2 2
n(CO)=(HCl)=0.1L×∼0.5mol/L=0.05mol,V(CO )=0.05mol×22.4L/mol=1.12L,故D错误;
2 2
故答案选:C。
6.已知向某碳酸盐溶液中滴加稀盐酸至过量,生成气体的质量(m)与加入盐酸的体积(V)
的关系如图一所示。现将1.12gKOH和1.38gK CO 混合并配成溶液,向其中滴加稀盐酸,
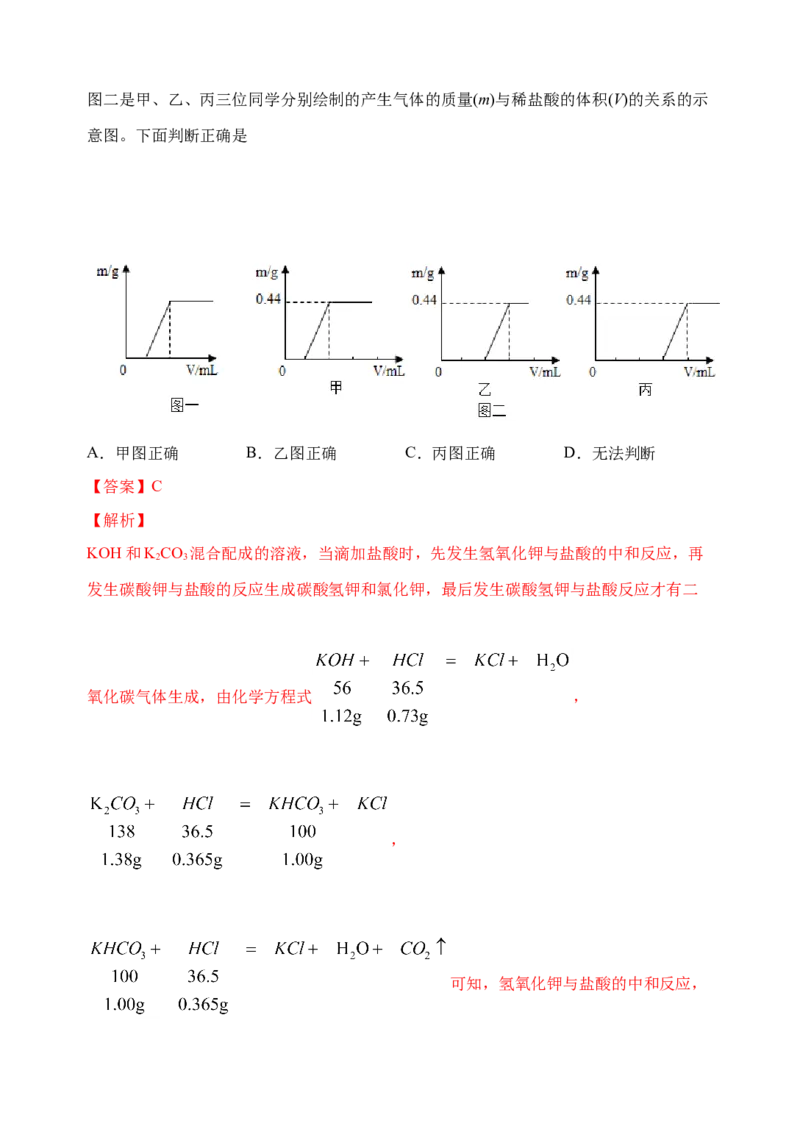
2 3图二是甲、乙、丙三位同学分别绘制的产生气体的质量(m)与稀盐酸的体积(V)的关系的示
意图。下面判断正确是
A.甲图正确 B.乙图正确 C.丙图正确 D.无法判断
【答案】C
【解析】
KOH和KCO 混合配成的溶液,当滴加盐酸时,先发生氢氧化钾与盐酸的中和反应,再
2 3
发生碳酸钾与盐酸的反应生成碳酸氢钾和氯化钾,最后发生碳酸氢钾与盐酸反应才有二
氧化碳气体生成,由化学方程式 ,
,
可知,氢氧化钾与盐酸的中和反应,碳酸钾与盐酸的反应生成碳酸氢钾,所用盐酸质量与碳酸氢钾与盐酸反应所用盐酸质量
的比为(0.73g+0.365g):0.365g=3:1.所以图象如图丙所示;C正确;答案为C。
7.向NaCO、NaHCO 混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化
2 3 3
关系如右图所示。则下列离子组在对应的溶液中一定能大量共存的是
A.a点对应的溶液中:Na+、 、 、
B.b点对应的溶液中:Ba2+、K+、 、Cl-
C.c点对应的溶液中:Na+、Ag+、Mg2+、
D.d点对应的溶液中:Cl-、 、Fe2+、Na+
【答案】B
【分析】
由图可知,a点对应的溶液含NaCO、NaHCO 和NaCl,b点溶液含NaHCO 和NaCl,c
2 3 3 3
点溶质为NaCl,显中性,而d点溶液显酸性,含NaCl和HCl,结合离子之间不能结合生
成沉淀、气体、水等,不能发生氧化还原反应、双水解反应等,则离子大量共存。
【解析】
A.a点存在HCO , 与HCO 发生反应生成氢氧化铝沉淀和 ,溶液中一定不
能大量共存,故A不符合题意;
B.b点存在HCO 、Na+和Cl-,与Ba2+、K+、 、Cl-不发生任何反应,故溶液中一定
能大量共存,故B符合题意;
C.c点正好生成NaCl溶液,Ag+与Cl-会生成氯化银沉淀,溶液中一定不能大量共存,故
C不符合题意;D.d点为NaCl与HCl的混合溶液, 、Fe2+在酸性条件下发生氧化还原反应,溶液
中不能大量共存,故D不符合题意;
答案选B。
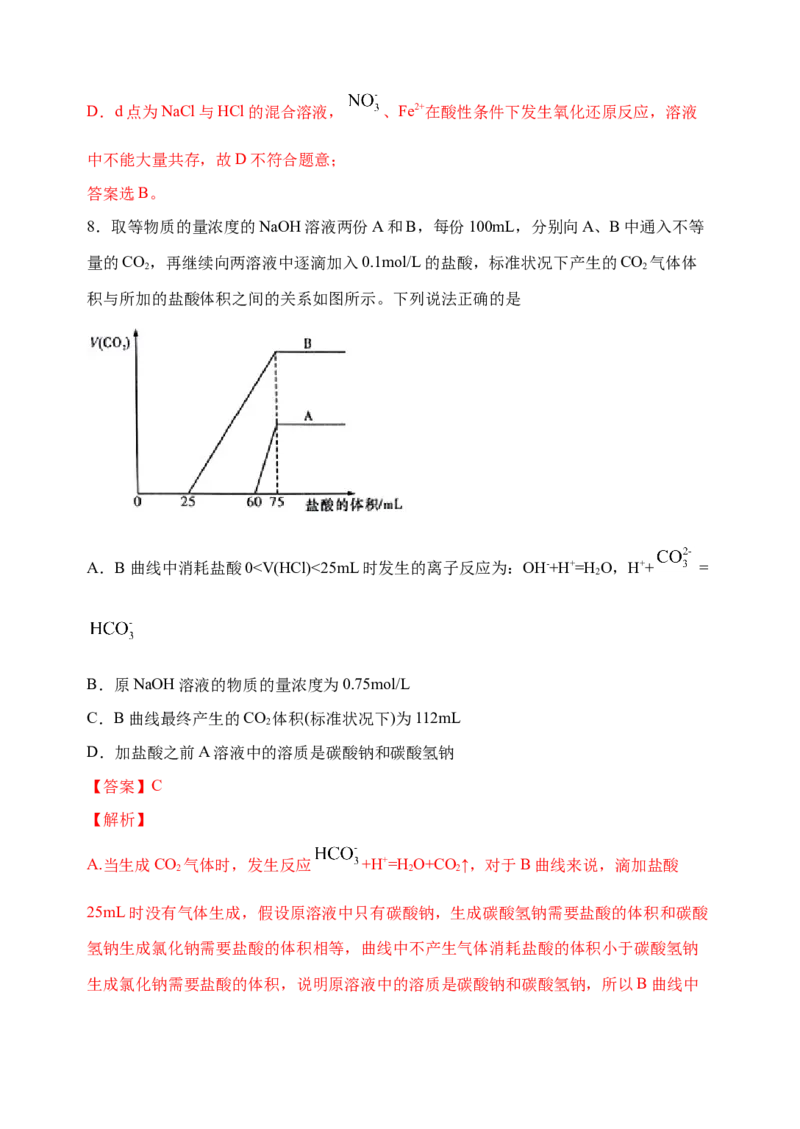
8.取等物质的量浓度的NaOH溶液两份A和B,每份100mL,分别向A、B中通入不等
量的CO,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO 气体体
2 2
积与所加的盐酸体积之间的关系如图所示。下列说法正确的是
A.B 曲线中消耗盐酸0