文档内容
微专题突破4 物质结构与性质一
一、选择题
1.(2024·南京市二模)2024年1月,我国自主研制的AG60E电动飞机成功首飞。AG60E采用了
SiC电控系统,SiC晶体属于
A.分子晶体 B.金属晶体
C.离子晶体 D.共价晶体
【答案】D
【解析】SiC中的Si和C以共价键结合形成空间网状结构,和金刚石结构相似,SiC属于共价晶体,
故选D项。
2.(2024·江苏南京市盐城市一模)下列说法正确的是
A.金刚石、石墨、C 三者互为同位素
60
B.C H 分子中存在两个π键
2 2
C.NaCO 晶体中存在离子键与非极性共价键
2 3
D.基态C原子的核外电子有6种空间运动状态
【答案】B
【解析】A项,金刚石、石墨、C 均是由碳元素形成的不同单质,三者互为同素异形体,错误;B
60
项,C H 分子中含有碳碳三键,存在两个π键,正确;C项,NaCO 晶体中存在离子键与极性共价键,
2 2 2 3
没有非极性键,错误;D项,基态C原子的核外电子排布式为1s22s22p2,占有4个轨道,有4种空间运动
状态,错误。
3.(2024·江苏省南通市三模)下列说法正确的是
A. O、 O、 O互为同素异形体
186 188 280
B.SO 的中心原子杂化轨道类型为sp3
2
C.NaO 晶体中阴阳离子数目之比为1∶2
2 2
D.1 mol SiO 晶体中含有2 mol Si-O σ键
2
【答案】C
【解析】A项, O、 O、 O三者质子数相同、而中子数不同,即互为同位素,错误;B项,SO 的
186 188 280 2
中心原子价层电子对数为3,即中心原子杂化轨道类型为sp2,错误;C项,NaO 晶体中含有钠离子Na+
2 2
和过氧根离子O2-,即阴阳离子数目之比为1∶2,正确;D项,二氧化硅晶体中1个硅原子周围结合4
2
个氧原子,即1 mol SiO 晶体中含有4 mol Si-O σ键,错误。
2
4.(2024·苏锡常镇二模)利用反应Na+KCl======K↑+NaCl可制备金属钾。下列说法正确的是
A.半径大小:r(K+)>r(Cl-) B.熔点高低:KCl>NaCl
C.电负性大小:χ(Cl)>χ(Na) D.金属性强弱:Na>K
【答案】C
【解析】A项,K+与Cl-的电子层结构相同,但K+的核电荷数比Cl+大,所以半径大小:r(K+)<
r(Cl-),错误;B项,K+的半径大于Na+,则KCl晶体中离子键键长大于NaCl晶体,键能较小,熔点
NaCl>KCl,错误;C项,在同一周期中,从左到右,元素的电负性是递增的,可知电负性χ(Na)<
χ(Cl),正确;D项,同一主族元素从上到下,原子半径增加,有效核电荷增加不多,则原子半径增大的
影响起主要作用,第一电离能由大变小,元素的金属性逐渐增强,金属性:Na<K,错误。
5.(2024·苏锡常镇一模)一种超导材料中含Cu、P、O、S等元素。下列说法正确的是
A.原子半径:r(P)>r(S)>r(O) B.第一电离能:I(O)>I(S)>I(P)
1 1 1
C.酸性强弱:HPO >HSO D.基态Cu原子3d轨道上有9个电子
3 4 2 4
【答案】A
【解析】A项,电子层数相同的,核电荷数越大的离子半径越小,则半径大小r(P)>r(S)>r(O),
正确;B项,同一周期主族元素从左向右第一电离能呈增大的趋势,但第Ⅱ A族、第ⅤA族比相邻元素
的大,则第一电离能:I(P)>I(S),错误;C项,元素非金属性越强,其最高价氧化物对应的水化物的
1 1微专题突破4 物质结构与性质一
酸性越强,非金属性:P<S,酸性:HPO <HSO ,错误;D项,基态Cu原子的价电子排布为3d104s1,
3 4 2 4
错误。
6.(2024·南京市二模)下列说法正确的是
A.碱金属和碱土金属元素均位于元素周期表的p区
B.NaCl中化学键的离子键百分数比MgCl 中的低
2
C.NaO 中存在Na+与O2-之间的强烈相互作用
2 2 2
D.NaCO 中CO2-的空间结构为三角锥形
2 3 3
【答案】C
【解析】A项,碱金属和碱土金属元素分别位于元素周期表的ⅠA、ⅡA族,都属于元素周期表的s
区,不正确;B项,Na的金属性比Mg强,NaCl比MgCl 的电负性差值大,则NaCl中化学键的离子键百
2
分数比MgCl 中的高,不正确;C项,NaO 由Na+和O2-构成,Na+与O2-之间存在离子键,则二者之
2 2 2 2 2
间存在强烈的相互作用,正确;D项,NaCO 中,CO2-的中心C原子的价层电子对数为3,发生sp2杂
2 3 3
化,则空间结构为平面正三角形,不正确。
7.(2024·南通市如皋二模)BN是一种无机非金属材料,立方BN的硬度仅次于金刚石,其晶胞如
下图所示.下列说法不正确的是
A.立方BN属于共价晶体 B.1个晶胞中含有4个B和4个N
C.距离每个B最近的N有4个 D.1 mol立方BN中含有2 mol共价键
【答案】D
【解析】A项,立方BN的硬度仅次于金刚石,属于共价晶体,正确;B项,根据均摊法,该晶胞中
位于顶点和面心的原子个数为8×+6×=4,位于晶胞内部的原子个数为4,则1个晶胞中含有4个B和4
个N,正确;C项,根据晶胞结构可知,每个B最近的N有4个,每个N最近的B有4个,正确;D项,
立方BN中每个B形成4个B-N键,1 mol立方BN中含有4 mol共价键,错误。
8.(2024·南通市二模)下列说法正确的是
A.Co位于元素周期表的ds区 B.NO2-和NO -中N原子均采取sp2杂化
3
C.1 mol [Co(NO)]3-中含有12 mol σ键 D.灼烧时火焰呈现紫色的物质一定是钾盐
2 6
【答案】B
【解析】A项,Co原子序数27,价电子排布:3d74s2,位于元素周期表d区,错误;B项,NO2-中
心原子N价层电子对数:2+=3,为sp2杂化;NO -中心原子N价层电子对数:3+=3,为sp2杂化,正
3
确;C项,配位键是特殊的共价键,1 mol [Co(NO)]3-中含有18 mol σ键,错误;D项,灼烧时火焰呈
2 6
现紫色的物质可能是钾盐,也可能时钾的其它化合物,错误。
9.(2024·徐州上学期期中)砷可用于制取新型半导体材料砷化镓,砷化镓晶胞如图所示。
下列说法正确的是
A.NO2-、NO -的空间构型均为平面三角形
3
B.基态As原子的核外电子排布式为[Ar]4s24p3
C.NH 的沸点比PH 高的原因是NH 能形成分子间氢键
3 3 3
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找D.砷化镓晶胞中每个As原子周围与它最近且距离相等的Ga原子有6个
【答案】C
【解析】A项,NO2-中N原子价层电子对数=2+=3,其中有一个孤电子对,所以其空间构型为V
形;NO -中N原子价层电子对数=3+=3,没有孤电子对,所以其空间构型为平面三角形形;错误;B
3
项,砷元素的原子序数为33,基态原子的电子排布式为[Ar]3d104s24p3,错误;C项,N属于电负性强的元
素,NH 能形成分子间氢键,使NH 的沸点比PH 高;正确;D项,由晶胞示意图可知,砷化镓晶胞中每
3 3 3
个As原子周围与它最近且距离相等的Ga原子有4个,错误。
10.(2024·苏州调研期初)下列说法正确的是
A.Fe元素位于周期表的第ⅧB族
B.Fe2+转化为Fe得到的2个电子基态时填充在3d轨道上
C.K[Fe(CN)]中提供空轨道形成配位键的是Fe3+
3 6
D.FeS 晶体(如图)中每个Fe2+周围距离最近且相等的S2-数目为8
2 2
【答案】C
【解析】A项,Fe元素位于周期表的第四周期Ⅷ族,错误;B项,Fe的核外电子排布为[Ar]3d64s2,
Fe2+的核外电子排布为[Ar]3d6,Fe2+转化为Fe得到的2个电子基态时填充在4s轨道上,错误;C项,
K[Fe(CN)]中提供空轨道的是Fe3+,CN-提供孤电子对,形成配位键,正确;D项,FeS 晶体(如图)中
3 6 2
每个Fe2+周围距离最近且相等的S2-数目为6,错误。
2
11.(2024·江苏二模)下列说法正确的是
A.4NH +3F====3NH F+NF 该反应氧化剂∶还原剂=3∶4
3 2 4 3
B.Fe3+得一个电子Fe2+电子排布式由[Ar]3d5变为[Ar]3d54s1
C.CH+的空间结构为平面三角形
3
D.1 mol 分子中,n(σ)∶n(π)=4∶1
【答案】C
【解析】A项,由方程式可知,4分子中氨中的1分子氨的氮化合价由-3变为+3,为还原剂,3分
子氟气中元素化合价降低为氧化剂,则氧化剂∶还原剂=3∶1,错误;B项,铁为26号元素,Fe2+的价
电子排布式为3d6,错误;C项,CH+中C原子的价层电子对数为3+=3,则中心原子为sp2杂化,空间
3
结构为平面三角形,正确;D项,单键均为σ键,双键中含有1个σ键1个π键,苯环中不存在单独的π
键,1 mol 分子中,,n(σ)∶n(π)=16∶1,错误。
12.(2024·江苏省南通市三模)前4周期主族元素X、Y、Z、W的原子序数依次增大。基态时,
X原子核外有6个电子,Y原子3p原子轨道半充满,Z原子3p原子轨道上有2个未成对电子。W与Y处
于同一主族。下列说法正确的是
A.第一电离能:Z<Y
B.Y的简单气态氢化物的热稳定性比W的弱
C.原子半径:r(W)<r(Z)
D.X的最高价氧化物对应水化物的酸性比Z的强
【答案】A微专题突破4 物质结构与性质一
【解析】前4周期主族元素X、Y、Z、W的原子序数依次增大,基态时,X原子核外有6个电子,
则X为C元素,Y原子3p原子轨道半充满,则Y为P元素,Z原子3p原子轨道上有2个未成对电子,则
Z为S元素,W与Y处于同一主族,则W为As元素。由分析知,X为C,Y为P,Z为S,W为As。
A项,由于P的3p能级处于稳定的半充满状态,难失去电子,则第一电离能比S的大,故第一电离
能:S<P,正确;B项,非金属性越强,其对应的简单气态氢化物越稳定,同主族元素从上往下非金属
性逐渐减弱,故P的非金属性大于As,则Y的简单气态氢化物的热稳定性比W的强,错误;C项,同主
族从上往下原子半径逐渐增大,从左至右原子半径逐渐减小,故原子半径:r(As)<r(S),错误;D项,
非金属性越强,其对应的最高价氧化物对应水化物的酸性越强,同周期元素从左至右非金属性逐渐增强,
故C的最高价氧化物对应水化物的酸性比S的弱,错误。
13.(2024·连云港一模)周期表中ⅡA族元素及其化合物应用广泛。铍的化合物性质与铝相似,
BeO的熔点为2 575℃,熔融时BeF 能导电,而BeCl 不能导电;下列有关说法正确的是
2 2
A.BeF 和BeCl 均为离子化合物
2 2
B.BeO的晶胞如图所示,晶胞中O2-的配位数为4
C.ⅡA族元素形成的氧化物均能与冷水直接化合成强碱
D.在空气中加热蒸发BeCl 和MgCl 溶液都能得到BeCl 和MgCl 固体
2 2 2 2
【答案】B
【解析】A项,BeCl 与AlCl 的结构性质相似,属于共价化合物,不符合题意;B项,BeO的晶胞如
2 3
图所示,白球为O2-,面心O2-与两个Be2+相连,面心O2-应连接两个晶胞,故晶胞中O2-的配位数为
4,符合题意;C项,ⅡA族中的Mg元素形成的氧化物为MgO,与冷水直接化合成的氢氧化镁不是强碱,
不符合题意;D项,BeCl 是很易水解的,一般溶液呈酸性是正常的,类似于AlCl 溶液,如果溶液呈酸
2 3
性或近中性,则蒸干灼烧后会得到BeO,不符合题意。
14.(2024·扬州市高三下学期开学考)氧、硫、铁可形成多种用途广泛的物质。HO 具有较强的
2 2
氧化性。亚硫酰氯(SOCl )遇水发生水解反应生成HSO 与HCl。Fe O 可用作锂离子电池的电极材料,电
2 2 3 2 3
池工作时有Li+嵌入其中生成LiFe O。FeS 可用于生产HSO ,其一种晶胞结构如图1所示。工业上可电
3 4 2 2 4
解HSO 与(NH )SO 混合溶液制备过二硫酸铵[(NH )SO],其结构如图2所示。酸与碱反应时放热,
2 4 4 2 4 4 2 2 8
中和热为57.3 kJ·mol-1。
下列说法正确的是
A.SOCl 中硫原子带正电,氯原子带负电
2
B.SO2-中硫原子的轨道杂化类型是sp2
3
C.该FeS 晶胞中含S2-的数目为14
2 2
D.该FeS 晶体中每个Fe2+周围距离最近且相等的S2-数目为8
2 2
【答案】A
【解析】A项,电负性:O>Cl>S,故在SOCl 中硫原子带正电,氯原子带负电,正确;B项,SO2
2 3
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找-的中心原子S的价层电子对数目3+=4,故S的杂化方式为sp3,错误;C项,FeS 的晶胞中Fe2+位于
2
体心和棱心,S2-位于顶点和面心,故晶胞中S2-的数目8×+6×=4,错误;D项,体心Fe2+为例,与其
2 2
等距离且最近的S2-位于6个面的面心,故数目为6,错误。
2
15.(2024·江苏镇江市高三开学考)ⅤA族氮、磷、砷(As)、锑(Sb)元素及其化合物应用广泛。
氨是重要的化工原料,广泛用于生产铵盐、硝酸、纯碱、医药等;肼(NH)的燃烧热为624 kJ·mol-1
2 4
,是常用的火箭燃料。白磷(P)晶胞如图所示,P元素可形成多种含氧酸,其中次磷酸(HPO )为一元弱
4 3 2
酸,HPO 为三元中强酸。锑是带有银色光泽的灰色金属,铅锑合金一般用作铅蓄电池的负极材料。
3 4
下列说法正确的是
A.PCl 是由极性键形成的非极性分子
3
B.NH 易液化是由于NH 与HO分子间形成氢键
3 3 2
C.ⅤA族元素单质的晶体类型相同
D.白磷晶体中1个P 分子周围有12个紧邻的P 分子
4 4
【答案】D
【解析】A项,PCl 中含共价键P-Cl键,属于极性键,中心原子P价层电子对数:3+=4,含1对
3
孤电子对,为三角锥形,属于极性分子,错误;B项,NH 易液化是由于NH 分子间形成氢键,错误;C
3 3
项,VA族氮、磷、砷(As)、锑(Sb)元素由非金属元素向金属过渡,氮、磷、砷形成的单质是分子晶体,
锑(Sb)单质晶体类型是金属晶体,错误;D项,由白磷晶胞结构图可知,与晶胞顶点距离最近且相等的
白磷分子有3个,分别位于3个面心,为2个晶胞所共用;而晶胞顶点上的白磷分子为8个晶胞所共用,
则晶体中与1个P 分子紧邻的P 分子有:3×8×=12,正确。
4 4
二、填空题
16.(2024·南通一模)利用氨水可捕集烟气中的CO 捕集、再生过程中含碳物种的变化如图所示。
2
液相中HNCOO-发生转化:HNCOO-+HOOH-\s\up 4()X+NH 。X的结构式为
2 2 2 ——→ 3
___________________。
【答案】
【解析】根据原子守恒,X能解吸出CO,判断X为碳酸氢根,结构式为: 。
2
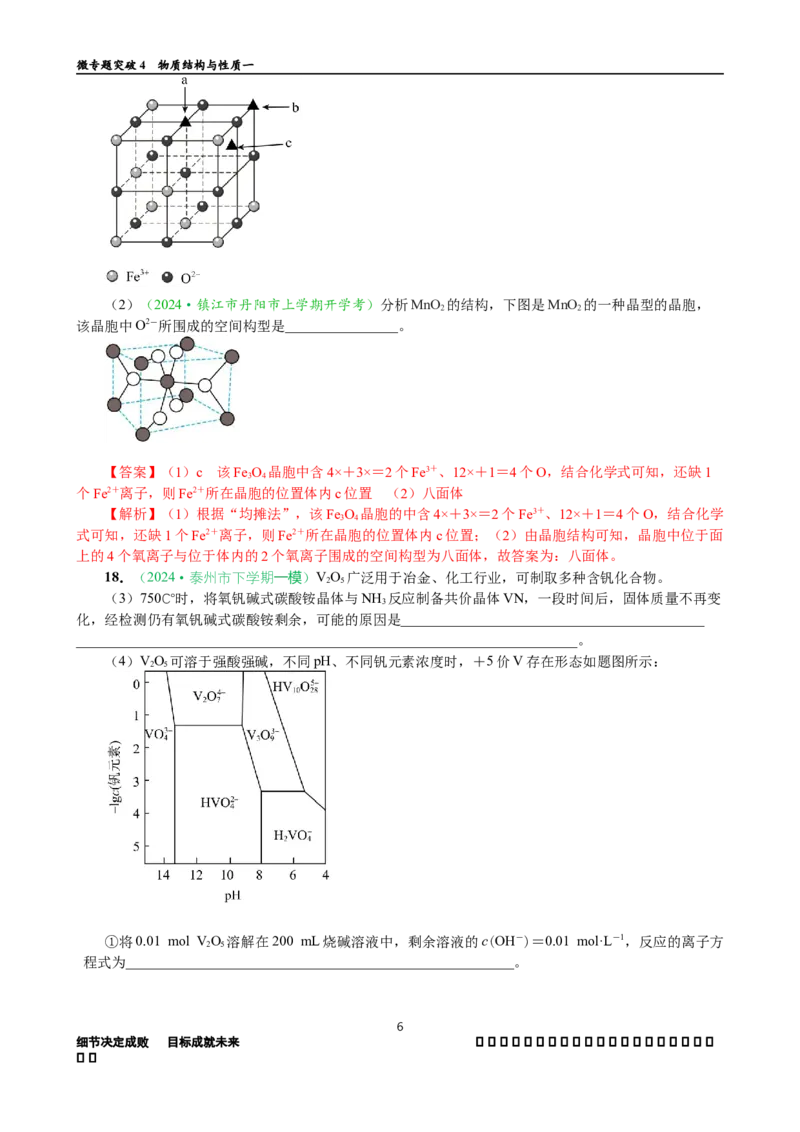
17.(1)(2024·淮安市高三上学期开学考)催化剂的回收。将回收的废催化剂进行处理,制成的
改性Fe O 是一种优良的磁性材料,该Fe O 晶胞的的结构如图所示,研究发现结构中的Fe2+只可能出现
3 4 3 4
在图中某一“▲”所示位置上,请确定Fe2+所在晶胞的位置_______,请说明确定理由:
_________________________________________________________________________________________。微专题突破4 物质结构与性质一
(2)(2024·镇江市丹阳市上学期开学考)分析MnO 的结构,下图是MnO 的一种晶型的晶胞,
2 2
该晶胞中O2-所围成的空间构型是________________。
【答案】(1)c 该Fe O 晶胞中含4×+3×=2个Fe3+、12×+1=4个O,结合化学式可知,还缺1
3 4
个Fe2+离子,则Fe2+所在晶胞的位置体内c位置 (2)八面体
【解析】(1)根据“均摊法”,该Fe O 晶胞的中含4×+3×=2个Fe3+、12×+1=4个O,结合化学
3 4
式可知,还缺1个Fe2+离子,则Fe2+所在晶胞的位置体内c位置;(2)由晶胞结构可知,晶胞中位于面
上的4个氧离子与位于体内的2个氧离子围成的空间构型为八面体,故答案为:八面体。
18.(2024·泰州市下学期一模)VO 广泛用于冶金、化工行业,可制取多种含钒化合物。
2 5
(3)750℃时,将氧钒碱式碳酸铵晶体与NH 反应制备共价晶体VN,一段时间后,固体质量不再变
3
化,经检测仍有氧钒碱式碳酸铵剩余,可能的原因是___________________________________________
_______________________________________________________________________。
(4)VO 可溶于强酸强碱,不同pH、不同钒元素浓度时,+5价V存在形态如题图所示:
2 5
①将0.01 mol VO 溶解在200 mL烧碱溶液中,剩余溶液的c(OH-)=0.01 mol·L-1,反应的离子方
2 5
程式为_______________________________________________________。
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找②VO4-具有对称结构,其结构式可表示为_______________________________。
2 7
【答案】(3)生成了致密的VN覆盖在氧钒碱式碳酸铵晶体表面,阻碍了氧钒碱式碳酸铵晶体与
NH 的接触 (4)①VO+4OH-=VO4-+2HO ②
3 2 5 2 7 2
【解析】(3)由题意可知,750℃时,将氧钒碱式碳酸铵晶体与氨气反应制备共价晶体氮化钒时,
一段时间后,固体质量不再变化,经检测仍有氧钒碱式碳酸铵剩余说明氧钒碱式碳酸铵未能完全反应,
可能是生成了致密的VN覆盖在氧钒碱式碳酸铵晶体表面,阻碍了氧钒碱式碳酸铵晶体与NH 的接触,故
3
答案为:生成了致密的VN覆盖在氧钒碱式碳酸铵晶体表面,阻碍了氧钒碱式碳酸铵晶体与NH 的接触;
3
(4)①由钒原子个数守恒可知,五氧化二钒与氢氧化钠溶液反应所得溶液中钒元素的浓度为=0.1
mol·L-1,则溶液中钒元素浓度—lgc=1,由溶液中氢氧根离子浓度为0.01 mol·L-1,溶液pH为12,
由图可知,—lgc为1和pH为12时,+5价钒元素的存在形式为VO4-,则五氧化二钒与氢氧化钠溶液
2 7
反应的离子方程式为VO+4OH-=VO4-+2HO,故答案为:VO+4OH-=VO4-+2HO;②由
2 5 2 7 2 2 5 2 7 2
VO4-中钒元素的化合价为+5价,离子具有对称结构可知,离子的结构式为 。
2 7