文档内容
微专题突破4 物质结构与性质二
一、选择题
1.(2024·海南省海口市摸底)氧和硫是元素周期表中第ⅥA族元素。下列说法正确的是
A.电负性:O<S B.沸点:HO<HS
2 2
C.SO 是极性分子 D.SO2-空间构型为平面三角形
2 3
【答案】C
【解析】A项,同族元素,电负性从上到下逐渐减小,即电负性:O>S,错误;B项,由于HO能
2
形成分子间氢键,HS不能,因此沸点:HO>HS,错误;C项,SO 中的S价层电子数为2+=3,有1
2 2 2 2
个孤电子对,为sp2杂化,空间构型为V形,其正负电荷中心不重合,属于极性分子,正确;D项,SO2
3
-中的S的价层电子对数为3+=4,有1个孤电子对,为sp3杂化,空间构型为三角锥形,错误。
2.(2024·广西北海市一模)Fe(NH )[Fe(CN)](俗称铵铁蓝)是一种蓝色的无机颜料。下列有关该
4 6
物质的说法错误的是
A.电负性:N>C>H
B.铵铁蓝中铁元素有两种化合价
C.NH中H-N-H的键角比NH 中的H-N-H的键角大
3
D.铵铁蓝中的配体是 ,该配体中σ键与π键的数目之比是2∶1
【答案】D
【解析】A项,同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,则电负性:N>
C>H,正确;B项,由化合物中正、负化合价的代数和为0可知,铵铁蓝中铁元素有+2和+3两种化合
价,正确;C项,根据价层电子对互斥理论可知,NH的空间结构为正四面体形,NH 的空间结构为三角
3
锥形,NH中H-N-H的键角比NH 中的H-N-H的键角大,正确;D项,CN-中C和N之间是三键,
3
与氮气互为等电子体,1个CN-中有1个σ键和2个π键,则该配体中σ键与π键的数目之比是1∶2,错
误。
3.(2025·江苏苏州市开学考)[Cu(NH )]SO 常用作杀虫剂、媒染剂。下列说法正确的是
3 4 4
A.原子半径:r(N)>r(O)>r(S) B.沸点:HS>HO>NH
2 2 3
C.第一电离能:I(N)>I(O)>I(S) D.电负性:χ(N)>χ(O)>χ(Cu)
1 1 1
【答案】C
【解析】A项,电子层数越多半径越大,电子层结构相同,核电荷数越大,半径越小,原子半径:
r(S)>r(N)>r(O),错误;B项,三种物质均是由分子构成的物质,相对分子质量越大,范德华力越大,
熔沸点越高,但是水分子间可形成氢键,因此水的沸点最高,故沸点:HS>HS>NH ,错误;C项,同
2 2 3
主族从上到下,第一电离能逐渐减小,同一周期从左往右元素的第一电离能呈增大趋势,但ⅡA与
ⅢA、ⅤA与ⅥA反常,故第一电离能:I(N)>I(O)>I(S),正确;D项,非金属性越强,电负性越
1 1 1
大,同周期元素,从左到右元素的非金属性依次增强,电负性依次增大,故电负性:χ(O)>χ(N)>
χ(Cu),错误。
4.(2024·河南省新乡市一模)茜草中的茜素与Al3+、Ca2+生成的红色配合物X是最早使用的媒染
染料之一、下列说法错误的是
A.Al与O形成配位键时,O提供孤电子对微专题突破4 物质结构与性质二
B.配合物X所含的元素中属于s区的只有H
C.配合物X中Al3+的配位数为6
D.茜素分子间存在范德华力、氢键
【答案】B
【解析】A项,Al与O形成配位键时,O提供孤电子对,Al提供空轨道,正确;B项,属于s区的
元素有H和Ca,错误;C项,由配合物X的结构式可知,Al3+的配位数为6,正确;D项,茜素为分子晶
体,故存在范德华力,茜素含有-OH,存在分子间氢键,正确。
5.(2024·无锡上学期期中)下列有关说法正确的是
A.NH 的空间构型是三角锥形 B.NH 是结构对称的非极性分子
3 2 4
C.1 mol [Ag(NH)]+中有2 mol σ键 D.[Ag(NH)]+和NH 中N-H键角相等
3 2 3 2 3
【答案】A
【解析】A项,NH 中心原子N周围价层电子对数为:3+=4,孤电子对数为1,根据价层电子对互
3
斥理论可知,NH 的空间构型是三角锥形,正确;B项,NH 分子中2个N为sp3杂化,均含一对孤电子,
3 2 4
由于其正、负电荷中心不重合,故为极性分子,错误;C项,1 mol [Ag(NH)]+中含有6 mol N-H σ键
3 2
和2 mol Ag-N σ键,一共有8 mol σ键,错误;D项,[Ag(NH)]+N周围无孤电子对,而NH 中N周
3 2 3
围还有1对孤电子对,孤电子对对孤电子对的排斥力>孤电子对对成键电子对的排斥力>成键电子对对
成键电子对的排斥力,故[Ag(NH)]+中N-H键角大于NH 中N-H键角,错误。
3 2 3
6.(2025·连云港市上学期期中)摩尔盐[(NH )Fe(SO )•6H O]可以用于配制标准溶液。下列说
4 2 4 2 2
法正确的是
A.半径:r(O2-)>r(S2-) B.第一电离能:I(N)>I(O)
1 1
C.电负性:χ(Fe)>χ(H) D.热稳定性:HS>HO
2 2
【答案】B
【解析】A项,O2-的核外电子数为10,电子层数为2,S2-的核外电子数为18,电子层数为3,电子
层数越多离子半径越大,则离子半径:r(O2-)>r(S2-),错误;B项,N、O为同周期元素,同周期元素
第一电离能从左到右呈增大趋势,但N最外层2p能级中电子为半满稳定结构,其第一电离能大于O,正
确;C项,Fe为金属元素,H为非金属元素,电负性:χ(Fe)<χ(H,错误;D项,非金属性:O>S,元
素的非金属性越强,其简单氢化物的稳定性越大,则热稳定性:HS<HO,错误。
2 2
7.(2024·苏锡常镇二模)周期表中ⅦA族元素及其化合物应用广泛。电解KHF 与HF的混合物时,
2
HF2-转化为F ;加热NaCl与浓HSO 的混合物,可制得HCl。氯还可形成HClO 、HClO 、HClO 等多
2 2 4 2 3 4
种含氧酸。ClO 是Al级高效安全灭菌消毒剂;Cl 与CH 反应可制备有机溶剂CCl。在照相底片的定影过
2 2 4 4
程中,底片上未曝光的AgBr浸入NaSO 溶液转变成[Ag(SO)]3-而溶解。氯化碘(ICl)性质与卤素单质
2 2 3 2 3 2
相似,常用作分析化学试剂。下列说法正确的是
A.基态F原子的核外电子排布式为2s22p5
B.KHF 中既含有离子键,又含有共价键
2
C.ClO2-、ClO -和ClO -中O-Cl-O键角依次逐渐减小
3 4
D.SO2-(结构如图 )中两个S原子均可作配位原子
2 3
【答案】B
【解析】A项,F为第9号元素,核外有9个电子,根据构造原理,基态F原子的核外电子排布式为
1s22s22p5,2s22p5是价层电子排布式,错误;B项,题中已知HF2-转化为F ,说明KHF 中含有钾离子和
2 2
HF2-,即KHF 为离子晶体,含有离子键,HF2-中存在共价键,正确;C项,ClO2-的中心原子Cl的价
2
层电子对数为2+=4,为sp3杂化,含有2对孤电子对;ClO -的中心原子Cl的价层电子对数为3+=4,
3
为sp3杂化,含有1对孤电子对;ClO -的中心原子Cl的价层电子对数为4+=4,为sp3杂化,无孤电子对;
4
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找杂化类型相同时,由于孤电子对对成键电子对之间的排斥力大于成键与成键电子的排斥力,因此孤电子
对数越多键角越小,所以ClO2-、ClO -和ClO -中O-Cl-O键角依次逐渐增大,错误;D项,具有孤电
3 4
子对的原子可以给中心原子提供电子配位,SO2-中的中心原子S的价层电子对数为4,无孤电子对,不
2 3
能做配位原子,端基S原子含有孤电子对,能做配位原子,错误。
8.(2024·江苏盐城市高三期中)元素镓( Ga)、锗( Ge)、砷( As)位于周期表中第四周期。下列
31 32 33
说法不正确的是
A.原子半径:r(Ga)>r(Ge)>r(As)
B.电负性:χ(Ga)<χ(Ge)<χ(As)
C.Ge、Ga、As都具有半导体性能
D.第一电离能:I(Ga)<I(As)<I(Ge)
1 1 1
【答案】D
【解析】A项,同周期元素,核电荷数越大原子半径越小,原子半径:r(Ga)>r(Ge)>r(As),正确;
B项,同周期元素,核电荷数越大电负性越大,电负性:χ(Ga)<χ(Ge)<χ(As),正确;C项,Ge、Ga、
As都在金属非金属分界线附近,具有半导体性能,正确;D项,同周期元素,核电荷数越大第一电离能
越大,第一电离能:I(Ga)<I(Ge)<I(As),错误。
1 1 1
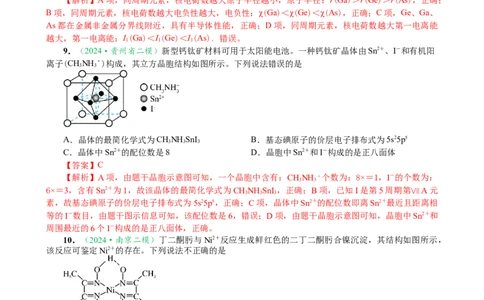
9.(2024·贵州省二模)新型钙钛矿材料可用于太阳能电池。一种钙钛矿晶体由Sn2+、I-和有机阳
离子(CHNH +)构成,其立方晶胞结构如图所示。下列说法错误的是
3 3
A.晶体的最简化学式为CHNH SnI B.基态碘原子的价层电子排布式为5s25p5
3 3 3
C.晶体中Sn2+的配位数是8 D.晶胞中Sn2+和I-构成的是正八面体
【答案】C
【解析】A项,由题干晶胞示意图可知,一个晶胞中含有:CHNH +个数为:8×=1,I-的个数为:
3 3
6×=3,含有Sn2+为1,故该晶体的最简化学式为CHNH SnI ,正确;B项,已知I是第5周期第ⅦA元
3 3 3
素,故基态碘原子的价层电子排布式为5s25p5,正确;C项,晶体中Sn2+的配位数即离Sn2+最近且距离相
等的I-数目,由题干图示信息可知,该配位数是6,错误;D项,由题干晶胞示意图可知,晶胞中Sn2+和
周围最近的6个I-构成的是正八面体,正确。
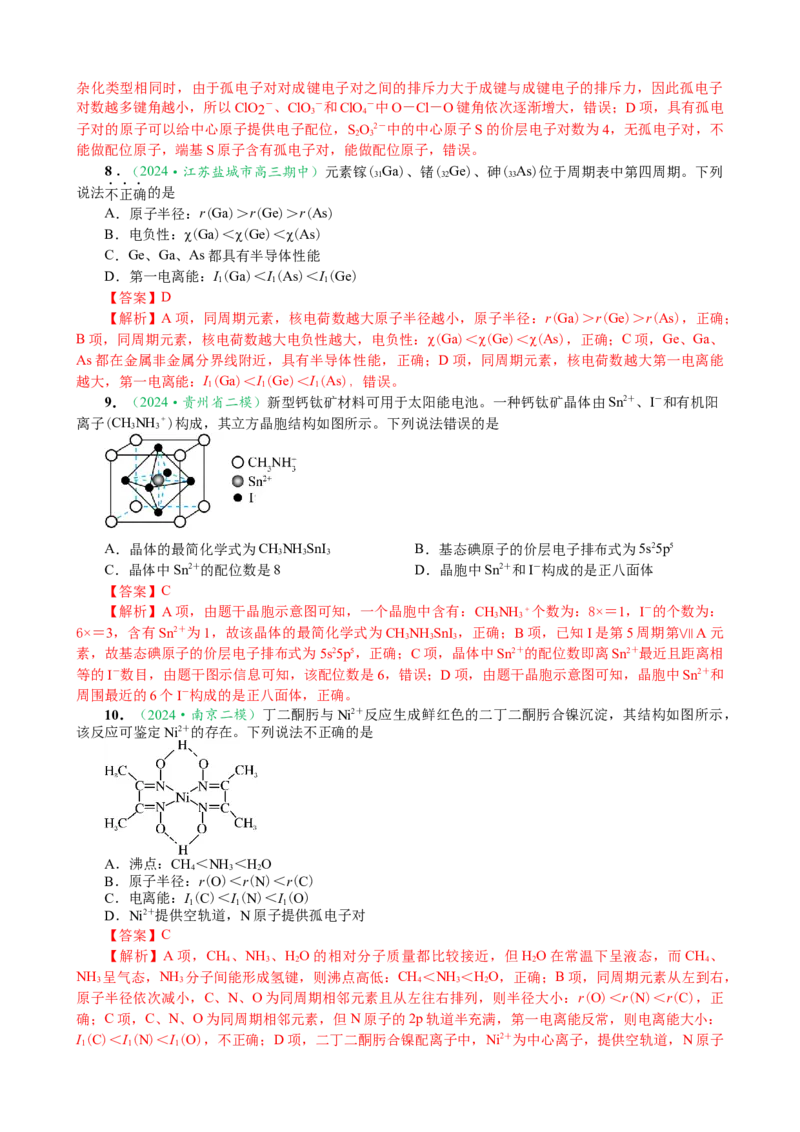
10.(2024·南京二模)丁二酮肟与Ni2+反应生成鲜红色的二丁二酮肟合镍沉淀,其结构如图所示,
该反应可鉴定Ni2+的存在。下列说法不正确的是
A.沸点:CH<NH <HO
4 3 2
B.原子半径:r(O)<r(N)<r(C)
C.电离能:I(C)<I(N)<I(O)
1 1 1
D.Ni2+提供空轨道,N原子提供孤电子对
【答案】C
【解析】A项,CH 、NH 、HO的相对分子质量都比较接近,但HO在常温下呈液态,而CH 、
4 3 2 2 4
NH 呈气态,NH 分子间能形成氢键,则沸点高低:CH <NH <HO,正确;B项,同周期元素从左到右,
3 3 4 3 2
原子半径依次减小,C、N、O为同周期相邻元素且从左往右排列,则半径大小:r(O)<r(N)<r(C),正
确;C项,C、N、O为同周期相邻元素,但N原子的2p轨道半充满,第一电离能反常,则电离能大小:
I(C)<I(N)<I(O),不正确;D项,二丁二酮肟合镍配离子中,Ni2+为中心离子,提供空轨道,N原子
1 1 1微专题突破4 物质结构与性质二
为配位原子,提供孤电子对,正确。
11.(2025·江苏苏州市开学考)VA族元素及其化合物应用广泛。NH 催化氧化生成NO,NO继续
3
被氧化为NO ,将NO 通入水中可制得HNO;肼(NH)常温下为液态,燃烧热为642 kJ·mol-1,产物
2 2 3 2 4
无污染,常用作火箭燃料:白磷(P)为正四面体结构,常用来制烟雾弹、燃烧弹;雄黄(As S)具有解毒、
4 4 4
杀虫功效,燃烧后生成砒霜(As O)和一种具有刺激性气味的气体;锑是一种银白色金属,其氧化物
2 3
Sb O 可用于制造颜料,铅锑合金可用作铅蓄电池的电极材料。
2 3
下列说法正确的是
A.NH 分子中既有极性键,又有非极性键 B.NH 中键角比P 中键角小
2 4 3 4
C.1 mol白磷含有4 mol P-P键 D.As基态原子核外电子排布式为[Ar]4s24p3
【答案】A
【解析】A项,NH 电子式为 ,两个N原子之间为非极性键,N原子与H原子之间为极性
2 4
键,正确;B项,白磷(P)是正四面体形分子,每个P原子处于正四面体顶点,其中 P-P-P夹角为
4
60°,NH 分子为三角锥形结构,其H-N-H键角为107.3°,错误;C项,白磷(P)是正四面体形分子,
3 4
如图 ,1 mol 白磷含有 6 mol P-P 键键,错误;D 项,As 基态原子核外电子排布式为
[Ar]3d104s24p3,故D错误。
12.(2023·苏州上学期期末)含锂物质在能源方面有重要应用。锂在氧气中燃烧与Mg相似,其燃
烧热为299 kJ·mol-1。锂与氮气反应得到的LiN可用作储氨材料。锂-空气电池是一种二次电池,放电
3
时主要产物为LiO ,充电时阴极产物易形成固态枝晶,导致电池短路。目前应用广泛的是锂离子电池,
2 2
例如,磷酸铁锂电池充电时锂离子由LiFePO 电极迁移至石墨电极形成LiC,LiFePO 的前体FePO 可由
4 x 4 4
NH HPO 、FeSO 、HO 在pH=12的条件下反应制得。下列物质结构与性质或物质性质与用途具有对应
4 2 4 4 2 2
关系的是
A.Mg有强还原性,可用于钢铁的电化学防护
B.LiOH可溶于水,可用作宇宙飞船中CO 吸收剂
2
C.石墨晶体层间存在范德华力,石墨易导电
D.HO 是极性分子,HO 有强氧化性
2 2 2 2
【答案】A
【解析】A项,Mg的还原性强于Fe,当Mg与Fe连接形成原电池,Mg作负极被腐蚀,钢铁被保护,
即牺牲阳极的阴极保护法,正确;B项,LiOH可用作宇宙飞船中CO 吸收剂,是由于其为碱,能与酸性
2
氧化物二氧化碳发生反应,与LiOH可溶于水无联系,错误;C项,石墨易导电是由于石墨为混合型晶体,
每个碳原子与其他碳原子只形成三个共价键,每个碳原子仍然保留一个自由电子来传递电荷,与范德华
力无关,错误;D项,HO 有强氧化性与其是极性分子无关,错误。
2 2
13.(2024·南通市如皋2月)NH
3
中的一个H原子被-OH取代可形成羟胺(NH
2
OH),被-NH
2
取代
可形成肼(NH),-OH吸电子能力比-NH 强。下列说法正确的是
2 4 2
A.NH 的键角比HO小 B.1 mol [Cu(NH )]2+中含12 mol σ键
3 2 3 4
C.NH OH难溶于水 D.NH OH中N结合H+的能力比NH 弱
2 2 2 4
【答案】D
【解析】A项,NH 和HO的中心原子都采用sp3杂化,NH 中N原子有1个孤电子对,HO中O原
3 2 3 2
子上有2个孤电子对,孤电子对越多键角越小,故HO的键角更小,错误;B项,1个[Cu(NH )]2+中有
2 3 4
12个N-H σ键、4个N-Cu σ键,共16个σ键,故1 mol [Cu(NH )]2+中含16 mol σ键,错误;C项,
3 4
NH OH有羟基和氨基,能与水形成分子间氢键,故易溶于水,错误;D项,-OH吸电子能力比-NH 强,
2 2
则NH OH中N原子的正电性大,比NH 中N原子更难以结合H+,正确。
2 2 4
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找的
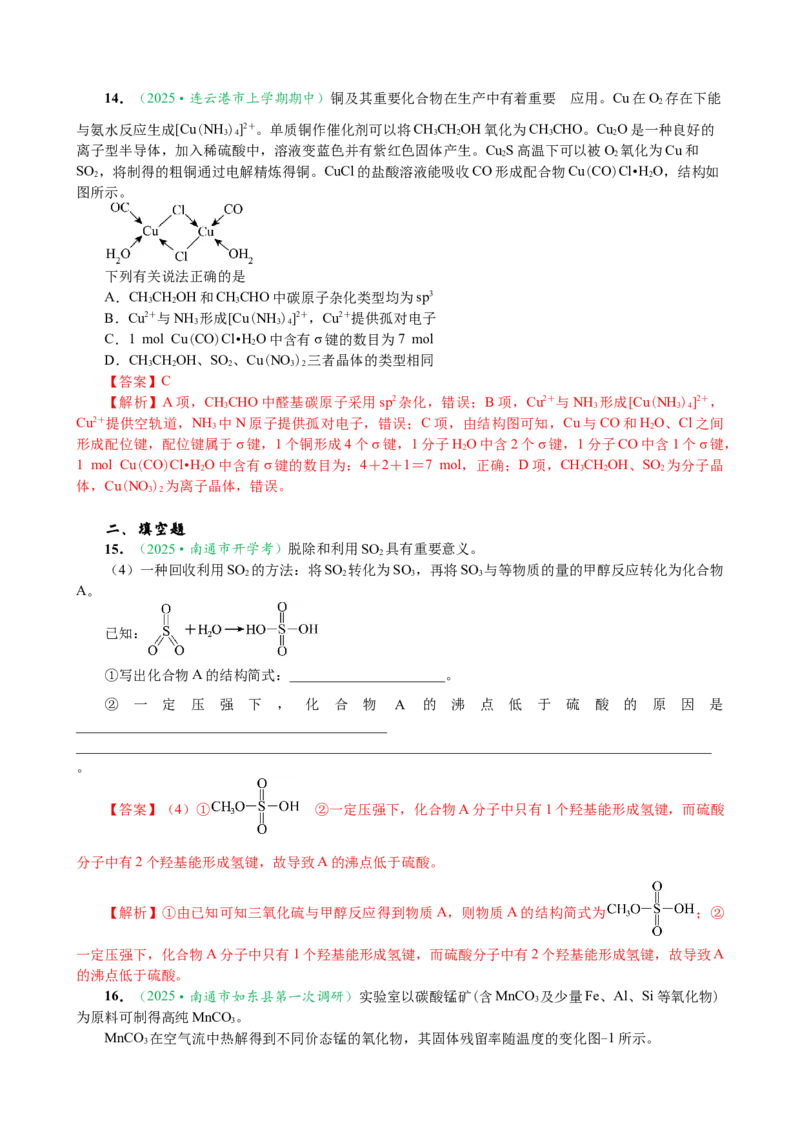
14.(2025·连云港市上学期期中)铜及其重要化合物在生产中有着重要 应用。Cu在O 存在下能
2
与氨水反应生成[Cu(NH )]2+。单质铜作催化剂可以将CHCHOH氧化为CHCHO。Cu O是一种良好的
3 4 3 2 3 2
离子型半导体,加入稀硫酸中,溶液变蓝色并有紫红色固体产生。Cu S高温下可以被O 氧化为Cu和
2 2
SO ,将制得的粗铜通过电解精炼得铜。CuCl的盐酸溶液能吸收CO形成配合物Cu(CO)Cl•HO,结构如
2 2
图所示。
下列有关说法正确的是
A.CHCHOH和CHCHO中碳原子杂化类型均为sp3
3 2 3
B.Cu2+与NH 形成[Cu(NH )]2+,Cu2+提供孤对电子
3 3 4
C.1 mol Cu(CO)Cl•HO中含有σ键的数目为7 mol
2
D.CHCHOH、SO 、Cu(NO ) 三者晶体的类型相同
3 2 2 3 2
【答案】C
【解析】A项,CHCHO中醛基碳原子采用sp2杂化,错误;B项,Cu2+与NH 形成[Cu(NH )]2+,
3 3 3 4
Cu2+提供空轨道,NH 中N原子提供孤对电子,错误;C项,由结构图可知,Cu与CO和HO、Cl之间
3 2
形成配位键,配位键属于σ键,1个铜形成4个σ键,1分子HO中含2个σ键,1分子CO中含1个σ键,
2
1 mol Cu(CO)Cl•HO中含有σ键的数目为:4+2+1=7 mol,正确;D项,CHCHOH、SO 为分子晶
2 3 2 2
体,Cu(NO ) 为离子晶体,错误。
3 2
二、填空题
15.(2025·南通市开学考)脱除和利用SO 具有重要意义。
2
(4)一种回收利用SO 的方法:将SO 转化为SO ,再将SO 与等物质的量的甲醇反应转化为化合物
2 2 3 3
A。
已知:
①写出化合物A的结构简式:______________________。
② 一 定 压 强 下 , 化 合 物 A 的 沸 点 低 于 硫 酸 的 原 因 是
____________________________________________
__________________________________________________________________________________________
。
【答案】(4)① ②一定压强下,化合物A分子中只有1个羟基能形成氢键,而硫酸
分子中有2个羟基能形成氢键,故导致A的沸点低于硫酸。
【解析】①由已知可知三氧化硫与甲醇反应得到物质A,则物质A的结构简式为 ;②
一定压强下,化合物A分子中只有1个羟基能形成氢键,而硫酸分子中有2个羟基能形成氢键,故导致A
的沸点低于硫酸。
16.(2025·南通市如东县第一次调研)实验室以碳酸锰矿(含MnCO 及少量Fe、Al、Si等氧化物)
3
为原料可制得高纯MnCO。
3
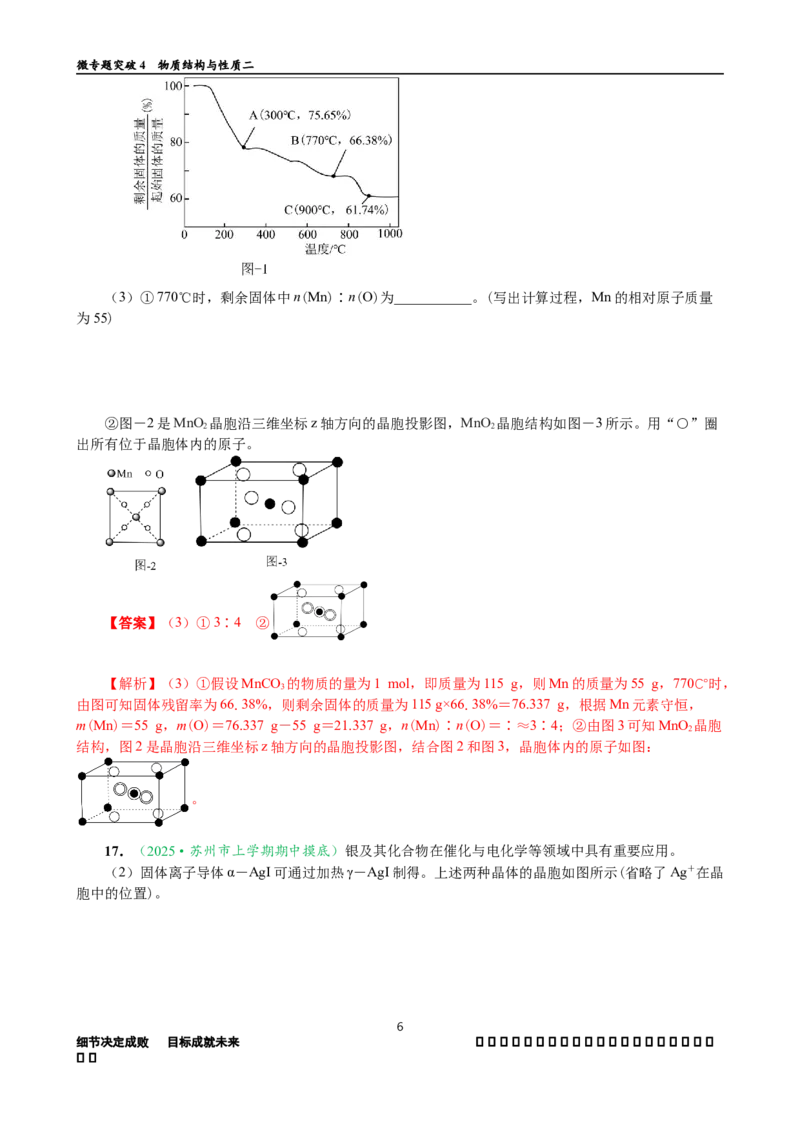
MnCO 在空气流中热解得到不同价态锰的氧化物,其固体残留率随温度的变化图-1所示。
3微专题突破4 物质结构与性质二
(3)①770℃时,剩余固体中n(Mn)∶n(O)为___________。(写出计算过程,Mn的相对原子质量
为55)
②图-2是MnO 晶胞沿三维坐标z轴方向的晶胞投影图,MnO 晶胞结构如图-3所示。用“○”圈
2 2
出所有位于晶胞体内的原子。
【答案】(3)①3∶4 ②
【解析】(3)①假设MnCO 的物质的量为1 mol,即质量为115 g,则Mn的质量为55 g,770℃时,
3
由图可知固体残留率为66.38%,则剩余固体的质量为115 g×66.38%=76.337 g,根据Mn元素守恒,
m(Mn)=55 g,m(O)=76.337 g-55 g=21.337 g,n(Mn)∶n(O)=∶≈3∶4;②由图3可知MnO 晶胞
2
结构,图2是晶胞沿三维坐标z轴方向的晶胞投影图,结合图2和图3,晶胞体内的原子如图:
。
17.(2025·苏州市上学期期中摸底)银及其化合物在催化与电化学等领域中具有重要应用。
(2)固体离子导体α-AgI可通过加热γ-AgI制得。上述两种晶体的晶胞如图所示(省略了Ag+在晶
胞中的位置)。
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找①测定晶体结构最常用的仪器是_____________________。
②α-AgI与γ-AgI晶胞的体积之比为_________________。
③判定α-AgI中导电离子类型的实验装置如图所示。实验前,H型管内填充满α-AgI,竖管a和
b(含α-AgI)的质量相同,两支Ag电极的质量也相同。通电一段时间后,可判定导电离子是Ag+而不是
I-的实验数据是___________________________________________________________。
【答案】(2)①X射线衍射仪 ②7∶12 ③a中银电极质量减小,b中银电极质量增大
【解析】①测定晶体结构最常用的仪器是X射线衍射仪;②α-AgI晶胞中AgI的个数为1+8×=
2,γ-AgI晶胞中AgI的个数为6×+8×=4,ρ==,则V=×AgI的个数,则α-AgI与γ-AgI晶胞的
体积之比为(×2)∶(×4)=7∶12;③由图可知,阳极Ag失电子生成Ag+进入溶液中,阴极溶液中Ag+得
电子生成Ag单质,Ag+能与I-结合生成AgI沉淀,而实验测得竖管a中AgI质量不变,则阳极生成的Ag
+移向阴极,导致阳极质量减小,Ag+在阴极得电子生成Ag,导致阴极质量增大,所以实验中导电离子是
Ag+而不是I-。