文档内容
微专题突破6 焓变与电化学
一、选择题
1.(2024·江苏南通市高三上学期期中)已知 25℃、101 KPa下,10 kg丁烷完全燃烧生成CO 和
2
液态水时,放出5×105 kJ的热量,下列热化学方程式书写正确的是
A.C H +O=4CO+5HO ∆H=-2 900 kJ·mol-1
4 10 2 2 2
B.C H (l)+O(g)=4CO(g)+5HO(l) ∆H=+2 900 kJ·mol-1
4 10 2 2 2
C.C H (l)+O(g)=4CO(g)+5HO(l) ∆H=+2 900 kJ
4 10 2 2 2
D.2C H (l)+13O(g)=8CO(g)+10HO(l) ∆H=-5 800 kJ·mol-1
4 10 2 2 2
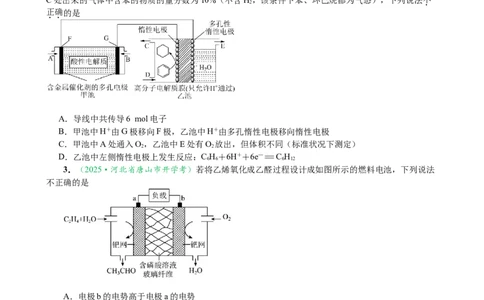
2.(2024·江苏泰州模拟预测)如图甲乙两个装置相连,甲池是一种常见的氢氧燃料电池装置,乙
池内,D中通入10 mol混合气体,其中苯的物质的量分数为20%(其余气体不参与反应),一段时间后,
C处出来的气体中含苯的物质的量分数为10%(不含H,该条件下苯、环己烷都为气态),下列说法不
2
正确的是
A.导线中共传导6 mol电子
B.甲池中H+由G极移向F极,乙池中H+由多孔惰性电极移向惰性电极
C.甲池中A处通入O,乙池中E处有O 放出,但体积不同(标准状况下测定)
2 2
D.乙池中左侧惰性电极上发生反应:C H+6H++6e—=C H
6 6 6 12
3.(2025·河北省唐山市开学考)若将乙烯氧化成乙醛过程设计成如图所示的燃料电池,下列说法
不正确的是
A.电极b的电势高于电极a的电势
B.H+的迁移方向:电极a→电极b
C.放电时,若电路中转移4 mol e—,理论上消耗O 2.24 L
2
D.电极a上反应式为C H-2e—+HO=CHCHO+2H+
2 4 2 3
4.(2024·泰州市期中)科学家利用氨硼烷设计成原电池装置如题图所示,常温下该电池总反应为
NH •BH+3HO=NH BO+4HO。下列说法正确的是
3 3 2 2 4 2 2微专题突破7 焓变与电化学
A.b室为该原电池的负极区
B.放电过程中,H+通过质子交换膜由b室移向a室
C.a室的电极反应式为NH •BH+2HO-6e—=NH+BO2-+6H+
3 3 2
D.其他条件不变时,向HO 溶液中加入适量NaOH溶液能增大电流强度
2 2
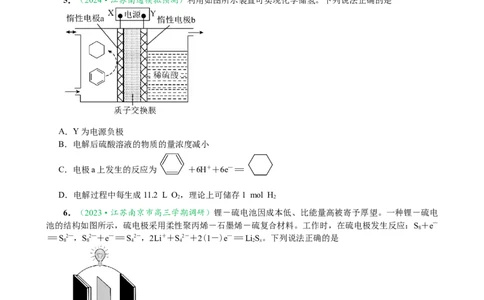
5.(2024·江苏南通模拟预测)利用如图所示装置可实现化学储氢。下列说法正确的是
A.Y为电源负极
B.电解后硫酸溶液的物质的量浓度减小
C.电极a上发生的反应为 +6H++6e—=
D.电解过程中每生成11.2 L O,理论上可储存1 mol H
2 2
6.(2023·江苏南京市高三学期调研)锂-硫电池因成本低、比能量高被寄予厚望。一种锂-硫电
池的结构如图所示,硫电极采用柔性聚丙烯-石墨烯-硫复合材料。工作时,在硫电极发生反应:S+e—
8
=S2—,S2—+e—=S2-,2Li++S2-+2(1-)e—=LiS。下列说法正确的是
8 8 4 4 2 x
A.充电时,Li+从b电极向a电极迁移
B.放电时,外电路电子流动的方向是a电极→b电极
C.放电时正极反应为:2Li++S-2e—=LiS
8 2 x
D.石墨烯的作用是增强硫电极导电性能
7.(2024·江苏省南通市、盐城市二模)一种电解法制备NaFeO 的装置如图所示。下列说法正确
2 4
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找的是
A.电解时化学能转化为电能
B.电解时应将铂电极与直流电源正极相连
C.电解过程中转移2 mol e-,理论上可获得标准状况下的H 11.2 L
2
D.电解时铁电极反应式:Fe-6e-+8OH-=FeO2-+4HO
4 2
8.(2024·江苏南京市盐城市一模)一种以钒基氧化物(VO )为正极材料的水系锌离子电池的工作
6 13
原理如图所示。通过使用孔径大小合适且分布均匀的新型离子交换膜,可提高离子传输通量的均匀性,
从而保持电池的稳定性。下列说法正确的是
A.放电过程中,Zn2+向Zn极一侧移动
B.放电过程中,电子由Zn极经电解质溶液向VO 极移动
6 13
C.充电时,VO 极与外接直流电源正极相连
6 13
D.充电时,阳极发生的电极反应可能为VO +xZn2++2xe—=ZnVO
6 13 x 6 13
9.(2024·江苏南通高三下开学考试)微生物电池具有高效、清洁、环保等优点。某微生物电池工
作原理如图所示,下列说法正确的是
A.电极a极为该电池的正极
B.放电过程中a极附近溶液pH增大
C.电极b极的电极反应式为[Fe(CN)]4--e—=[Fe(CN)]3-
6 6
D.每消耗23 g CHCHOH,理论上会有6 mol H+通过质子交换膜移向b极
3 2
二、填空题
10.(2024·江苏南京市盐城市一模)乙醇是一种清洁的替代能源,催化加氢制备乙醇技术是当前
的研究热点。
(1)CO催化加氢制备乙醇的反应为2CO(g)+6H(g)=C HOH(l)+3HO(l)。
2 2 2 5 2
①若要计算上述反应的∆H,须查阅的两个数据是C HOH(l)的燃烧热和____________________。
2 5
11.(2023·江苏南京市高三学期调研)“碳达峰、碳中和”是我国社会发展重大战略之一。CH 与
4
CO 经催化重整可制得CO和H,相关反应为:
2 2
主反应:CH(g)+CO(g)=2CO(g)+2H(g) ∆H
4 2 2微专题突破7 焓变与电化学
副反应:Ⅰ.H(g)+CO(g)=HO(g)+CO(g) ∆H
2 2 2 1
Ⅱ.2CO(g)=CO(g)+C(s) ∆H
2 2
Ⅲ.CH(g)=C(s)+2H(g) ∆H
4 2 3
Ⅳ.CO(g)+H(g)=C(s)+HO(g) ∆H
2 2 4
则主反应:CH(g)+CO(g)=2CO(g)+2H(g) ∆H=_________________。
4 2 2
12.(2024·苏州调研期初)研究二氧化碳的资源化利用具有重要的意义。
(1)CO 催化加氢制CH 是CO 的有机资源转化途径之一
2 4 2
反应I:CO(g)+4H(g)=CH(g)+2HO(g) ∆H=-164.7 kJ·mol-1
2 2 4 2 1
反应Ⅱ:CO(g)+H(g)=CO(g)+HO(g) ∆H=41.2 kJ·mol-1
2 2 2 2
①反应:2CO(g)+2H(g)=CO(g)+CH(g) ∆H=___________kJ·mol-1
2 2 4
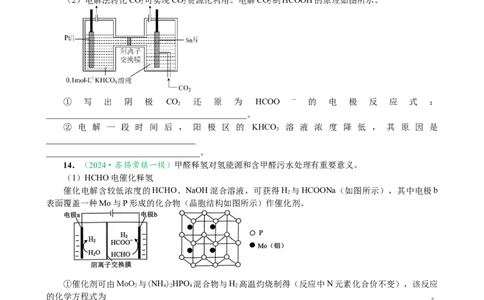
13.(2024·南通市如皋2月)二氧化碳的综合利用具有重要意义。
(2)电解法转化CO 可实现CO 资源化利用。电解CO 制HCOOH的原理如图所示。
2 2 2
① 写 出 阴 极 CO 还 原 为 HCOO - 的 电 极 反 应 式 :
2
_______________________________________________。
② 电 解 一 段 时 间 后 , 阳 极 区 的 KHCO 溶 液 浓 度 降 低 , 其 原 因 是
3
___________________________________
____________________________________。
14.(2024·苏锡常镇一模)甲醛释氢对氢能源和含甲醛污水处理有重要意义。
(1)HCHO电催化释氢
催化电解含较低浓度的HCHO、NaOH混合溶液,可获得H 与HCOONa(如图所示),其中电极b
2
表面覆盖一种Mo与P形成的化合物(晶胞结构如图所示)作催化剂。
①催化剂可由MoO 与(NH )HPO 混合物与H 高温灼烧制得(反应中N元素化合价不变),该反应
2 4 2 4 2
的化学方程式为____________________________________________________________________________。
②电解时,电极b上同时产生H 与HCOO-的物质的量之比为1∶2,则电极b上的电极反应式为
2
_____________________________________________________________。
③电解过程中每产生1 mol H,通过阴离子交换膜的OH-为______mol。
2
15.(2024·江苏省南通市三模)以氧化镁为载体,化学链方法分解氯化铵工艺的示意图如图1所
示。“释氯”过程中可能发生反应的焓变如图2所示。
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找①已知NH Cl(s)=NH (g)+HCl(g) ∆H=a kJ·mol-1。温度越高,越有利于NH Cl分解。
4 3 4
a_____(填“>0”“<0”或“=0”)。
②“释氨”主反应为MgO(s)+NH Cl(s)=MgOHCl(s)+NH (g),该反应∆H=__________。
4 3
④“释氯”装置中含有少量HO可提高“释氯”时HCl的平衡产率,主要原因是
2
__________________________________________________________________。
⑤已知CH(g)+2O(g)=CO(g)+2HO(g) ∆H=-d kJ·mol-1,燃烧CH 的热量用于该化学链
4 2 2 2 4
分解NH Cl反应。每分解20 mol NH Cl,需要196 L CH (已折算为标况)。忽略温度对化学反应焓变的影
4 4 4
响,该化学链的热量利用率为___________。