文档内容
微专题突破4 物质结构与性质
不经历风雨,怎能见彩虹,没有人能随随便便成功。
目标定位
1.能正确书写有关微粒的排布式、配离子的结构式。
2.能判断电离能、电负性、熔沸点的大小或强弱关系,判断所给微粒中的化学键类型与σ、π键数目。
3.能判断晶体的类型与微粒的作用力类型,会用有关原理解释有关物质性质的差异。
4.能应用杂化轨道理论与价层电子对互斥模型判断有关微粒的空间构型,能据等电子原理写出粒子电子式。
教学重点难点
1.分子结构与性质原因解释。
2.微粒的空间构型。
教学方法
讨论、归纳
教学过程
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
1.共价键的类型
共价键 举例 说明
①相同原子之间形成的共价键不一定是非极性键,如
单键(σ键)
O 中的共价键是非极性键,O 中的共价键是极性键;不同
2 3
原子之间形成的共价键是极性键。
双键 ②分子中的大π键可用符号Π表示,其中m代表参与
(1个σ键、1个π键) 形成大π键的原子数,n代表参与形成大π键的电子数(如
σ键 苯分子中的大π键可表示为Π)。
π键 三键 ③配位键也是共价键,属于σ键。
—C≡C—
(1个σ键、2个π键) a. 配合物举例。
大π键
①配合物的组成。 冰晶石 氢化铝锂
以[Cu(NH )](OH) 为例:
3 4 2
硼氢化钠 Al Cl(AlCl 二聚体)
2 6 3
注:冰晶石——六氟合铝酸钠(工业上用于电解制铝,可
配位键 一般来说,配合物内界与外界之间为 以降低氧化铝的熔融温度);AlCl 3 是共价化合物。
离子键,电荷相互抵消。 b. 含有特殊配体——π 键配位体[CO、环戊二烯基(—
②配体可能有多个配位原子,与中心 C H)等]的配合物举例。
5 5
原子形成螯合物。
以铜离子与乙二胺形成的配离子为
例:
四羰基镍 二茂铁 金属EDTA螯合物
2.判断中心原子杂化类型的“四方法”
(1)根据中心原子的价电子对数判断
中心原子价电子对数 2 3 4微专题突破4 物质结构与性质 问题的态度:问则少;辩则明
杂化类型 sp sp2 sp3
(2)根据分子的结构式判断(一般用于有机物分子中C、N的杂化类型判断)
杂化类型 sp3 sp2 sp
C的成键方式 4个单键 1个双键和2个单键 2个双键或1个三键和1个单键
N的成键方式 3个单键 1个双键和1个单键 1个三键
(3)根据键角判断
若键角为109°28'或接近109°28',则为sp3杂化;若键角为120°或接近120°,则为sp2杂化;若键角为
180°,则为sp杂化。
(4)根据杂化轨道的空间结构判断
①若杂化轨道在空间的分布为四面体形,则分子的中心原子发生sp3杂化。
②若杂化轨道在空间的分布呈平面三角形,则分子的中心原子发生sp2杂化。
③若杂化轨道在空间的分布呈直线形,则分子的中心原子发生sp杂化。
3.等电子体的判断方法
把同族元素原子(同族原子 以寻找NH 的等电子体为例:
竖换 3
价电子数相同)上下交换 NH 把N原\s\up 4()PH 、AsH
3子换成 3 3
换相邻族的原子,这时价 以寻找CO的等电子体为例:
横换 电子发生变化,再通过得 CO把O原少了1CN- CN-把N原少了1C 2-
子换成个电子 子换成个电子 2
失电子使价电子总数相等 CO把C原把O原N
子换成子换成 2
4.审题与答题
看清题目的要求,如“从大到小”还是“从小到大”、“外围/价电子排布式”还是“电子排
审题
布式”(是原子还是离子)、“电负性”还是“电离能”、“结构式”还是“结构简式”或“空
注意点
间构型”等。
①注意同周期中,第一电离能电离能有反常现象,而电负性没有反常现象。
答题 ②离子核外电子排布式书写时,要先写出原子电子排布式再按由外到里失去电子。
注意点 ③陌生离子或分子空间构型的判断:一是根据中心原子杂化轨道类型判断;二是通过等电子
体,转换成熟悉的物质,再判断。
考考考考考
1.(2024·江苏卷)我国探月工程取得重大进展。月壤中含有Ca、Fe等元素的磷酸盐,下列元素位于元
素周期表第二周期的是
A.O B.P C.Ca D.Fe
【答案】A
【解析】A项,O元素位于元素周期表第二周期ⅥA,符合题意;B项,P元素位于元素周期表第三周期
ⅤA,不符合题意;C项,Ca元素位于元素周期表第四周期ⅡA,不符合题意;D项,Fe元素位于元素周期表
第四周期Ⅷ族,不符合题意。
2.(2024·江苏卷)明矾[KAl(SO )•12HO]可用作净水剂。下列说法正确的是
4 2 2
A.半径:r(Al3+)>r(K+) B.电负性:χ(O)>χ(S)
C.沸点:HS>HO D.碱性:Al(OH)>KOH
2 2 3
【答案】B
【解析】A项,Al3+有2个电子层,而K+有3个电子层,因此,K+的半径较大,错误;B项,同一主族的
元素,其电负性从上到下依次减小,O和S都是ⅥA的元素,O元素的电负性较大,正确;C项,虽然HS的
2
相对分子质量较大,但是HO分子间可形成氢键,因此HO的沸点较高,错误;D项,元素的金属性越强,其
2 2
最高价的氧化物的水化物的碱性越强,K的金属性强于Al,因此KOH的碱性较强,错误。
3.(2024·江苏卷)下列有关反应描述正确的是
A.CHCHOH催化氧化为CHCHO,CHCHOH断裂C-O键
3 2 3 3 2
B.氟氯烃破坏臭氧层,氟氯烃产生的氯自由基改变O 分解的历程
3
C.丁烷催化裂化为乙烷和乙烯,丁烷断裂σ键和π键
D.石墨转化为金刚石,碳原子轨道的杂化类型由sp3转变为sp2
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找【答案】B
【解析】A项,CHCHOH催化氧化为CHCHO,CHCHOH断裂C-H键和O-H生成C=O,错误;B
3 2 3 3 2
项,根据题意,氯自由基催化O 分解氟氯烃破坏臭氧层,则氟氯烃产生的氯自由基改变O 分解的历程,正确;
3 3
C项,丁烷催化裂化为乙烷和乙烯,丁烷断裂σ键,丁烷是饱和烷烃,没有π键,错误;D项,石墨碳原子轨
道的杂化类型为转化为sp2,金刚石碳原子轨道的杂化类型为 sp3,石墨转化为金刚石,碳原子轨道的杂化类型
由sp2转变为sp3,错误。
4.(2024·江苏卷)铁酸铋晶胞如图所示(图中有4个Fe原子位于晶胞体对角线上,O原子未画出),其
中原子数目比N(Fe)∶N(Bi)=__________。
【答案】2∶1
【解析】由铁酸铋晶胞结构示意图可知,晶胞中体内有 4个Fe原子,面上有8个Fe原子,根据均摊法可
知,Fe 原子的数目为 4×1+8×=8;Bi 原子全部在晶胞的面上,共有 8×=4,因此,其中原子数目比
N(Fe)∶N(Bi)=2∶1。
【问题解决1】
1.请完成下表内容(⑤~⑧判正误并改正):
① Ti电子排布式 1s22s22p63s23p63d24s2 ⑤ Cu电子排布式:[Ar]3d94s2 错
② Co价电子排布式 3d74s2 ⑥ Ga电子排布式:[Ar]4s24p1 错
③ Ni2+电子排布式 1s22s22p63s23p63d8 ⑦ Fe2+价电子排布式:3d44s2 错
④ Mn2+电子排布式 1s22s22p63s23p63d5 ⑧ Cr价电子排布式:3d44s2 错
2.(2024·南通市二模)NH Al(SO )•12HO可用作净水剂、媒染剂等。下列说法正确的是
4 4 2 2
A.电负性:χ(N)>χ(O) B.原子半径:r(Al)>r(N)
C.第一电离能:I(S)>I(O) D.热稳定性:HS(g)>HO(g)
1 1 2 2
【答案】B
【解析】A项,同周期元素,从左到右元素的非金属性依次增强,电负性依次增大,则 N元素的电负性小
干O元素,错误;B项,一般电子层数越多半径越大,则半径Al>N,正确;C项,同主族自上而下第一电离
能减小,因此O的第一电离能大于S,错误;D项,同主族元素,从上到下元素的非金属性依次减弱,简单氢
化物的稳定性越弱,则热稳定性HS(g)<HO(g),错误。
2 2
原子结构与元素性质
化学式 最简式(实验式)、电子式、分子式、结构式、结构简式
原子或离子 结构示意图、电子排布式、价/外围电子排布式、轨道表示式(通常不考)
判断同周期元素的第一电离能时,注意两个主族:______Ⅱ A 族的第一电离能大于
第一电离能 ______ⅢA族、______ⅤA族的第一电离能大于______ⅦA族。
即电离能的几组特殊性:Be>B、N>O、Mg>Al、P>S
①在书写过渡元素电子排布式时,应先写(n-1)d亚层,后写ns亚层。
②过渡元素失电子生成离子时,先失ns亚层上的电子,再失(n-1)d亚层上的电子。即离
温馨提醒
子的核外外电子排布式都是由外向内失电子。
③Ga以后的原子3d轨道上排满了10个电子。
考点精练
1.(2024·江苏镇江市高三开学考)实验室可由Ca(OH) 与NH Cl反应制备NH 。下列说法正确的是
2 4 3
A.半径大小:r(Ca2+)<r(Cl-) B.电负性大小χ(O)<χ(H)
C.电离能大小:I(N)<I(O) D.键角大小:NH<NH
1 1 3微专题突破4 物质结构与性质 问题的态度:问则少;辩则明
【答案】A
【解析】A项,电子层结构相同的离子,核电荷数越大,离子半径越小,则氯离子的离子半径大于钙离子,
正确;B项,元素的非金属性越强,电负性越大,氧元素的非金属性强于氢元素,电负性大于氢元素,错误;C
项,同周期元素,从左到右第一电离能呈增大趋势,氮原子的 2p轨道为稳定的半充满结构,元素的第一电离能
大于相邻元素,则氮元素的第一电离能大于氧元素,错误;D项,孤对电子对数越多,对成键电子对的斥力越
大,键角越小,铵根离子和氨分子的孤对电子对数分别为0和1,则铵根离子的键角大于氨分子,错误。
2(2024·江苏南通市高三上学期期中)m、n、p、q、w五种元素,其核电荷数依次增大。m元素基态原
子核外只有三个能级,且各能级电子数相等,p、q元素位于同一族,且两者核电荷数之和为24,w元素原子核
外有4个能层,最外层只有1个电子,其余各层均排满电子。下列说法错误的是
A.m、n、p元素的第一电离能依次增大
B.n元素基态原子的轨道表示式:
C.w元素原子的价电子排布式为3d104s1
D.w单质分别与p、q单质反应,产物中w的化合价不同
【答案】A
【解析】m、n、p、q、w五种元素,其核电荷数依次增大。m元素基态原子核外只有三个能级,且各能级
电子数相等,则原子核外电子排布式为 1s22s22p2,故m为C元素;w元素原子核外有4个能层,最外层只有1
个电子,其余各层均排满电子,原子核外电子数为 2+8+18+1=29,故w为Cu;p、q元素位于同一族,它们
的原子序数大于碳而小于Cu,只能处于第二、三周期、第三、四或第二、四周期,且两者核电荷数之和为24,
可推知p为O元素、q为S元素;n的原子序数介于C、O之间,故n为N元素。综合以上分析,m、n、p、q、
w分别为C、N、O、S、Cu元素,据此分析解答。
A项,同周期元素随原子序数增大,第一电离能呈增大趋势,但N元素原子2p轨道为半充满状态,第一电
离能高于同周期相邻元素,故第一电离能C(m)<O(p)<N(n),错误;B项,n为N,核外电子数为7,基态原
子的轨道表示式: ,正确;C项,w为Cu,是29号元素,处于第四周期第IB族,属于过渡元
素,价电子包括3d、4s电子,w元素原子的价电子排布式为3d104s1,正确;D项,Cu单质与氧气反应生成
CuO,与硫单质反应生成Cu S,产物中Cu元素化合价分别为+2价、+1价,正确。
2
3.(2024·江苏南通市高三上学期期中)下列选项中,所叙述的粒子按半径由大到小排列时,顺序正确的
是
①基态X的原子结构示意图为
②基态Y原子的价电子排布式为3s23p5
③基态Z2-的轨道表示式为
④基态T原子有2个电子层,电子式为·T·
A.①>②>③>④ B.③>④>①>②
C.③>①>②>④ D.①>②>④>③
【答案】C
【解析】①基态X的原子结构示意图为 ,X为S原子;②基态Y原子的价电子排布式为3s23p5,Y
为Cl原子;③基态Z2-的轨道表示式为 ,Z2-原子为S2-;④基态T原子有2个电
子层,电子式为·T·,T为O原子;电子层数越多半径越大,电子层数相同,质子数越多半径越小,S、S2-的
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找电子层数相同、质子数相等,S2-的电子数多,S原子的半径小于S2-,所以半径由大到小排列顺序为③(S2-)>
①(S)>②(Cl)>④(O),故选C项。
【问题解决2】
1.如何判断一个微粒中,σ、π的数目?请完成下表:
① (2024江苏省淮安市5校联考)1 mol [Cu(NH )]2⁺中含有4 mol σ键 错
3 4
② (2023·江苏扬州扬州中学校考模拟预测)1 mol [Fe(HO)]2+含有σ键数目为12 mol 错
2 6
③ (2023·江苏连云港高中校考模拟预测)1 mol NaCO 中含有3 mol 键 对
2 3
④
(2023·江苏南京统考模拟预测)Ag(CN)2-中σ键与π键的个数比为1∶2
错
σ
⑤ 1 mol吡咯( )中σ键数目为10N 对
A
⑥ (2024·江苏盐城市高三期中)1个CHCHOH分子中含有7个σ键 错
3 2
【解析】①1 mol [Cu(NH )]2⁺中含有4 mol Cu-N σ键和12 mol N-H σ键,即共16 mol σ键,错误;
3 4
②1 mol [Fe(HO)]2+含有σ键数目为(6+2×6)N =18N ,错误;③1个碳酸根离子中存在3个σ键,则1
2 6 A A
mol NaCO 中含有3 mol 键,正确;④Ag(CN)2-的结构式为 ,则一个Ag(CN)2-中由4
2 3
个σ键和4个π键,故σ键与π键的个数比为1∶1,错误;⑤吡咯分子中含有1个N—H σ键、4个C—H σ键、
σ
3个C—C σ键、2个C—N σ键,故1 mol吡咯含有10 mol σ键,正确;⑥根据CHCHOH结构可知1个分子中
3 2
含8个σ键,错误。
2.(2023·苏州上学期期末)Al(OH) 胶体中,两分子Al(OH) 以配位键聚合成含四元环的二聚分子。该
3 3
二聚分子结构式为_____________________________。
【答案】
【解析】Al(OH) 胶体中,两分子Al(OH) 以配位键聚合成含四元环的二聚分子,该二聚分子结构式为
3 3
,故答案为 。
化学键与配合物
1.化学键判断
①画出结构式,单键全是σ键,双键中一个是σ键一个是π键,三键一个是σ键二个是π键。
②陌生微粒,根据等电子原理判断,如CO与N 互为等电子体,含1个σ键、2个π键。
2
2.部分原子的常见成键数目
原子 键数 举例 原子 键数 举例
H、F、Cl 1 —H、—F、—Cl C、Si 4 —C≡C—
N 3或4 N≡ O 2 —O—、 、O=C=O
2或4
P 3或5 S —O—
或6
B 3或4 Be 2 —Be—
3.配合物
配合物的形成 由提供孤电子对的分子或离子与接受孤电子对的原子或离子以配位键结合形成的化合微专题突破4 物质结构与性质 问题的态度:问则少;辩则明
物。配位键本质上属于共价键
配合物所含化学键 配位键和离子键或配位键;配体或外界中可能还含有共价键
配合物的常见性质 多数能溶解、能电离、有颜色
配位体有多个
多
配位原子,与
齿
中心原子形成
配合物的组成 配
螯合物。如铜
位
离子与乙二胺
体
形成的配离子
典型配合物 [Cu(NH )]SO K[Fe(CN)] [Ag(NH )]OH NaAlF
3 4 4 3 6 3 2 3 6
中心原子 Cu2+ Fe3+ Ag+ Al3+
中心原子结构特点 一般是金属原子或离子,特别是过渡金属原子或离子,必须有空轨道
配位体 NH CN- NH F-
3 3
配位原子 N C N F
配位体结构特点 分子或离子,必须含有孤电子对
配位数 4 6 2 6
外界 SO 2- K+ OH- Na+
4
画结构式 注意配位键中原子的连接顺序
考点精练
1.判断正误:
① (2024·江苏泰州模拟预测)NH 和NH都可做配体 错
2 4
② (2021·江苏)NH 与Ag+形成的[Ag(NH )]+中有6个配位键 错
3 3 2
(2023·浙江1月选考)共价化合物Al Cl 中所有原子均满足8电子稳定结构,Al Cl 的结构式
2 6 2 6
③ 对
为
④ 丁二酮肟镍( )该分子内微粒之间存在的作用力有共价键、配位键、离子键、氢键 错
⑤ (2024·苏锡常镇二模)SO2-( )中两个S原子均可作配位原子 错
2 3
【解析】①NH 中2个N原子的最外层都存在1个孤电子对,而NH的中心N原子的最外层不存在孤电子
2 4
对,所以NH 能做配体,但NH不能做配体,不正确;②[Ag(NH )]+中含有2个配位键,错误;③由双聚氯
2 4 3 2
化铝分子中所有原子均满足8电子稳定结构可知,分子的结构式为 ,是结构对称的非极性分子,
正确;④该分子不是离子化合物,不含离子键,错误;⑤具有孤电子对的原子可以给中心原子提供电子配位,
SO2-中的中心原子S的价层电子对数为4,无孤电子对,不能做配位原子,端基S原子含有孤电子对,能做配
2 3
位原子,错误。
2.(2024·江苏南京市盐城市一模)碲广泛应用于冶金工业。以碲铜废料(主要含Cu Te)为原料回收碲
2
单质的一种工艺流程如下:
“沉铜”时NaC O 过多会导致Cu2+与C O2-生成环状结构的配离子[Cu(C O)]2-,该配离子的结构式为
2 2 4 2 4 2 4 2
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找___________________________(不考虑立体异构)。
【答案】
【解析】在环状结构的配离子[Cu(C O)]2−中,C O2-的碳氧单键中的O给出孤电子对,Cu2+接受电子对,
2 4 2 2 4
以4个配位键形成[Cu(C O)]2−,则该配离子的结构式为: 。
2 4 2
2.用锌还原TiCl 的盐酸溶液,经后续处理可制得绿色的配合物[TiCl(HO)]Cl·HO。1 mol该配合物中
4 2 5 2 2
含有σ键的数目为_______N 。
A
【答案】18
【解析】该配合物的配位离子中有6个配位σ键、10个O—H σ键,结晶水中又有2个O—H σ键,故共含
18个σ键,即1 mol该配合物中含有σ键的数目为18×6.02×1023个。
3.是一种配合物,其结构如右图所示。在XCl·2CO·2HO中,每个X原子能与
2 2 2
其他原子形成3个配位键,在图中用“→”标出相应的配位键。该配合物中氯原子的杂化
方式为______________。
【答案】 sp3杂化
【解析】该配合物的氯原子只有单键,成对电子对数有4对,故氯原子是sp3杂化。
【问题解决3】
1.如何判断一个微粒中,原子的杂化类型?
微粒 (CH)Ga NO - NH HClO HO+ CN- B(OH) C HOC H
3 3 2 2 4 3 3 2 5 2 5
杂化类型 Ga:sp2 N:sp2 N:sp3 O:sp3 O:sp3 C:sp B:sp2 O:sp3
2.AlCl 在下述反应中作催化剂。分子③中碳原子的杂化类型为________。sp2杂化、sp3杂化
3
3.判断是否正确:(2024·苏锡常镇二模)ClO2-、ClO -和ClO -中O-Cl-O键角依次逐渐减小。
3 4
【答案】错误
【解析】ClO2-的中心原子Cl的价层电子对数为2+=4,为sp3杂化,含有2对孤电子对;ClO -的中心原
3
子Cl的价层电子对数为3+=4,为sp3杂化,含有1对孤电子对;ClO -的中心原子Cl的价层电子对数为4+=
4
4,为sp3杂化,无孤电子对;杂化类型相同时,由于孤电子对对成键电子对之间的排斥力大于成键与成键电子
的排斥力,因此孤电子对数越多键角越小,所以ClO2-、ClO -和ClO -中O-Cl-O键角依次逐渐增大,错误。
3 4
杂化类型与分子空间构型
1.杂化轨道
sp3杂化 sp2杂化 sp杂化
类型 全为单键:C、N、O 苯环、>C=、单键的B —C≡、=C=、Be
微粒 CHCHOH、HNNH、NH OH 、HCHO、BCl C H、CS、BeCl
3 2 2 2 2 3 2 2 2 2
孤电子对+单键数=4 孤电子对+单键数=3 孤电子对+单键数=2
判断 杂化轨道类数=孤电子对+单键数 杂化轨道数=中心原子的孤电子对数+相连的其他原子个数
根据熟悉物质的原子杂化类型等效替换—→用熟悉的原子替换、用熟悉的分子替换
2.价层电子对互斥模型
AX:价层电子对数=A原子σ键数(即m)+孤电子对数
孤电子对数=微专题突破4 物质结构与性质 问题的态度:问则少;辩则明
3.利用价层电子对互斥模型比较键角的方法
序号 比较方法 具体规律
比较中心原子价层 中心原子价层电子对数越少,键角越大
①
电子对数 如CO>SO >CH
2 3 4
中心原子价层电子对数相同时,孤电子对数越多,排斥力越大,键角越
比较中心原子的孤
② 小
电子对数
如NH >HO
3 2
同主族元素形成的同类化合物,中心原子的电负性越大,键角越大
③ 比较中心原子的电负性
如HO>HS
2 2
④ 比较成键原子的电负性 当中心原子相同时,成键原子的电负性越大,键角越小,如NF <NCl
3 3
考点精练
1.判断说法是否正确。
① (2024·江苏盐城市高三期中)CO 和CO2-中心原子轨道杂化类型均为sp 错
2 3
② (2024·江苏省南通市、盐城市二模)SeO 分子中O-Se-O的键角大于120° 错
2
③ (2024·淮安市高三上学期开学考)SO 与CO中键角都为180° 错
2
④ (2024·连云港上学期调研一)NH 分子中N原子轨道的杂化方式为sp2 错
2 4
⑤ (2023·苏州上学期期末)PO 3-原子轨道的杂化类型为sp3 对
4
⑥ (2024·江苏泰州中学、宿迁中学、宜兴中学调研测试)HO的VSEPR模型名称:直线形 错
2
⑦ (2024·江苏南通第二次调研测试)NO2-和NO -中N原子均采取sp2杂化 对
3
⑧ (2024·江苏苏州市名校高三大联考)PCl 和[PBr ]+中磷原子的杂化方式相同 对
3 4
【解析】①CO 中心原子碳原子价层电子对数为2,杂化类型sp杂化;CO2-中心原子碳原子价层电子对数:
2 3
3+=3,杂化类型为sp2杂化,错误;②SeO 分子中Se是sp2杂化,Se原子价层电子对数为2+=3,有一对孤
2
电子对,对两个成键电子对有排斥作用,O-Se-O的键角小于120°,错误;③SO 中S原子上的孤电子对数为
2
=1,σ键电子对数为2,价层电子对数为3,VSEPR模型为平面三角形,由于有1对孤电子对,SO 的空间构型
2
为V形,由于孤电子对有较大的斥力,SO 的键角小于120°,错误;④NH 分子中N原子轨道的杂化方式为
2 2 4
sp3,错误;⑤PO 3-价层电子对数为4+=4,原子轨道杂化类型为sp3,正确;⑥HO的价层电子对数是4,
4 2
VSEPR模型名称:四面体形,,错误;⑦NO中氮原子价电子数为2+=3,NO中氮原子价电子数为3+=3,均
为sp2杂化,正确;⑧PCl 分子的中心原子(P)的价层电子对数=3+=4,中心原子(P)采取sp3杂化,[PBr ]+的
3 4
中心原子(P)的价层电子对数=4+=4,中心原子(P)采取sp3杂化,二者磷原子的杂化方式相同,正确。
2.(2024·南通市海门市第一次调研)周期表中VIA族元素及其化合物应用广泛。 O、 O、 O是氧元素
186 187 188
的3种核素,可以形成多种重要的化合物。亚硫酰氯(SOCl )为黄色液体,其结构式为( ),遇水发生
2
水解。工业上可电解HSO 与(NH )SO 混合溶液制备过二硫酸铵[(NH )SO],过二硫酸铵与双氧水中都含有
2 4 4 2 4 4 2 2 8
过氧键(-O-O-)。硝化法制硫酸的主要反应为:NO (g)+SO (g)=SO (g)+NO(g) ∆H=+41.8 kJ·mol-
2 2 3
1。SO 和SO 都是酸性氧化物,是制备硫酸的中间产物。下列说法正确的是
2 3
A. O、 O、 O具有相同的中子数
186 187 188
B.亚硫酰氯空间构型为平面三角形
C.SO 、SO 的中心原子轨道杂化类型均为sp2
2 3
D.SO 晶体中存在S和O 之间的强烈作用
2 2
【答案】C
【解析】A项, O中子数为16-8=8、的中子数为17-8=9、 O的中子数为18-8=10,错误;B项,
186 187 188
亚硫酰氯S为sp3杂化,空间构型属于三角锥形,错误;C项,SO 中σ键为2,S的孤电子对为=1,SO 中σ键
2 3
为3,S的孤电子对为=0,中心原子轨道杂化类型均为sp2,正确;D项,SO 晶体中存在S和O之间的共价键,
2
为强烈相互作用,错误。
3.(2024·泰州市下学期一模)氟是已知元素中电负性最大、单质氧化性最强的元素,与稀有气体Xe形成
8
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找的XeF 分子是非极性分子,与其他卤素形成的卤素互化物(如ClF、ClF )具有与Cl 相似的化学性质,与氮形成
2 3 2
的NF 可与NH 反应生成NF(结构式:F-N=N-F)。自然界中,含氯矿石有萤石(CaF)、冰晶石(NaAlF)
3 3 2 2 2 3 6
等,萤石可与浓硫酸共热制取HF气体。工业上,可通过电解 的无水HF溶液(含F-和HF2-离子)制取F。
2
下列有关说法正确的
A.XeF 的空间结构为Ⅴ形 B.ClF与ClF 互为同素异形体
2 3
C.键角:NF>NH D.NF 存在顺反异构现象
3 3 2 2
【答案】D
【解析】A项,由题可知XeF 是非极性分子,故空间构型不是V形,错误;B项,ClF与ClF 是两种不同
2 3
的化合物,不是同素异形体,错误;C项,NF 和NH 分子中N原子的价层电子对数都为4,且均含有1个孤电
3 3
子对,F的电负性强于H,NF 中成键电子对更偏向于F原子,导致N上的电子云密度减小,排斥力减小,键角
3
变小,故键角:NF <NH ,错误;D项,由于氟原子只能成一个共价键,所以两个F原子一定在分子结构的两
3 3
边,而N原子处于中间N原子要形成三个共价键,所以两个N原子除了与 F原子形成一个共价键外,两个N原
子之间还有两个共价键,一个σ键和一个π键,类似于乙烯的结构,是平面型的,F原子可以同时在双键的一
侧,也可以在双键的两侧,因此NF 存在顺反异构,正确。
2 2
4.(2024·江苏南通高三下阶段练习)氰基丙烯酸乙酯是一种粘合剂的主要成分,其结构式如图1所示。
KSO(过硫酸钾)是一种强氧化剂,其中SO2-的结构式如图2所示。下列说法正确的是
2 2 8 2 8
A.1 mol氰基丙烯酸乙酯分子中含3 mol π键
B.氰基丙烯酸乙酯分子中sp3、sp2杂化的碳原子数之比为2∶3
C.KSO 中S元素的化合价为+7价
2 2 8
D.SO2-结构中“S-O-O-S”的4个原子处于同一条直线
2 8
【答案】B
【解析】A项,双键中有1个π键,三键中有2个π键,故1 mol氰基丙烯酸乙酯分子中含4 mol π键,错
误;B项,三键碳原子为sp杂化,双键碳原子为sp2杂化,饱和碳原子为sp3杂化,故氰基丙烯酸乙酯分子中
sp3、sp2杂化的碳原子数分别为2个、3个,个数比为2∶3,正确;C项,KSO 中有一个过氧键,其中两个O
2 2 8
为-1价,其余O为-2价,根据化合物元素化合价代数和为O,S为+6价,错误;D项,SO2-结构中
2 8
“S−O−O−S”的O为sp3杂化,有两对孤对电子,故4个原子不处于同一条直线,错误。
【问题解决4】
1.判断说法是否正确:
① (2024·南通市如皋2月)晶体类型一定是纯粹的,不存在过渡晶体 错
② (2024·南通市如皋2月)NH OH难溶于水 错
2
(2024·江苏南京市盐城市一模)干冰中CO 分子间的范德华力较弱,CO 具有较好的热稳定
③ 2 2 错
性
④ (2024·江苏省南通市、盐城市二模)SO 是由极性键构成的非极性分子 错
2
⑤ (2024·淮安市高三上学期开学考)H、Li、NaH晶体类型相同 错
2
⑥ (2024·连云港上学期调研一)NH 的沸点低于C H 错
2 4 2 6
⑦ (2024·南通市如皋市开学考)氯化亚砜(SOCl )属于非极性分子 错
2
⑧ (2024·扬州市高三下学期开学考)SO 易液化,SO 是极性分子,分子间作用力较大 对
2 2
【解析】①晶体类型不一定是纯粹的,存在过渡晶体,错误;②NH OH有羟基和氨基,能与水形成分子间
2
氢键,故易溶于水,错误;③干冰中CO 分子间的范德华力较弱,导致其熔沸点低,而 CO 具有较好的热稳定
2 2
性,是由分子内原子间的共价键决定的,错误;④SO 是V形结构,是由极性键构成的极性分子,错误;⑤H
2 2
为分子晶体、Li为金属晶体,NaH为离子晶体,错误;⑥NH 分子间有氢键,NH 的沸点高于C H ,错误;
2 4 2 4 2 6
⑦氯化亚砜(SOCl )分子中正负电荷重心不重合,属于极性分子,错误;⑧SO 是极性分子,相对分子质量也较
2 2
大,分子间作用力大,因此沸点高,即易液化,正确。微专题突破4 物质结构与性质 问题的态度:问则少;辩则明
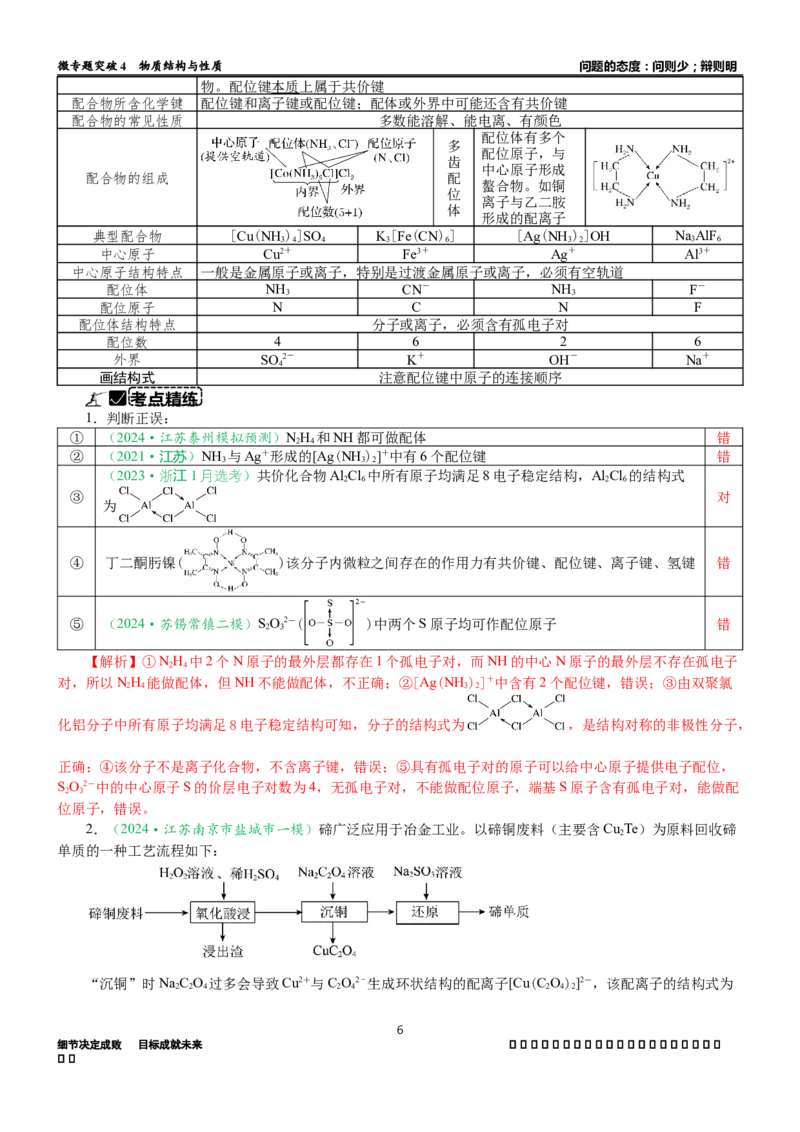
2.(2024·苏锡常镇二模)净化时生成的CaF 沉淀晶胞结构如图所示。在CaF 晶胞中F-周围距离最近的
2 2
Ca2+形成的空隙构型为_________________。
【答案】正四面体形
【解析】晶胞中以体心中的任意一个Ca2+与周围距离最近的4个F-标记后连接,形成的空隙构型为正四面
体形,故答案为:正四面体形。
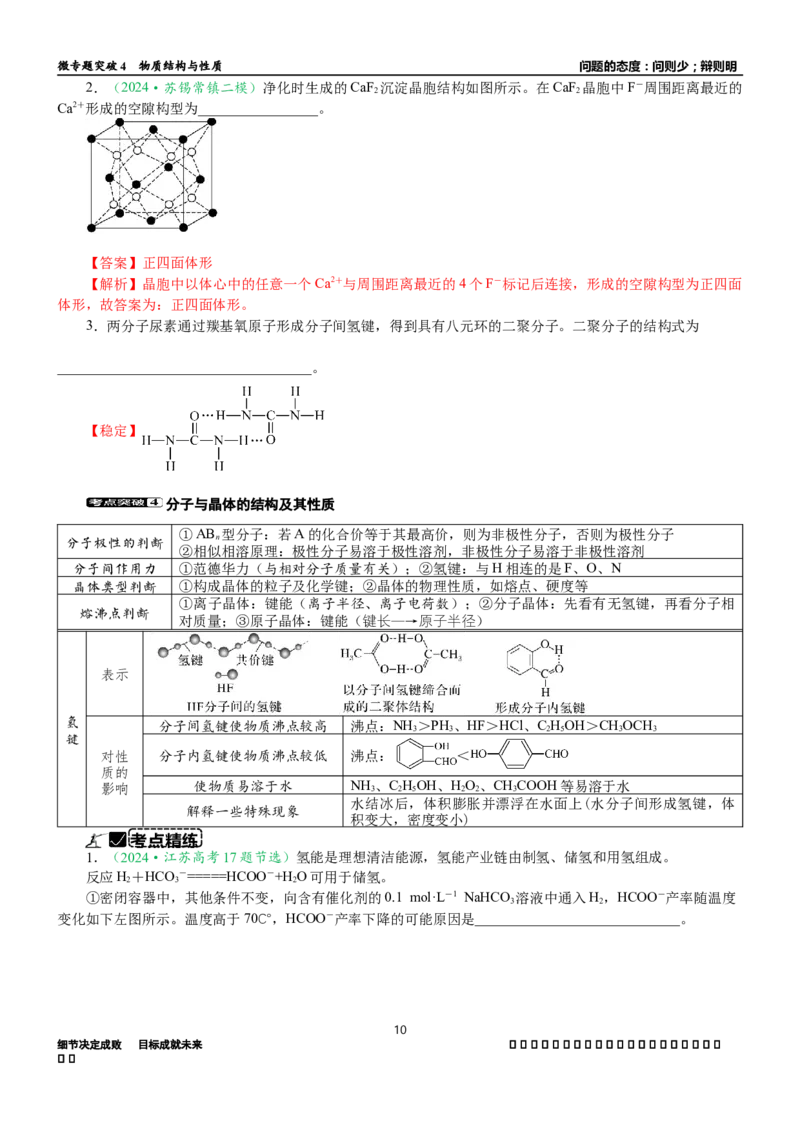
3.两分子尿素通过羰基氧原子形成分子间氢键,得到具有八元环的二聚分子。二聚分子的结构式为
____________________________________。
【稳定】
分子与晶体的结构及其性质
①AB 型分子:若A的化合价等于其最高价,则为非极性分子,否则为极性分子
分子极性的判断 n
②相似相溶原理:极性分子易溶于极性溶剂,非极性分子易溶于非极性溶剂
分子间作用力 ①范德华力(与相对分子质量有关);②氢键:与H相连的是F、O、N
晶体类型判断 ①构成晶体的粒子及化学键;②晶体的物理性质,如熔点、硬度等
①离子晶体:键能(离子半径、离子电荷数);②分子晶体:先看有无氢键,再看分子相
熔沸点判断
对质量;③原子晶体:键能(键长—→原子半径)
表示
氢 分子间氢键使物质沸点较高 沸点:NH >PH 、HF>HCl、C HOH>CHOCH
3 3 2 5 3 3
键
对性 分子内氢键使物质沸点较低 沸点: <
质的
影响 使物质易溶于水 NH 3 、C 2 H 5 OH、H 2 O 2 、CH 3 COOH等易溶于水
水结冰后,体积膨胀并漂浮在水面上(水分子间形成氢键,体
解释一些特殊现象
积变大,密度变小)
考点精练
1.(2024·江苏高考17题节选)氢能是理想清洁能源,氢能产业链由制氢、储氢和用氢组成。
反应H+HCO -=====HCOO-+H O可用于储氢。
2 3 2
①密闭容器中,其他条件不变,向含有催化剂的0.1 mol·L-1 NaHCO 溶液中通入H,HCOO-产率随温度
3 2
变化如下左图所示。温度高于70℃,HCOO-产率下降的可能原因是_____________________________。
10
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找②使用含氨基物质(化学式为CN-NH ,CN是一种碳衍生材料)联合Pd-Au催化剂储氢,可能机理如上右图
2
所示。氨基能将HCO -控制在催化剂表面,其原理是_______________________________;用重氢气(D)代替
3 2
H,通过检测是否存在_____________(填化学式)确认反应过程中的加氢方式。
2
【答案】① NaHCO 受热分解,导致 HCOO-产率下降 ②-NH 可以与 HCO -形成氢键 N-H…O
3 2 3
③DCOOH-和-NHD
【解析】①NaHCO 受热易分解,导致HCOO-产率下降。②氨基中的H原子连在电负性较大的N原子上,
3
HCO -中的H原子连在电负性较大的O原子上,二者之间可以形成氢键N-H…O;看图分析反应机理,氨基和
3
HCO -形成氢键,将HCO -控制在催化剂表面,再反应生成HO和酰胺基,H 形成H原子再与酰胺基形成甲酸
3 3 2 2
根离子和氨基,故可通过检测是否存在DCOOH-和-NHD来确认加氢方式。
2.(2023·江苏南京市高三学期调研)氧及其化合物具有广泛用途。O 是常用的氧化剂,C H 的燃烧热
2 2 2
为1 299.6 kJ·mol-1,氧炔焰产生的高温可用于焊接金属。O 可用于水处理,pH约为8时,O 可与CN-反应
3 3
生成HCO -、N 和O。C H18OH可用于研究酯化反应的机理。CaO可用于烟气(含N、O、CO、SO 等)脱硫。
3 2 2 2 5 2 2 2 2
HO 是一种绿色氧化剂,电解NH HSO 饱和溶液产生的(NH )SO 经水解可制得HO。下列物质结构与性质
2 2 4 4 4 2 2 8 2 2
或物质性质与用途具有对应关系的是
A.N 分子中含共价三键,N 的沸点比O 的低
2 2 2
B.HO 分子之间形成氢键,可与水任意比例互溶
2 2
C.O 具有氧化性,可作为燃料电池的氧化剂
2
D.O 的溶解度比O 大,可用于饮用水消毒杀菌
3 2
【答案】C
【解析】A项,N 相对分子质量大于O ,即N 范德华力大于O ,所以N 的沸点比O 的高,错误;B项,
2 2 2 2 2 2
HO 可与水任意比例互溶,是因为HO 与水分子间形成氢键,错误;C项,O 具有氧化性,可作为燃料电池的
2 2 2 2 2
氧化剂,正确;D项,O 可用于饮用水消毒杀菌是因为其具有氧化性,与溶解性无关,错误。
3
3.(2024·江苏南通高三下阶段练习)H与O可以形成HO和HO 两种化合物,其中HO 的结构如图所
2 2 2 2 2
示。H+可与HO形成HO+。下列说法正确的是
2 3
A.HO 分子中O原子采用sp杂化
2 2
B.相同条件下HO 在CCl 中的溶解度大于在水中的溶解度
2 2 4
C.液态水中的作用力由强到弱的顺序是:氢键>O—H>范德华力
D.HO+的空间结构为三角锥形
3
【答案】D
【解析】A项,HO 分子中O原子形成2个σ键且有2个孤电子对,价层电子对数为4,采用sp3杂化,错
2 2
误;B项,HO、HO都属于极性分子,CCl 属于非极性分子,根据相似相溶原理,及HO 与HO分子间能形
2 2 2 4 2 2 2
成氢键,HO 在水中的溶解度大于在CCl 中的溶解度,错误;C项,液态水中的作用力由强到弱的顺序是:O
2 2 4
-H>氢键>范德华力,错误;D项,HO+中O原子采用sp3杂化,空间结构为三角锥形,正确。
3
4.在下列反应生成的配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4)。微专题突破4 物质结构与性质 问题的态度:问则少;辩则明
Ni2++ —→ +2H+
【答案】
【问题解决5】
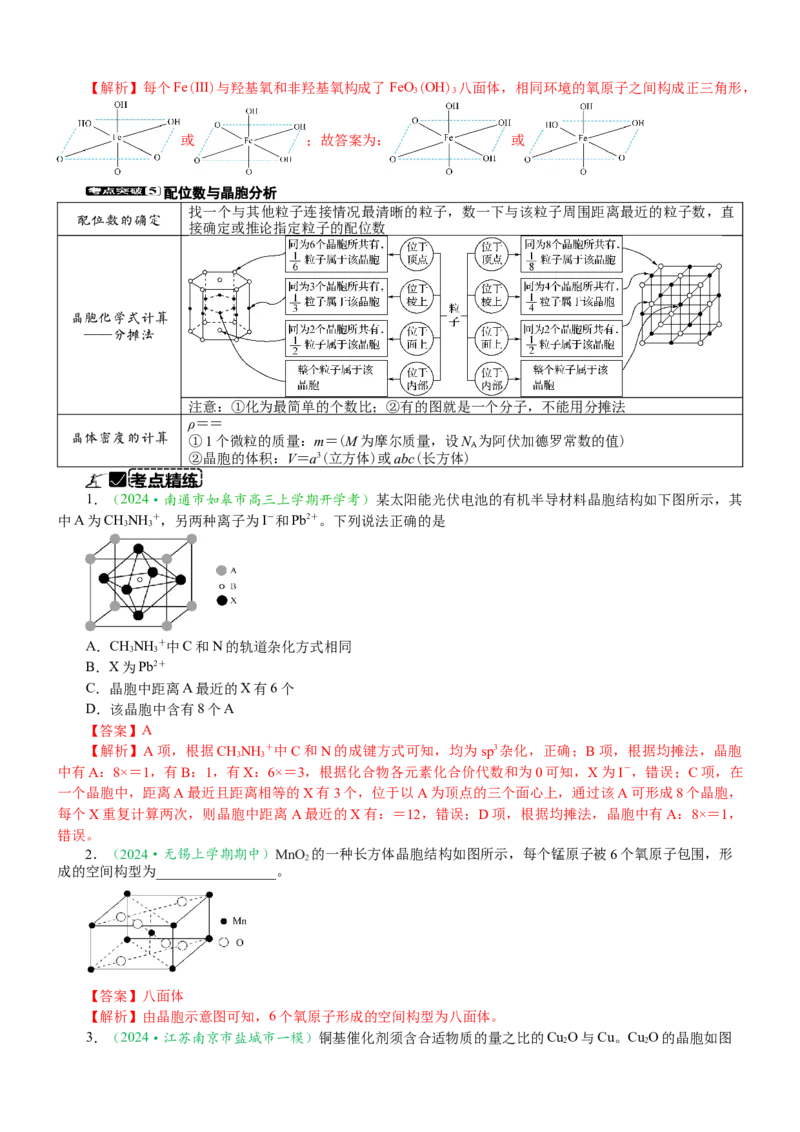
1.(2024·徐州上学期期中)FeS 晶胞如图所示,阴、阳离子的个数比为___________。
2
【答案】1∶1
【解析】晶胞结构中Fe2+处于棱上和体心,晶胞中Fe2+的个数为12×+1=4,S2-处于晶胞顶点和面心,S2
2 2
-个数为8×+6×=4,阴、阳离子的个数比为1∶1。
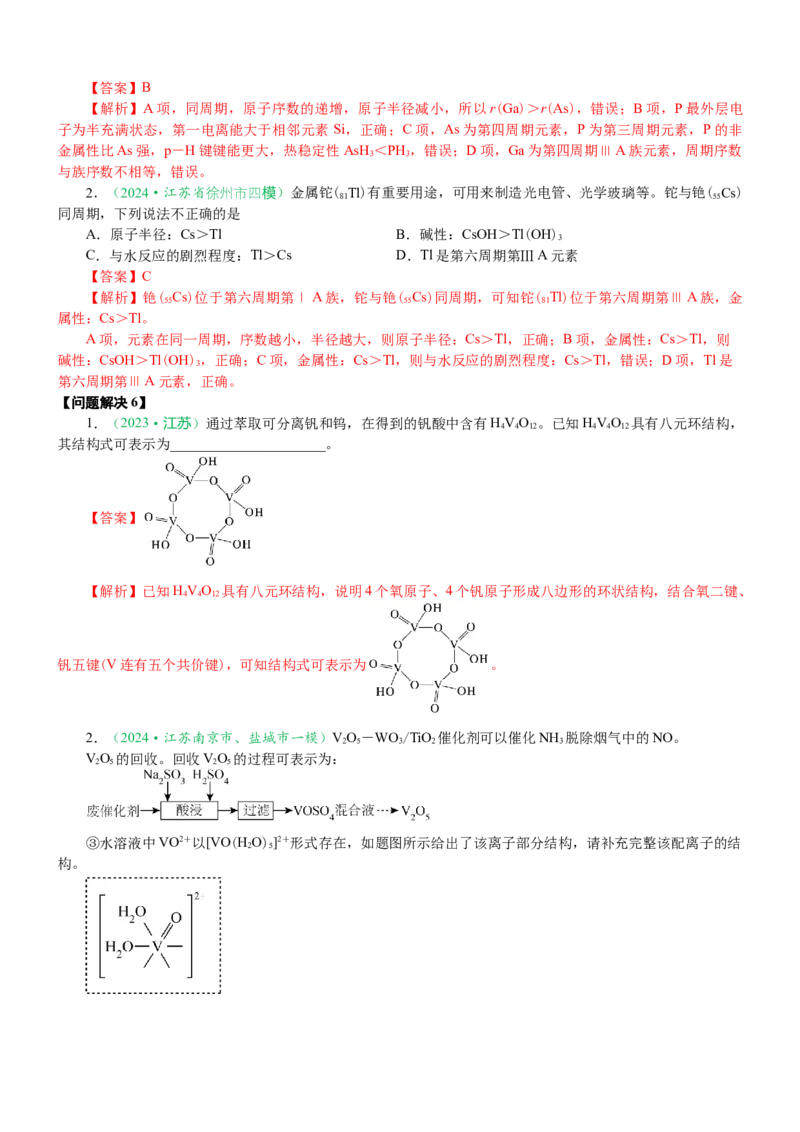
2.(2024·南京市二模)β-FeSO 的晶胞沿c轴(c轴垂直于a、b轴)方向投影的平面图如下图所示,其中
4
硫原子的杂化方式为___________;已知该晶胞中S原子的数目为4,试预测Fe2+是否占据该晶胞的所有顶点、
面心和体心,并说明理由_______________________________________________。
【答案】sp3 否,若Fe2+占据晶胞所有顶点、面心和体心,则Fe2+的数目为8×+6×+1=5个,而S原子只
有4个,不符合FeSO 的化学式
4
【解析】②在β-FeSO 的晶胞中,SO 2-中硫原子的价层电子对数为4+=4,则杂化方式为sp3;已知该晶
4 4
胞中S原子的数目为4,依据化学式,该晶胞中所含Fe2+的数目应为4。若Fe2+占据该晶胞的所有顶点、面心和
体心,则该晶胞中含Fe2+数目不是4,理由:否,若Fe2+占据晶胞所有顶点、面心和体心,则Fe2+的数目为8×
+6×+1=5个,而S原子只有4个,不符合FeSO 的化学式。
4
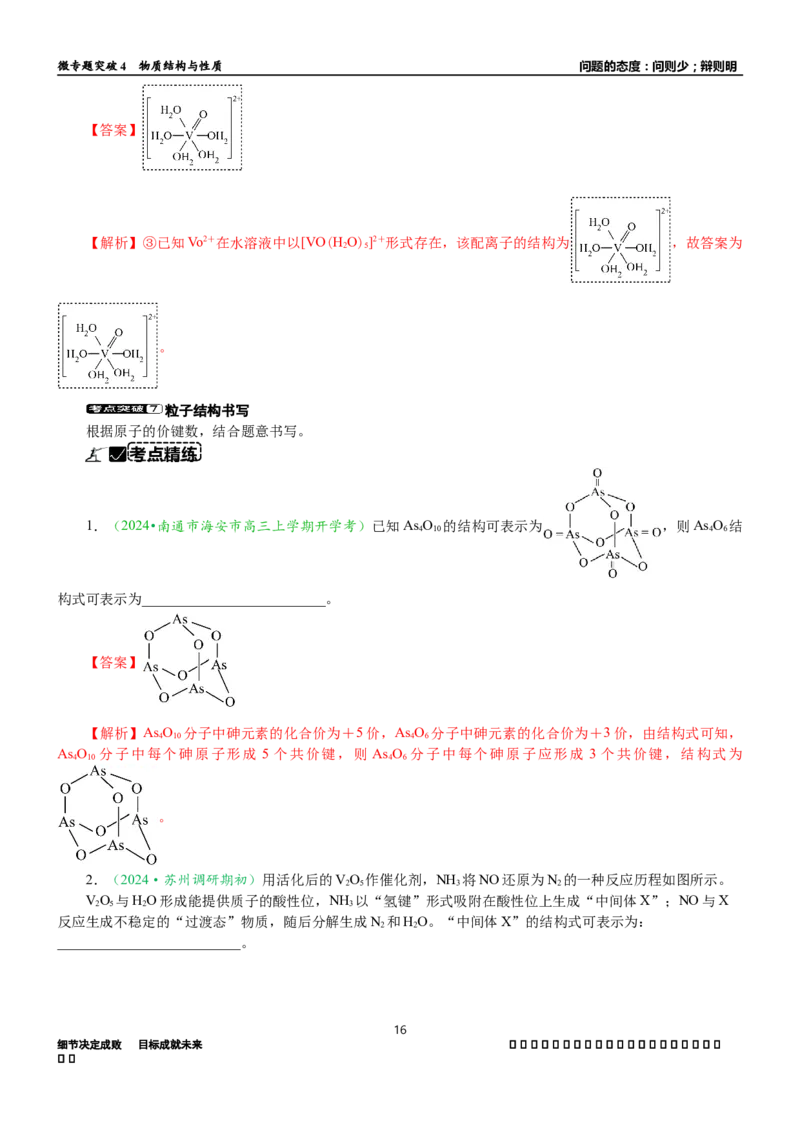
3.(2024·南通一模)α-FeOOH的结构中,每个Fe(Ⅲ)与羟基氧和非羟基氧构成了FeO(OH) 八面体,
3 3
相同环境的氧原子之间构成正三角形。补充完整该八面体的结构___________________________________。
【答案】 或
12
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找【解析】每个Fe(III)与羟基氧和非羟基氧构成了FeO(OH) 八面体,相同环境的氧原子之间构成正三角形,
3 3
或 ;故答案为: 或
配位数与晶胞分析
找一个与其他粒子连接情况最清晰的粒子,数一下与该粒子周围距离最近的粒子数,直
配位数的确定
接确定或推论指定粒子的配位数
晶胞化学式计算
——分摊法
注意:①化为最简单的个数比;②有的图就是一个分子,不能用分摊法
ρ==
晶体密度的计算 ①1个微粒的质量:m=(M为摩尔质量,设N 为阿伏加德罗常数的值)
A
②晶胞的体积:V=a3(立方体)或abc(长方体)
考点精练
1.(2024·南通市如皋市高三上学期开学考)某太阳能光伏电池的有机半导材料晶胞结构如下图所示,其
中A为CHNH +,另两种离子为I-和Pb2+。下列说法正确的是
3 3
A.CHNH +中C和N的轨道杂化方式相同
3 3
B.X为Pb2+
C.晶胞中距离A最近的X有6个
D.该晶胞中含有8个A
【答案】A
【解析】A项,根据CHNH +中C和N的成键方式可知,均为sp3杂化,正确;B项,根据均摊法,晶胞
3 3
中有A:8×=1,有B:1,有X:6×=3,根据化合物各元素化合价代数和为0可知,X为I-,错误;C项,在
一个晶胞中,距离A最近且距离相等的X有3个,位于以A为顶点的三个面心上,通过该A可形成8个晶胞,
每个X重复计算两次,则晶胞中距离A最近的X有:=12,错误;D项,根据均摊法,晶胞中有A:8×=1,
错误。
2.(2024·无锡上学期期中)MnO 的一种长方体晶胞结构如图所示,每个锰原子被6个氧原子包围,形
2
成的空间构型为_________________。
【答案】八面体
【解析】由晶胞示意图可知,6个氧原子形成的空间构型为八面体。
3.(2024·江苏南京市盐城市一模)铜基催化剂须含合适物质的量之比的Cu O与Cu。Cu O的晶胞如图
2 2微专题突破4 物质结构与性质 问题的态度:问则少;辩则明
所示(立方体),Cu O晶体的密度可表示为_________________g·cm-3(用含a、N 的代数式表示,N 表示阿
2 A A
伏加德罗常数的值)。
【答案】
【解析】①据“均摊法”,晶胞中含8×+1=2个黑球、4个白球,结合化学式可知,黑球为氧、白球为铜,
则晶体密度为 g·cm-3= g·cm-3。
【问题解决6】
(2024·江苏南京市、盐城市一模)短周期主族元素X、Y、Z、W的原子序数依次增大,X的一种核素没
有中子,基态Y原子的p轨道为半充满,Z单质是植物光合作用的产物之一,W与Z同族。下列说法正确的是
A.X位于周期表中第二周期ⅣA族
B.共价键的极性:X—Y<X—Z<X—W
C.简单气态氢化物的稳定性:W<Y<Z
D.X、Y、Z三种元素形成化合物的水溶液一定呈酸性
【答案】C
【解析】短周期主族元素X、Y、Z、W的原子序数依次增大,X的一种核素没有中子,则X为H元素;基
态Y原子的p轨道为半充满,则其轨道排布式为1s2s22p3,所以Y为N元素;Z单质是植物光合作用的产物之一,
则Z为O元素;W与Z同族,则W为S元素。
A项,由分析可知,X为H元素,则X位于周期表中第一周期ⅠA族,错误;B项,由分析可知,X为H
元素,Y为N元素,Z为O元素,W为S元素,电负性:S<N<O,则共价键的极性:H—S<H—N<H—O,
错误;C项,由分析可知,Y为N元素,Z为O元素,W为S元素,非金属性越强,其对应的简单气态氢化物
的越稳定,非金属性:S<N<O,简单气态氢化物的稳定性:HS<NH <HO,正确;D项,由分析可知,X
2 3 2
为H元素,Y为N元素,Z为O元素,X、Y、Z三种元素可形成化合物NH ·HO,其水溶液呈碱性,错误。
3 2
周期表与周期律
①知道原子结构与元素在表中位置关系
周期表 ②能书写22~36元素的电子排布式
③熟记周期表的分区
第一电离能:同周期增大趋势(注意第Ⅱ A
周期律 理解同主族、同周期元素化合物性质的递变规律
族、 第Ⅴ A 族的特殊性 )
考点精练
1.(2023·苏州上学期期末)太阳能电池可由Si、GaP、GaAs等半导体材料构成。有关元素在元素周期
表中的位置如图所示,下列说法正确的是
Si P
Ga As
A.原子半径:r(Ga)<r(As) B.第一电离能:I(Si)<I(P)
1 1
C.热稳定性:AsH>PH D.Ga的周期序数与族序数相等
3 3
14
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找【答案】B
【解析】A项,同周期,原子序数的递增,原子半径减小,所以r(Ga)>r(As),错误;B项,P最外层电
子为半充满状态,第一电离能大于相邻元素 Si,正确;C项,As为第四周期元素,P为第三周期元素,P的非
金属性比As强,p-H键键能更大,热稳定性AsH <PH ,错误;D项,Ga为第四周期ⅢA族元素,周期序数
3 3
与族序数不相等,错误。
2.(2024·江苏省徐州市四模)金属铊( Tl)有重要用途,可用来制造光电管、光学玻璃等。铊与铯( Cs)
81 55
同周期,下列说法不正确的是
A.原子半径:Cs>Tl B.碱性:CsOH>Tl(OH)
3
C.与水反应的剧烈程度:Tl>Cs D.Tl是第六周期第ⅢA元素
【答案】C
【解析】铯( Cs)位于第六周期第ⅠA族,铊与铯( Cs)同周期,可知铊( Tl)位于第六周期第ⅢA族,金
55 55 81
属性:Cs>Tl。
A项,元素在同一周期,序数越小,半径越大,则原子半径:Cs>Tl,正确;B项,金属性:Cs>Tl,则
碱性:CsOH>Tl(OH),正确;C项,金属性:Cs>Tl,则与水反应的剧烈程度:Cs>Tl,错误;D项,Tl是
3
第六周期第ⅢA元素,正确。
【问题解决6】
1.(2023·江苏)通过萃取可分离钒和钨,在得到的钒酸中含有HVO 。已知HVO 具有八元环结构,
4 4 12 4 4 12
其结构式可表示为______________________。
【答案】
【解析】已知HVO 具有八元环结构,说明4个氧原子、4个钒原子形成八边形的环状结构,结合氧二键、
4 4 12
钒五键(V连有五个共价键),可知结构式可表示为 。
2.(2024·江苏南京市、盐城市一模)VO-WO/TiO 催化剂可以催化NH 脱除烟气中的NO。
2 5 3 2 3
VO 的回收。回收VO 的过程可表示为:
2 5 2 5
③水溶液中VO2+以[VO(HO)]2+形式存在,如题图所示给出了该离子部分结构,请补充完整该配离子的结
2 5
构。微专题突破4 物质结构与性质 问题的态度:问则少;辩则明
【答案】
【解析】③已知Vo2+在水溶液中以[VO(HO)]2+形式存在,该配离子的结构为 ,故答案为
2 5
。
粒子结构书写
根据原子的价键数,结合题意书写。
考点精练
1.(2024•南通市海安市高三上学期开学考)已知As O 的结构可表示为 ,则As O 结
4 10 4 6
构式可表示为__________________________。
【答案】
【解析】As O 分子中砷元素的化合价为+5价,As O 分子中砷元素的化合价为+3价,由结构式可知,
4 10 4 6
As O 分子中每个砷原子形成 5 个共价键,则 As O 分子中每个砷原子应形成 3 个共价键,结构式为
4 10 4 6
。
2.(2024·苏州调研期初)用活化后的VO 作催化剂,NH 将NO还原为N 的一种反应历程如图所示。
2 5 3 2
VO 与HO形成能提供质子的酸性位,NH 以“氢键”形式吸附在酸性位上生成“中间体X”;NO与X
2 5 2 3
反应生成不稳定的“过渡态”物质,随后分解生成N 和HO。“中间体X”的结构式可表示为:
2 2
__________________________。
16
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找【答案】
【解析】VO 与HO形成能提供质子的酸性位,NH 以“氢键”形式吸附在酸性位上生成“中间体X”,
2 5 2 3
NO与X反应生成不稳定的“过渡态”物质,结合反应历程的图示可知,“中间体X”的结构式为
。
3.草酸的结构简式为HOOC-COOH,BFC O -具有五元环结构,B原子的轨道杂化类型为sp3,其结构
2 2 4
式可表示为______________________________。
【答案】
成功体验
1.(2024·南通市如皋2月)臭氧(O)在[Fe(HO)]2+催化下能将烟气中的SO、NO 分别氧化为SO 2-和
3 2 6 x 4
NO -。下列关于N、O、S、Fe元素及其化合物的说法正确的是
3
A.原子半径:N>O>S B.第一电离能:I(N)>I(O)>I(S)
1 1 1
C.沸点:HS>HO>NH D.电负性:χ(Fe)<χ(O)<χ(N)
2 2 3
【答案】B
【解析】A项,同主族从上到下原子半径增大,同周期从左到右原子半径减小,原子半径:S>N>O,错微专题突破4 物质结构与性质 问题的态度:问则少;辩则明
误;B项,根据第一电离能递变规律,第一电离能:I(N)>I(O)>I(S),正确;C项,HO和NH 都能形成分
1 1 1 2 3
子间氢键,但是HO中氢键更多,而HS不能形成氢键,故沸点:HO>NH >HS,错误;D项,金属电负性
2 2 2 3 2
一般小于非金属,N与O同周期,O的电负性大于N,电负性:χ(Fe)<χ(N)<χ(O),错误。
2.(2024·江苏省南通市、盐城市二模)由SiCl 制备高纯SiH 的反应为SiCl +LiAlH ======SiH↑+
4 4 4 4 4
LiCl+AlCl 。下列说法正确的是
3
A.热稳定性:HCl>SiH B.离子半径:r(Li+)>r(H-)
4
C.第一电离能:I(Al)>I(Cl) D.共价键的极性:Si-Cl>Al-Cl
1 1
【答案】A
【解析】A项,元素的非金属性Cl>Si,则简单氢化物的稳定性HCl>SiH,正确;B项,Li+和H-的电子
4
层数相同,Li的核电核数大,故半径小,即r(Li+)<r(H-),错误;C项,Al的失电子能力大于Cl,故第一电
离能I(Al)<I(Cl),错误;D项,元素电负性差值越大,共价键极性越强,Si与Cl的电负性差值小于Al,故
1 1
共价键的极性Si-Cl<Al-Cl,错误。
3.(2024·江苏南通高三下期中)CO 不仅可以和H 反应生成CHOH,还可以在电解条件下生成C H、
2 2 3 2 4
HCOOH、CH、尿素[CO(NH )]等多种物质。下列说法正确的是
4 2 2
A. CO、 CO 和 CO 属于同素异形体
162 2 163 2 164 2
B.HCOOH分子中的化学键均为极性共价键
C.CO 转化为有机物一定发生了还原反应
2
D.C H、HCOOH、CH 中碳原子的杂化轨道类型相同
2 4 4
【答案】B
【解析】A项,同素异形体是同种元素形成的结构不同单质,而 CO、 CO 和 CO 属于化合物,错误;B
162 2 163 2 164 2
项,HCOOH分子中的C-H、C-O、H-O键均为极性共价键,正确;C项,CO 中碳为+4价,有机物中的
2
碳也可以为+4价,不一定发生了还原反应,错误;D项,C H 中碳原子的杂化轨道类型sp2、HCOOH中碳原
2 4
子的杂化轨道sp2、CH 中碳原子的杂化轨道类型sp3,错误。
4
4.(2024·江苏宿迁三模)硫元素约占地球总质量的1.9%,广泛分布并循环于地球内部各圈层。硫有
32S、34S、33S和36S四种同位素。硫元素主要以氢化物、硫化物、含氧酸和含氧酸盐等形式存在。硫的单质有
S、S、S 等多种分子形态;硫的氢化物(HS、HS)均有弱酸性;低价硫易被氧气氧化。硫在生物圈的演化中
2 4 8 2 2 2
扮演了重要角色,在细菌作用下硫元素可发生氧化或还原反应,促进了硫元素在地球各圈层中的循环。下列说
法正确的是
A.32S、34S、33S、36S原子的中子数均相同
B.SO 和SO2-中S的杂化类型均为sp2
3 3
C.S、S、S 均难溶于水,易溶于CS
2 4 8 2
D.HS 分子的构型为直线形
2 2
【答案】C
【解析】A项,32S、34S、33S、36S原子的质子数均相同,中子数分别为:16、18、17、20,错误;B项,
SO 的价层电子数为:3+=3,SO2-的价层电子数为:3+=4,前者sp2杂化,后者sp3杂化,错误;C项,
3 3
S、S、S 与CS 均为非极性分子,水为极性分子,根据相似相溶可知,S、S、S 均难溶于水,易溶于CS,
2 4 8 2 2 4 8 2
正确;D项,HS 与HO 为等电子体,分子构型相似,所以HS 分子的构型为: ,错误。
2 2 2 2 2 2
5.(2024·江苏南京模拟预测)由金属钛、铝形成的Tebbe试剂常用作有机反应的烯化试剂,其结构如图
所示。下列说法正确的是
18
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找A.Al3+与Cl-具有相同的电子层结构
B.该结构中不存在配位键
C.Tebbe试剂中的Al原子轨道杂化类型为sp3
D.该结构中Al的化合价为+4
【答案】C
【解析】A项,Al3+有2个电子层、Cl-有3个电子层,不具有相同的电子层结构,错误;B项,Al提供空
轨道,Cl提供孤电子对,形成配位键,错误;C项,Al形成4个σ键,无孤电子对,为sp3杂化,正确;D项,
该结构中Al的化合价为+3,错误。