文档内容
微专题突破16 归因类问题考点透视
当你还不能对自己说今天学到了什么东西时,你就不要去睡觉。——利希顿堡
目标定位
1.认识化学变化的多样性和复杂性,能分析化学反应的主要影响因素。
2.能根据反应速率和化学平衡原理,说明影响化学反应速率和化学平衡的因素。
3.能收集并应用数据、图表等多种方式描述实验证据,能基于现象和数据进行分析推理得出合理结论。
4.能运用化学原理解释生产、生活中与化学相关的一些实际问题。
5.能从调控反应速率、提高反应转化率等方面综合分析反应的条件,提出有效控制反应条件的措施。
教学重点难点
1.速率与平衡归因分析。
2.催化剂归因分析。
教学方法
讨论、归纳
教学过程
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
1.有关多重平衡及选择性的问题
在多重平衡中,几个可逆反应是相互影响的。
①如果主反应的生成物又与主反应的某一反应物发生另一个可逆反应,那么该反应物的平衡转化率就会增
大。
②在一定温度下,特定的混合体系,多重平衡选择性为定值。因为平衡常数只与温度有关,且催化剂不能
改变某一物质的平衡转化率。
③如果在同一条件下,两个物质同时可以发生几个可逆反应,那么催化剂的选用就可以使其中某一反应的
选择性提高。
2.物质能量、能垒变化图像分析
A+B—C―→[A…B…C]―→A—B+C
备注:
(1)A+B—C―→[A…B…C]―→A—B+C
过渡态 为一种基元反应,其中正反应活化能E =b
正
-a,逆反应活化能E =b-c,ΔH=E -E 。
逆 正 逆
(2)过渡态(A…B…C)不稳定。
备注:
处于能量最高点的是反应的过渡态,在多步
中间体
反应中两个过渡态之间的是中间体,中间体很活
泼,寿命很短,但是会比过渡态更稳定些。
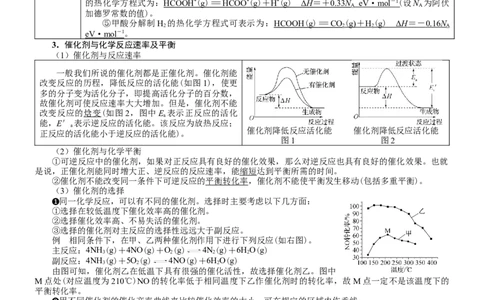
在Ru的催化下,单分子甲酸分解制 H 反应的过 (1)图中反应前的最左侧能量下降
2
程如下图所示,其中带“*”的物种表示吸附在Rh表 0.21 eV,即气态的甲酸分子被吸附在催
面。 化剂表面的活性位点上,所以能量下
催化机理 降。
能垒图 (2)可以用图中每步基元反应前后的
活性物质。注意:如果纵坐标相对能量
的单位是电子伏特(eV),焓变应转化成
每摩尔。微专题突破16 归因类问题考点透视 问题的态度:问则少;辩则明
①在催化机理能垒图中,有几个活化状态,就有几个基元反应。该反应机理有3 个基元反
应。
②每步基元反应的快慢取决于其能垒的大小,能垒越大,反应速率越慢。所以决定该反应速
率的是过渡态i。
③可依据图中每步基元反应前后的活性物质和能量变化,如该反应过程中决定反应速率步骤
的热化学方程式为: HCOOH * ( g ) = HCOO * ( g ) + H * ( g ) Δ H =+ 0.33 N eV · mo l - 1(设N 为阿伏
A A
加德罗常数的值)。
⑤甲酸分解制H 的热化学方程式可表示为: HCOOH ( g ) = CO ( g ) + H ( g ) Δ H =- 0.1 6 N
2 2 2 A
eV · mol - 1 。
3.催化剂与化学反应速率及平衡
(1)催化剂与反应速率
一般我们所说的催化剂都是正催化剂。催化剂能
改变反应的历程,降低反应的活化能(如图1),使更
多的分子变为活化分子,即提高活化分子的百分数,
故催化剂可使反应速率大大增加。但是,催化剂不能
改变反应的焓变(如图2,图中E 表示正反应的活化
a
能,E' 表示逆反应的活化能。该反应为放热反应;
a
催化剂降低反应活化能 催化剂降低反应活化能
正反应的活化能小于逆反应的活化能)。
图1 图2
(2)催化剂与化学平衡
①可逆反应中的催化剂,如果对正反应具有良好的催化效果,那么对逆反应也具有良好的催化效果。也就
是说,正催化剂能同时增大正、逆反应的反应速率,能缩短达到平衡所需的时间。
②催化剂不能改变同一条件下可逆反应的平衡转化率,催化剂不能使平衡发生移动(包括多重平衡)。
(3)催化剂的选择
❶同一化学反应,可以有不同的催化剂。选择时主要考虑以下几方面:
①选择在较低温度下催化效率高的催化剂。
②选择催化效率高、不易失活的催化剂。
③选择的催化剂对主反应的选择性远远大于副反应。
例 相同条件下,在甲、乙两种催化剂作用下进行下列反应(如右图)。
主反应:4NH (g)+4NO(g)+O(g) 4N(g)+6HO(g)
3 2 2 2
副反应:4NH (g)+5O(g) 4NO(g)+6HO(g)
3 2 2
由图可知,催化剂乙在低温下具有很强的催化活性,故选择催化剂乙。图中
M点处(对应温度为210℃)NO的转化率低于相同温度下乙作催化剂时的转化率,故M点一定不是该温度下的
平衡转化率。
❷用不同催化剂的催化产率曲线来比较催化效率的大小:可在规定的区域内作垂线。
例 利用光能和光催化剂可将CO(g)和HO(g)转化为CH(g)和O(g)。紫外光照射时,在不同催化剂
2 2 4 2
(Ⅰ、Ⅱ、Ⅲ)作用下,CH 产量随光照时间的变化如右图所示。
4
在0~15 h内,CH 的平均生成速率Ⅰ、Ⅱ和Ⅲ从大到小的顺序的确定方
4
法:选择横坐标在0~15 h内的任一点作横轴的垂线,CH 产量越高,CH 的平
4 4
均生成速率越大,故速率: Ⅱ > Ⅲ > Ⅰ 。
考考位位位
(2022·江苏卷)氢气是一种清洁能源,绿色环保制氢技术研究具有重要意义。
(2)“Fe-HCO-HO热循环制氢和甲酸”的原理为:在密闭容器中,铁粉与吸收CO 制得的NaHCO 溶
2 2 3
2
细节决定成败 目标成就未来 找找找题找找找题找找找找找找找找找找找找
找找液反应,生成H、HCOONa和Fe O;Fe O 再经生物柴油副产品转化为Fe。
2 3 4 3 4
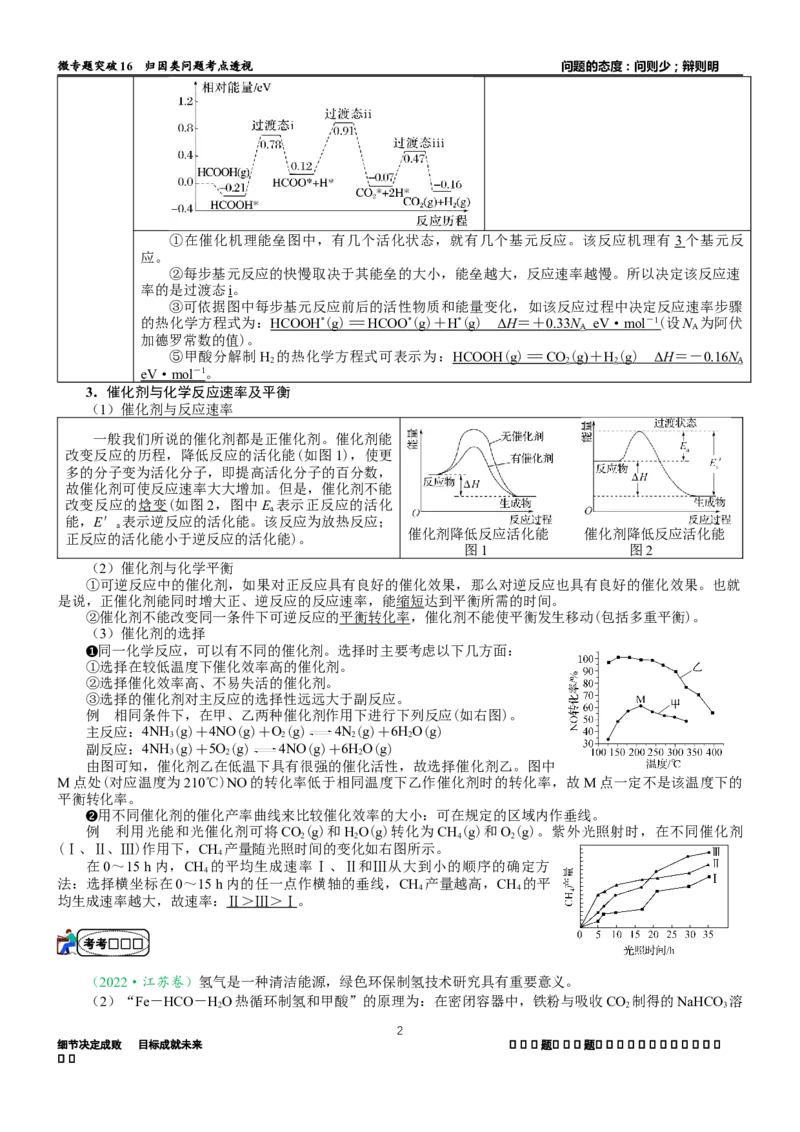
②随着反应进行,FeCO 迅速转化为活性Fe O ,活性Fe O 是HCO转化为HCOO-的催化剂,其可能
3 3 4-x 3 4-x
反 应 机 理 如 图 2 所 示 。 根 据 元 素 电 负 性 的 变 化 规 律 。 如 图 所 示 的 反 应 步 骤 Ⅰ 可 描 述 为
_________________________
_________________________________________________________________________________________________
_________________________________________________________________________________________________
____________________。
③在其他条件相同时,测得Fe的转化率、HCOO-的产率随c(HCO)变化如图3所示。HCOO-的产率随
c(HCO)增加而增大的可能原因是___________________________________________________________________。
(3)从物质转化与资源综合利用角度分析,“Fe-HCO --HO热循环制氢和甲酸”的优点是
3 2
________________________________________________________________________。
【答案】(2)②H的电负性大于Fe,小于O,在活性Fe O 表面,H 断裂为H原子,一个吸附在催化剂
3 4-x 2
的铁离子上,略带负电,一个吸附在催化剂的氧离子上,略带正电,前者与HCO中略带正电的碳结合,后者与
HCO中略带负电的羟基氧结合生成HO,HCO转化为HCOO-;③随c(HCO)增加,生成FeCO 速率更快、产
2 3
量增大,从而生成了更多的活性Fe O ,用于催化HCO转化为HCOO-的反应 (3)高效、经济、原子利用
3 4-x
率高、无污染
【解析】(2)③在其他条件相同时,随c(HCO)增加,其与铁粉反应加快,从图中得知Fe的转化率也增
大,即生成FeCO 的速率更快,量更大,则得到活性Fe O 的速度更快,量也更多,生成HCOO-的速率更快,
3 3 4-x
产率也更大;(3)“Fe-HCO-HO热循环制氢和甲酸”系统将HCO转化为HCOO-和生成H 的速率快,原
2 2
子利用率高,不产生污染物,Fe初期生成FeCO 后迅速转化为活性Fe O ,Fe O 被氧化为Fe O 再经生物柴
3 3 4-x 3 4-x 3 4
油副产品转化为Fe,得到循环利用,故该原理的优点是高效、经济、原子利用率高、无污染。
【问题解决1】
1.(2024·江苏卷)回收磁性合金钕铁硼(Nd Fe B)可制备半导体材料铁酸铋和光学材料氧化钕。
2 14
(1)钕铁硼在空气中焙烧转化为Nd O、Fe O 等(忽略硼的化合物),用0.4 mol·L-1盐酸酸浸后过滤得到
2 3 2 3
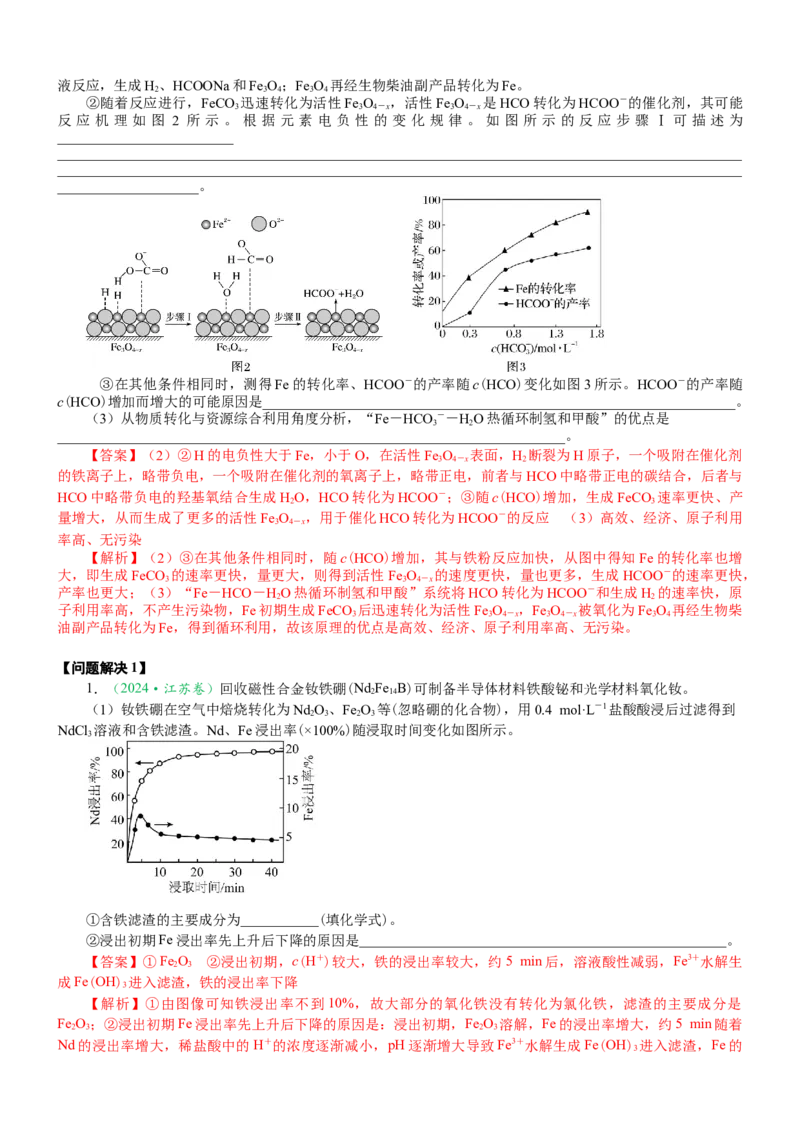
NdCl 溶液和含铁滤渣。Nd、Fe浸出率(×100%)随浸取时间变化如图所示。
3
①含铁滤渣的主要成分为___________(填化学式)。
②浸出初期Fe浸出率先上升后下降的原因是____________________________________________________。
【答案】①Fe O ②浸出初期,c(H+)较大,铁的浸出率较大,约5 min后,溶液酸性减弱,Fe3+水解生
2 3
成Fe(OH) 进入滤渣,铁的浸出率下降
3
【解析】①由图像可知铁浸出率不到10%,故大部分的氧化铁没有转化为氯化铁,滤渣的主要成分是
Fe O ;②浸出初期Fe浸出率先上升后下降的原因是:浸出初期,Fe O 溶解,Fe的浸出率增大,约5 min随着
2 3 2 3
Nd的浸出率增大,稀盐酸中的H+的浓度逐渐减小,pH逐渐增大导致Fe3+水解生成Fe(OH) 进入滤渣,Fe的
3微专题突破16 归因类问题考点透视 问题的态度:问则少;辩则明
浸出率又减小。
2.(2023·江苏)VO -WO/TiO 催化剂能催化 NH 脱除烟气中的 NO,反应为 4NH (g)+O(g)+
2 5 3 2 3 3 2
4NO(g)=4N(g)+6HO(g) ΔH=-1 632.4 kJ·mol-1。
2 2
(3)废催化剂的回收。回收VO-WO/TiO 废催化剂并制备NH VO 的过程可表示为
2 5 3 2 4 3
③向pH=8的NaVO 溶液中加入过量的NH Cl溶液,生成NH VO 沉淀。已知:K (NH VO )=1.7×10-
3 4 4 3 sp 4 3
3,加过量NH Cl溶液的目的是___________________________________。
4
【答案】增加铵根离子浓度,促进平衡向析出沉淀的方向移动,提高NH VO 的产量
4 3
【解析】K (NH VO )=1.7×10-3,饱和NH VO 溶液中溶解平衡:NH VO (s) NH(aq)+VO -(aq),
sp 4 3 4 3 4 3 3
加入过量NH Cl溶液,溶液中c(NH)增大,促进溶解平衡逆向移动,生成NH VO 沉淀,提高的NH VO 产率
4 4 3 4 3
3.(2024·江苏卷)回收磁性合金钕铁硼(Nd Fe B)可制备半导体材料铁酸铋和光学材料氧化钕。
2 14
(2)含铁滤渣用硫酸溶解,经萃取、反萃取提纯后,用于制备铁酸铋。
①用含有机胺(R N)的有机溶剂作为萃取剂提纯一定浓度的Fe (SO ) 溶液,原理为:
3 2 4 3
(R NH)SO +Fe3++SO 2-+HO H++(R NH)Fe(OH)(SO )(有机层)
3 2 4 4 2 3 2 4 2
已知:(R NH)SO +H++HSO - 2(R NH•HSO )
3 2 4 4 3 4
其他条件不变,水层初始pH在0.2~0.8范围内,随水层pH增大,有机层中Fe元素含量迅速增多的原因
是_______________________________________________________________________________________________
_________________________________________________________________________________________________
_________________________________________________________________________________________________
____________________________________________________________。
【答案】随水层pH增大,H+的浓度减小,(R NH)SO +Fe3++SO 2-+HO H++(R NH)Fe(OH)
3 2 4 4 2 3 2
(SO ) 的化学平衡向正反应方向移动,(R NH)SO +H++HSO - 2(R NH•HSO )的化学平衡逆向移动,该
4 2 3 2 4 4 3 4
平衡逆向移动引起(R NH)SO 浓度的增大,进一步促进萃取平衡向萃取方向移动,导致(R NH)Fe(OH)(SO )
3 2 4 3 2 4 2
的浓度增大,因此,有机层中Fe元素含量迅速增多
【解析】①减小生成物浓度,化学平衡向正反应方向移动,因此,其他条件不变,水层初始pH在0.2~
0.8范围内,随水层pH增大,H+的浓度减小,(R NH)SO +Fe3++SO 2-+HO H++(R NH)Fe(OH)
3 2 4 4 2 3 2
(SO ) 的化学平衡向正反应方向移动,又H+的浓度减小使平衡(R NH)SO +H++HSO - 2(R NH•HSO )
4 2 3 2 4 4 3 4
逆向移动,引起(R NH)SO 浓度的增大,进一步促进平衡(R NH)SO +Fe3++SO 2-+HO H++
3 2 4 3 2 4 4 2
(R NH)Fe(OH)(SO ) 向萃取方向移动,导致(R NH)Fe(OH)(SO ) 的浓度增大,因此,有机层中Fe元素含量
3 2 4 2 3 2 4 2
迅速增多。
注意:HSO - H++SO 2-,c(OH-)增大,SO 2-量增多,(R NH)SO 量增多,萃取正向进行程度增大。
4 4 4 3 2 4
化工生产中物质转化外界因素的影响归因
基于物质的性质,在转化过程中对反应进行调控,改变外界因素,体现对原理的应用,完成对性质、规律、
原理的考查。
1.外界因素(反应调控的角度)
——\s\up 4()答题角\s\up 4()——\s\up 4()
→ 度—— →
2.外界因素的影响原因解释答题策略
(1)设问逻辑
内容—\s\up 4()基于—\s\up 4()受影响\s\up 4()调控原\s\up 4()
—→ —→ 于—— 因——
(2)答题思路
——— \s\up 0()——— \s\up 0()——— \s\up 0()已有知信
→ → → 识—— 息
说明:
4
细节决定成败 目标成就未来 找找找题找找找题找找找找找找找找找找找找
找找物理性质(溶解性、挥发性) 元素存在形式
物质 物质
化学性质(热稳定性、酶活性) 对氧化还原性的影响
溶液的pH
温度 反应速率 反应速率
(H+浓度)
反应 反应 平衡移动(水解平衡)与K 相结
平衡移动 sp
合定量角度
2.考查类型
①根据有关原理解释图像中曲线的变化原因。
②根据平衡移动原理解释试剂过量的原因。
③考查反应中pH的变化对反应的影响。
考点精练
(2022·江苏卷)硫铁化合物(FeS、FeS 等)应用广泛。
2
(1)纳米FeS可去除水中微量六价铬[Cr(Ⅵ)]。在pH=4~7的水溶液中,纳米FeS颗粒表面带正电荷,
主要以HCrO、Cr O、CrO形式存在,纳米FeS去除水中Cr(Ⅵ)主要经过“吸附→反应→沉淀”的过程。
2
③ 在 pH = 4 ~ 7 溶 液 中 , pH 越 大 , FeS 去 除 水 中 Cr(Ⅵ) 的 速 率 越 慢 , 原 因 是
_____________________________
___________________________________________。
【答案】pH越大,c(OH-)越大。FeS表面带正电荷,易吸引阴离子,c(OH-)增大,降低了对三种含
Cr(Ⅵ)阴离子吸引,致使有效接触面积减小,反应速率下降
【解析】虽然在整个pH=4~7范围内,纳米FeS表面均带正电荷,但随着pH升高(接近中性),其表面
正电荷密度逐渐降低。这会减弱对带负电的Cr(VI)阴离子(如HCrO₄⁻、Cr₂O₇²⁻、CrO₄²⁻)的静电吸附能力,从
而减少Cr(VI)的吸附量,导致后续反应和沉淀步骤的速率下降。
【解析】FeS表面带正电荷,易吸引阴离子,在pH=4~7溶液中,随着pH越大,c(OH-)增大,其表面正
电荷密度逐渐降低。降低了对三种铬阴离子的吸引,从而减少Cr(VI)的吸附量,导致后续反应和沉淀步骤的速
率下降。
【问题解决2】
(2024·江苏卷)氢能是理想清洁能源,氢能产业链由制氢、储氢和用氢组成。
(2)一定条件下,将氮气和氢气按n(N)∶n(H)=1∶3混合匀速通入合成塔,发生反应N+3H
2 2 2 2
α-F高温、2NH 。海绵状的α-Fe作催化剂,多孔Al O 作为α-Fe的“骨架”和气体吸附剂。
e/A高压 3 2 3
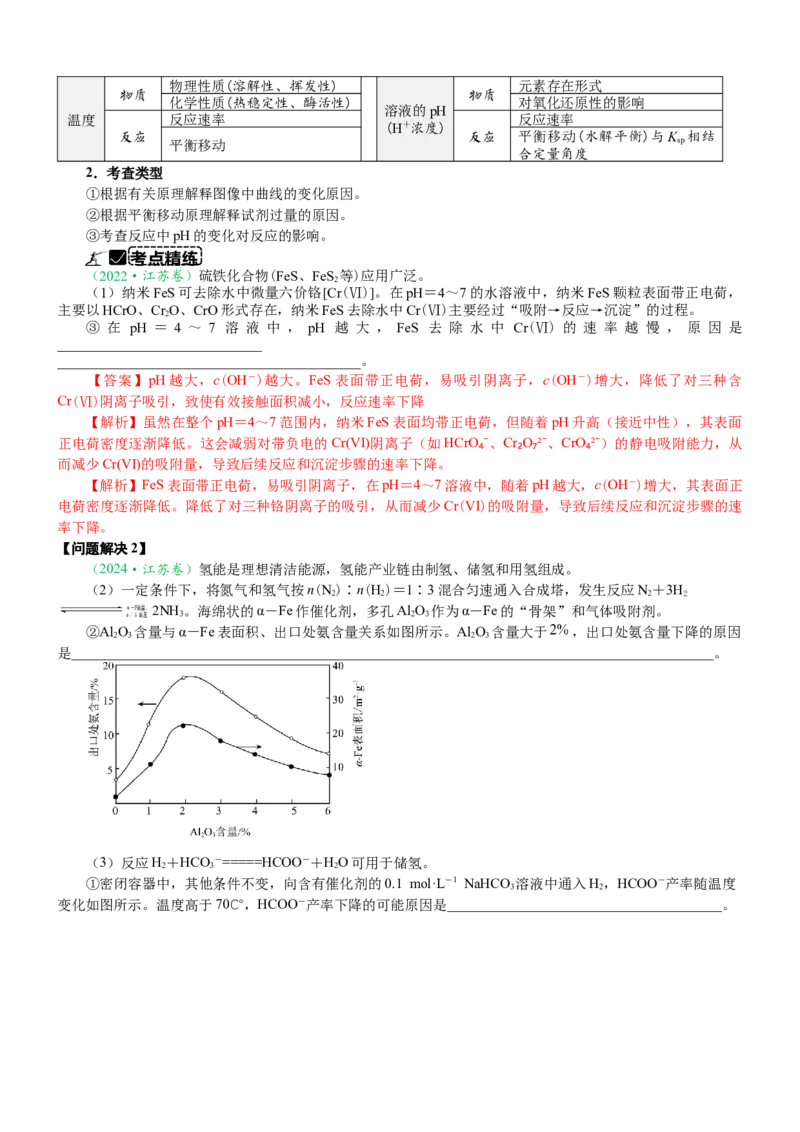
②Al O 含量与α-Fe表面积、出口处氨含量关系如图所示。Al O 含量大于 ,出口处氨含量下降的原因
2 3 2 3
是___________________________________________________________________________________________。
(3)反应H+HCO -=====HCOO-+HO可用于储氢。
2 3 2
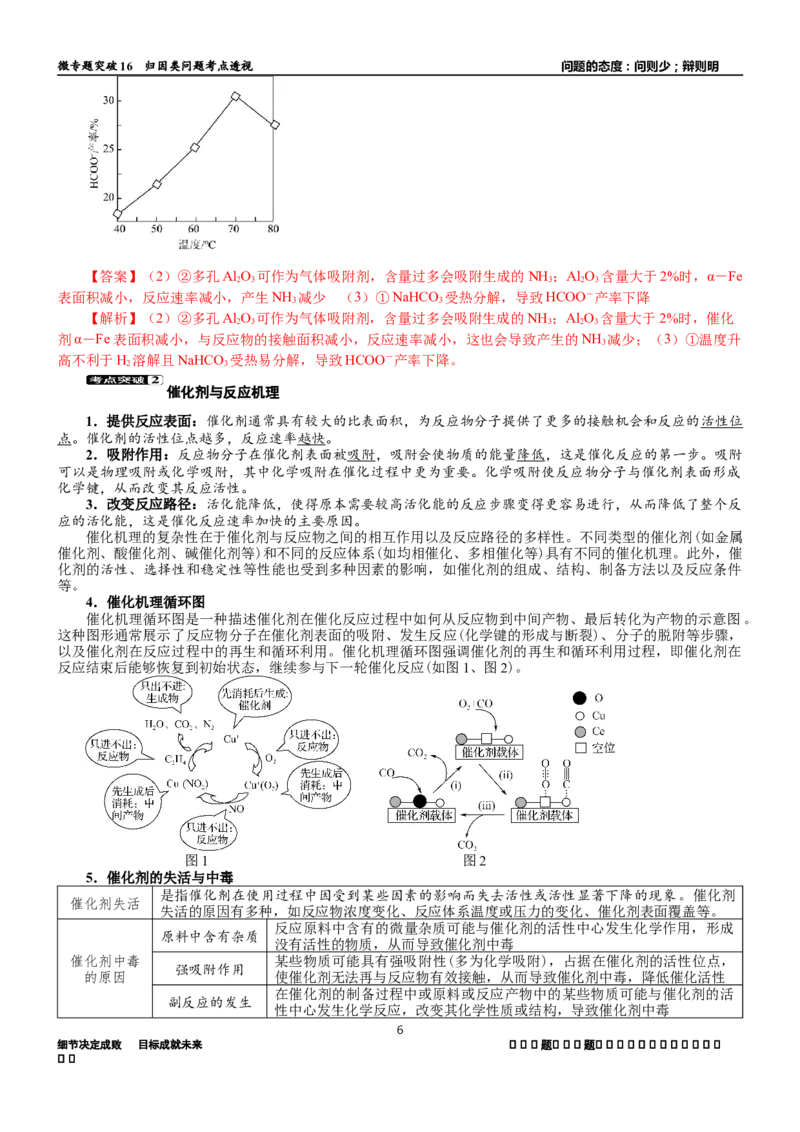
①密闭容器中,其他条件不变,向含有催化剂的0.1 mol·L-1 NaHCO 溶液中通入H,HCOO-产率随温度
3 2
变化如图所示。温度高于70℃,HCOO-产率下降的可能原因是_______________________________________。微专题突破16 归因类问题考点透视 问题的态度:问则少;辩则明
【答案】(2)②多孔Al O 可作为气体吸附剂,含量过多会吸附生成的NH ;Al O 含量大于2%时,α-Fe
2 3 3 2 3
表面积减小,反应速率减小,产生NH 减少 (3)①NaHCO 受热分解,导致HCOO-产率下降
3 3
【解析】(2)②多孔Al O 可作为气体吸附剂,含量过多会吸附生成的NH ;Al O 含量大于2%时,催化
2 3 3 2 3
剂α-Fe表面积减小,与反应物的接触面积减小,反应速率减小,这也会导致产生的NH 减少;(3)①温度升
3
高不利于H 溶解且NaHCO 受热易分解,导致HCOO-产率下降。
2 3
催化剂与反应机理
1.提供反应表面:催化剂通常具有较大的比表面积,为反应物分子提供了更多的接触机会和反应的活性位
点。催化剂的活性位点越多,反应速率越快。
2.吸附作用:反应物分子在催化剂表面被吸附,吸附会使物质的能量降低,这是催化反应的第一步。吸附
可以是物理吸附或化学吸附,其中化学吸附在催化过程中更为重要。化学吸附使反应物分子与催化剂表面形成
化学键,从而改变其反应活性。
3.改变反应路径:活化能降低,使得原本需要较高活化能的反应步骤变得更容易进行,从而降低了整个反
应的活化能,这是催化反应速率加快的主要原因。
催化机理的复杂性在于催化剂与反应物之间的相互作用以及反应路径的多样性。不同类型的催化剂(如金属
催化剂、酸催化剂、碱催化剂等)和不同的反应体系(如均相催化、多相催化等)具有不同的催化机理。此外,催
化剂的活性、选择性和稳定性等性能也受到多种因素的影响,如催化剂的组成、结构、制备方法以及反应条件
等。
4.催化机理循环图
催化机理循环图是一种描述催化剂在催化反应过程中如何从反应物到中间产物、最后转化为产物的示意图。
这种图形通常展示了反应物分子在催化剂表面的吸附、发生反应(化学键的形成与断裂)、分子的脱附等步骤,
以及催化剂在反应过程中的再生和循环利用。催化机理循环图强调催化剂的再生和循环利用过程,即催化剂在
反应结束后能够恢复到初始状态,继续参与下一轮催化反应(如图1、图2)。
图1 图2
5.催化剂的失活与中毒
是指催化剂在使用过程中因受到某些因素的影响而失去活性或活性显著下降的现象。催化剂
催化剂失活
失活的原因有多种,如反应物浓度变化、反应体系温度或压力的变化、催化剂表面覆盖等。
反应原料中含有的微量杂质可能与催化剂的活性中心发生化学作用,形成
原料中含有杂质
没有活性的物质,从而导致催化剂中毒
催化剂中毒 某些物质可能具有强吸附性(多为化学吸附),占据在催化剂的活性位点,
强吸附作用
的原因 使催化剂无法再与反应物有效接触,从而导致催化剂中毒,降低催化活性
在催化剂的制备过程中或原料或反应产物中的某些物质可能与催化剂的活
副反应的发生
性中心发生化学反应,改变其化学性质或结构,导致催化剂中毒
6
细节决定成败 目标成就未来 找找找题找找找题找找找找找找找找找找找找
找找催化剂恢复 升温还原、酸碱 为了防止催化剂失活,可以在生产过程中采取一些预防措施,如定期更换
活性的方法 再生或焚烧 催化剂、控制反应条件、避免反应物浓度过高等
随着温度升高,催化剂的催化活性会增加。但是往往会出现拐点,即到达
一般规律
一定的温度之后,温度增加,催化剂的活性下降
催化剂的活 温度太低,催化活性较低,温度较高,酶发生变性,催化活性降低。见例
酶作催化剂时
性与温度 1
依据催化剂的催化效率随温度升高出现的这个“拐点”是无法确定反应达到平衡点的。因为
很有可能在可逆反应还没达到平衡之前,其催化剂的活性就随着温度的升高而下降了。见例2
以TiO/Cu Al O 为催化剂,可以将CO 和CH 直接转化成
2 2 2 4 2 4
乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率
的关系如图所示。乙酸的生成速率主要取决于温度影响的
例1
范围是________。根据图像,温度超过250 ℃时,催化剂
效率降低,在300 ℃时失去活性,故300~400℃时乙酸
的生成速率主要取决于温度影响。
反应6H(g)+2CO(g) CH =CH(g)+4HO(g),温
2 2 2 2 2
例2 度对CO 的平衡转化率和催化剂催化效率的影响关系如右
2
图,在250 ℃时催化效率达到最高,但是并未达到平衡
考点精练
1.(2024·南通市如皋2月)二氧化碳的综合利用具有重要意义。
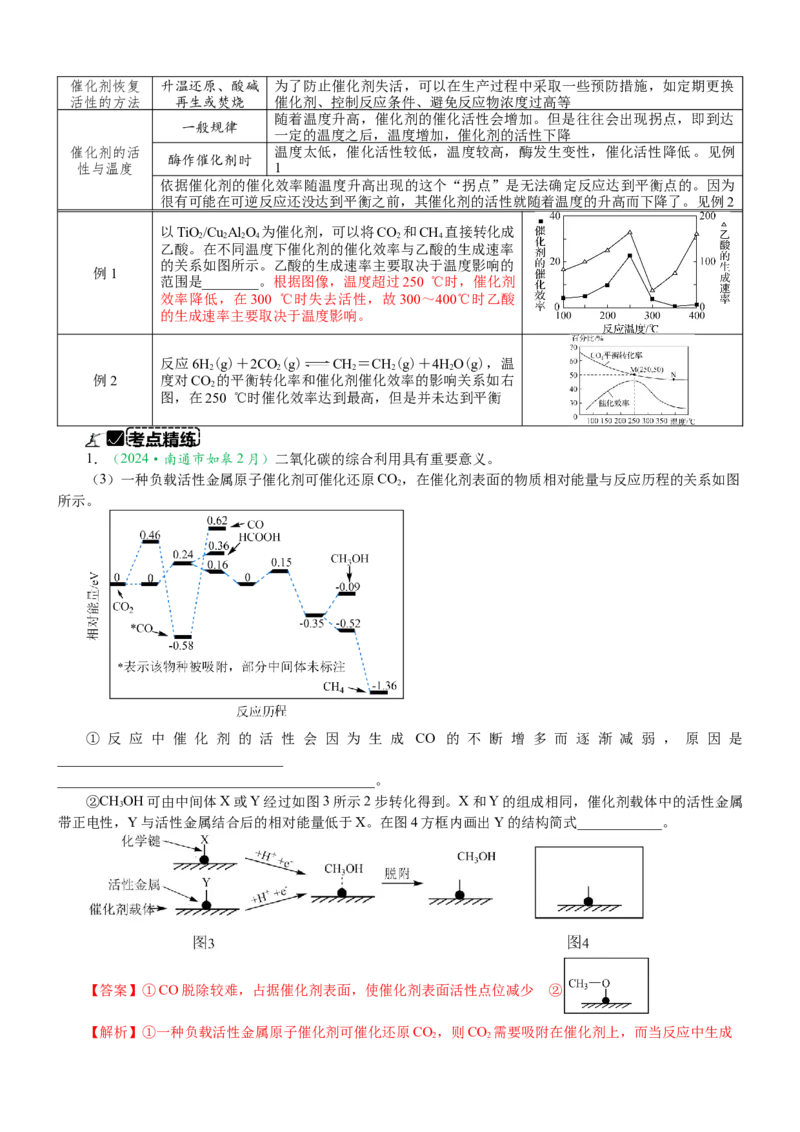
(3)一种负载活性金属原子催化剂可催化还原CO,在催化剂表面的物质相对能量与反应历程的关系如图
2
所示。
① 反 应 中 催 化 剂 的 活 性 会 因 为 生 成 CO 的 不 断 增 多 而 逐 渐 减 弱 , 原 因 是
________________________________
_____________________________________________。
②CHOH可由中间体X或Y经过如图3所示2步转化得到。X和Y的组成相同,催化剂载体中的活性金属
3
带正电性,Y与活性金属结合后的相对能量低于X。在图4方框内画出Y的结构简式____________。
【答案】①CO脱除较难,占据催化剂表面,使催化剂表面活性点位减少 ②
【解析】①一种负载活性金属原子催化剂可催化还原CO,则CO 需要吸附在催化剂上,而当反应中生成
2 2微专题突破16 归因类问题考点透视 问题的态度:问则少;辩则明
CO的不断增多,CO脱除较难,占据催化剂表面,使催化剂表面活性点位减少,导致催化剂再难被CO 吸附,
2
催化剂活性减弱;故答案为:CO脱除较难,占据催化剂表面,使催化剂表面活性点位减少;②催化剂载体中的
活性金属带正电性,说明是带孤电子对较多的原子与催化剂结合,Y与活性金属结合后的相对能量低于X,且
X和Y的组成相同,说明Y的结构简式为: ,故答案为: 。
2.(2024·江苏南京市、盐城市一模)在催化剂作用下,以CO 和H 为原料合成CHOH,主要反应为:
2 2 3
反应Ⅰ:CO(g)+3H(g)=CHOH(g)+HO(g) ∆H=-49 kJ·mol-1
2 2 3 2 1
反应Ⅱ:CO(g)+H(g)=CO(g)+HO(g) ∆H=+41 kJ·mol-1
2 2 2 2
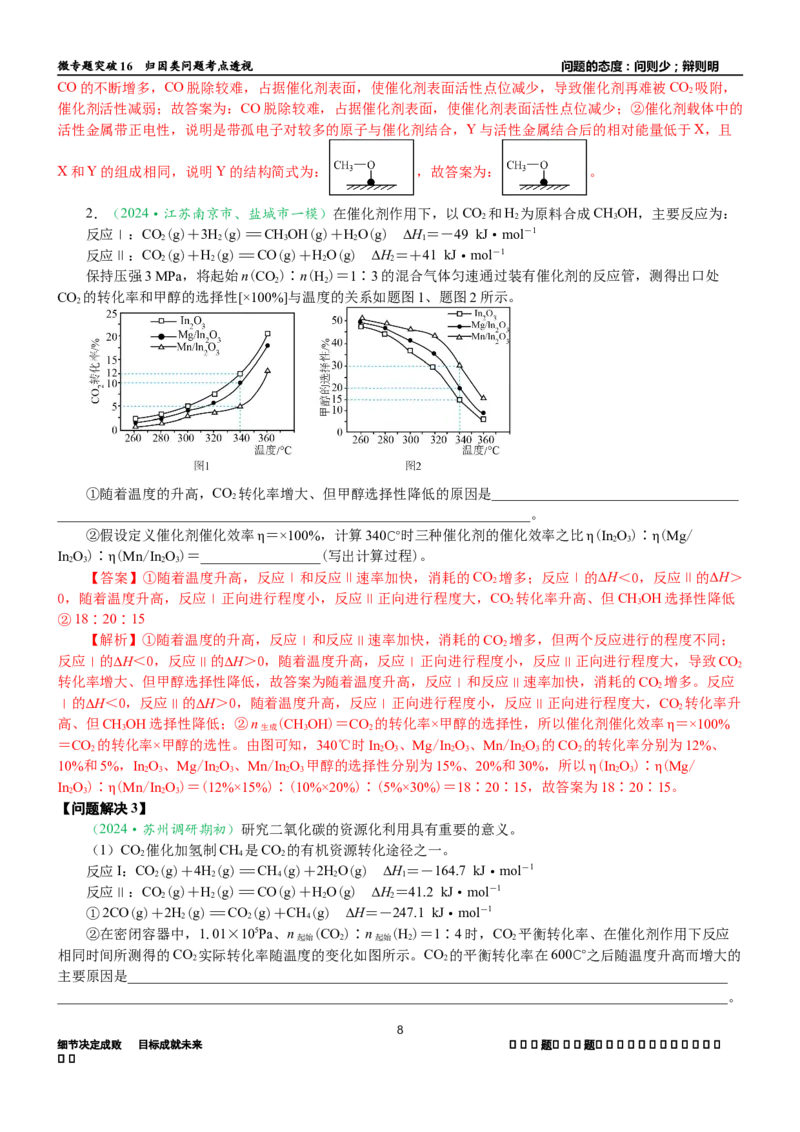
保持压强3 MPa,将起始n(CO)∶n(H)=1∶3的混合气体匀速通过装有催化剂的反应管,测得出口处
2 2
CO 的转化率和甲醇的选择性[×100%]与温度的关系如题图1、题图2所示。
2
①随着温度的升高,CO 转化率增大、但甲醇选择性降低的原因是___________________________________
2
___________________________________________________________________。
②假设定义催化剂催化效率η=×100%,计算340℃时三种催化剂的催化效率之比η(InO)∶η(Mg/
2 3
InO)∶η(Mn/InO)=_________________(写出计算过程)。
2 3 2 3
【答案】①随着温度升高,反应Ⅰ和反应Ⅱ速率加快,消耗的CO 增多;反应Ⅰ的∆H<0,反应Ⅱ的∆H>
2
0,随着温度升高,反应Ⅰ正向进行程度小,反应Ⅱ正向进行程度大,CO 转化率升高、但CHOH选择性降低
2 3
②18∶20∶15
【解析】①随着温度的升高,反应Ⅰ和反应Ⅱ速率加快,消耗的CO 增多,但两个反应进行的程度不同;
2
反应Ⅰ的∆H<0,反应Ⅱ的∆H>0,随着温度升高,反应Ⅰ正向进行程度小,反应Ⅱ正向进行程度大,导致CO
2
转化率增大、但甲醇选择性降低,故答案为随着温度升高,反应Ⅰ和反应Ⅱ速率加快,消耗的CO 增多。反应
2
Ⅰ的∆H<0,反应Ⅱ的∆H>0,随着温度升高,反应Ⅰ正向进行程度小,反应Ⅱ正向进行程度大,CO 转化率升
2
高、但CHOH选择性降低;②n (CHOH)=CO 的转化率×甲醇的选择性,所以催化剂催化效率η=×100%
3 生成 3 2
=CO 的转化率×甲醇的选性。由图可知,340℃时InO、Mg/InO、Mn/InO 的CO 的转化率分别为12%、
2 2 3 2 3 2 3 2
10%和5%,InO、Mg/InO、Mn/InO 甲醇的选择性分别为15%、20%和30%,所以η(InO)∶η(Mg/
2 3 2 3 2 3 2 3
InO)∶η(Mn/InO)=(12%×15%)∶(10%×20%)∶(5%×30%)=18∶20∶15,故答案为18∶20∶15。
2 3 2 3
【问题解决3】
(2024·苏州调研期初)研究二氧化碳的资源化利用具有重要的意义。
(1)CO 催化加氢制CH 是CO 的有机资源转化途径之一。
2 4 2
反应I:CO(g)+4H(g)=CH(g)+2HO(g) ∆H=-164.7 kJ·mol-1
2 2 4 2 1
反应Ⅱ:CO(g)+H(g)=CO(g)+HO(g) ∆H=41.2 kJ·mol-1
2 2 2 2
①2CO(g)+2H(g)=CO(g)+CH(g) ∆H=-247.1 kJ·mol-1
2 2 4
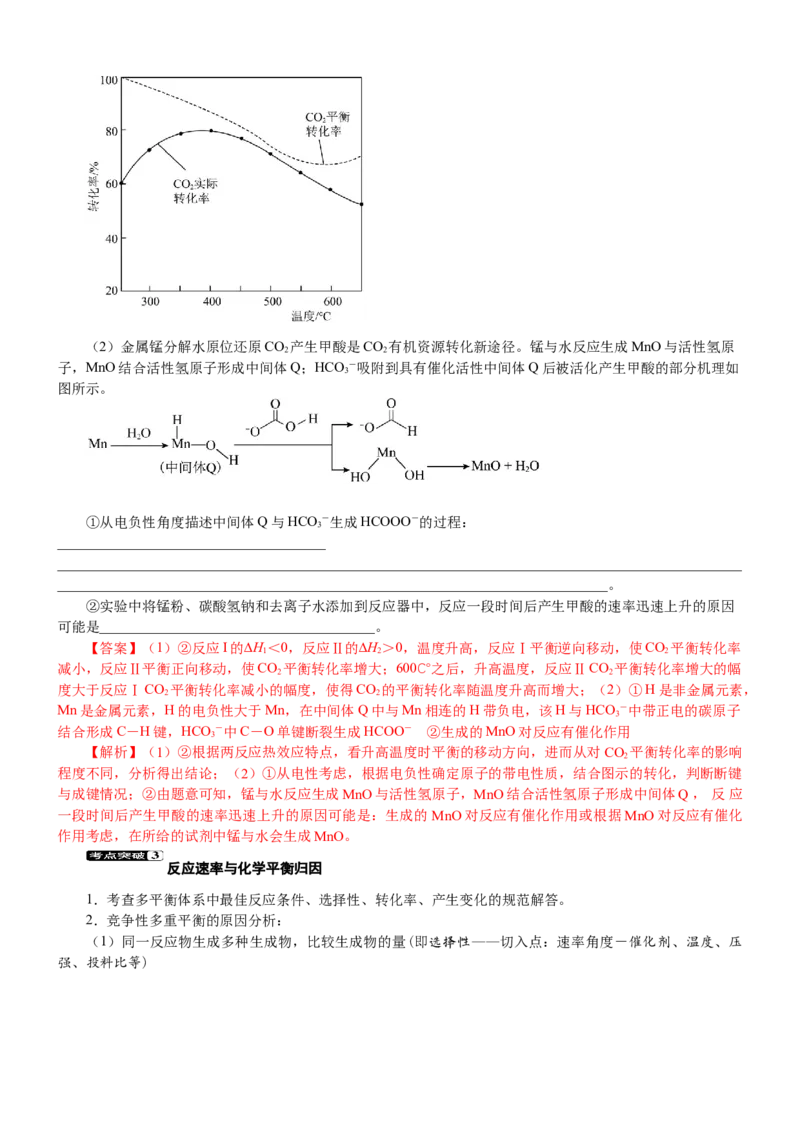
②在密闭容器中,1.01×105Pa、n (CO)∶n (H)=1∶4时,CO 平衡转化率、在催化剂作用下反应
起始 2 起始 2 2
相同时间所测得的CO 实际转化率随温度的变化如图所示。CO 的平衡转化率在600℃之后随温度升高而增大的
2 2
主要原因是_____________________________________________________________________________________
_______________________________________________________________________________________________。
8
细节决定成败 目标成就未来 找找找题找找找题找找找找找找找找找找找找
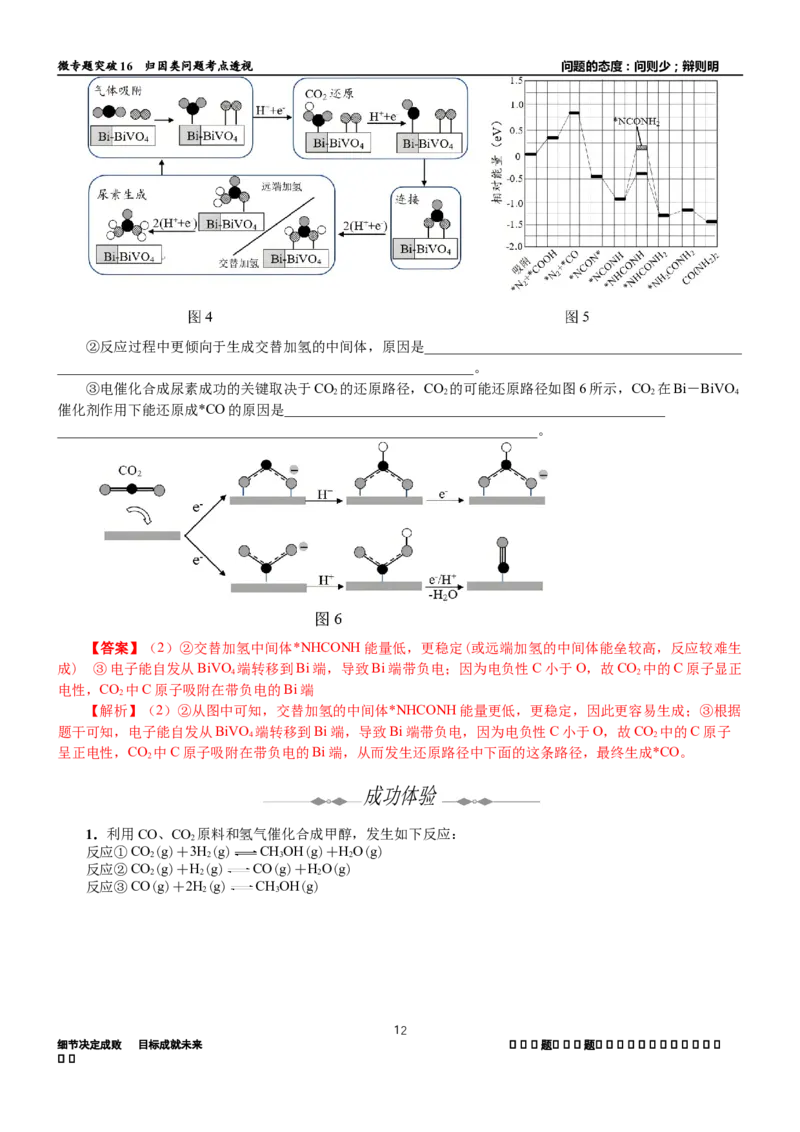
找找(2)金属锰分解水原位还原CO 产生甲酸是CO 有机资源转化新途径。锰与水反应生成MnO与活性氢原
2 2
子,MnO结合活性氢原子形成中间体Q;HCO -吸附到具有催化活性中间体Q后被活化产生甲酸的部分机理如
3
图所示。
①从电负性角度描述中间体Q与HCO -生成HCOOO-的过程:
3
______________________________________
_________________________________________________________________________________________________
______________________________________________________________________________。
②实验中将锰粉、碳酸氢钠和去离子水添加到反应器中,反应一段时间后产生甲酸的速率迅速上升的原因
可能是_______________________________________。
【答案】(1)②反应I的∆H<0,反应Ⅱ的∆H>0,温度升高,反应Ⅰ平衡逆向移动,使CO 平衡转化率
1 2 2
减小,反应Ⅱ平衡正向移动,使CO 平衡转化率增大;600℃之后,升高温度,反应ⅡCO 平衡转化率增大的幅
2 2
度大于反应ⅠCO 平衡转化率减小的幅度,使得CO 的平衡转化率随温度升高而增大;(2)①H是非金属元素,
2 2
Mn是金属元素,H的电负性大于Mn,在中间体Q中与Mn相连的H带负电,该H与HCO -中带正电的碳原子
3
结合形成C-H键,HCO -中C-O单键断裂生成HCOO- ②生成的MnO对反应有催化作用
3
【解析】(1)②根据两反应热效应特点,看升高温度时平衡的移动方向,进而从对CO 平衡转化率的影响
2
程度不同,分析得出结论;(2)①从电性考虑,根据电负性确定原子的带电性质,结合图示的转化,判断断键
与成键情况;②由题意可知,锰与水反应生成MnO与活性氢原子,MnO结合活性氢原子形成中间体Q , 反 应
一段时间后产生甲酸的速率迅速上升的原因可能是:生成的 MnO对反应有催化作用或根据MnO对反应有催化
作用考虑,在所给的试剂中锰与水会生成MnO。
反应速率与化学平衡归因
1.考查多平衡体系中最佳反应条件、选择性、转化率、产生变化的规范解答。
2.竞争性多重平衡的原因分析:
(1)同一反应物生成多种生成物,比较生成物的量(即选择性——切入点:速率角度-催化剂、温度、压
强、投料比等)微专题突破16 归因类问题考点透视 问题的态度:问则少;辩则明
(2)不同反应生成物的量随条件改变而发生的变化,切入点:平衡角度
先判断以哪个反应为主,再描述平衡移动
3.答题模板:
叙特点(正反应特点)— \s\up 0()变条件(浓度、压强、温度改变、催化剂作用等)— \s\up 0()判方向(平衡
→ →
向正/逆方向移动、不移动)— \s\up 0()叙结果(各反应物/生成物的“量”的变化)— \s\up 0()得结论(通过“移
→ →
动结果”作出合理判断)
考点精练
1.(2023·江苏卷)空气中CO 含量的控制和CO 资源利用具有重要意义。
2 2
合成尿素[CO(NH )]是利用CO 的途径之一、尿素合成主要通过下列反应实现
2 2 2
反应Ⅰ:2NH (g)+CO(g)=NH COONH(l)
3 2 2 4
反应Ⅱ:NH COONH(l)=CO(NH )(l)+HO(l)
2 4 2 2 2
反应体系中除发生反应Ⅰ、反应Ⅱ外,还发生尿素水解、尿素缩合生成缩二脲[(NH CO)NH]和尿素转化为
2 2
氰酸铵(NH OCN)等副反应。尿素生产中实际投入NH 和CO 的物质的量之比为n(NH )∶n(CO)=4∶1,其实
4 3 2 3 2
际投料比值远大于理论值的原因是___________________________________________________________________。
【答案】提高二氧化碳的转化率,抑制尿素水解,抑制尿素缩合生成缩二脲
【解析】增加NH 与CO 投料量的比值,可以提高CO 的转化率,从而抑制尿素水解CO(NH)+2HO
3 2 2 2 2 2
HCO+2NH 、抑制尿素缩合生成缩二脲[2CO(NH ) (NH CO)NH+NH ]。
2 3 3 2 2 2 2 3
2.(2024·南通市海安市9月)黄铁矿(FeS)可用于制硫和处理废水。
2
(2)制硫反应所得气体经冷凝回收S 后,尾气中还含有CO和SO 。将尾气通
2 2
过催化剂进行处理,发生反应Ⅰ,同时发生副反应Ⅱ。
反应Ⅰ:2SO (g)+4CO(g) S(g)+4CO(g) ∆H<0
2 2 2
反应Ⅱ:SO (g)+3CO(g) COS(g)+2CO(g) ∆H<0
2 2
理论分析及实验结果表明,600~1 000K范围内,SO 平衡转化率接近100%。其
2
他条件相同,不同温度下,S、COS平衡产率和10 min时S 实际产率如图所示。
2 2
①10 min时,S 实际产率大于平衡产率的原因是________________________________
2
____________________________________________________。
②随温度升高,S 平衡产率上升的原因是_______________________________________________________
2
____________________________________________________________________________________________。
【答案】①反应①的活化能较低,反应速率Ⅰ反应比反应Ⅱ快,SO 与CO主要生成S,超过平衡产率 ②
2 2
温度升高,反应Ⅱ平衡逆向移动,使c(SO )、c(CO)增大;对于反应Ⅰ,浓度改变对平衡的影响超过温度改变
2
的影响,平衡正向移动(3分,无比较关系0分)
【问题解决4】
1.(2023·江苏卷)金属硫化物(MS)催化反应CH(g)+2HS(g)=CS(g)+4H(g),既可以除去天然
x y 4 2 2 2
气中的HS,又可以获得H。
2 2
10
细节决定成败 目标成就未来 找找找题找找找题找找找找找找找找找找找找
找找判断以下说法:题图所示的反应机理中,步骤Ⅰ可理解为HS中带部分负电荷的S与催化剂中的M之间发
2
生作用
【答案】正确
【解析】由图可知,HS中S与催化剂中的M之间成键,即反应机理步骤Ⅰ中HS中带部分负电荷的S与
2 2
催化剂中的M之间发生作用,正确。
说明:吸附是开始化学反应的前提,如何能吸附?— \s\up 0()存在静电作用力 与电负性有关
→
2.肼催化还原羰基化合物。肼在NiO催化下还原丙酮的反应机理如下:
据元素电负性的变化规律,步骤2可描述为_____________________________________________________
________________________________________________________________________________________。
【答案】电负性大小:O>N>C>H,丙酮中C=O键断裂,NH 中其中一个N-H键断裂,带负电的O
2 4
与带正电的H结合,带正电的C与带负电的N结合,形成*(CH)C(OH)NHNH
3 2 2
结构与反应机理归因
1.模型考点——电负性
2.思考步骤:
① 比较涉及元素的电负性,判断原子所带正电荷还是负电荷
② 观察图像或反应机理,确定化学键如何断裂
③ 带相反电荷的原子重新结合形成新的化学键
④ 关注化学用语(如吸附或脱附,形成化学键或化学键断裂)的规范使用,构建叙述答题模版
考点精练
1.(2024·江苏仿真模拟)Fe O 可以催化脱除HS,脱除反应为Fe O(g)+3HS(g)=S(s)+2FeS(s)+
2 3 2 2 3 2
3HO(g),脱除过程如下图所示。
2
请你判断:图乙中催化剂对HS的吸附强度强于图甲的理由是______________________________________
2
_______________________________________________________________________________________________。
【答案】因电负性S>H,HS分子中H带正电、S带负电;电负性O>Fe,Fe O 中Fe带正电,O带负电;
2 2 3
甲吸附方式为同种电性微粒靠近,吸附能力弱,乙吸附方式为不同电性微粒靠近,吸附能力强。
2.(2024•无锡期中)尿素在工业、农业、医药等诸多领域应用广泛。
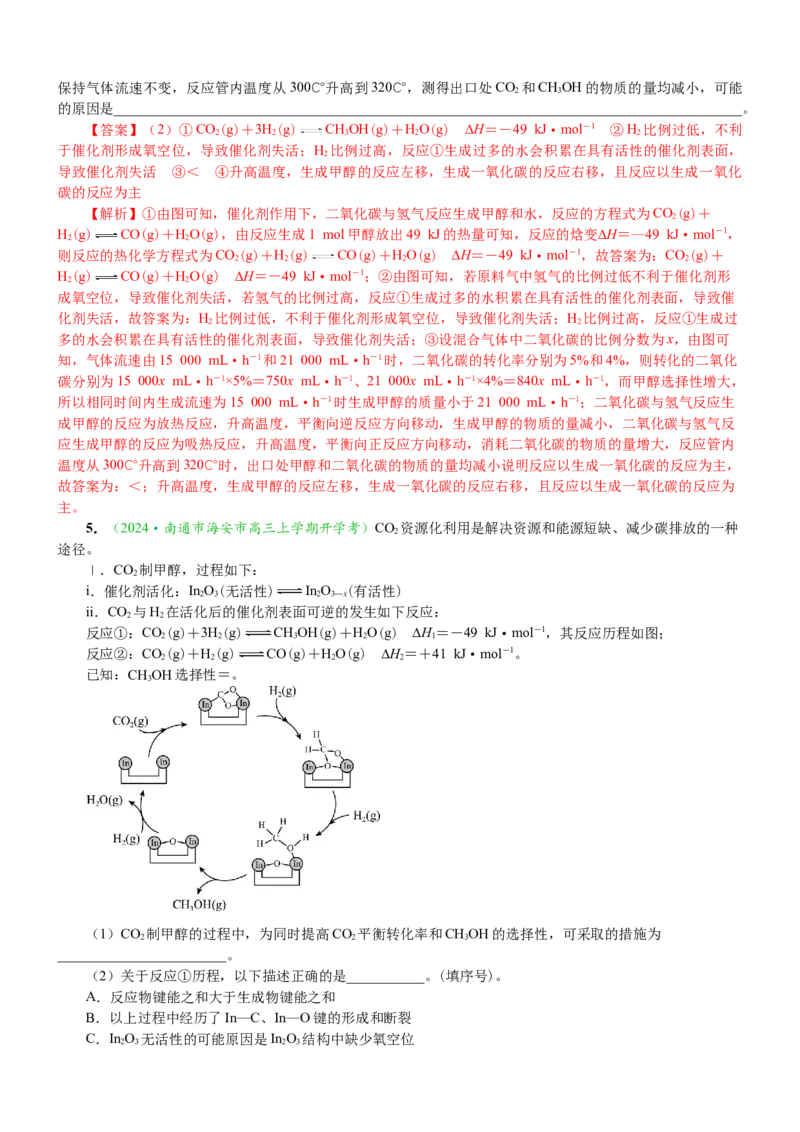
(2)电催化法合成尿素。一种新型异质结构Bi-BiVO 催化剂用于酸性介质中CO 和N 电化学合成尿素。
4 2 2
反应过程中,电子能自发从BiVO 端转移到Bi端,在Bi-BiVO 催化剂这一极可能的反应机理如图4所示,反
4 4
应部分历程及能量关系如图5所示。微专题突破16 归因类问题考点透视 问题的态度:问则少;辩则明
②反应过程中更倾向于生成交替加氢的中间体,原因是_____________________________________________
___________________________________________________________。
③电催化合成尿素成功的关键取决于CO 的还原路径,CO 的可能还原路径如图6所示,CO 在Bi-BiVO
2 2 2 4
催化剂作用下能还原成*CO的原因是______________________________________________________
____________________________________________________________________。
【答案】(2)②交替加氢中间体*NHCONH能量低,更稳定(或远端加氢的中间体能垒较高,反应较难生
成) ③电子能自发从BiVO 端转移到Bi端,导致Bi端带负电;因为电负性C小于O,故CO 中的C原子显正
4 2
电性,CO 中C原子吸附在带负电的Bi端
2
【解析】(2)②从图中可知,交替加氢的中间体*NHCONH能量更低,更稳定,因此更容易生成;③根据
题干可知,电子能自发从BiVO 端转移到Bi端,导致Bi端带负电,因为电负性C小于O,故CO 中的C原子
4 2
呈正电性,CO 中C原子吸附在带负电的Bi端,从而发生还原路径中下面的这条路径,最终生成*CO。
2
成功体验
1.利用CO、CO 原料和氢气催化合成甲醇,发生如下反应:
2
反应①CO(g)+3H(g) CHOH(g)+HO(g)
2 2 3 2
反应②CO(g)+H(g) CO(g)+HO(g)
2 2 2
反应③CO(g)+2H(g) CHOH(g)
2 3
12
细节决定成败 目标成就未来 找找找题找找找题找找找找找找找找找找找找
找找温 度 超 过 210℃ , 随 着 温 度 的 升 高 CO 的 产 率 下 降 的 原 因 是
___________________________________________
________________________________________________________________。
【答案】温度超过210℃,随着温度的升高,反应②生成CO的量小于反应③消耗CO的量。
【解析】上升阶段,以反应②生成CO为主;下降阶段,以反应③消耗CO为主。
2.(2021·江苏卷)利用铜-铈氧化物(xCuO·yCeO2,Ce 是活泼金属)催化氧化可除去H2中少量CO,
催 化 氧 化 过 程 中 Cu 、 Ce 的 化 合 价 均 发 生 变 化 , 可 能 机 理 如 题 18 图 - 2 所 示 。 将
n(CO)∶n(O2)∶n(H2)∶n(N2)=1∶1∶49∶49的混合气体以一定流速通过装有xCuO·yCeO2催化剂的反应
器,CO的转化率随温度变化的曲线如题18图-3所示。
题18图-2 题18图-3
② 当 催 化 氧 化 温 度 超 过 150℃ 时 , 催 化 剂 的 催 化 活 性 下 降 , 其 可 能 原 因 是
_______________________________
___________________________________________________________________________________。
【答案】②温度高于150℃,H2或CO将氧化铜或氧化亚铜还原为Cu
【解析】由于高温下,Cu(+2价)或Cu(+1价)被H 还原为金属Cu,所以当催化氧化温度超过150℃时,
2
催化剂的催化活性下降。
3.(2024·连云港上学期调研一)我国要在2030年前实现碳达峰、2060年前实现碳中和的目标,CO 的
2
捕集与转化是研究的重要课题。
的
(2)光催化还原法实现CO 甲烷化可能 反应机理如图所示,该过程可描述为:光照条件下,催化剂TiO
2 2
的价带(VB)中的电子激发至导带(CB)中,价带中形成电子空穴(h+),_______________________________
_____________________________________。
(4)CO 和H 可合成甲烷,合成过程中发生如下反应:
2 2
CO(g)+4H(g)=CH(g)+2HO(g) ∆H=-167 kJ·mol-1
2 2 4 2
CO(g)+H(g)=CO(g)+HO(g) ∆H=+40.0 kJ·mol-1
2 2 2
反应的压强和CO 与H 气体比例一定,在两种不同催化剂条件下反应相同时间,测得CO 的转化率随温度
2 2 2
变化关系如图所示,高于320℃后,以Ni-CeO 为催化剂,CO 转化率略有下降,以Ni为催化剂,CO 转化率
2 2 2微专题突破16 归因类问题考点透视 问题的态度:问则少;辩则明
大幅上升,其原因是__________________________________________________________________________
___________________________________________________________________________________________。
【答案】(2)H+作用下CO 在导带上得到电子生成CH ,HO在价带上失去电子生成O 和H+ (4)
2 4 2 2
320℃时,以Ni-CeO 为催化剂,CO 甲烷化反应已达平衡,升高温度平衡左移;以Ni为催化剂,CO 甲烷化
2 2 2
反应速率较慢,升高温度反应速度加快,反应相同时间时CO 转化率增加
2
【解析】(2)由图可知,二氧化碳甲烷化可能的反应机理为光照条件下,催化剂二氧化钛的价带中的电子
激发至导带中,价带中形成电子空穴,氢离子作用下二氧化碳在导带上得到电子生成甲烷,水分子在价带上失
去电子生成氧气和氢离子,故答案为:H+作用下CO 在导带上得到电子生成CH ,HO在价带上失去电子生成
2 4 2
O 和H+ H+作用下CO 在导带上得到电子生成CH ,HO在价带上失去电子生成O 和H+;(4)由图可知,
2 2 4 2 2
320℃时,以Ni-CeO 为催化剂,CO 甲烷化反应已达平衡,升高温度平衡左移;以Ni为催化剂,CO 甲烷化
2 2 2
反应速率较慢,升高温度反应速度加快,反应相同时间时 CO 转化率增加,所以高于320℃后,以Ni−CeO 为
2 2
催化剂,CO 转化率略有下降,以Ni为催化剂,CO 转化率大幅上升,故答案为:320℃时,以Ni-CeO 为催
2 2 2
化剂,CO 甲烷化反应已达平衡,升高温度平衡左移;以 Ni为催化剂,CO 甲烷化反应速率较慢,升高温度反
2 2
应速度加快,反应相同时间时CO 转化率增加。
2
4.(2024·泰州市下学期一模)空气中CO 含量的控制和CO 资源利用具有重要意义。
2 2
(2)利用铟氧化物催化CO、H 制取CHOH的可能机理如图2所示,InO 无催化活性,形成氧空位后具
2 2 3 2 3
有较强催化活性,将固定比例的CO、H 混合气体以不同流速通过装有催化剂的反应管,CHOH选择性、CO
2 2 3 2
转化率随气体流速变化曲线如图3所示,
①图2中的反应每生成1 mol CHOH(g)放出49 kJ的热量,其热化学方程式为:
3
_____________________________________________________________________________________。
② 若 原 料 气 中 H 比 例 过 低 、 过 高 均 会 减 弱 催 化 剂 活 性 , 原 因 是
2
________________________________________
_____________________________________________________________________________________________。
③制取CHOH时,同时发生反应CO(g)+H(g) CO(g)+HO(g) ∆H>0,气体流速分别为15 000
3 2 2 2
mL·h-1和21 000 mL·h-1,相同时间内生成CHOH的质量,前者______后者(选填“>”、“="或“<”);
3
14
细节决定成败 目标成就未来 找找找题找找找题找找找找找找找找找找找找
找找保持气体流速不变,反应管内温度从300℃升高到320℃,测得出口处CO 和CHOH的物质的量均减小,可能
2 3
的原因是_________________________________________________________________________________________。
【答案】(2)①CO(g)+3H(g) CHOH(g)+HO(g) ∆H=-49 kJ·mol-1 ②H 比例过低,不利
2 2 3 2 2
于催化剂形成氧空位,导致催化剂失活;H 比例过高,反应①生成过多的水会积累在具有活性的催化剂表面,
2
导致催化剂失活 ③< ④升高温度,生成甲醇的反应左移,生成一氧化碳的反应右移,且反应以生成一氧化
碳的反应为主
【解析】①由图可知,催化剂作用下,二氧化碳与氢气反应生成甲醇和水,反应的方程式为CO(g)+
2
H(g) CO(g)+HO(g),由反应生成1 mol甲醇放出49 kJ的热量可知,反应的焓变∆H=—49 kJ·mol-1,
2 2
则反应的热化学方程式为CO(g)+H(g) CO(g)+HO(g) ∆H=-49 kJ·mol-1,故答案为:CO(g)+
2 2 2 2
H(g) CO(g)+HO(g) ∆H=-49 kJ·mol-1;②由图可知,若原料气中氢气的比例过低不利于催化剂形
2 2
成氧空位,导致催化剂失活,若氢气的比例过高,反应①生成过多的水积累在具有活性的催化剂表面,导致催
化剂失活,故答案为:H 比例过低,不利于催化剂形成氧空位,导致催化剂失活;H 比例过高,反应①生成过
2 2
多的水会积累在具有活性的催化剂表面,导致催化剂失活;③设混合气体中二氧化碳的比例分数为x,由图可
知,气体流速由15 000 mL·h-1和21 000 mL·h-1时,二氧化碳的转化率分别为5%和4%,则转化的二氧化
碳分别为15 000x mL·h-1×5%=750x mL·h-1、21 000x mL·h-1×4%=840x mL·h-1,而甲醇选择性增大,
所以相同时间内生成流速为15 000 mL·h-1时生成甲醇的质量小于21 000 mL·h-1;二氧化碳与氢气反应生
成甲醇的反应为放热反应,升高温度,平衡向逆反应方向移动,生成甲醇的物质的量减小,二氧化碳与氢气反
应生成甲醇的反应为吸热反应,升高温度,平衡向正反应方向移动,消耗二氧化碳的物质的量增大,反应管内
温度从300℃升高到320℃时,出口处甲醇和二氧化碳的物质的量均减小说明反应以生成一氧化碳的反应为主,
故答案为:<;升高温度,生成甲醇的反应左移,生成一氧化碳的反应右移,且反应以生成一氧化碳的反应为
主。
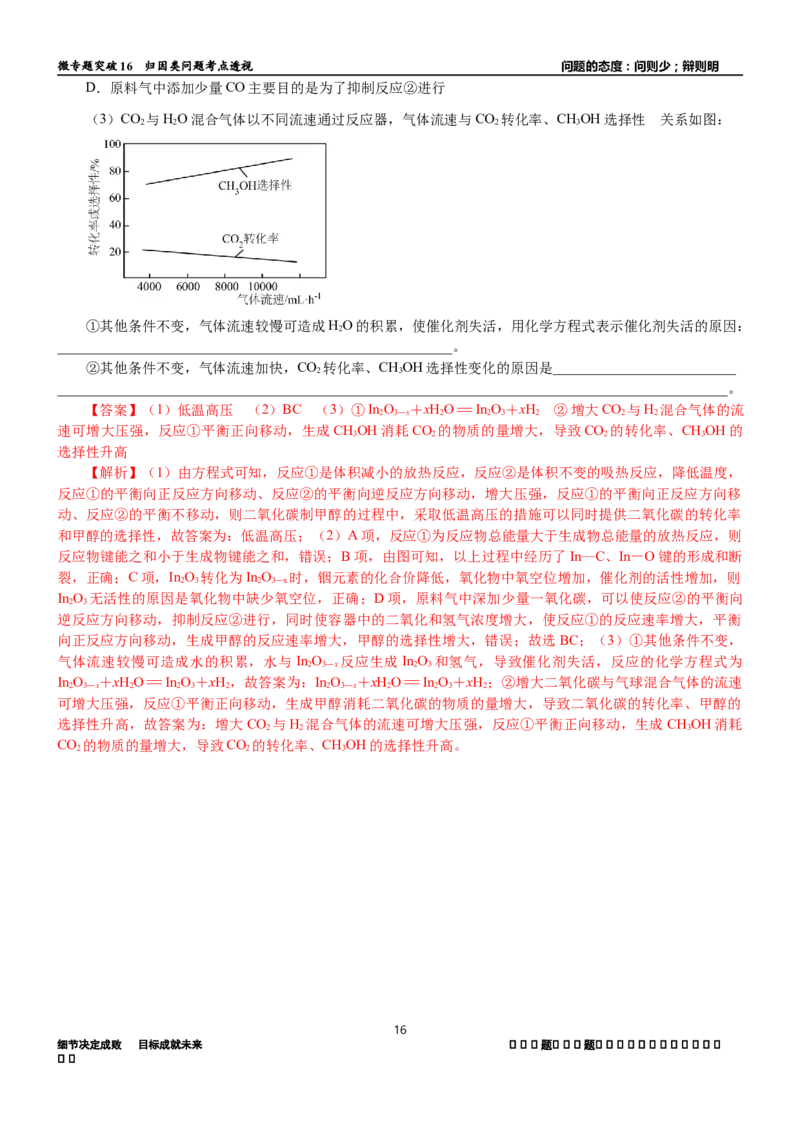
5.(2024·南通市海安市高三上学期开学考)CO 资源化利用是解决资源和能源短缺、减少碳排放的一种
2
途径。
Ⅰ.CO 制甲醇,过程如下:
2
i.催化剂活化:InO(无活性) InO (有活性)
2 3 2 3—x
ii.CO 与H 在活化后的催化剂表面可逆的发生如下反应:
2 2
反应①:CO(g)+3H(g) CHOH(g)+HO(g) ∆H=-49 kJ·mol-1,其反应历程如图;
2 2 3 2 1
反应②:CO(g)+H(g) CO(g)+HO(g) ∆H=+41 kJ·mol-1。
2 2 2 2
已知:CHOH选择性=。
3
(1)CO 制甲醇的过程中,为同时提高CO 平衡转化率和CHOH的选择性,可采取的措施为
2 2 3
________________________。
(2)关于反应①历程,以下描述正确的是___________。(填序号)。
A.反应物键能之和大于生成物键能之和
B.以上过程中经历了In—C、In—O键的形成和断裂
C.InO 无活性的可能原因是InO 结构中缺少氧空位
2 3 2 3微专题突破16 归因类问题考点透视 问题的态度:问则少;辩则明
D.原料气中添加少量CO主要目的是为了抑制反应②进行
的
(3)CO 与HO混合气体以不同流速通过反应器,气体流速与CO 转化率、CHOH选择性 关系如图:
2 2 2 3
①其他条件不变,气体流速较慢可造成HO的积累,使催化剂失活,用化学方程式表示催化剂失活的原因:
2
________________________________________________________。
②其他条件不变,气体流速加快,CO 转化率、CHOH选择性变化的原因是__________________________
2 3
_______________________________________________________________________________________________。
【答案】(1)低温高压 (2)BC (3)①InO +xHO=InO+xH ②增大CO 与H 混合气体的流
2 3—x 2 2 3 2 2 2
速可增大压强,反应①平衡正向移动,生成CHOH消耗CO 的物质的量增大,导致CO 的转化率、CHOH的
3 2 2 3
选择性升高
【解析】(1)由方程式可知,反应①是体积减小的放热反应,反应②是体积不变的吸热反应,降低温度,
反应①的平衡向正反应方向移动、反应②的平衡向逆反应方向移动,增大压强,反应①的平衡向正反应方向移
动、反应②的平衡不移动,则二氧化碳制甲醇的过程中,采取低温高压的措施可以同时提供二氧化碳的转化率
和甲醇的选择性,故答案为:低温高压;(2)A项,反应①为反应物总能量大于生成物总能量的放热反应,则
反应物键能之和小于生成物键能之和,错误;B项,由图可知,以上过程中经历了In—C、In-O键的形成和断
裂,正确;C项,InO 转化为InO 时,铟元素的化合价降低,氧化物中氧空位增加,催化剂的活性增加,则
2 3 2 3—x
InO 无活性的原因是氧化物中缺少氧空位,正确;D项,原料气中深加少量一氧化碳,可以使反应②的平衡向
2 3
逆反应方向移动,抑制反应②进行,同时使容器中的二氧化和氢气浓度增大,使反应①的反应速率增大,平衡
向正反应方向移动,生成甲醇的反应速率增大,甲醇的选择性增大,错误;故选 BC;(3)①其他条件不变,
气体流速较慢可造成水的积累,水与InO 反应生成InO 和氢气,导致催化剂失活,反应的化学方程式为
2 3—x 2 3
InO +xHO=InO +xH ,故答案为:InO +xHO=InO +xH ;②增大二氧化碳与气球混合气体的流速
2 3—x 2 2 3 2 2 3—x 2 2 3 2
可增大压强,反应①平衡正向移动,生成甲醇消耗二氧化碳的物质的量增大,导致二氧化碳的转化率、甲醇的
选择性升高,故答案为:增大CO 与H 混合气体的流速可增大压强,反应①平衡正向移动,生成 CHOH消耗
2 2 3
CO 的物质的量增大,导致CO 的转化率、CHOH的选择性升高。
2 2 3
16
细节决定成败 目标成就未来 找找找题找找找题找找找找找找找找找找找找
找找