文档内容
押江苏卷第 13 题
化学反应速率与化学平衡
核心考点 考情统计 考向预测 备考策略
1.化学反应速率及化学平衡往往
2023·江苏卷,13 结合图表信息,对化学平衡的影响
因素、平衡转化率进行综合考查;
化学反应速率
2022·江苏卷,13
结合多平衡图像综合考查平衡移
与化学平衡 动、转化率、选择性等知识点 2.能运用浓度、压强、温度对化
2021·江苏卷,14
学平衡的影响规律,推测平衡移动
方向及浓度、转化率等相关物理量
的变化
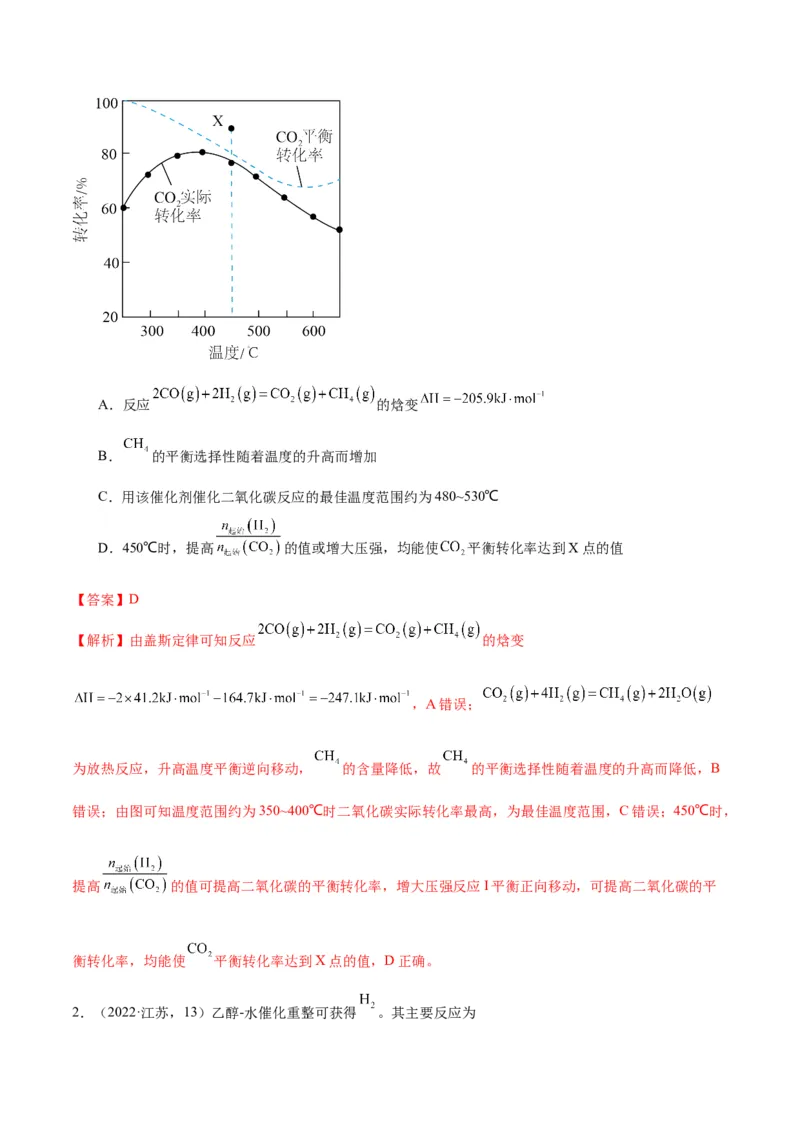
1.(2023·江苏,13)二氧化碳加氢制甲烷过程中的主要反应为
在密闭容器中, 、 时, 平衡转化率、在催化剂作用下反应相同
时间所测得的 实际转化率随温度的变化如题图所示。 的选择性可表示为 。下列
说法正确的是A.反应 的焓变
B. 的平衡选择性随着温度的升高而增加
C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃
D.450℃时,提高 的值或增大压强,均能使 平衡转化率达到X点的值
【答案】D
【解析】由盖斯定律可知反应 的焓变
,A错误;
为放热反应,升高温度平衡逆向移动, 的含量降低,故 的平衡选择性随着温度的升高而降低,B
错误;由图可知温度范围约为350~400℃时二氧化碳实际转化率最高,为最佳温度范围,C错误;450℃时,
提高 的值可提高二氧化碳的平衡转化率,增大压强反应I平衡正向移动,可提高二氧化碳的平
衡转化率,均能使 平衡转化率达到X点的值,D正确。
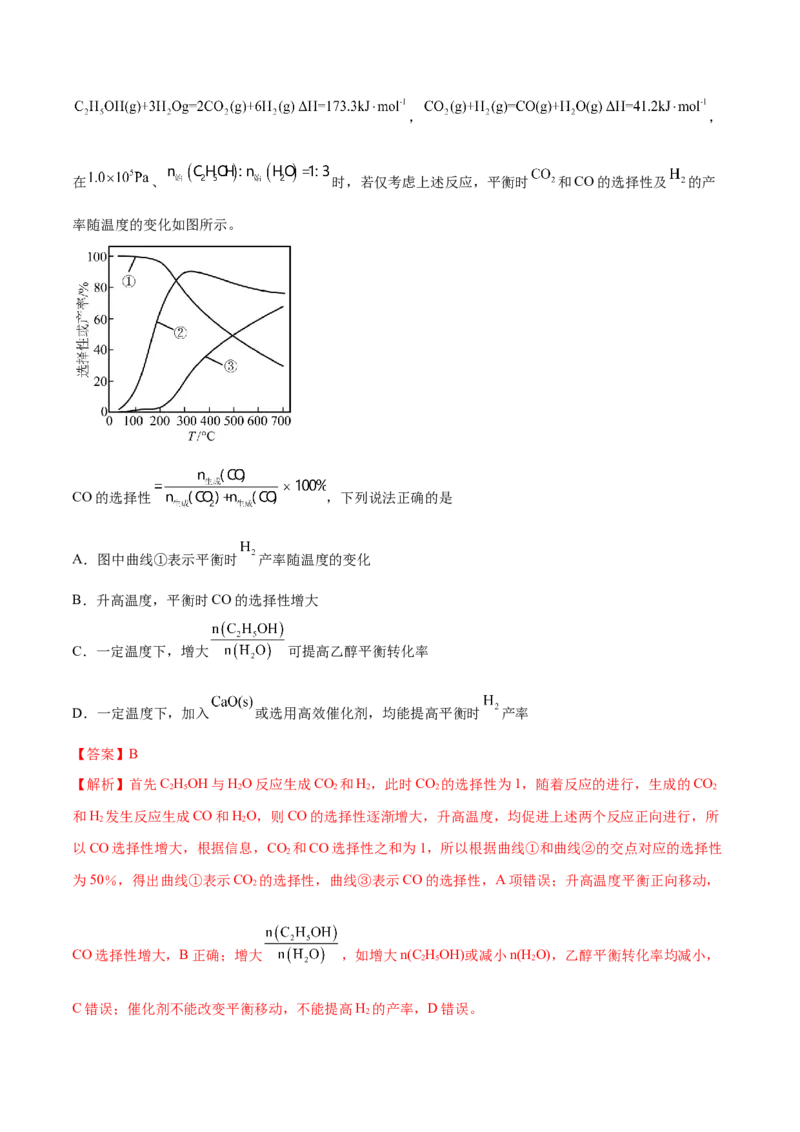
2.(2022·江苏,13)乙醇-水催化重整可获得 。其主要反应为, ,
在 、 时,若仅考虑上述反应,平衡时 和CO的选择性及 的产
率随温度的变化如图所示。
CO的选择性 ,下列说法正确的是
A.图中曲线①表示平衡时 产率随温度的变化
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入 或选用高效催化剂,均能提高平衡时 产率
【答案】B
【解析】首先C HOH与HO反应生成CO 和H,此时CO 的选择性为1,随着反应的进行,生成的CO
2 5 2 2 2 2 2
和H 发生反应生成CO和HO,则CO的选择性逐渐增大,升高温度,均促进上述两个反应正向进行,所
2 2
以CO选择性增大,根据信息,CO 和CO选择性之和为1,所以根据曲线①和曲线②的交点对应的选择性
2
为50%,得出曲线①表示CO 的选择性,曲线③表示CO的选择性,A项错误;升高温度平衡正向移动,
2
CO选择性增大,B正确;增大 ,如增大n(C HOH)或减小n(H O),乙醇平衡转化率均减小,
2 5 2
C错误;催化剂不能改变平衡移动,不能提高H 的产率,D错误。
23.(2021·江苏,14)NH 与O 作用分别生成N、NO、NO的反应均为放热反应。工业尾气中的NH 可
3 2 2 2 3
通过催化氧化为N 除去。将一定比例的NH 、O 和N 的混合气体以一定流速通过装有催化剂的反应管,
2 3 2 2
NH 的转化率、生成N 的选择性[ 100%]与温度的关系如图所示。
3 2
下列说法正确的是
A.其他条件不变,升高温度,NH 的平衡转化率增大
3
B.其他条件不变,在175~300 ℃范围,随温度的升高,出口处N 和氮氧化物的量均不断增大
2
C.催化氧化除去尾气中的NH 应选择反应温度高于250 ℃
3
D.高效除去尾气中的NH ,需研发低温下NH 转化率高和N 选择性高的催化剂
3 3 2
【答案】D
【解析】NH 与O 作用分别生成N、NO、NO的反应均为放热反应,根据勒夏特列原理,升高温度,平
3 2 2 2
衡向逆反应方向进行,氨气的平衡转化率降低,A错误;根据图像,在175~300 ℃范围,随温度的升高,
N 的选择率降低,即产生氮气的量减少,B错误;根据图像,温度高于250℃ N 的选择率降低,且氨气的
2 2
转化率变化并不大,浪费能源,根据图像,温度应略小于225℃,此时氨气的转化率、氮气的选择率较大,
C错误;氮气对环境无污染,氮的氧化物污染环境,因此高效除去尾气中的NH ,需研发低温下NH 转化
3 3
率高和N 选择性高的催化剂,D正确。
2
1.化学平衡移动方向的判断
(1)根据浓度商(Q)规则判断:若某温度下Q<K,则反应向正反应方向进行;Q>K,反应向逆反应方向进
行。
(2)根据化学平衡移动原理判断在一定条件下,aA(g)+bB(g)mC(g) ΔH<0达到平衡后,若其他条件不变,改变下列条件对平衡的影
响如下:
改变的条件(其他条件不变) 化学平衡的移动
增大反应物浓度或减小生成物浓度 向正反应方向移动
浓度
减小反应物浓度或增大生成物浓度 向逆反应方向移动
压强(对于 增大压强 向气体总体积减小的方向移动
a+b≠m
有气体存 减小压强 向气体总体积增大的方向移动
在的反应) a+b=m 改变压强 平衡不移动
升高温度 向吸热方向移动
温度
降低温度 向放热方向移动
催化剂 使用催化剂 平衡不移动
2.化工生产适宜条件选择的一般原则
条件 原则
从化学反应速率分析 既不能过快,又不能太慢
既要注意外界条件对速率和平衡影响的一致性,又要注意
从化学平衡移动分析
二者影响的矛盾性
增加易得廉价原料,提高难得高价原料的利用率,从而降
从原料的利用率分析
低生产成本
从实际生产能力分析 如设备承受高温、高压能力等
从催化剂的使用活性分析 注意温度对催化剂活性的限制
3.多重平衡定性分析
(1) 找准目标物质及所在反应,根据原理(勒夏特列原理以及影响速率的因素等)推断条件改变的影响,作出
判断。
(2) 竞争型多重平衡解题思路
①先分析是速率问题,还是平衡问题。
②若是速率问题,考虑温度、压强、投料比、催化剂选择性等。
③若是平衡问题,先判断以哪个反应为主,再描述平衡移动。
④若改变条件出现两种相反的结论,要结合问题中的结论抓住矛盾的主要方面解题。
(3)有关多重平衡及选择性的问题
在多重平衡中,几个可逆反应是相互影响的。
①如果主反应的生成物又与主反应的某一反应物发生另一个可逆反应,那么该反应物的平衡转化率就会增
大。
②在一定温度下,特定的混合体系,多重平衡选择性为定值。因为平衡常数不变,催化剂的选用与品种无
关。催化剂不能提高某一物质的平衡转化率。
③如果在同一条件下,两个物质同时可以发生几个可逆反应,那么催化剂的选用就可以使其中某一反应的选择性提高。
④多重平衡体系中随着温度的增加,如果两个物质的选择之和等于 100%,那么两者的选择性变化曲线呈
镜像对称。
考点 化学反应速率与化学平衡
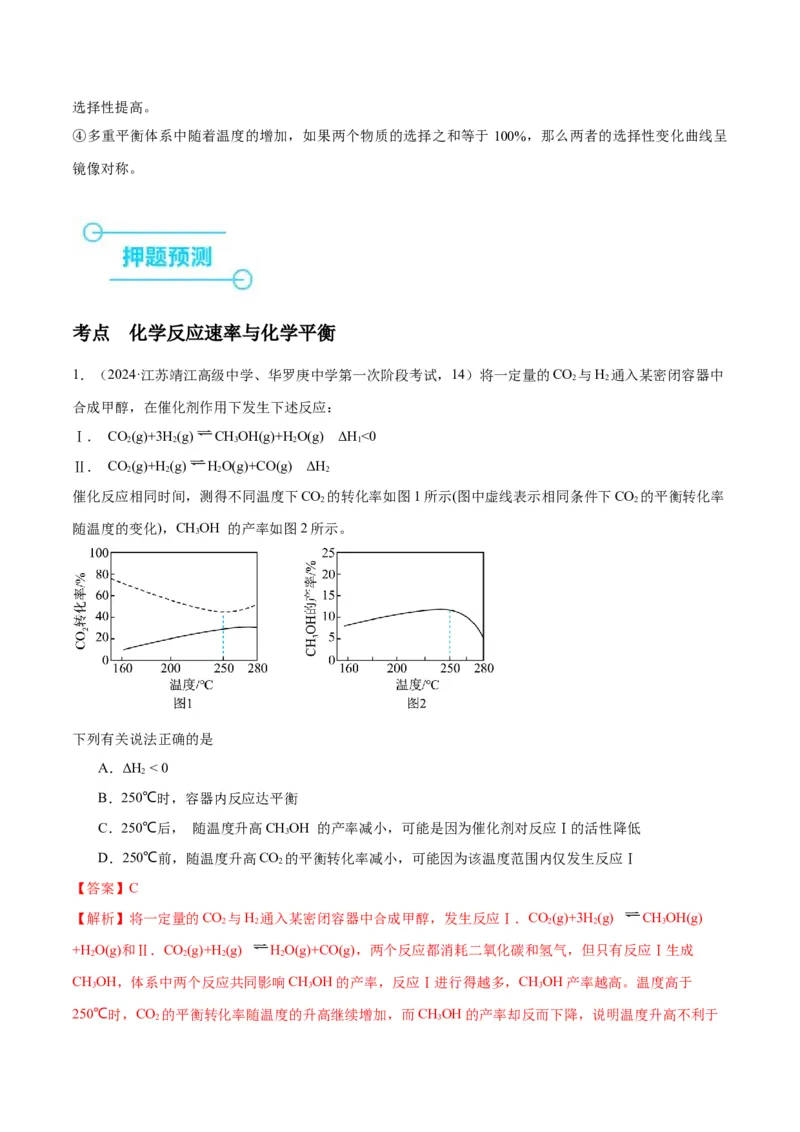
1.(2024·江苏靖江高级中学、华罗庚中学第一次阶段考试,14)将一定量的CO 与H 通入某密闭容器中
2 2
合成甲醇,在催化剂作用下发生下述反应:
Ⅰ. CO(g)+3H(g) CHOH(g)+H O(g) ΔH<0
2 2 3 2 1
Ⅱ. CO(g)+H(g) HO(g)+CO(g) ΔH
2 2 2 2
催化反应相同时间,测得不同温度下CO 的转化率如图1所示(图中虚线表示相同条件下CO 的平衡转化率
2 2
随温度的变化),CHOH 的产率如图2所示。
3
下列有关说法正确的是
A.ΔH < 0
2
B.250℃时,容器内反应达平衡
C.250℃后, 随温度升高CHOH 的产率减小,可能是因为催化剂对反应Ⅰ的活性降低
3
D.250℃前,随温度升高CO 的平衡转化率减小,可能因为该温度范围内仅发生反应Ⅰ
2
【答案】C
【解析】将一定量的CO 与H 通入某密闭容器中合成甲醇,发生反应Ⅰ.CO(g)+3H(g) CHOH(g)
2 2 2 2 3
+H O(g)和Ⅱ.CO(g)+H(g) HO(g)+CO(g),两个反应都消耗二氧化碳和氢气,但只有反应Ⅰ生成
2 2 2 2
CHOH,体系中两个反应共同影响CHOH的产率,反应Ⅰ进行得越多,CHOH产率越高。温度高于
3 3 3
250℃时,CO 的平衡转化率随温度的升高继续增加,而CHOH的产率却反而下降,说明温度升高不利于
2 3CO 转化为甲醇,温度升高有利CO 转化为CO,反应Ⅱ是吸热反应,ΔH>0,A错误;由图1可知250℃
2 2 2
时CO 的转化率不是最大值,温度高于250℃时,CO 的转化率继续增加,说明容器内反应还没有达到平
2 2
衡,B错误;250℃后,随着温度升高,CHOH的产率减小,说明升高温度抑制了反应Ⅰ的进行,可能是
3
因为催化剂对反应Ⅰ的活性降低,C正确;250℃前,随着温度升高,CO 的平衡转化率减小,原因是升高
2
温度对反应Ⅰ的抑制效果大于对反应Ⅱ的促进效果,不是因为该温度范围内仅发生反应Ⅰ,D错误。
2.(2024·江苏泰州中学期初调研,13)用草酸二甲酯 (H COOCCOOCH )和氢气为原料制备乙二醇的反
3 3
应原理如下:
在 条件下,将氢气和草酸二甲酯体积比(氢酯比)为 的混合气体以一定流速通过装有催化剂的反
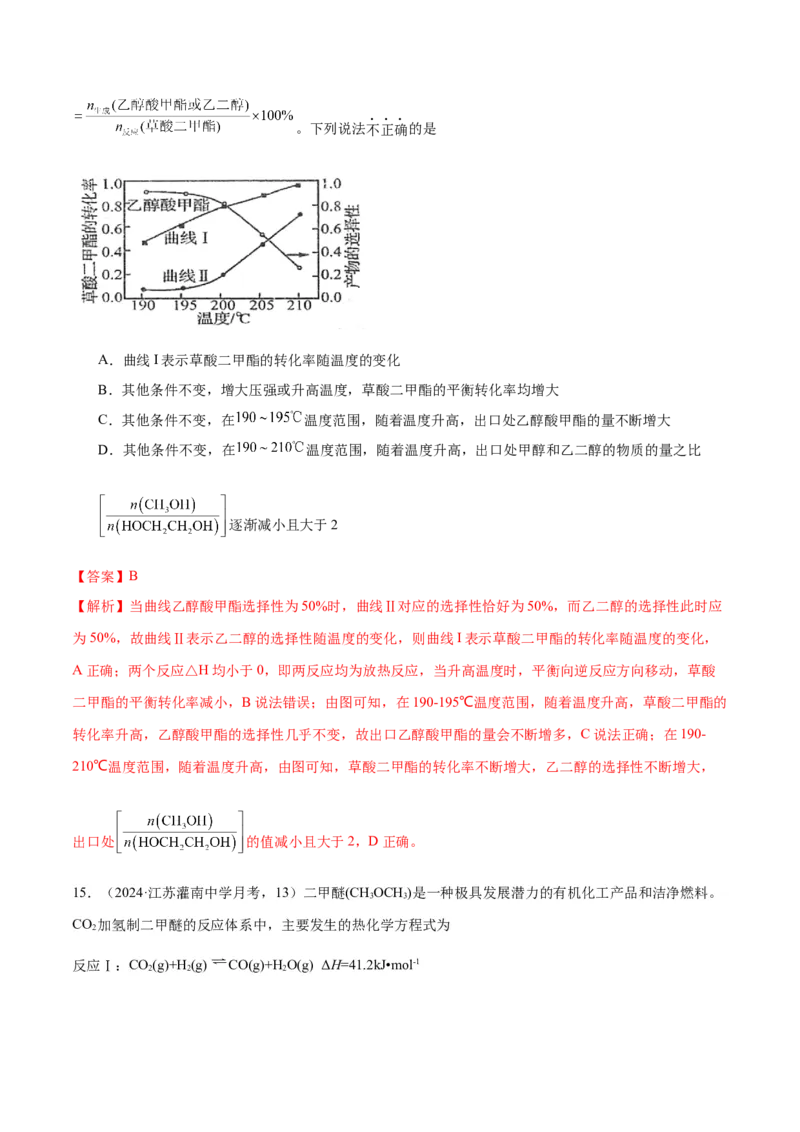
应管,草酸二甲酯的转化率、产物的选择性与温度的关系如下图所示。产物的选择性
。下列说法不正确的是
A.曲线I表示草酸二甲酯的转化率随温度的变化
B.其他条件不变,增大压强或升高温度,草酸二甲酯的平衡转化率均增大
C.其他条件不变,在 温度范围,随着温度升高,出口处乙醇酸甲酯的量不断增大
D.其他条件不变,在 温度范围,随着温度升高,出口处甲醇和乙二醇的物质的量之比
逐渐减小且大于2
【答案】B
【解析】当曲线乙醇酸甲酯选择性为50%时,曲线Ⅱ对应的选择性恰好为50%,而乙二醇的选择性此时应为50%,故曲线Ⅱ表示乙二醇的选择性随温度的变化,则曲线I表示草酸二甲酯的转化率随温度的变化,
A正确;两个反应△H均小于0,即两反应均为放热反应,当升高温度时,平衡向逆反应方向移动,草酸
二甲酯的平衡转化率减小,故B错误;由图可知,在190-195℃温度范围,随着温度升高,草酸二甲酯的
转化率升高,乙醇酸甲酯的选择性几乎不变,故出口乙醇酸甲酯的量会不断增多,C正确;在190-210℃温
度范围,随着温度升高,由图可知,草酸二甲酯的转化率不断增大,乙二醇的选择性不断增大,出口处
的值减小且大于2,D正确。
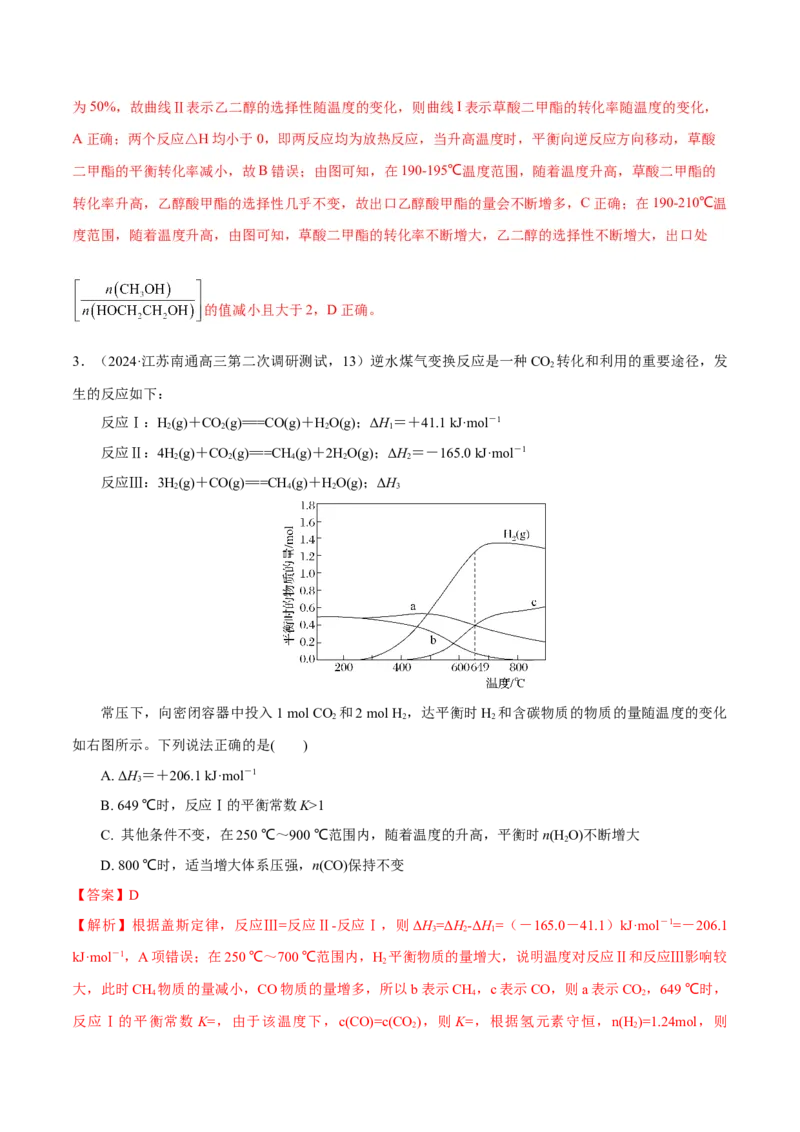
3.(2024·江苏南通高三第二次调研测试,13)逆水煤气变换反应是一种CO 转化和利用的重要途径,发
2
生的反应如下:
反应Ⅰ:H(g)+CO(g)===CO(g)+HO(g);ΔH=+41.1 kJ·mol-1
2 2 2 1
反应Ⅱ:4H(g)+CO(g)===CH (g)+2HO(g);ΔH=-165.0 kJ·mol-1
2 2 4 2 2
反应Ⅲ:3H(g)+CO(g)===CH (g)+HO(g);ΔH
2 4 2 3
常压下,向密闭容器中投入1 mol CO 和2 mol H ,达平衡时H 和含碳物质的物质的量随温度的变化
2 2 2
如右图所示。下列说法正确的是( )
A. ΔH=+206.1 kJ·mol-1
3
B. 649 ℃时,反应Ⅰ的平衡常数K>1
C. 其他条件不变,在250 ℃~900 ℃范围内,随着温度的升高,平衡时n(H O)不断增大
2
D. 800 ℃时,适当增大体系压强,n(CO)保持不变
【答案】D
【解析】根据盖斯定律,反应Ⅲ=反应Ⅱ-反应Ⅰ,则ΔH=ΔH-ΔH=(-165.0-41.1)kJ·mol-1=-206.1
3 2 1
kJ·mol-1,A项错误;在250 ℃~700 ℃范围内,H 平衡物质的量增大,说明温度对反应Ⅱ和反应Ⅲ影响较
2
大,此时CH 物质的量减小,CO物质的量增多,所以b表示CH ,c表示CO,则a表示CO ,649 ℃时,
4 4 2
反应Ⅰ的平衡常数 K=,由于该温度下,c(CO)=c(CO ),则 K=,根据氢元素守恒,n(H )=1.24mol,则
2 2n(H O)=0.6mol,K=<1,B项错误;根据氢元素守恒,当H 物质的量增加时,HO的物质的量减小,所以
2 2 2
700 ℃之前,n(H O)减小,700 ℃之后,n(H O)增大,C项错误;800 ℃时,n(CH)=0mol,说明反应Ⅱ和反
2 2 4
应Ⅲ逆向进行彻底,仅考虑反应Ⅰ,改变压强对反应Ⅰ的平衡无影响,D项正确。
4.(2024·江苏海安高级中学开学考试,13)逆水煤气变换体系中存在以下两个反应:
反应Ⅰ: ;
反应Ⅱ: 。
在恒压条件下,按 投料比进行反应,含碳物质的平衡体积分数随温度的变化如图所
示。下列说法正确的是
A.反应
B. 点反应Ⅰ的平衡常数 约为1
C.加入合适的催化剂可由 点到 点
D. 后,温度升高,反应Ⅰ的改变程度大于反应Ⅱ导致 转化率明显减小
【答案】B
【解析】根据盖斯定律可知,反应CO(g)+3H
2
(g)⇌CH
4
(g)+H
2
O(g)为反应Ⅱ-反应Ⅰ,由图可知,随着温度
升高,甲烷含量减小,一氧化碳含量增大,则说明随着温度升高,反应Ⅱ逆向移动,反应Ⅰ正向移动,则
反应Ⅰ为吸热反应,ΔH>0,反应Ⅱ为放热反应,ΔH<0,则,ΔH-ΔH <0,A项错误;M点没有甲烷产物,
1 2 2 1
且二氧化碳、一氧化碳含量相等,投料比V(CO ):V(H )=1:1,说明CO 、H 都转化一半,则此时反应Ⅰ
2 2 2 2平衡时二氧化碳、氢气、一氧化碳、水的物质的量相等,反应Ⅰ的平衡常数 K= =1,B项
正确;催化剂不影响化学平衡,主要影响反应速率,故体积分数不会上升,C项错误;500℃后,CO 体积
2
分数明显减小,转化率明显增大,D项错误。
5.(2024·江苏苏州高三期末,13)CH 与CO 重整生成H 和CO的过程中主要发生下列反应:
4 2 2
CH(g)+CO(g)===2H (g)+2CO(g);ΔH=247.1 kJ·mol-1
4 2 2
H(g)+CO(g)===H O(g)+CO(g);ΔH=41.2 kJ·mol-1
2 2 2
在恒压、反应物起始物质的量比n(CH)∶n(CO)=1∶1条件下,CH 和CO 的平衡转化率随温度变化的曲
4 2 4 2
线如图所示。下列有关说法正确的是( )
A. 曲线A表示CH 的平衡转化率随温度的变化。
4
B. 工业上为提高H 和CO的产率,需要研发低温下的高效催化剂
2
C. 高于900 K时,随着温度升高,平衡体系中逐渐减小
D. 恒压,800 K、n(CH)∶n(CO)=1∶1条件下,反应至CH 转化率达到X点的值,延长反应时间,CH
4 2 4 4
转化率能达到Y点的值
【答案】D
【解析】CH(g)+CO(g)═2H (g)+2CO(g)中CH 和CO 以1:1反应,且CO 也参加H(g)+CO(g)═H O(g)
4 2 2 4 2 2 2 2 2
+CO(g)的反应,导致相同条件下CH 转化率小于CO 的转化率,根据图知,相同温度下转化率:曲线A
4 2
大于曲线B,所以曲线B表示CH 的平衡转化率随温度的变化,A项错误;CH(g)+CO(g)═2H (g)+
4 4 2 2
2CO(g)和H(g)+CO(g)═H O(g)+CO(g)为反应前后气体体积增大的吸热反应,升高温度平衡正向移动,H
2 2 2 2
和CO的产率高,所以应该研发高温下的高效催化剂,B项错误;高于900K时,随着温度升高,率仍然增
大,两个反应的平衡均正向移动,平衡体系中 逐渐增大,C项错误;恒压、800K、n(CH):n(CO)
4 2=1:1 条件下,除了改变温度外,还可以通过改变生成物浓度使平衡正向移动,从而提高反应物转化率,
所以可以通过减小生成物浓度使平衡正向移动来提高CH4转化率,即改变除温度外的特定条件继续反应,
减小生成物浓度CH 转化率能达到Y点的值,充入CO 也能使得CH 转化率达到Y点的值,D项正确。
4 2 4
6.(2024·江苏淮安市5校高三10月份联考,13)一定条件下,将一定量的CO 和H 混合气体通过装有催
2 2
化剂的反应器可得到甲烷。
已知:Ⅰ. CO(g)+H(g)=CO(g)+HO(g);ΔH=+41 kJ·mol-l。
2 2 2
Ⅱ. CO(g)+4H(g)=CH (g)+2HO(g);ΔH=-165 kJ·mol-1。
2 2 4 2
在两种不同催化剂作用下反应相同时间,CO 转化率和生成CH 选择性随温度变化关系如图所示(CH 选择
2 4 4
性= ×100%)。
下列说法不正确的是
A.反应CO(g)+3H(g)=CH (g)+HO(g);ΔH=-206 kJ·mol-1
2 4 2
B.在280 ℃条件下反应制取CH,应选择催化剂A的效果较好
4
C.260~300 ℃间,使用催化剂A或B,升高温度时CH 的产率都增大
4
D.M点可能是该温度下的平衡点,延长反应时间,不一定能提高CH 的产率
4
【答案】D
【解析】根据盖斯定律反应Ⅱ-反应Ⅰ可得CO(g)+3H(g)=CH (g)+HO(g) ΔH=-165 kJ·mol-1-41 kJ·mol-
2 4 2
l=-206 kJ·mol-1,A正确;据图可知在280 ℃条件下反应,使用催化剂A时CH 的选择性更高,B正确;由
4
图可知,260~300 ℃间,使用催化剂A或B,升高温度时CO 的转化率都增大,CH 的选择性都增大,则
2 4
产率都增大,C正确;据图可知选用催化剂A时,在与M点相同温度条件下,CO 有更高的转化率,而催
2
化剂不影响平衡,说明M点一定不是平衡点,D错误。7.(2024·江苏南京、盐城高三期末,13)乙醇-水催化重整可获得 。其主要反应为
在密闭容器中, 、起始 时,若仅考虑上述反应,平衡时
的体积分数随温度的变化如题图所示。下列说法项正确的是
A.一定温度下,增大 可提高乙醇平衡转化率
B.反应 的
C.研发高效催化剂可提高 的平衡产率
D.控制反应的最佳温度约为
【答案】D
【解析】 ,增大 ,相当于减少HO的投入,平衡逆
2向移动,乙醇平衡转化率减小,A项错误;已知① ,
② ,所以反应
可为②-①, ,B项错误;催化剂不影响平衡的移动,C项错
误;由图可知,温度在约为 时,H 的物质的体积分数最大,而且温度继续升高变化不大,所以反应
2
的最佳温度约为 ,D项正确。
8.(2024·江苏常州高三11月期中,13)工业上用 和 的高温气相反应制备苯硫酚( ),
其主要反应为:
已知:高温下, 热解形成 和 , 与卤代苯中C-X的碳成键,首先形成中间体 ,反
应速率较慢;中间体再迅速脱去 ,形成苯硫酚,将 的混合气以一定流速(反
应停留时间45s)通过管式反应器,测得 的转化率、 与 的产率随温度的变化如图所示,
下列说法不正确的
A.图中曲线①表示 的产率随温度的变化
B.反应中还可能存在二苯硫醚( )等副产物C.一定温度下,增大 一定可提高 的产率
D.保持其他条件不变,若改用 作原料,可提高卤代苯的转化率
【答案】C
【解析】由题给信息可知,高温条件下氯苯与硫化氢生成硫酚的反应速率快于生成苯的反应速率,由图可
知,反应①的反应速率快于反应②,所以曲线①表示硫酚的产率随温度的变化,A正确;由题给信息可知,
高温条件下氯苯与硫化氢生成硫酚的反应速率快于生成苯的反应速率,则反应生成的硫酚可能发生取代反
应生成二苯硫醚,B正确;由题给方程式可知,一定温度下,增大 的值,题给两个反应均能
向正反应方向移动,则二苯硫醚和苯的产率均可能增大,C错误;溴元素的电负性小于氯元素,碳溴键易
于碳氯键断裂,则保持其他条件不变,若改用溴苯作原料,可提高卤代苯的转化率,D正确。
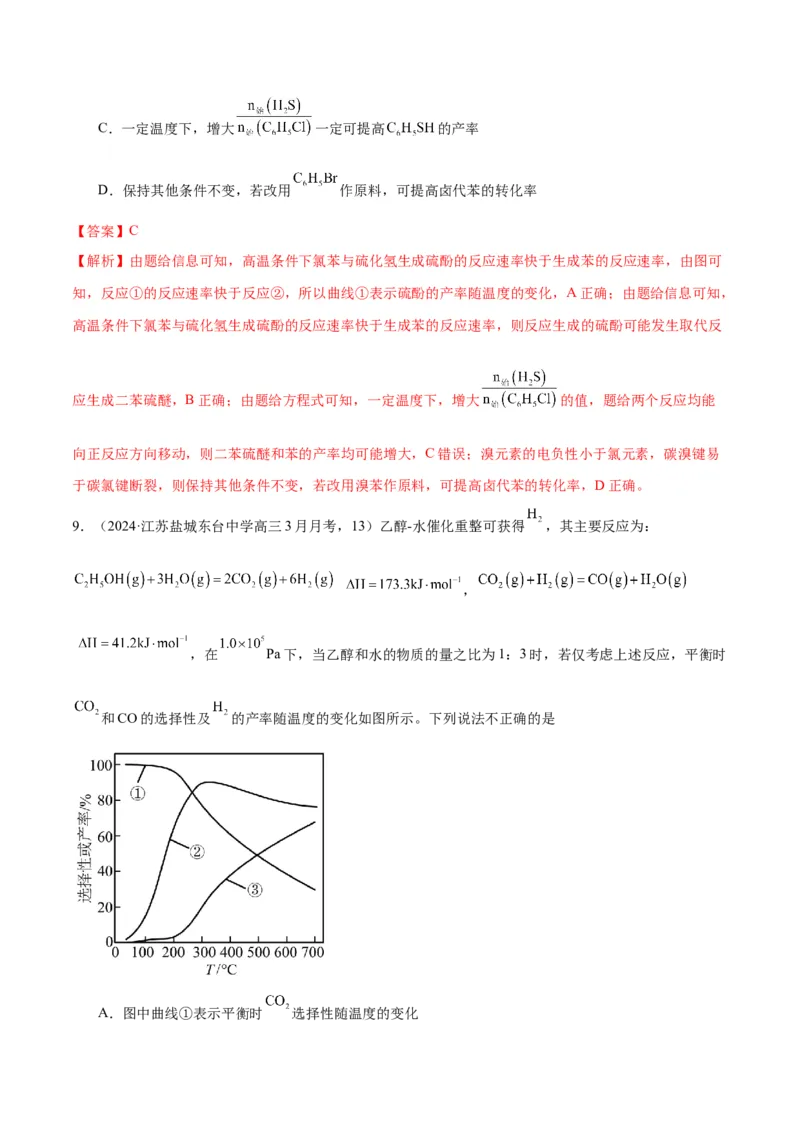
9.(2024·江苏盐城东台中学高三3月月考,13)乙醇-水催化重整可获得 ,其主要反应为:
,
,在 Pa下,当乙醇和水的物质的量之比为1:3时,若仅考虑上述反应,平衡时
和CO的选择性及 的产率随温度的变化如图所示。下列说法不正确的是
A.图中曲线①表示平衡时 选择性随温度的变化B.升高温度,平衡时 产率和CO选择性均增大
C.一定温度下,增大 或适当减压,均可提高乙醇平衡转化率
D.一定温度下,加入少量生石灰或者熟石灰固体,均能提高平衡时 产率
【答案】B
【解析】根据已知反应C
2
H
5
OH(g)+3H
2
O(g)⇌2CO
2
(g)+6H
2
(g)ΔH=173.3 kJ/molⅠ;②CO
2
(g)+H
2
(g)⇌CO(g)
+H O(g)ΔH=41.2 Ⅱ,可知Ⅰ的热效应更大,故温度升高时对反应Ⅰ的影响更大一些,即二氧化碳
2
选择性减小,同时CO的选择性增大,根据CO的选择性定义可知③代表一氧化碳的选择性,①代表CO
2
的选择性,②代表氢气的产率。由分析可知,曲线①表示平衡时CO 选择性随温度的变化,A正确;升高
2
温度,反应Ⅰ、反应Ⅱ平衡右移,生成的CO增多,CO选择性增大,消耗的H 也增多,H 产率先增大后
2 2
减小,B错误;两种物质参加反应,增大 ,即相对来说n(C HOH)不变,增大
2 5
n(H O),HO的浓度增大,会使化学平衡向正反应方向移动,适当减压,也会使平衡正向移动,从而可提
2 2
高乙醇的平衡转化率,C正确;加入生石灰或熟石灰固体能吸附CO,促进反应正向进行,可以提高H 的
2 2
产率,D正确。
10.(2024·江苏百师联盟高三开学考试,13)压强一定的条件下,将 和 按一定流
速通过装有催化剂的反应管,利用 催化加氢制乙二醇。主要发生如下反应:
ⅰ.
ⅱ.
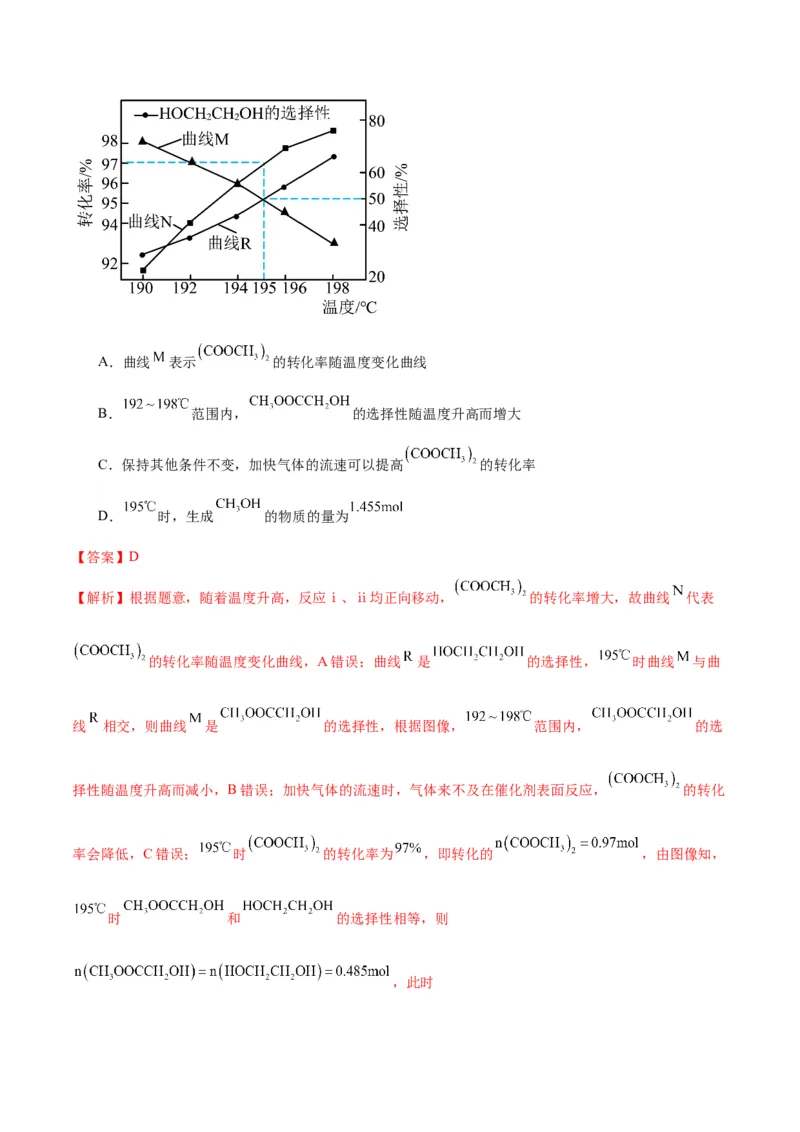
测得 的转化率及 的选择性与温度的关系如图所示。已知:选
择性定义为 。下列说法正确的是A.曲线 表示 的转化率随温度变化曲线
B. 范围内, 的选择性随温度升高而增大
C.保持其他条件不变,加快气体的流速可以提高 的转化率
D. 时,生成 的物质的量为
【答案】D
【解析】根据题意,随着温度升高,反应ⅰ、ⅱ均正向移动, 的转化率增大,故曲线 代表
的转化率随温度变化曲线,A错误;曲线 是 的选择性, 时曲线 与曲
线 相交,则曲线 是 的选择性,根据图像, 范围内, 的选
择性随温度升高而减小,B错误;加快气体的流速时,气体来不及在催化剂表面反应, 的转化
率会降低,C错误; 时 的转化率为 ,即转化的 ,由图像知,
时 和 的选择性相等,则
,此时,D正确。
11.(2024·江苏扬州中学年高三1月月考,13)逆水煤气变换体系中存在以下两个反应:
反应Ⅰ:
反应Ⅱ:
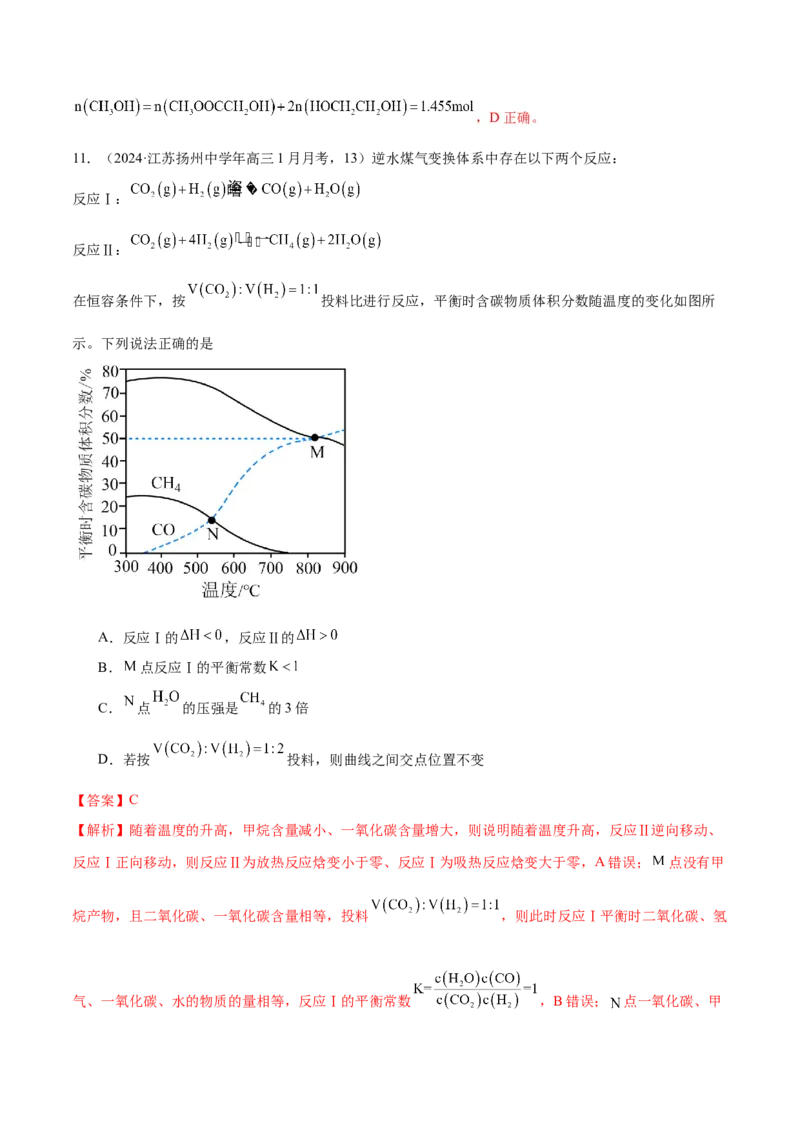
在恒容条件下,按 投料比进行反应,平衡时含碳物质体积分数随温度的变化如图所
示。下列说法正确的是
A.反应Ⅰ的 ,反应Ⅱ的
B. 点反应Ⅰ的平衡常数
C. 点 的压强是 的3倍
D.若按 投料,则曲线之间交点位置不变
【答案】C
【解析】随着温度的升高,甲烷含量减小、一氧化碳含量增大,则说明随着温度升高,反应Ⅱ逆向移动、
反应Ⅰ正向移动,则反应Ⅱ为放热反应焓变小于零、反应Ⅰ为吸热反应焓变大于零,A错误; 点没有甲
烷产物,且二氧化碳、一氧化碳含量相等,投料 ,则此时反应Ⅰ平衡时二氧化碳、氢
气、一氧化碳、水的物质的量相等,反应Ⅰ的平衡常数 ,B错误; 点一氧化碳、甲烷物质的量相等,结合反应方程式的系数可知,生成水的总的物质的量为甲烷的3倍,结合阿伏加德罗定
律可知, 的压强是 的3倍,C正确;反应Ⅰ为气体分子数不变的反应、反应Ⅱ为气体分子数减小
的反应;若按 投料,相当于增加氢气的投料,会使得甲烷含量增大,导致甲烷、一
氧化碳曲线之间交点位置发生改变,D错误。
12.(2024·江苏常熟高三抽测,13) 催化加氢合成甲醇是 资源化利用的重要途径。 催化加氢
主要反应有:
反应Ⅰ
反应Ⅱ
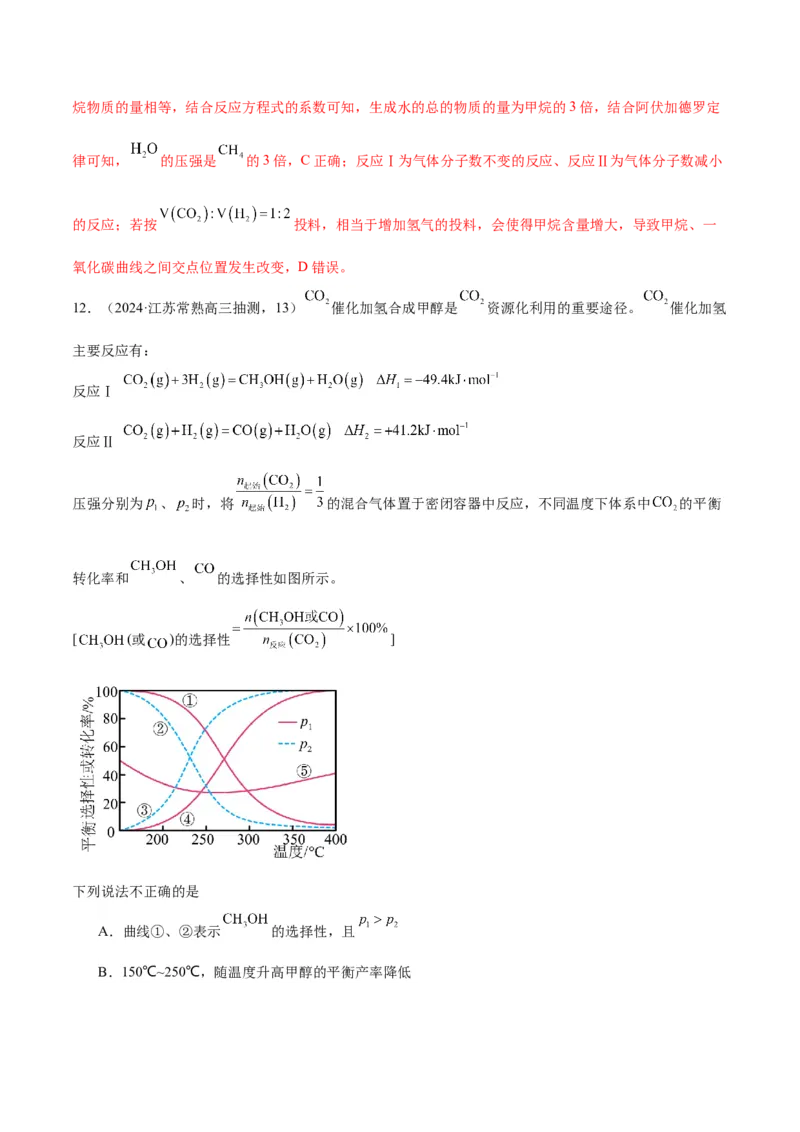
压强分别为 、 时,将 的混合气体置于密闭容器中反应,不同温度下体系中 的平衡
转化率和 、 的选择性如图所示。
[ (或 )的选择性 ]
下列说法不正确的是
A.曲线①、②表示 的选择性,且
B.150℃~250℃,随温度升高甲醇的平衡产率降低C.一定温度下,调整 可提高 的平衡转化率
D.相同温度下,反应Ⅰ和反应Ⅱ的平衡常数
【答案】D
【解析】随着温度的升高,反应Ⅰ平衡逆向移动,反应Ⅱ平衡正向移动,则CHOH的选择性随温度的升
3
高而减小,CO的选择性随温度的升高而增大,故曲线①、②表示CHOH的选择性,曲线③、④表示CO
3
的选择性,同时压强增大,反应Ⅰ平衡正向移动,反应物浓度减小,促使反应Ⅱ化学平衡逆向移动,使
CO选择性减小,故p>p。根据以上分析可知曲线①、②表示 的选择性,且 ,故A正确;
1 2
曲线①、②表示 的选择性,根据图像可知150℃~250℃,随温度升高 的选择性减小,CO的
选择性升高,因此甲醇的平衡产率降低,故B正确;一定温度下,调整 ,相当于增大氢气
的浓度,因此可提高 的平衡转化率,故C正确;随着温度的升高,反应Ⅰ平衡逆向移动,反应Ⅱ平衡
正向移动,在未给定具体温度的情况下,无法比较反应Ⅰ、Ⅱ的化学平衡常数大小,故D错误。
13.(2024·江苏百校联考第二次考试,13)用草酸二甲酯( )和氢气为原料制备乙二醇的
反应原理如下:
在2MPa条件下,将氢气和草酸二甲酯体积比(氢酯比)为80:1的混合气体以一定流速通过装有催化剂的反
应管,草酸二甲酯的转化率、产物的选择性与温度的关系如图所示。产物的选择性
下列说法正确的是
A.曲线I表示乙二醇的选择性随温度的变化
B.其他条件不变,增大压强或升高温度,草酸二甲酯的平衡转化率均增大
C.其他条件不变,在190~195℃温度范围,随着温度升高,出口处乙醇酸甲酯的量不断减小
D.其他条件不变,在190~210℃温度范围,随着温度升高,出口处甲醇和乙二醇的物质的量之比[
]减小
【答案】D
【解析】当曲线乙醇酸甲酯选择性为50%时,曲线Ⅱ对应的选择性恰好为50%,而乙二醇的选择性此时应
为50%,故曲线Ⅱ表示乙二醇的选择性随温度的变化,A错误;两个反应 H均小于0,即两反应均为放热
反应,当升高温度时,平衡向逆反应方向移动,草酸二甲酯的平衡转化率△减小,B错误;由图可知,在
190-195摄氏度温度范围,随着温度升高,草酸二甲酯的转化率升高,乙醇酸甲酯的选择性几乎不变,故
出口乙醇酸甲酯的量会不断增多,C错误;在190-210摄氏度温度范围,随着温度升高,由图可知,草酸
二甲酯的转化率不断增大,乙二醇的选择性不断增大,出口处甲醇和乙二醇的物质的量之比减小,D正确。
14.(2024·江苏扬州中学高三3月月考,13)用草酸二甲酯 (H COOCCOOCH )和氢气为原料制备乙二醇
3 3
的反应原理如下:
在 条件下,将氢气和草酸二甲酯体积比(氢酯比)为 的混合气体以一定流速通过装有催化剂的反
应管,草酸二甲酯的转化率、产物的选择性与温度的关系如下图所示。产物的选择性。下列说法不正确的是
A.曲线I表示草酸二甲酯的转化率随温度的变化
B.其他条件不变,增大压强或升高温度,草酸二甲酯的平衡转化率均增大
C.其他条件不变,在 温度范围,随着温度升高,出口处乙醇酸甲酯的量不断增大
D.其他条件不变,在 温度范围,随着温度升高,出口处甲醇和乙二醇的物质的量之比
逐渐减小且大于2
【答案】B
【解析】当曲线乙醇酸甲酯选择性为50%时,曲线Ⅱ对应的选择性恰好为50%,而乙二醇的选择性此时应
为50%,故曲线Ⅱ表示乙二醇的选择性随温度的变化,则曲线I表示草酸二甲酯的转化率随温度的变化,
A正确;两个反应△H均小于0,即两反应均为放热反应,当升高温度时,平衡向逆反应方向移动,草酸
二甲酯的平衡转化率减小,B说法错误;由图可知,在190-195℃温度范围,随着温度升高,草酸二甲酯的
转化率升高,乙醇酸甲酯的选择性几乎不变,故出口乙醇酸甲酯的量会不断增多,C说法正确;在190-
210℃温度范围,随着温度升高,由图可知,草酸二甲酯的转化率不断增大,乙二醇的选择性不断增大,
出口处 的值减小且大于2,D正确。
15.(2024·江苏灌南中学月考,13)二甲醚(CHOCH )是一种极具发展潜力的有机化工产品和洁净燃料。
3 3
CO 加氢制二甲醚的反应体系中,主要发生的热化学方程式为
2
反应Ⅰ:CO(g)+H(g) CO(g)+HO(g) ΔH=41.2kJ•mol-1
2 2 2反应Ⅱ:CO(g)+3H(g) CHOH(g)+H O(g) ΔH=-495kJ•mol-1
2 2 3 2
反应Ⅲ:2CHOH(g) CHOCH (g)+HO(g) ΔH=-23.5kJ•mol-1
3 3 3 2
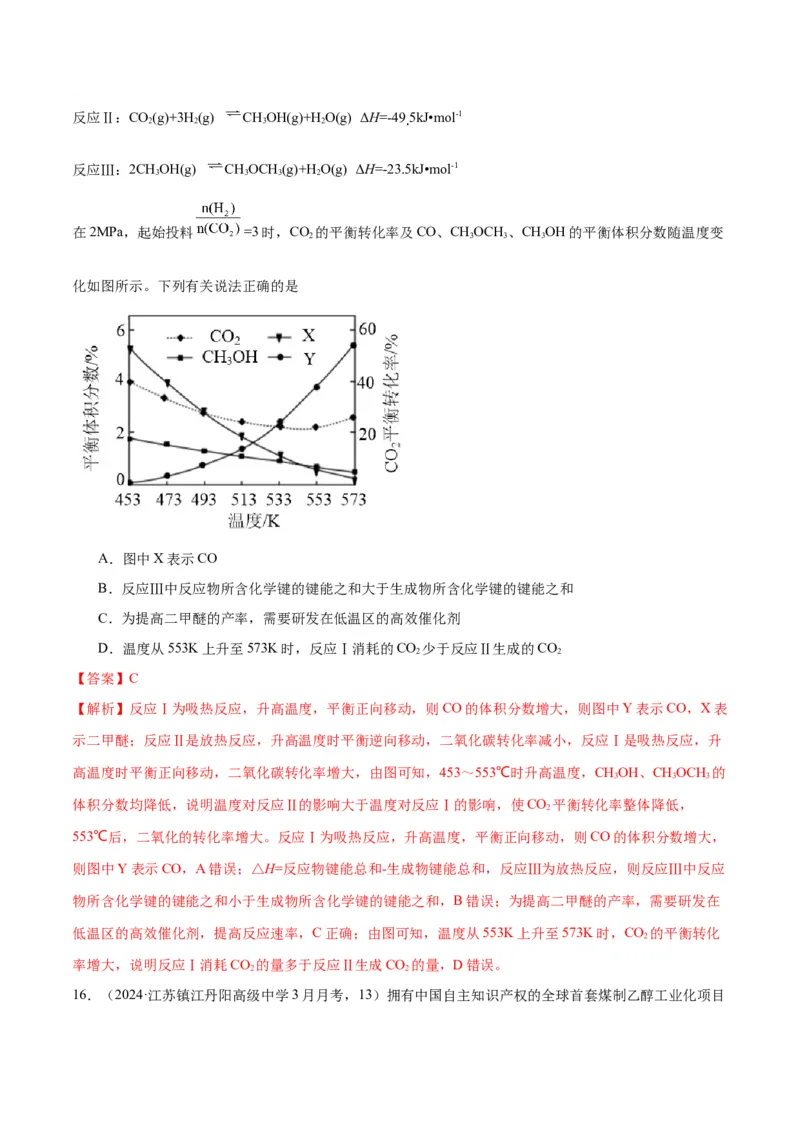
在2MPa,起始投料 =3时,CO 的平衡转化率及CO、CHOCH 、CHOH的平衡体积分数随温度变
2 3 3 3
化如图所示。下列有关说法正确的是
A.图中X表示CO
B.反应Ⅲ中反应物所含化学键的键能之和大于生成物所含化学键的键能之和
C.为提高二甲醚的产率,需要研发在低温区的高效催化剂
D.温度从553K上升至573K时,反应Ⅰ消耗的CO 少于反应Ⅱ生成的CO
2 2
【答案】C
【解析】反应Ⅰ为吸热反应,升高温度,平衡正向移动,则CO的体积分数增大,则图中Y表示CO,X表
示二甲醚;反应Ⅱ是放热反应,升高温度时平衡逆向移动,二氧化碳转化率减小,反应Ⅰ是吸热反应,升
高温度时平衡正向移动,二氧化碳转化率增大,由图可知,453~553℃时升高温度,CHOH、CHOCH 的
3 3 3
体积分数均降低,说明温度对反应Ⅱ的影响大于温度对反应Ⅰ的影响,使CO 平衡转化率整体降低,
2
553℃后,二氧化的转化率增大。反应Ⅰ为吸热反应,升高温度,平衡正向移动,则CO的体积分数增大,
则图中Y表示CO,A错误;△H=反应物键能总和-生成物键能总和,反应Ⅲ为放热反应,则反应Ⅲ中反应
物所含化学键的键能之和小于生成物所含化学键的键能之和,B错误;为提高二甲醚的产率,需要研发在
低温区的高效催化剂,提高反应速率,C正确;由图可知,温度从553K上升至573K时,CO 的平衡转化
2
率增大,说明反应Ⅰ消耗CO 的量多于反应Ⅱ生成CO 的量,D错误。
2 2
16.(2024·江苏镇江丹阳高级中学3月月考,13)拥有中国自主知识产权的全球首套煤制乙醇工业化项目投产成功。某煤制乙醇过程表示如下:
过程a包括以下3个主要反应:
I.
Ⅱ.
Ⅲ.
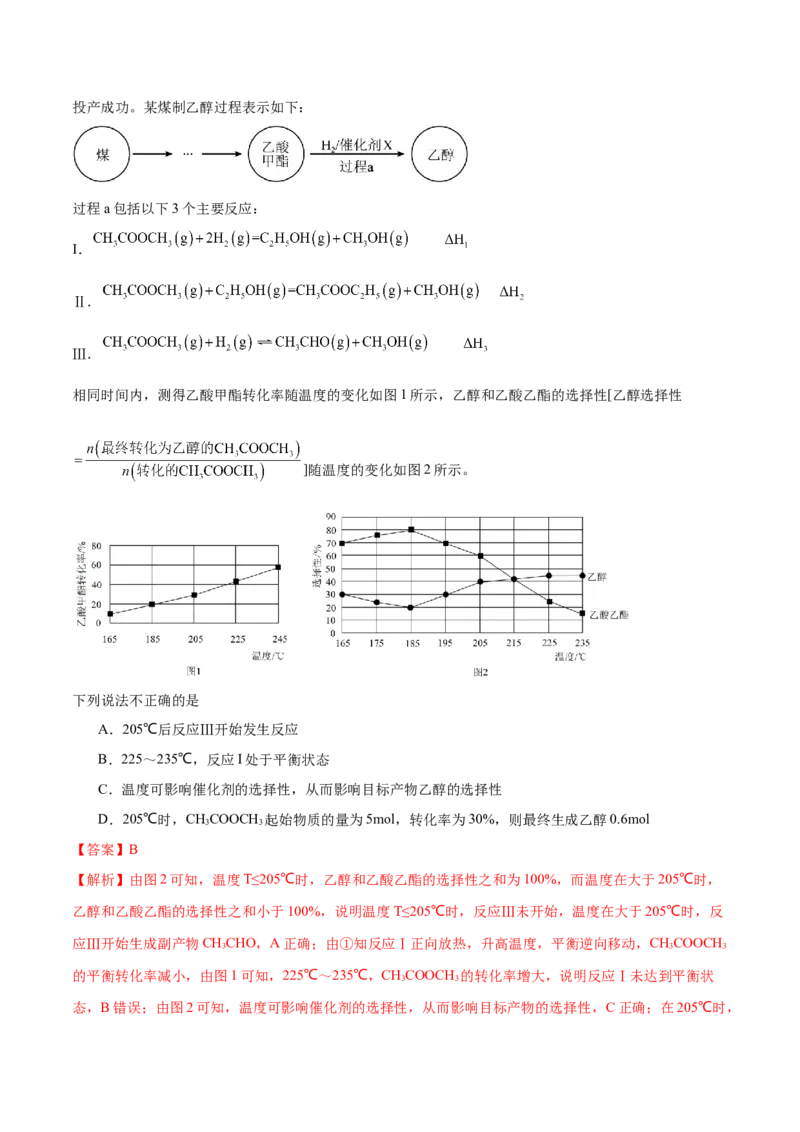
相同时间内,测得乙酸甲酯转化率随温度的变化如图1所示,乙醇和乙酸乙酯的选择性[乙醇选择性
]随温度的变化如图2所示。
下列说法不正确的是
A.205℃后反应Ⅲ开始发生反应
B.225~235℃,反应I处于平衡状态
C.温度可影响催化剂的选择性,从而影响目标产物乙醇的选择性
D.205℃时,CHCOOCH 起始物质的量为5mol,转化率为30%,则最终生成乙醇0.6mol
3 3
【答案】B
【解析】由图2可知,温度T≤205℃时,乙醇和乙酸乙酯的选择性之和为100%,而温度在大于205℃时,
乙醇和乙酸乙酯的选择性之和小于100%,说明温度T≤205℃时,反应Ⅲ未开始,温度在大于205℃时,反
应Ⅲ开始生成副产物CHCHO,A正确;由①知反应Ⅰ正向放热,升高温度,平衡逆向移动,CHCOOCH
3 3 3
的平衡转化率减小,由图1可知,225℃~235℃,CHCOOCH 的转化率增大,说明反应Ⅰ未达到平衡状
3 3
态,B错误;由图2可知,温度可影响催化剂的选择性,从而影响目标产物的选择性,C正确;在205℃时,CHCOOCH 起始物质的量为5mol,转化率为30%,则n(转化的CHCOOCH )=5mol×30%=1.5mol,由图2
3 3 3 3
可知,乙醇的选择性为40%,则n(最终转化为为乙醇的CHCOOCH )=n(转化的
3 3
CHCOOCH )×40%=1.5mol×40%=0.6mol,根据反应Ⅰ可知,生成乙醇的物质的量为0.6mol,D正确。
3 3
17.(2024·江苏南京六校联合体10月调研,13)中国科学家在淀粉人工光合成方面取得重大突破性进展,
该实验方法首先将CO 催化还原为CHOH。已知CO 催化加氢的主要反应有:
2 3 2
①CO(g)+3H(g) CHOH(g)+H O(g) △H=-49.4kJ•mol-1
2 2 3 2 1
②CO (g)+H(g) CO(g)+HO(g) △H=+41.2kJ•mol-1
2 2 2 2
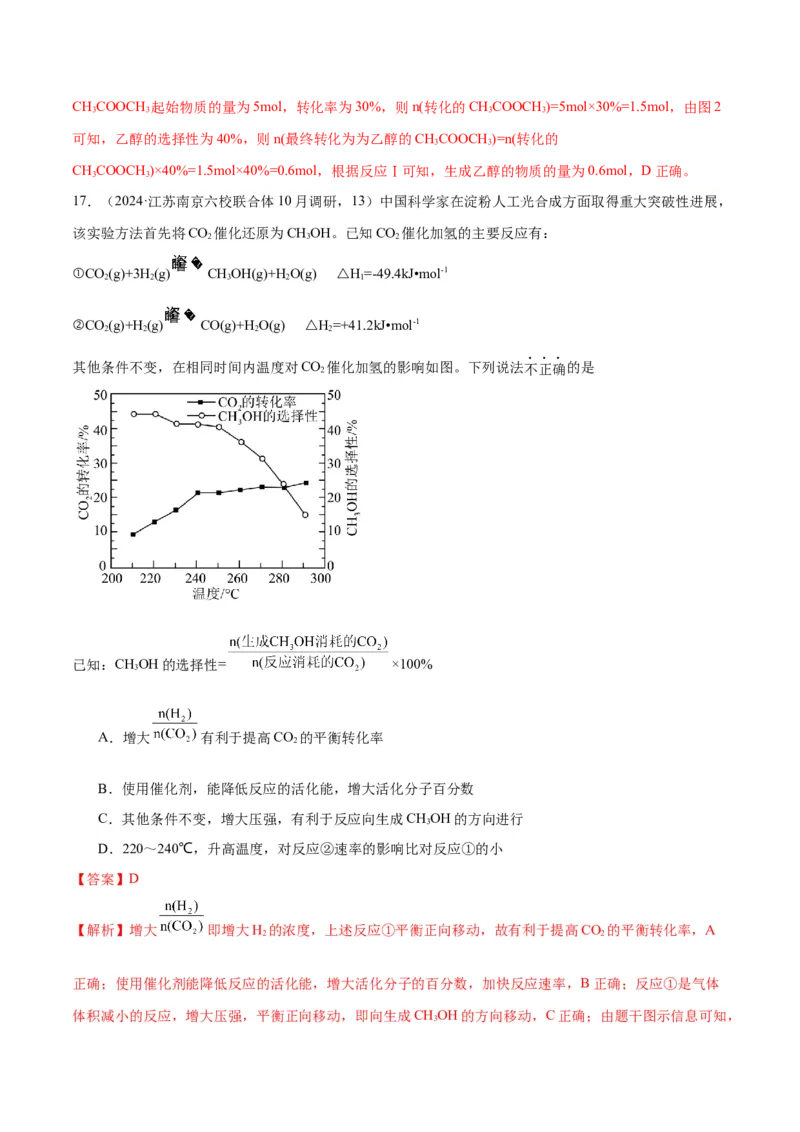
其他条件不变,在相同时间内温度对CO 催化加氢的影响如图。下列说法不正确的是
2
已知:CHOH的选择性= ×100%
3
A.增大 有利于提高CO 的平衡转化率
2
B.使用催化剂,能降低反应的活化能,增大活化分子百分数
C.其他条件不变,增大压强,有利于反应向生成CHOH的方向进行
3
D.220~240℃,升高温度,对反应②速率的影响比对反应①的小
【答案】D
【解析】增大 即增大H 的浓度,上述反应①平衡正向移动,故有利于提高CO 的平衡转化率,A
2 2
正确;使用催化剂能降低反应的活化能,增大活化分子的百分数,加快反应速率,B正确;反应①是气体
体积减小的反应,增大压强,平衡正向移动,即向生成CHOH的方向移动,C正确;由题干图示信息可知,
3220~240℃,升高温度,二氧化碳的转化率增大,但甲醇的选择性下降,说明对反应②速率的影响比对反
应①的大,D错误。
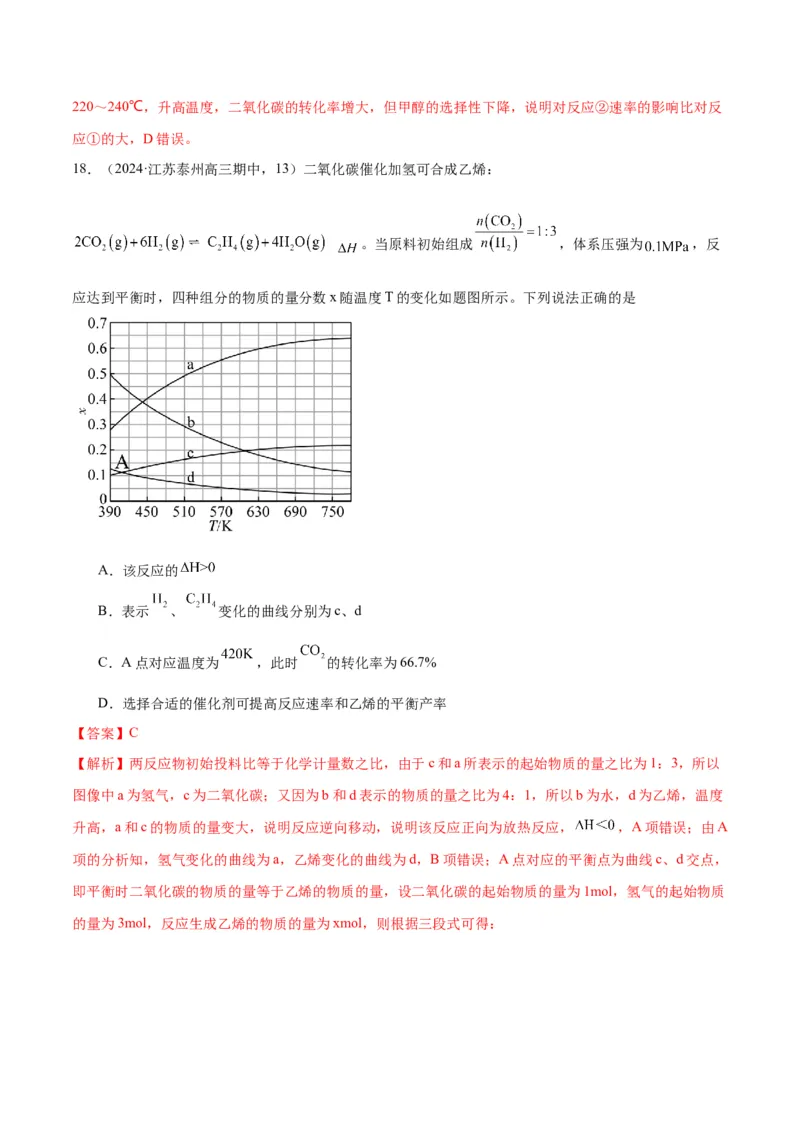
18.(2024·江苏泰州高三期中,13)二氧化碳催化加氢可合成乙烯:
。当原料初始组成 ,体系压强为 ,反
应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图所示。下列说法正确的是
A.该反应的
B.表示 、 变化的曲线分别为c、d
C.A点对应温度为 ,此时 的转化率为66.7%
D.选择合适的催化剂可提高反应速率和乙烯的平衡产率
【答案】C
【解析】两反应物初始投料比等于化学计量数之比,由于c和a所表示的起始物质的量之比为1:3,所以
图像中a为氢气,c为二氧化碳;又因为b和d表示的物质的量之比为4:1,所以b为水,d为乙烯,温度
升高,a和c的物质的量变大,说明反应逆向移动,说明该反应正向为放热反应, ,A项错误;由A
项的分析知,氢气变化的曲线为a,乙烯变化的曲线为d,B项错误;A点对应的平衡点为曲线c、d交点,
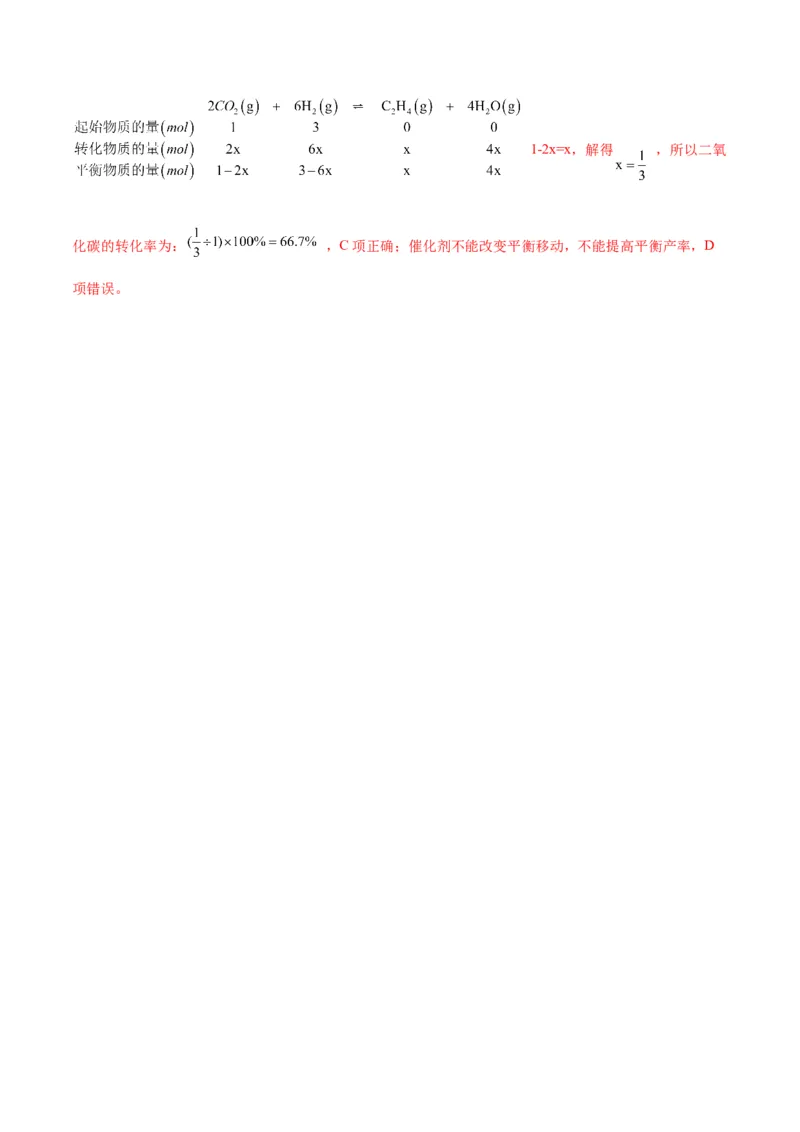
即平衡时二氧化碳的物质的量等于乙烯的物质的量,设二氧化碳的起始物质的量为1mol,氢气的起始物质
的量为3mol,反应生成乙烯的物质的量为xmol,则根据三段式可得:1-2x=x,解得 ,所以二氧
化碳的转化率为: ,C项正确;催化剂不能改变平衡移动,不能提高平衡产率,D
项错误。