文档内容
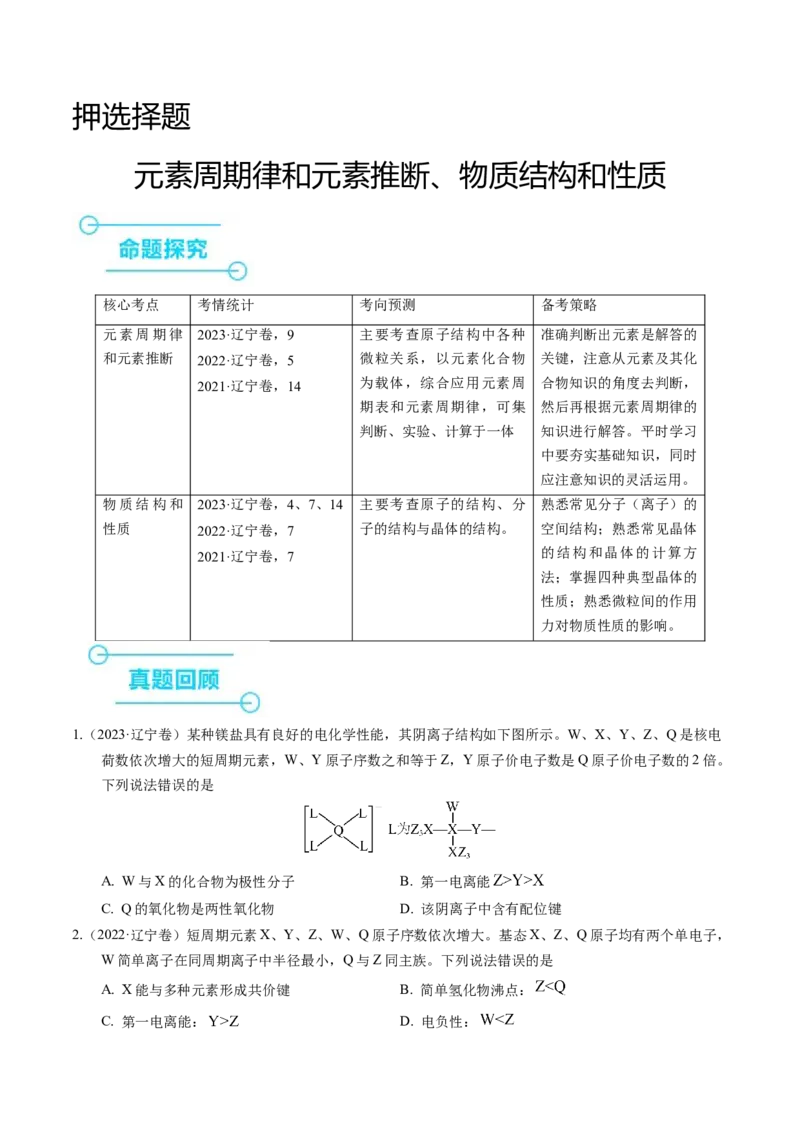
押选择题
元素周期律和元素推断、物质结构和性质
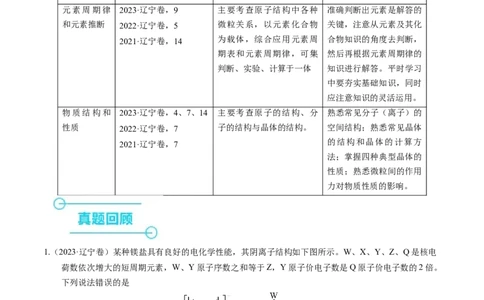
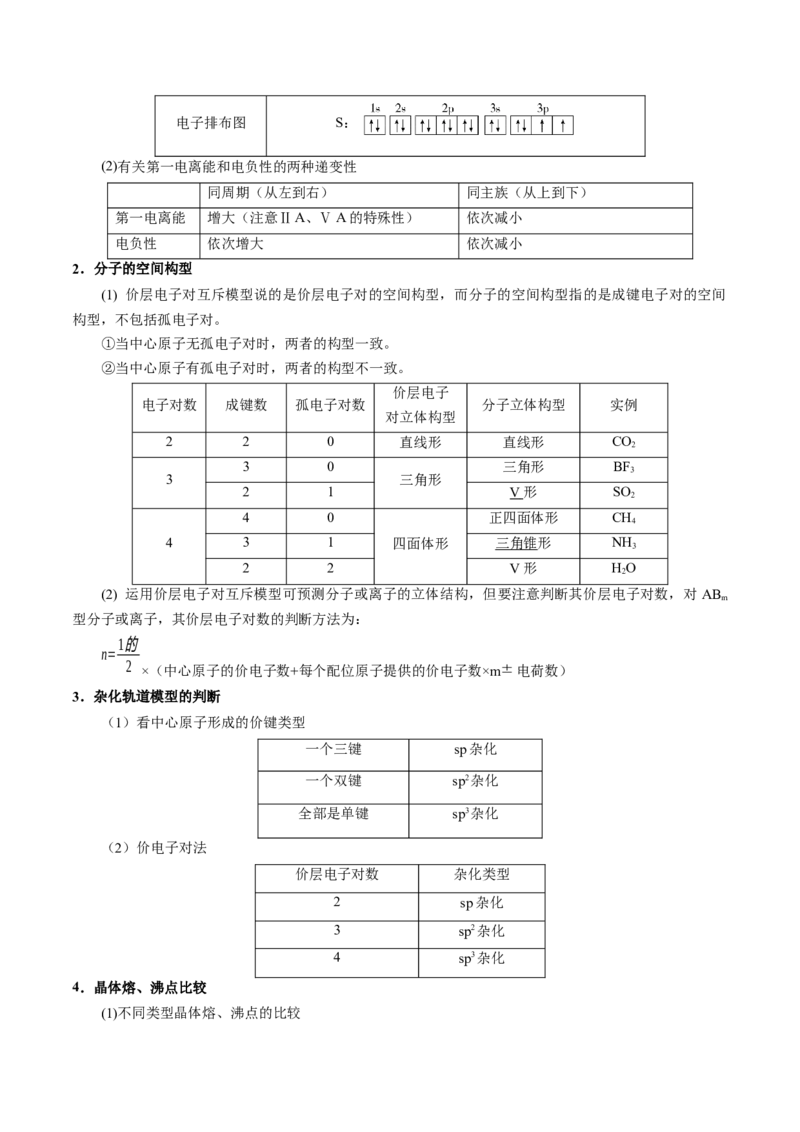
核心考点 考情统计 考向预测 备考策略
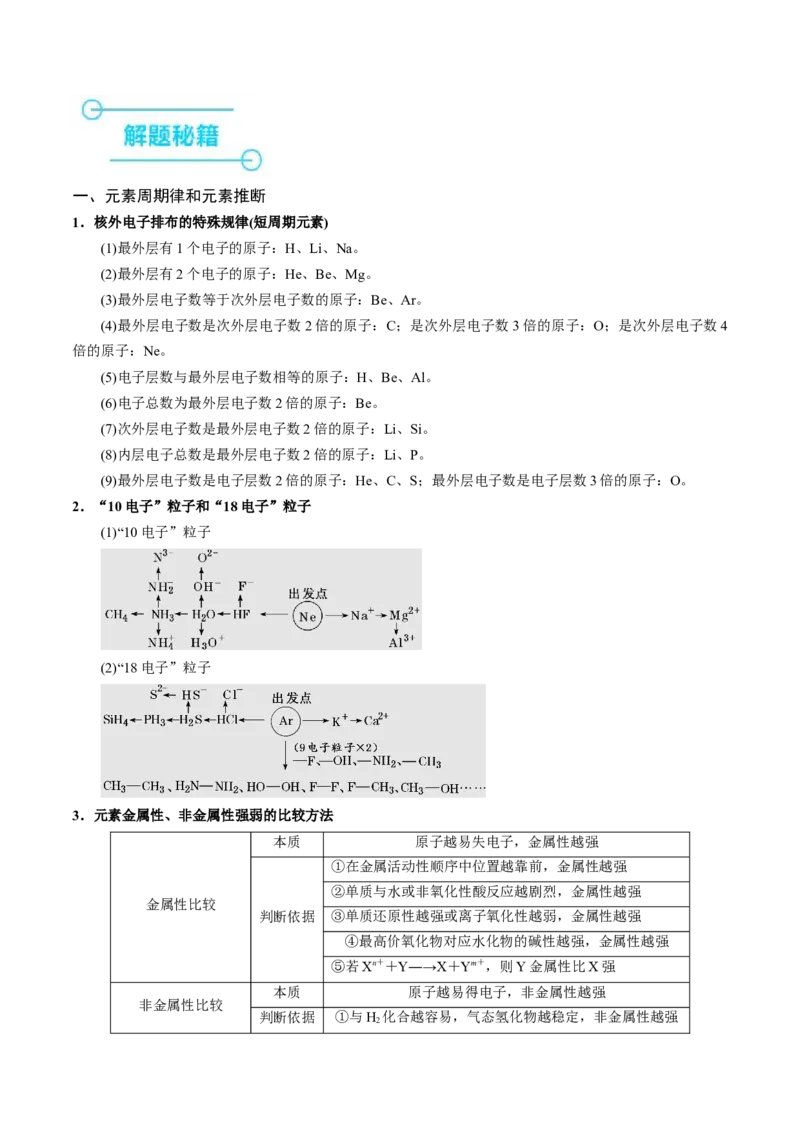
元素周期律 2023·辽宁卷,9 主要考查原子结构中各种 准确判断出元素是解答的
和元素推断 2022·辽宁卷,5 微粒关系,以元素化合物 关键,注意从元素及其化
2021·辽宁卷,14 为载体,综合应用元素周 合物知识的角度去判断,
期表和元素周期律,可集 然后再根据元素周期律的
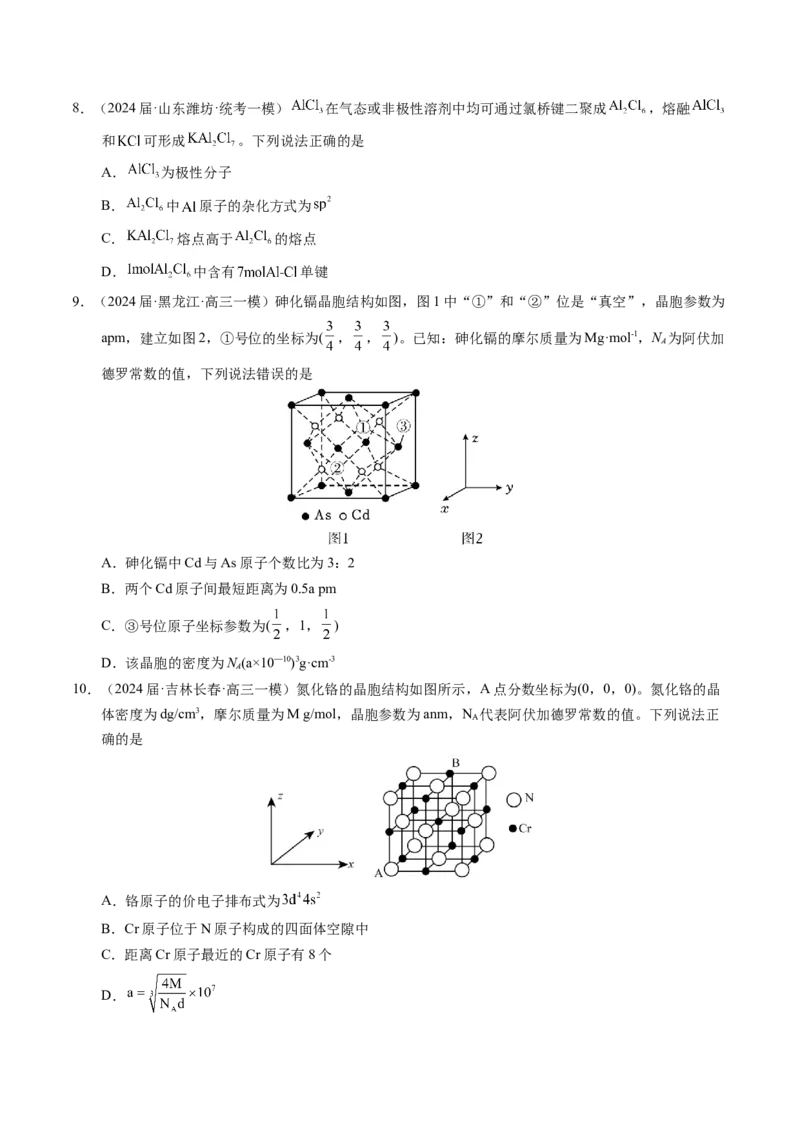
判断、实验、计算于一体 知识进行解答。平时学习
中要夯实基础知识,同时
应注意知识的灵活运用。
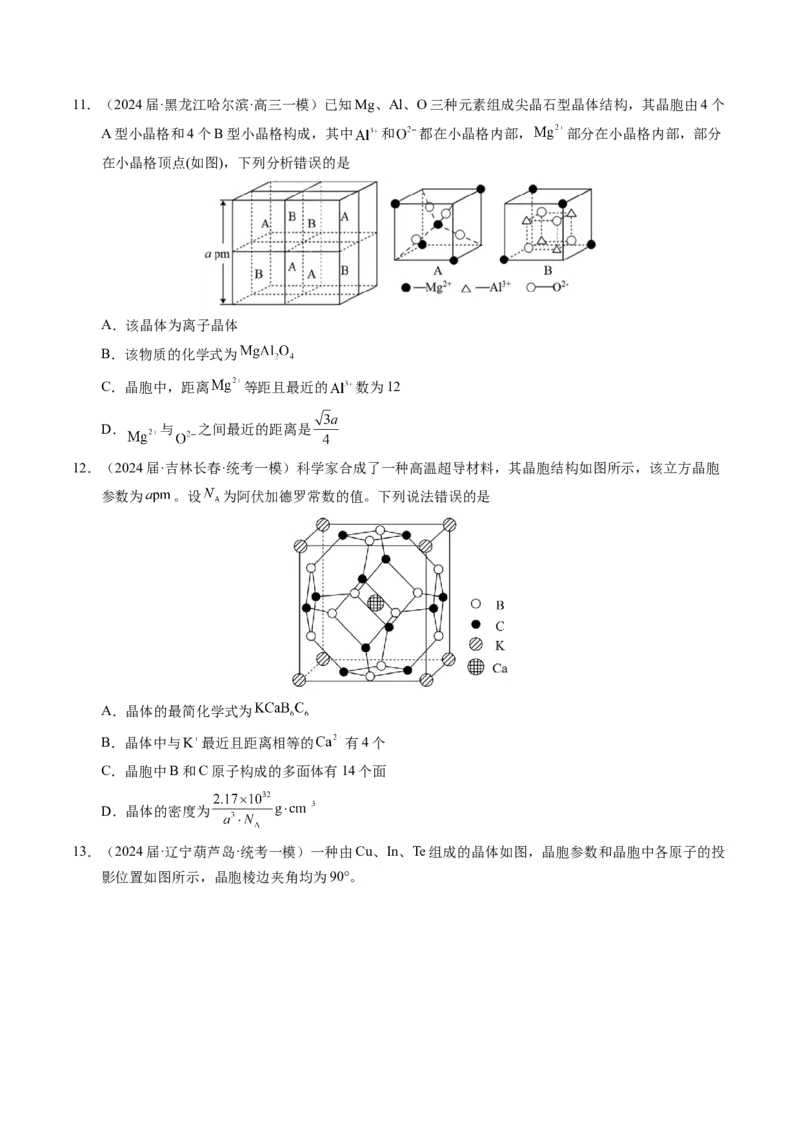
物质结构和 2023·辽宁卷,4、7、14 主要考查原子的结构、分 熟悉常见分子(离子)的
性质 2022·辽宁卷,7 子的结构与晶体的结构。 空间结构;熟悉常见晶体
2021·辽宁卷,7 的结构和晶体的计算方
法;掌握四种典型晶体的
性质;熟悉微粒间的作用
力对物质性质的影响。
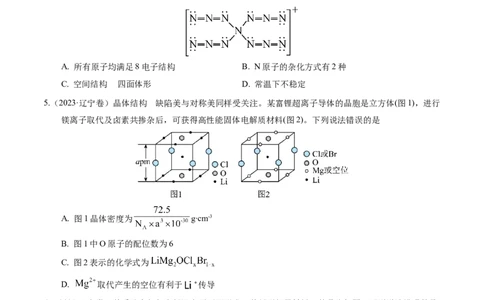
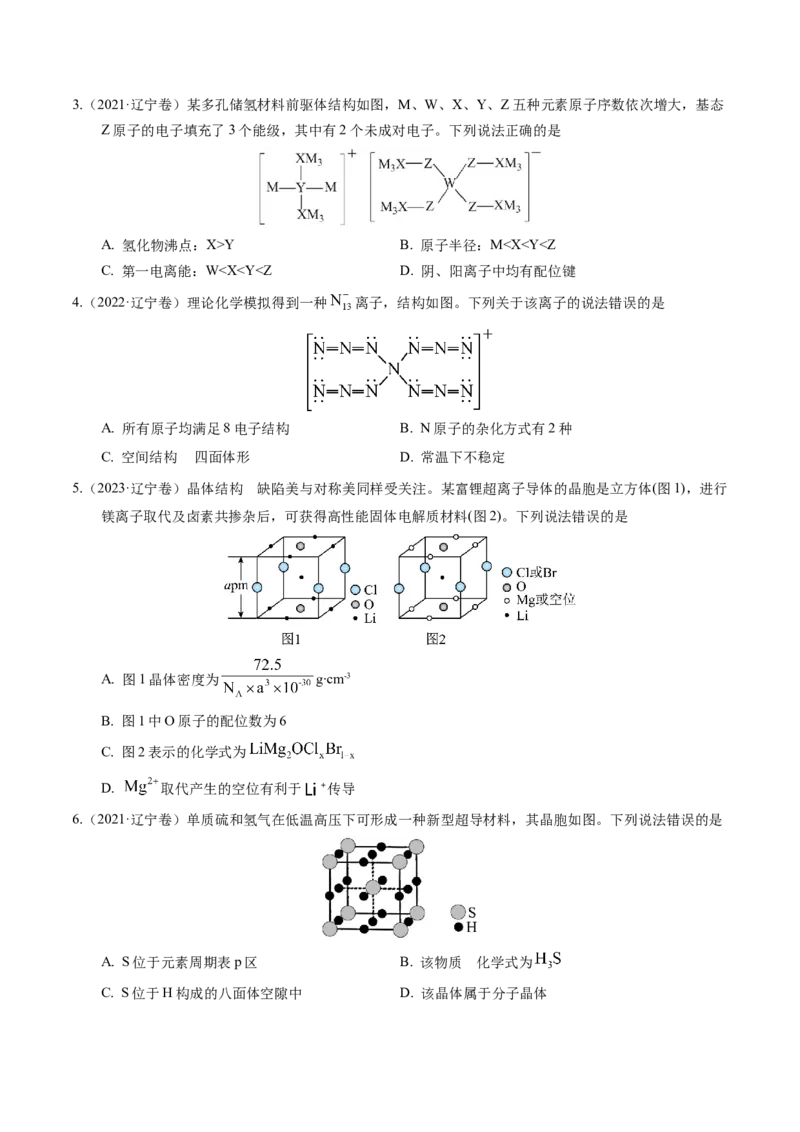
1.(2023·辽宁卷)某种镁盐具有良好的电化学性能,其阴离子结构如下图所示。W、X、Y、Z、Q是核电
荷数依次增大的短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是Q原子价电子数的2倍。
下列说法错误的是
A. W与X的化合物为极性分子 B. 第一电离能
C. Q的氧化物是两性氧化物 D. 该阴离子中含有配位键
2.(2022·辽宁卷)短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均有两个单电子,
W简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误的是
A. X能与多种元素形成共价键 B. 简单氢化物沸点:
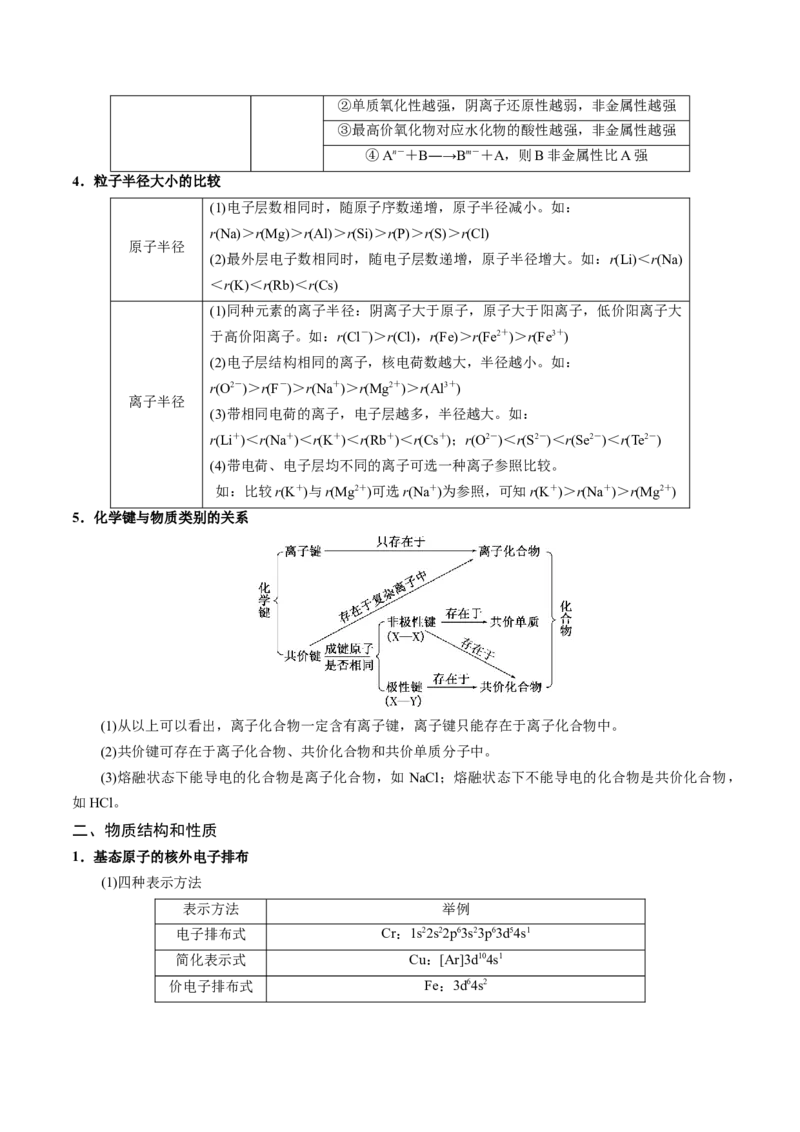
C. 第一电离能: D. 电负性:3.(2021·辽宁卷)某多孔储氢材料前驱体结构如图,M、W、X、Y、Z五种元素原子序数依次增大,基态
Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法正确的是
A. 氢化物沸点:X>Y B. 原子半径:M
3 2 2 2 3
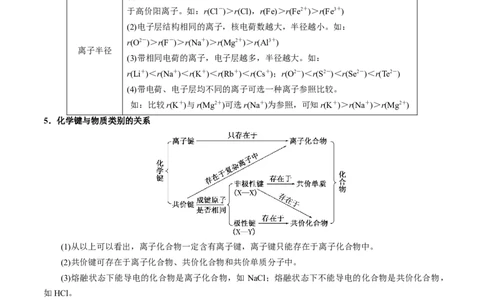
④金属晶体
金属离子半径越小,离子电荷数越多,其金属键越强,金属晶体的熔、沸点越高,如熔、沸点:Na<
Mg<Al。
5.有关晶胞的计算
(1)有关晶胞中的微粒个数的计算
晶胞中粒子的计算应用均摊法,立方体晶胞计算:顶点贡献1/8、棱边1/4、面心1/2、体心1;六棱柱
晶胞计算顶点贡献1/6、侧棱边1/3、其它棱边1/4、面心1/2、体心1,三棱柱晶胞顶点贡献1/12,侧棱边
为1/6,上下棱上为1/4,面上的算为1/2,如果是分子簇团,就不能按照晶胞来计算,应该作为一个整体进
行计数,解题时仔细审题,看清每个粒子的所代表的图形符号及在晶胞中所处的位置。
(2)晶体的密度计算
计算晶体密度的一般思维模型是:(1)求晶胞的质量m,根据摩尔质量(以g·mol−1为单位时在数值
与相对分子质量相同)除以阿伏伽德罗常数计算出每个微粒的质量,再根据计算出晶胞中所含微粒的个数,
从而得出晶胞的总质量=晶胞中所含粒子的个数×每个微粒的质量;(2)求晶胞的体积v,应用立体几何知
识,根据提供的晶胞参数(边长)求出晶胞的体积,如常见的立方晶胞、六棱柱、三棱柱晶体结构单元的
体积计算,注意单位的换算如1nm(纳米)=1×10-9m=1×10-7cm,1pm(皮米)=1×10-12m=1×10-10cm;(3)
再由ρ=m/v,得出其密度,因此晶胞中粒子计算是基础,晶胞体积的计算是关键,注意单位的换算是要留
意的细节,同时要注意密度、晶胞参数、晶胞中粒子个数的之间相互换算的考查,结合阿伏加德罗常数、晶胞体积、密度的计算,可以把微观的晶胞结构和宏观物质的密度、摩尔质量等联系起来,体现高考中
“宏观辨识”与“微观探析”的化学学科核心素养的要求,也贯彻了必备知识与关键能力的考查要求,因
此要引起足够的重视。
(3)有关晶胞参数的计算
晶胞是能完整反映晶体内部原子或离子在三维空间分布结构特征的最小单元的平行六面体。用来表示
晶胞的形状和大小的6个特征参数,简称晶胞参数,包括晶胞的3组棱长(即晶体的轴长)a、b、c和3组
棱相互间的夹角(即晶体的轴角)α、β、γ。高考中晶胞参数a指的是正四面体的边长,通过晶体密度求解晶
胞参数a的基本思路是:通过摩尔质量、阿伏伽德罗常数、晶胞所含微粒数计算出晶胞质量,建立已经密
度与体积的关系,而体积可以通过晶胞参数a进行求解,从而求出a值,同时注意晶胞参数的计算可以延
伸到晶胞中原子坐标、原子间距离、原子半径的考查,因此这不仅仅是化学知识的简单考查,而是要具备
利用数学工具,通过计算和推理解决化学问题的能力要求,高考试题不仅是不同知识点的融合,更是跨越
不同学科间的相互渗透。
(4)有关晶胞中原子占体积百分率的计算
晶胞中原子的体积占晶胞体积的百分率也称为空间利用率,指构成晶体的原子、离子或分子在整个晶
体空间中所占有的体积百分比。晶胞都是平行六面体,整块晶体可以看成是无数晶胞无隙并置而成的,空
间利用率=晶胞中原子的体积之和÷晶胞的总体积×100%,因此计算的关键是:(1)把原子当成球体,根
据原子半径r计算体积为4/3πr3,计算出晶胞中原子的体积之和=晶胞中所含原子个数×4/3πr3;(2)计算
晶胞的总体积,可以通过晶胞参数a进行求解,如立方晶胞时v=a3,其它晶体结构单元结合几何知识求解,
也可以通过晶胞的质量÷晶体密度求解。同时也要注意已知晶胞中原子的空间利用率,然后反推出原子的
半径或者晶胞参数的表达式。
考点一 元素周期律和元素推断
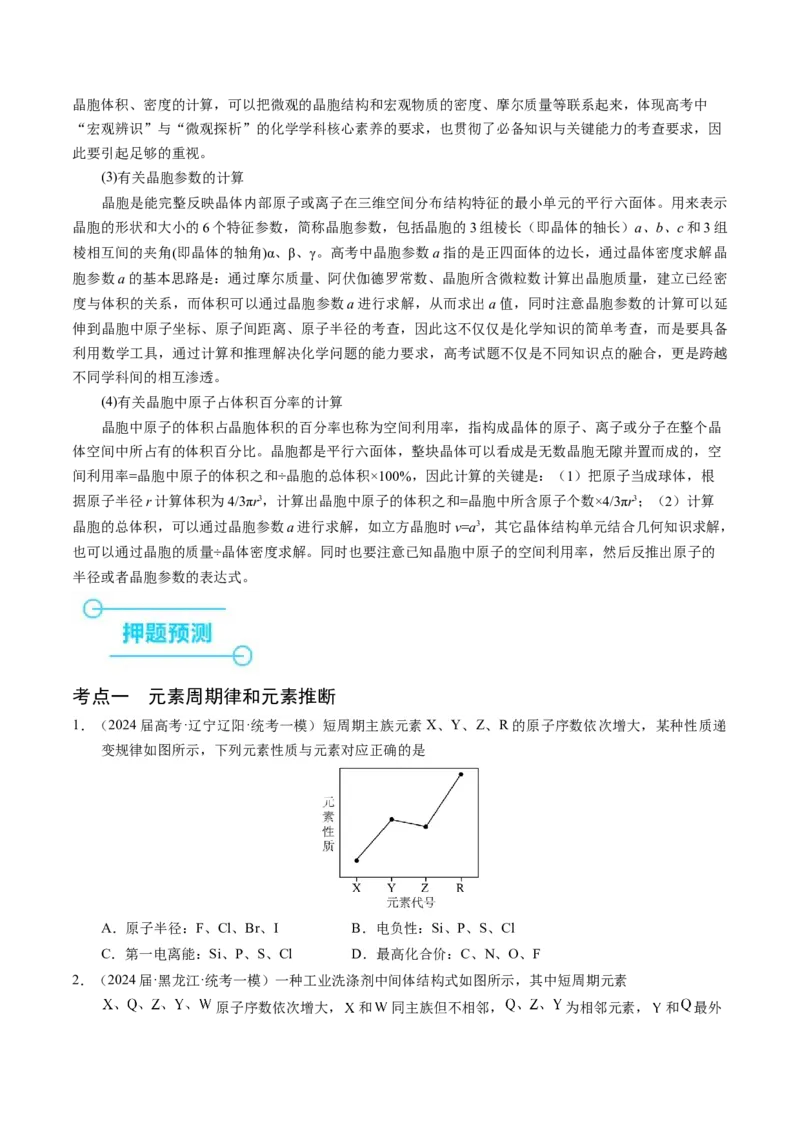
1.(2024届高考·辽宁辽阳·统考一模)短周期主族元素X、Y、Z、R的原子序数依次增大,某种性质递
变规律如图所示,下列元素性质与元素对应正确的是
A.原子半径:F、Cl、Br、I B.电负性:Si、P、S、Cl
C.第一电离能:Si、P、S、Cl D.最高化合价:C、N、O、F
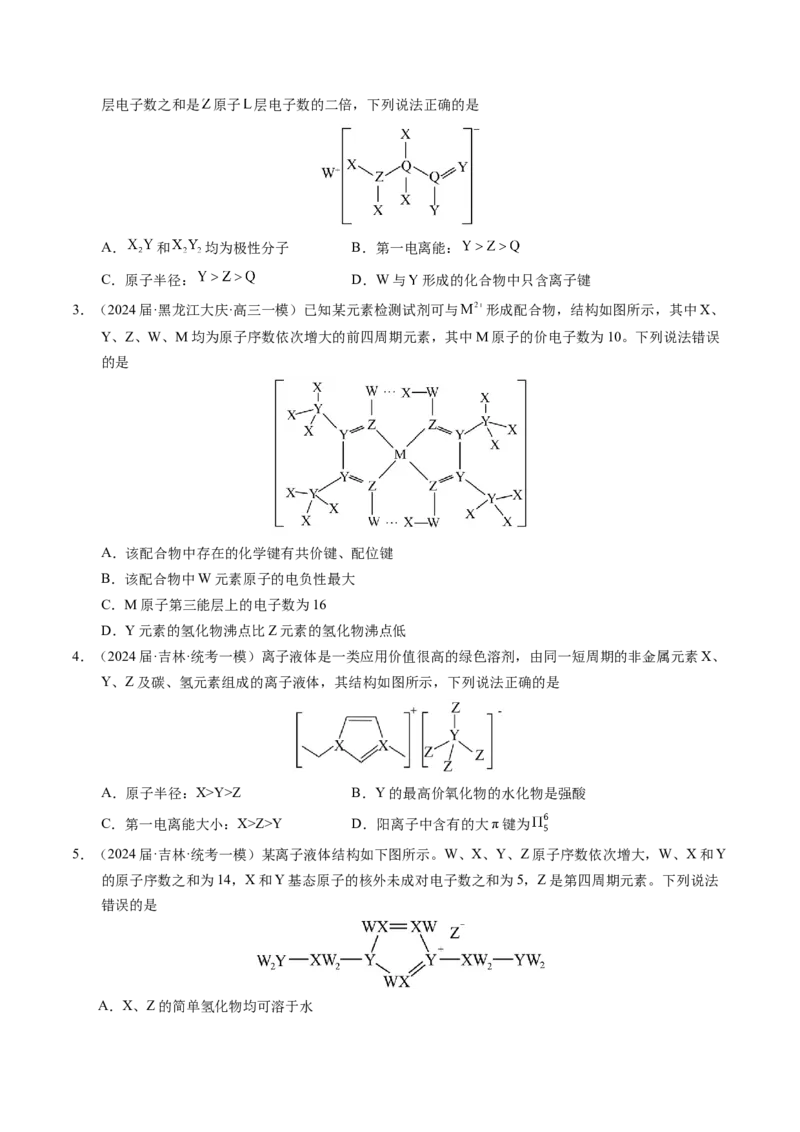
2.(2024届·黑龙江·统考一模)一种工业洗涤剂中间体结构式如图所示,其中短周期元素
原子序数依次增大, 和 同主族但不相邻, 为相邻元素, 和 最外层电子数之和是 原子 层电子数的二倍,下列说法正确的是
A. 和 均为极性分子 B.第一电离能:
C.原子半径: D.W与 形成的化合物中只含离子键
3.(2024届·黑龙江大庆·高三一模)已知某元素检测试剂可与 形成配合物,结构如图所示,其中X、
Y、Z、W、M均为原子序数依次增大的前四周期元素,其中M原子的价电子数为10。下列说法错误
的是
A.该配合物中存在的化学键有共价键、配位键
B.该配合物中W元素原子的电负性最大
C.M原子第三能层上的电子数为16
D.Y元素的氢化物沸点比Z元素的氢化物沸点低
4.(2024届·吉林·统考一模)离子液体是一类应用价值很高的绿色溶剂,由同一短周期的非金属元素X、
Y、Z及碳、氢元素组成的离子液体,其结构如图所示,下列说法正确的是
A.原子半径:X>Y>Z B.Y的最高价氧化物的水化物是强酸
C.第一电离能大小:X>Z>Y D.阳离子中含有的大π键为
5.(2024届·吉林·统考一模)某离子液体结构如下图所示。W、X、Y、Z原子序数依次增大,W、X和Y
的原子序数之和为14,X和Y基态原子的核外未成对电子数之和为5,Z是第四周期元素。下列说法
错误的是
A.X、Z的简单氢化物均可溶于水B.电负性:
C.第一电离能:
D.W、Y、Z可形成既含离子键又含共价键的化合物
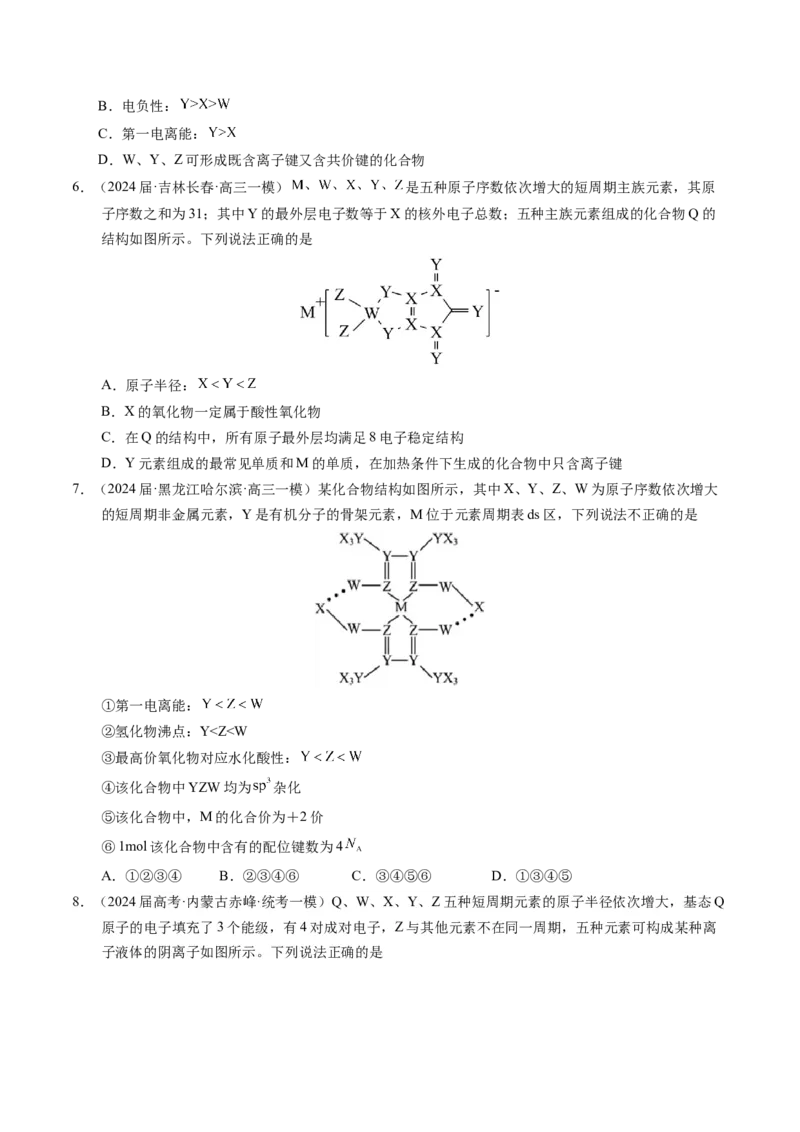
6.(2024届·吉林长春·高三一模) 是五种原子序数依次增大的短周期主族元素,其原
子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的
结构如图所示。下列说法正确的是
A.原子半径:
B.X的氧化物一定属于酸性氧化物
C.在Q的结构中,所有原子最外层均满足8电子稳定结构
D.Y元素组成的最常见单质和M的单质,在加热条件下生成的化合物中只含离子键
7.(2024届·黑龙江哈尔滨·高三一模)某化合物结构如图所示,其中X、Y、Z、W为原子序数依次增大
的短周期非金属元素,Y是有机分子的骨架元素,M位于元素周期表ds区,下列说法不正确的是
①第一电离能:
②氢化物沸点:YQ>X>Y
9.(2024届·四川绵阳·校联考一模)已知A、B、C、D、E是五种短周期主族元素,其原子半径与原子序
数的关系如图1,且A、B、C、D可物成化合物X如图2,C与E同主族。下列说法正确的是
A.氢化物的沸点;C>B
B.简单离子的半径:E>D>C
C.含氧酸的酸性:E>B
D.化合物X在低温的的碱性溶液中更加稳定
10.(2023春·辽宁大连·高三辽师大附中校考阶段练习)离子液体是室温下呈液态的离子化合物。由原子
序数依次增大的短周期主族元素X、Y、Z、W、R组成的一种离子液体的结构如图所示,W的简单氢
化物易液化,可用作制冷剂,R的简单阴离子含10个电子。下列说法正确的是
A.简单氢化物的沸点:R>W
B.电负性:Z>Y>X
C.分子YR 的空间构型为三角锥形
3
D.含氧酸的酸性:W>Z
11.(2023·辽宁·校联考三模)短周期非金属元素X、Y、Z、W的原子序数依次增大,基态X原子的未成
对电子数是其所在周期中最多的,基态W原子的电子总数是其最高能级电子数的4倍,这四种元素与
元素组成的化合物的结构如图所示,下列说法错误的是A.简单氢化物的沸点:
B. 和 的VSEPR模型不同
C.第一电离能:
D.同浓度时,最高价含氧酸的 :
12.(2023·辽宁·校联考三模)X、Y、Z、W、Q均为短周期元素,在元素周期表中的相对位置如图所示。
W的最高价氧化物的水化物是一种三元酸。
X
Y Z W Q
下列说法正确的是
A.元素的第一电离能:Q>W>Z
B.X与氢元素能组成直线形分子
C.X的单质的晶体类型一定和Z的单质的晶体类型相同
D.Y的最高价氧化物能被Q元素的简单氢化物的水溶液溶解
13.(2023·辽宁·模拟预测)X、Y、Z、W是原子序数依次增大的前四周期元素,X元素的简单氢化物能
与其最高价氧化物对应水化物反应生成盐; Y元素原子的核外电子只有8种运动状态;Z为短周期金
属元素,其简单离子的半径在同周期中最小;基态W原子的未成对电子数为6。下列说法错误的是
A.第一电离能: X>Y> Z
B.键角 >
C.W为第四周期d区元素
D.X和Y的最简单气态氢化物中,前者更易液化
14.(2023·辽宁·统考三模)第二周期主族元素X、Y,基态原子均有两个未成对电子,可形成化学式为
,且分子中每个原子均满足8电子稳定结构。下列叙述错误的是
A. 的结构式为
B.X与Y的氢化物的熔、沸点一定是前者低于后者
C. 分子中所有原子都在一条直线上
D. 分子很活泼,能与 、HCl等发生加成反应
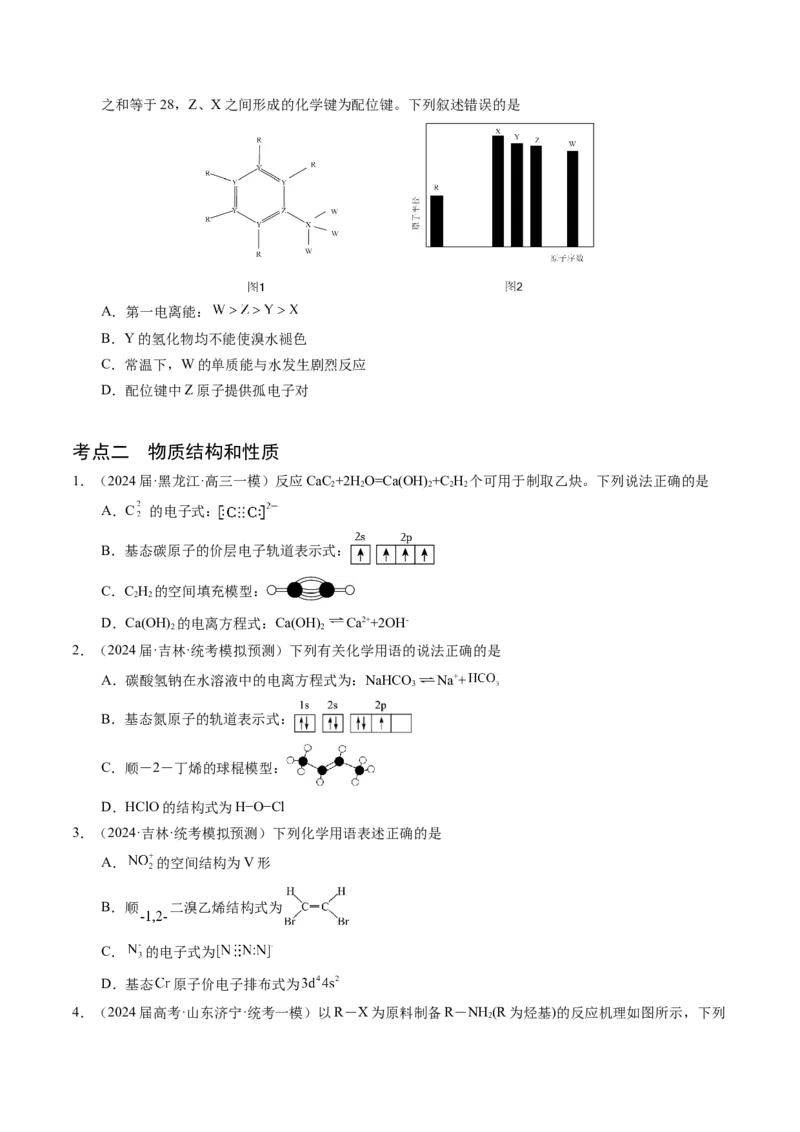
15.(2023·辽宁·校联考模拟预测)短周期主族元素R、X、Y、Z、W可以组成一种锂离子电池的电解质
溶液添加剂,其结构如图1所示。它们的原子半径与原子序数关系如图2所示。已知它们的原子序数之和等于28,Z、X之间形成的化学键为配位键。下列叙述错误的是
A.第一电离能:
B.Y的氢化物均不能使溴水褪色
C.常温下,W的单质能与水发生剧烈反应
D.配位键中Z原子提供孤电子对
考点二 物质结构和性质
1.(2024届·黑龙江·高三一模)反应CaC +2H O=Ca(OH) +C H 个可用于制取乙炔。下列说法正确的是
2 2 2 2 2
A.C 的电子式:
B.基态碳原子的价层电子轨道表示式:
C.C H 的空间填充模型:
2 2
D.Ca(OH) 的电离方程式:Ca(OH) Ca2++2OH-
2 2
2.(2024届·吉林·统考模拟预测)下列有关化学用语的说法正确的是
A.碳酸氢钠在水溶液中的电离方程式为:NaHCO Na++
3
B.基态氮原子的轨道表示式:
C.顺-2-丁烯的球棍模型:
D.HClO的结构式为H−O−Cl
3.(2024·吉林·统考模拟预测)下列化学用语表述正确的是
A. 的空间结构为V形
B.顺 二溴乙烯结构式为
C. 的电子式为
D.基态 原子价电子排布式为
4.(2024届高考·山东济宁·统考一模)以R-X为原料制备R-NH (R为烃基)的反应机理如图所示,下列
2说法错误的是
A.叠氮酸根N 中存在两套π 大π键,N 的中心氮原子采用sp杂化
B.氮原子a、b、c杂化方式未发生变化
C.R-N 分子中∠CNN=120°
3
D.若R为甲基,则戊的碱性比NH 强
3
5.(2024届·黑龙江·高三一模)下列关于物质结构或性质及解释存在错误的是
选项 物质结构或性质 解释
CO 中C原子为sp杂化,为直线形分子;CH 中C原子为sp3
2 4
A 键角:
杂化,为正四面体形分子
B 稳定性: 分子间可以形成氢键, 没有氢键
BF 与NH 形成
3 3
中的 有空轨道接受 中 的孤电子对
[H N→BF ]
3 3
冠醚能加快KMnO 与环 冠醚上不同大小的空穴适配不同大小的碱金属离子,冠醚通
4
D
己烯的反应速率 过与K+结合将 带入有机相,起到催化剂的作用
6.(2024届·贵州贵阳·统考一模)氯乙酸( )是重要的分析试剂和有机合成中间体。一种制
备氯乙酸的方法为 。下列说法正确的是
A. 分子中 键数 键数
B. 键比 键的键长更短、键能更小
C. 的酸性比 更强
D.标准状况下, 是一种液态物质
7.(2024届·江苏泰州·统考一模)氟是已知元素中电负性最大、单质氧化性最强的元素,与稀有气体
形成的 分子是非极性分子,与其他卤素形成的卤素互化物(如 )具有与 相似的化学性
质,与氮形成的 可与 反应生成 (结构式: )。自然界中,含氯矿石有萤石
、冰晶石 等,萤石可与浓硫酸共热制取 气体。工业上,可通过电解 的无水
溶液(含 和 离子)制取 。下列有关说法正确的
A. 的空间结构为Ⅴ形 B. 与 互为同素异形体
C.键角: D. 存在顺反异构现象8.(2024届·山东潍坊·统考一模) 在气态或非极性溶剂中均可通过氯桥键二聚成 ,熔融
和 可形成 。下列说法正确的是
A. 为极性分子
B. 中 原子的杂化方式为
C. 熔点高于 的熔点
D. 中含有 单键
9.(2024届·黑龙江·高三一模)砷化镉晶胞结构如图,图1中“①”和“②”位是“真空”,晶胞参数为
apm,建立如图2,①号位的坐标为( , , )。已知:砷化镉的摩尔质量为Mg·mol-1,N 为阿伏加
A
德罗常数的值,下列说法错误的是
A.砷化镉中Cd与As原子个数比为3:2
B.两个Cd原子间最短距离为0.5a pm
C.③号位原子坐标参数为( ,1, )
D.该晶胞的密度为N (a×10—10)3g·cm-3
A
10.(2024届·吉林长春·高三一模)氮化铬的晶胞结构如图所示,A点分数坐标为(0,0,0)。氮化铬的晶
体密度为dg/cm3,摩尔质量为M g/mol,晶胞参数为anm,N 代表阿伏加德罗常数的值。下列说法正
A
确的是
A.铬原子的价电子排布式为
B.Cr原子位于N原子构成的四面体空隙中
C.距离Cr原子最近的Cr原子有8个
D.11.(2024届·黑龙江哈尔滨·高三一模)已知Mg、Al、O三种元素组成尖晶石型晶体结构,其晶胞由4个
A型小晶格和4个B型小晶格构成,其中 和 都在小晶格内部, 部分在小晶格内部,部分
在小晶格顶点(如图),下列分析错误的是
A.该晶体为离子晶体
B.该物质的化学式为
C.晶胞中,距离 等距且最近的 数为12
D. 与 之间最近的距离是
12.(2024届·吉林长春·统考一模)科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞
参数为 。设 为阿伏加德罗常数的值。下列说法错误的是
A.晶体的最简化学式为
B.晶体中与 最近且距离相等的 有4个
C.晶胞中B和C原子构成的多面体有14个面
D.晶体的密度为
13.(2024届·辽宁葫芦岛·统考一模)一种由Cu、In、Te组成的晶体如图,晶胞参数和晶胞中各原子的投
影位置如图所示,晶胞棱边夹角均为90°。已知:A点、B点原子的分数坐标分别为 、 ,下列叙述不正确的是
A.In原子的配位数为2
B.该晶体的化学式为
C.C点原子的分数坐标为
D.晶胞中A、D原子间距离为
14.(2024届·吉林·高三一模)硫代硫酸盐是一类具有应用前景的浸金试剂,硫代硫酸根 可看作是
中的一个 原子被 原子取代的产物,浸金时 与 配位形成 。
的晶胞形状为长方体,结构如图所示,下列说法正确的是
A. 中 键数目为12
B. 的空间结构是四面体形
C.与 配位时, 中心 原子可作配位原子
D. 晶体的密度为:
15.(2024届·辽宁辽阳·统考一模)氧化铈(CeO 常用作玻璃工业添加剂,在其立方晶胞中掺杂YO,
2) 2 3
Y3+占据原来Ce4+的位置,可以得到更稳定的结构,这种稳定的结构使得氧化铈具有许多独特的性质
和应用,CeO 晶胞中Ce4+与最近O2-的核间距为apm。下列说法正确的是
2已知: 。
A.已知M点原子的分数坐标为(0,0,0),则N点原子的分数坐标为(1,0,1)
B.CeO 晶胞中与Ce4+最近的Ce4+的个数为6
2
C.CeO 晶体的密度为
2
D.若掺杂YO 后得到n(CeO):n(YO)=0.6:0.2的晶体,则此晶体中O2-的空缺率为10%
2 3 2 2 3