文档内容
易错点11 氮元素及其化合物
易错题【01】氮的固定
易错题【02】氮的氧化物
(1)氮有多种价态的氧化物,如NO、NO、NO、NO (或NO)、NO,其中属于酸性氧
2 2 3 2 2 4 2 5
化物的是NO、NO。
2 3 2 5
(2)氮的氧化物都有毒,其中NO 与NO 之间存在平衡:2NO NO,在阿伏加德罗
2 2 4 2 2 4
常数问题中要考虑该平衡的存在;
(3)NO、CO均能与血红蛋白结合而使人中毒。。
易错题【03】硝酸的强氧化性
稀硝酸与铜反应的化学方程式: 3Cu+8HNO(稀)===3Cu(NO)+2NO↑+4HO
3 3 2 2
与金属反应
浓硝酸与铜反应的化学方程式: Cu+4HNO(浓)===Cu(NO)+2NO ↑+2HO
3 3 2 2 2
与非金属反应 浓硝酸与C反应的化学方程式: C+4HNO(浓)=====CO↑+4NO ↑+2HO
3 2 2 2
与还原性化合 硝酸可氧化Fe2+、HS、SO 、NaSO 、HI等还原性物质。如稀硝酸与FeSO 溶液
2 2 2 3 4
物反应 反应的离子方程式: 3Fe2++4H++NO===3Fe3++NO↑+2HO
2
①HNO 中N元素显+5价,处于最高价态,因此浓、稀硝酸均具有强氧化性,浓度越大,
3
氧化性越强,其还原产物的价态越高。
②反应过程中,HNO 的还原产物一般为HNO(浓)―→NO ,HNO(稀)―→NO。
3 3 2 3
③浓硝酸能使紫色石蕊溶液先变红,后褪色,该反应过程中浓硝酸表现出强酸性和强氧化
性。
④常温下,铁、铝遇浓硝酸能发生“钝化”,表面生成致密的氧化膜,并非不发生反应,
故浓硝酸可以用铁桶盛放。
易错题【04】实验室制取氨的其他方法
方法 化学方程式(或原理) 气体发生装置
加热浓氨水 化学方程式为NH ·H O=====NH ↑+HO
3 2 3 2
浓氨水+ NaOH溶于水放热,促使氨水分解。且OH
NaOH固体 -浓度的增大有利于NH 的生成
3CaO与水反应,使溶剂(水)减少;反应放
浓氨水+
热,促使氨水分解,化学方程式为
CaO固体
NH ·H O+CaO==NH↑+Ca(OH)
3 2 3 2
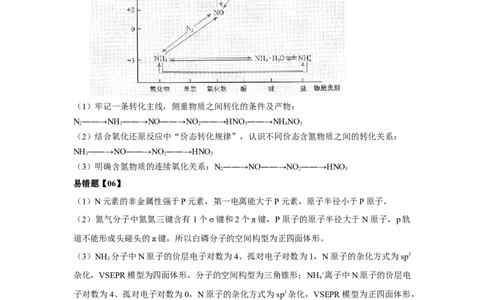
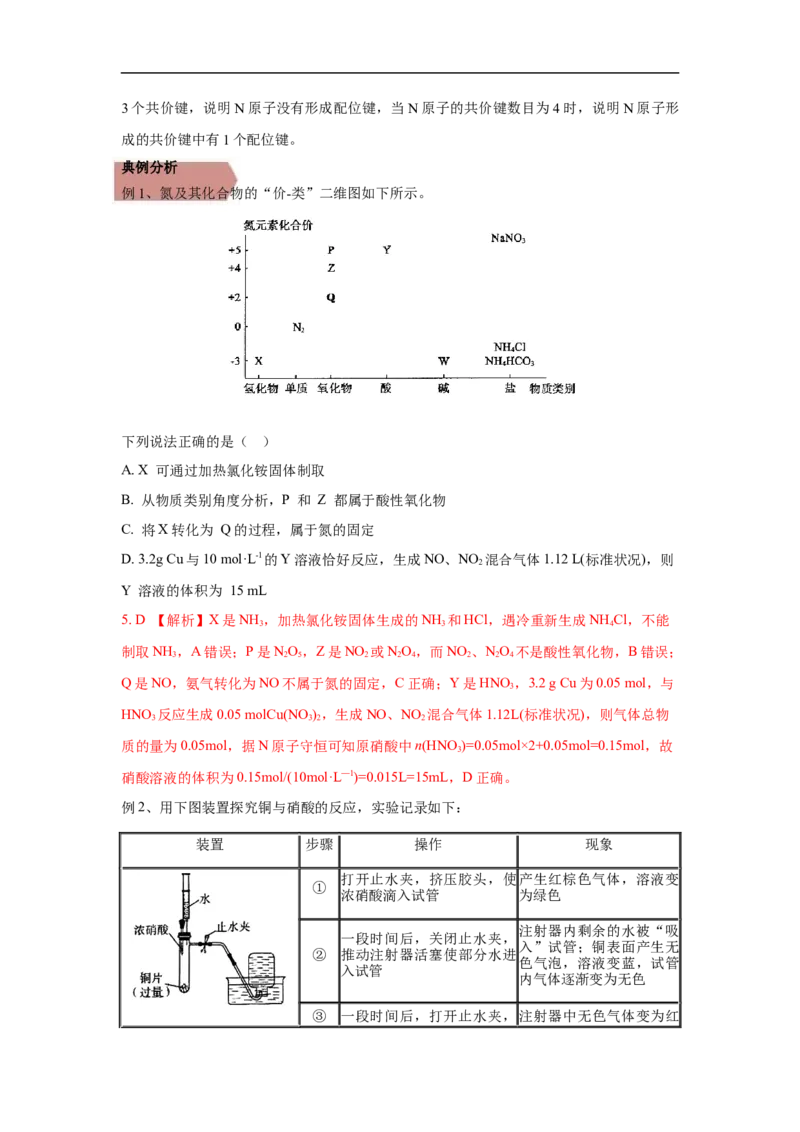
氮元素“价-类二维图”
(1)牢记一条转化主线,侧重物质之间转化的条件及产物:
N――→NH ――→NO――→NO ――→HNO――→NH NO
2 3 2 3 4 3
(2)结合氧化还原反应中“价态转化规律”,认识不同价态含氮物质之间的转化关系:
NH ――→NO――→NO ――→HNO
3 2 3
(3)明确含氮物质的连续氧化关系:N――→NO――→NO ――→HNO
2 2 3
易错题【06】
(1)N元素的非金属性强于P元素,第一电离能大于P元素,原子半径小于P原子。
(2)氮气分子中氮氮三键含有1个σ键和2个π键,P原子的原子半径大于N原子,p轨
道不能形成头碰头的π键,所以白磷分子的空间构型为正四面体形。
(3)NH 分子中N原子的价层电子对数为4、孤对电子对数为1,N原子的杂化方式为sp3
3
杂化,VSEPR模型为四面体形,分子的空间构型为三角锥形;NH +离子中N原子的价层电
4
子对数为4、孤对电子对数为0,N原子的杂化方式为sp3杂化,VSEPR模型为正四面体形,
分子的空间构型为正四面体形。
(4)NH 分子能形成分子间氢键,分子间作用力大于PH ,沸点高于PH ;NH 分子能与
3 3 3 3
水分子形成分子间氢键,氨气极易溶于水。
(5)NO —和NO —离子中N原子的价层电子对数都为3、孤对电子对数分别为0、1,N原
3 2
子的杂化方式为sp2杂化,VSEPR模型都为平面三角形,分子的空间构型分别为平面三角
形和V形。
(6)NH 分子能与具有空轨道的氢离子、铜离子等形成配位键,所以化合物中N原子形成
33个共价键,说明N原子没有形成配位键,当N原子的共价键数目为4时,说明N原子形
成的共价键中有1个配位键。
典例分析
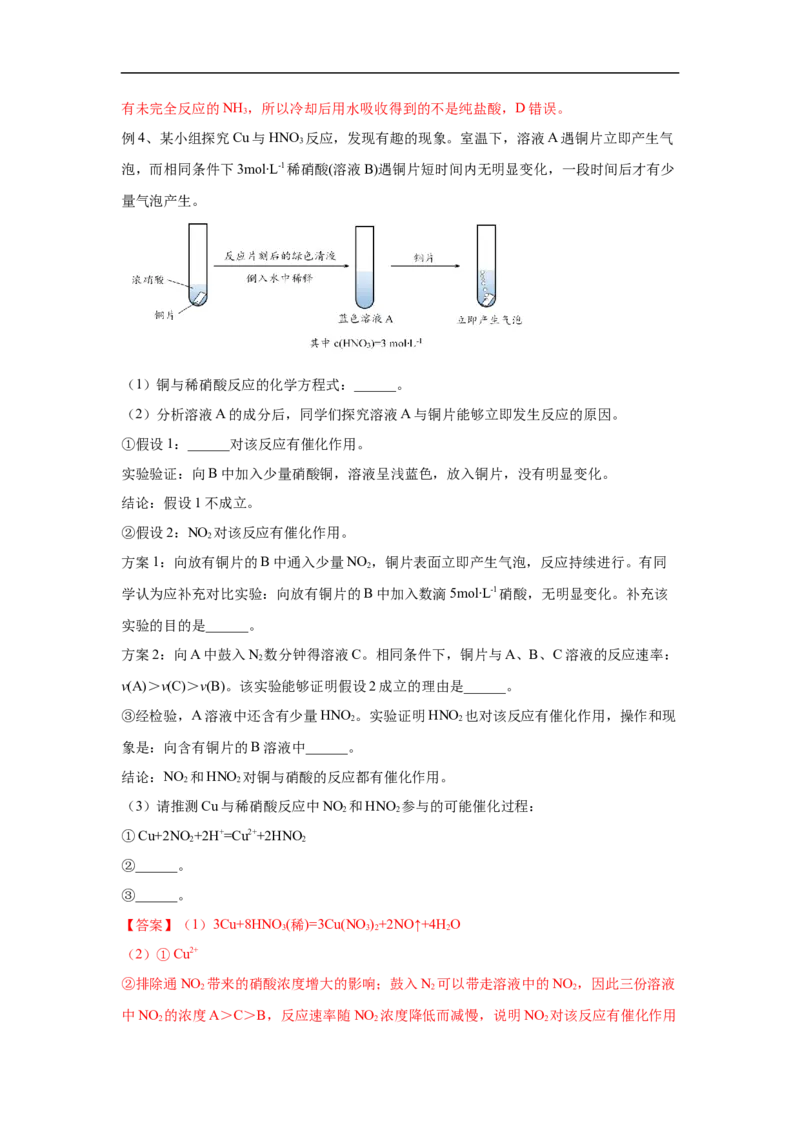
例1、氮及其化合物的“价-类”二维图如下所示。
下列说法正确的是( )
A. X 可通过加热氯化铵固体制取
B. 从物质类别角度分析,P 和 Z 都属于酸性氧化物
C. 将X转化为 Q的过程,属于氮的固定
D. 3.2g Cu与10 mol·L-1的Y溶液恰好反应,生成NO、NO 混合气体1.12 L(标准状况),则
2
Y 溶液的体积为 15 mL
5. D 【解析】X是NH ,加热氯化铵固体生成的NH 和HCl,遇冷重新生成NH Cl,不能
3 3 4
制取NH ,A错误;P是NO,Z是NO 或NO,而NO 、NO 不是酸性氧化物,B错误;
3 2 5 2 2 4 2 2 4
Q是NO,氨气转化为NO不属于氮的固定,C正确;Y是HNO,3.2 g Cu为0.05 mol,与
3
HNO 反应生成0.05 molCu(NO ),生成NO、NO 混合气体1.12L(标准状况),则气体总物
3 3 2 2
质的量为0.05mol,据N原子守恒可知原硝酸中n(HNO)=0.05mol×2+0.05mol=0.15mol,故
3
硝酸溶液的体积为0.15mol/(10mol·L—1)=0.015L=15mL,D正确。
例2、用下图装置探究铜与硝酸的反应,实验记录如下:
装置 步骤 操作 现象
打开止水夹,挤压胶头,使产生红棕色气体,溶液变
①
浓硝酸滴入试管 为绿色
注射器内剩余的水被“吸
一段时间后,关闭止水夹,
入”试管;铜表面产生无
② 推动注射器活塞使部分水进
色气泡,溶液变蓝,试管
入试管
内气体逐渐变为无色
③ 一段时间后,打开止水夹,注射器中无色气体变为红拉动注射器活塞吸取少量无
色气体;拔下注射器,再拉棕色
动活塞吸入少量空气
下列说法不正确的是( )
A.①中反应的化学方程式是
B.②中注射器内剩余的水被“吸入”试管的原因可能是 与 反应导致压强减小
C.③中的实验现象能证明②中Cu与硝酸反应生成了NO
D.待②中反应停止后,向试管内滴加少量稀硫酸,有气体产生
C【解析】①中用与浓硝酸反应生成Cu(NO ) 、NO 和HO,产生红棕色气体NO ,A正确;
3 2 2 2 2
NO 与水发生反应:3NO +H O=2HNO +NO,气体的总物质的量减小,压强减小,注射器
2 2 2 3
内剩余的水被“吸入”试管,B正确;②中推动注射器活塞使部分水进入试管,NO 与水
2
反应生成NO,故③的现象不能证明②中Cu与硝酸生成NO,C错误;②中反应停止后,
铜片剩余,溶液中含 Cu(NO ) ,滴加少量稀硫酸,发生反应:3Cu+2NO—+8H+==3Cu2+
3 2 3
+2NO↑+4HO,D正确。
2
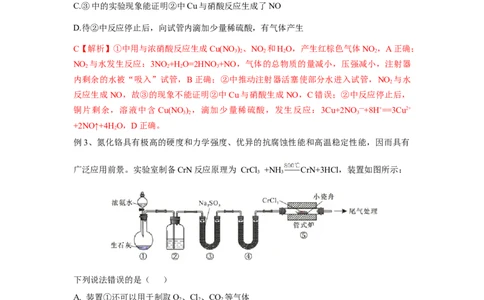
例3、氮化铬具有极高的硬度和力学强度、优异的抗腐蚀性能和高温稳定性能,因而具有
广泛应用前景。实验室制备CrN反应原理为 CrCl +NH CrN+3HCl,装置如图所示:
3 3
下列说法错误的是( )
A. 装置①还可以用于制取O、Cl、CO 等气体
2 2 2
B. 装置②、④中分别盛装NaOH溶液、KOH固体
C. 装置③中也可盛装维生素C ,其作用是除去氧气
D. 装置⑤ 中产生的尾气冷却后用水吸收得到纯盐酸
D【解析】装置①可以用双氧水(MnO 作催化剂)制取氧气,用浓盐酸与高锰酸钾制取氯
2
气,用盐酸与碳酸钙制取二氧化碳气体,A正确;装置②中的NaOH溶液可以吸收装置中
的二氧化碳气体,④中的KOH固体可以吸收水分,B正确;装置③中的亚硫酸钠可以除去
装置中的氧气,也可盛装维生素C,C正确; 装置⑤中产生的尾气有反应生成的HCl,还有未完全反应的NH ,所以冷却后用水吸收得到的不是纯盐酸,D错误。
3
例4、某小组探究Cu与HNO 反应,发现有趣的现象。室温下,溶液A遇铜片立即产生气
3
泡,而相同条件下3mol∙L-1稀硝酸(溶液B)遇铜片短时间内无明显变化,一段时间后才有少
量气泡产生。
(1)铜与稀硝酸反应的化学方程式:______。
(2)分析溶液A的成分后,同学们探究溶液A与铜片能够立即发生反应的原因。
①假设1:______对该反应有催化作用。
实验验证:向B中加入少量硝酸铜,溶液呈浅蓝色,放入铜片,没有明显变化。
结论:假设1不成立。
②假设2:NO 对该反应有催化作用。
2
方案1:向放有铜片的B中通入少量NO ,铜片表面立即产生气泡,反应持续进行。有同
2
学认为应补充对比实验:向放有铜片的B中加入数滴5mol∙L-1硝酸,无明显变化。补充该
实验的目的是______。
方案2:向A中鼓入N 数分钟得溶液C。相同条件下,铜片与A、B、C溶液的反应速率:
2
v(A)>v(C)>v(B)。该实验能够证明假设2成立的理由是______。
③经检验,A溶液中还含有少量HNO。实验证明HNO 也对该反应有催化作用,操作和现
2 2
象是:向含有铜片的B溶液中______。
结论:NO 和HNO 对铜与硝酸的反应都有催化作用。
2 2
(3)请推测Cu与稀硝酸反应中NO 和HNO 参与的可能催化过程:
2 2
①Cu+2NO+2H+=Cu2++2HNO
2 2
②______。
③______。
【答案】(1)3Cu+8HNO (稀)=3Cu(NO)+2NO↑+4HO
3 3 2 2
(2)①Cu2+
②排除通NO 带来的硝酸浓度增大的影响;鼓入N 可以带走溶液中的NO ,因此三份溶液
2 2 2
中NO 的浓度A>C>B,反应速率随NO 浓度降低而减慢,说明NO 对该反应有催化作用
2 2 2③加入少量的NaNO ,B中铜片上立即生成气泡,反应持续进行
2
(3)②NO +HNO +H+=2NO+H O
2 2 2
③2HNO=NO+NO +H O(或Cu+2HNO +2H+=Cu2++2NO+2HO等)
2 2 2 2 2
【解析】(1)铜与稀硝酸反应生成硝酸铜、一氧化氮和水,反应的化学方程式为
3Cu+8HNO (稀)=3Cu(NO)+2NO↑+4HO,故答案为:
3 3 2 2
3Cu+8HNO (稀)=3Cu(NO)+2NO↑+4HO;
3 3 2 2
(2)①由实验设计和实验结论可知,假设1为铜离子对铜与硝酸的反应有催化作用,故答
案为:Cu2+;
②由假设2可知,方案1设计的目的是通过向含有铜片的B溶液中通入二氧化氮,反应速
率明显加快,而含有铜片的B溶液中滴入稀硝酸,反应无明显变化证明二氧化氮与水反应
生成生成硝酸,硝酸浓度增大对铜与硝酸的反应速率加快无影响;方案2设计的目的是通
过向含有铜片的A溶液中通入氮气排出溶液中的二氧化氮,降低溶液中二氧化氮的浓度得
到溶液中二氧化氮浓度大的A、二氧化氮浓度小的C和没有二氧化氮的B三组对比实验,
由反应速率v(A)>v(C)>v(B)证明二氧化氮的浓度越大,对铜与硝酸的反应催化效果越好,
从而说明二氧化氮对铜与硝酸的反应有催化作用,故答案为:排除通NO 带来的硝酸浓度
2
增大的影响;鼓入N 可以带走溶液中的NO ,因此三份溶液中NO 的浓度A>C>B,反应
2 2 2
速率随NO 浓度降低而减慢,说明NO 对该反应有催化作用;
2 2
③由实验目的可知,向含有铜片的B溶液中加入亚硝酸钠后,亚硝酸钠与溶液中的硝酸反
应生成亚硝酸,亚硝酸浓度增大,若铜片上立即生成气泡,反应持续进行证明亚硝酸对铜
与硝酸的反应有催化作用,故答案为:加入少量的NaNO ,B中铜片上立即生成气泡,反
2
应持续进行;
(3)由铜与稀硝酸反应的方程式和反应①可知,若二氧化氮和亚硝酸参与反应,反应②和
③中硝酸和亚硝酸应是反应的反应物,一氧化氮和二氧化氮是反应的生成物,则反应②可
能为硝酸与亚硝酸反应生成二氧化氮和水,反应③可能为亚硝酸分解生成一氧化氮、二氧
化氮和水或铜与硝酸、亚硝酸反应生成硝酸铜、一氧化氮和水,反应的离子方程式为NO
+HNO +H+=2NO+H O、2HNO=NO+NO +H O(或Cu+2HNO +2H+=Cu2++2NO+2HO等),
2 2 2 2 2 2 2 2
故答案为:NO +HNO +H+=2NO+H O;2HNO=NO+NO +H O(或Cu+2HNO +2H+=Cu2+
2 2 2 2 2 2 2+2NO+2HO等)。
2
1.(2022·江苏·高考真题)氮及其化合物的转化具有重要应用。下列说法不正确的是
A.自然固氮、人工固氮都是将 转化为
B.侯氏制碱法以 、 、 、 为原料制备 和
C.工业上通过 催化氧化等反应过程生产
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
2.(2022·广东深圳·一模)下列关于HF、 、 的说法不正确的是
A.HF、 、 都是由极性键形成的极性分子
B.HF、 、 中共价键键长逐渐增大,键能逐渐减小
C. 、 的中心原子杂化方式相同
D. 比HF的沸点高是由于HF分子间不能形成氢键
3.(2022·广东·梅州市梅江区梅州中学模拟预测)已知反应:
,该反应可用于提纯末端炔烃。下列
说法不正确的是
A. 的电子式为 B.基态氮原子的价电子排布图:C. 的空间充填模型为 D. 中 键与 键的个数比为1:1
4.(2022·上海金山·二模)液氨中存在:2NH (l) NH +NH 。下列有关化学用语
3
表示正确的是
A.NH 的比例模型: B.NH 的空间构型:三角锥形
3
C.NH 的电子式: D.平衡常数表达式:
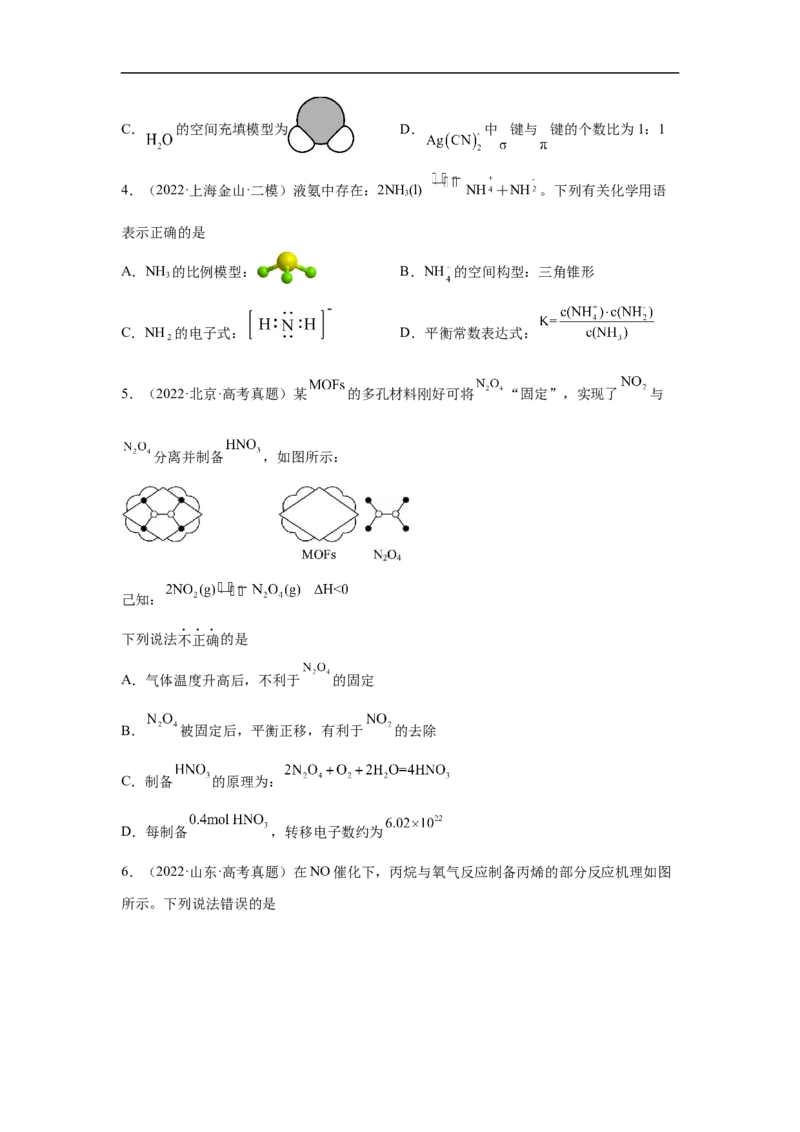
5.(2022·北京·高考真题)某 的多孔材料刚好可将 “固定”,实现了 与
分离并制备 ,如图所示:
己知:
下列说法不正确的是
A.气体温度升高后,不利于 的固定
B. 被固定后,平衡正移,有利于 的去除
C.制备 的原理为:
D.每制备 ,转移电子数约为
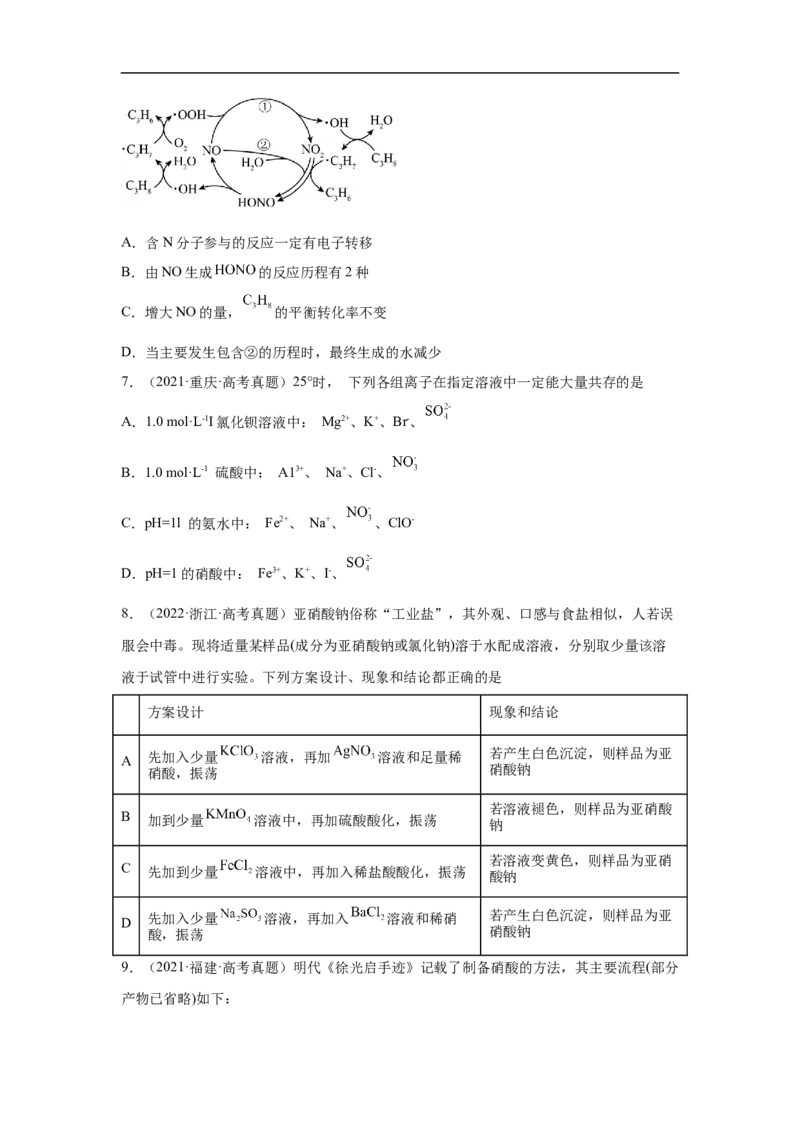
6.(2022·山东·高考真题)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图
所示。下列说法错误的是A.含N分子参与的反应一定有电子转移
B.由NO生成 的反应历程有2种
C.增大NO的量, 的平衡转化率不变
D.当主要发生包含②的历程时,最终生成的水减少
7.(2021·重庆·高考真题)25°时, 下列各组离子在指定溶液中一定能大量共存的是
A.1.0 mol·L-1I氯化钡溶液中: Mg2+、K+、Br-、
B.1.0 mol·L-1 硫酸中: A13+、 Na+、Cl-、
C.pH=1l 的氨水中: Fe2+、 Na+、 、ClO-
D.pH=1的硝酸中: Fe3+、K+、I-、
8.(2022·浙江·高考真题)亚硝酸钠俗称“工业盐”,其外观、口感与食盐相似,人若误
服会中毒。现将适量某样品(成分为亚硝酸钠或氯化钠)溶于水配成溶液,分别取少量该溶
液于试管中进行实验。下列方案设计、现象和结论都正确的是
方案设计 现象和结论
先加入少量 溶液,再加 溶液和足量稀 若产生白色沉淀,则样品为亚
A
硝酸,振荡 硝酸钠
若溶液褪色,则样品为亚硝酸
B 加到少量 溶液中,再加硫酸酸化,振荡
钠
若溶液变黄色,则样品为亚硝
C 先加到少量 溶液中,再加入稀盐酸酸化,振荡
酸钠
先加入少量 溶液,再加入 溶液和稀硝 若产生白色沉淀,则样品为亚
D
酸,振荡 硝酸钠
9.(2021·福建·高考真题)明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分
产物已省略)如下:下列说法错误的是
A.FeSO 的分解产物X为FeO B.本流程涉及复分解反应
4
C.HNO 的沸点比HSO 的低 D.制备使用的铁锅易损坏
3 2 4
10.(2022·江苏·启东中学模拟预测) 发生催化氧化反应生成 ,强碱条件下能被
氧化生成 ; 可被 继续氧化生成 ,也可被 氧化生成 ,
能与 溶液反应产生银镜; 是一种弱酸,酸性与醋酸相当。下列有关含氮
化合物的性质与制备说法正确的是
A.分析结构可推得, 难溶于水
B.分析结构可推得,相同条件下 还原性应强于
C.制备 时应将 慢慢通入 溶液中
D.可向 溶液中通 来制备
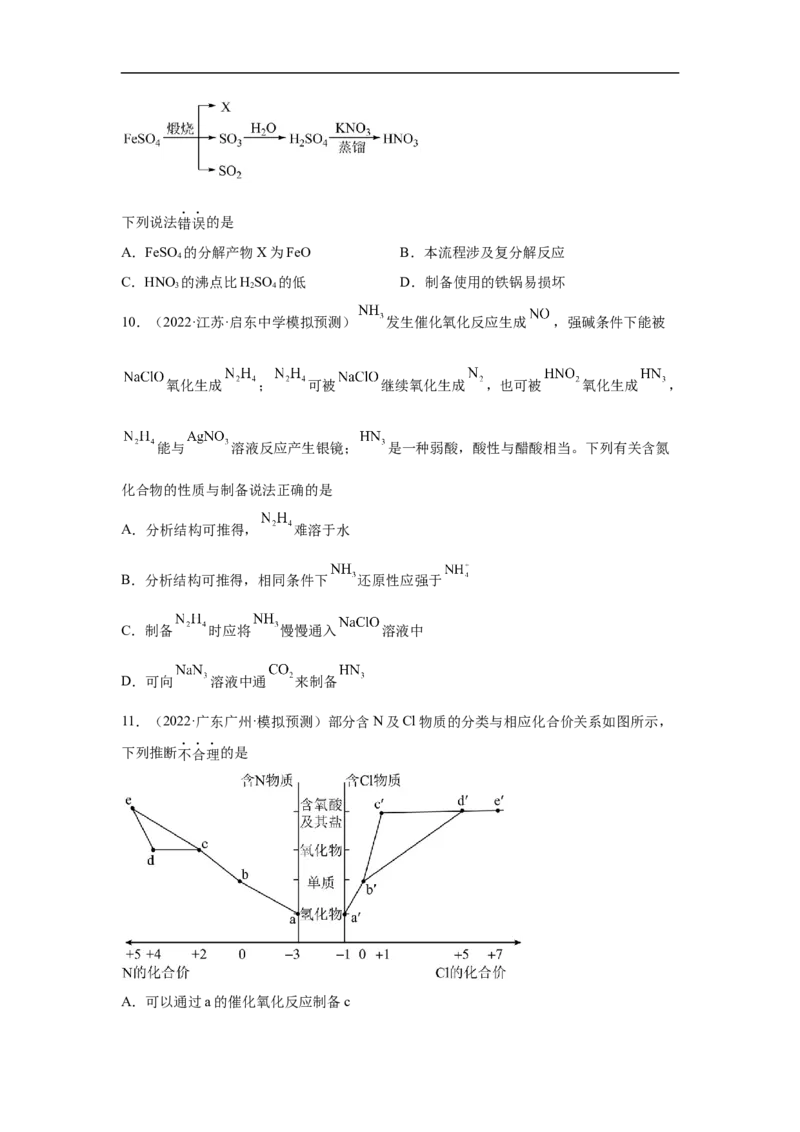
11.(2022·广东广州·模拟预测)部分含N及Cl物质的分类与相应化合价关系如图所示,
下列推断不合理的是
A.可以通过a的催化氧化反应制备cB.工业上通过a→b→c→d→e来制备
C.浓的a′溶液和浓的c溶液反应可以得到b′
D.加热d′的固态钟盐可以产生
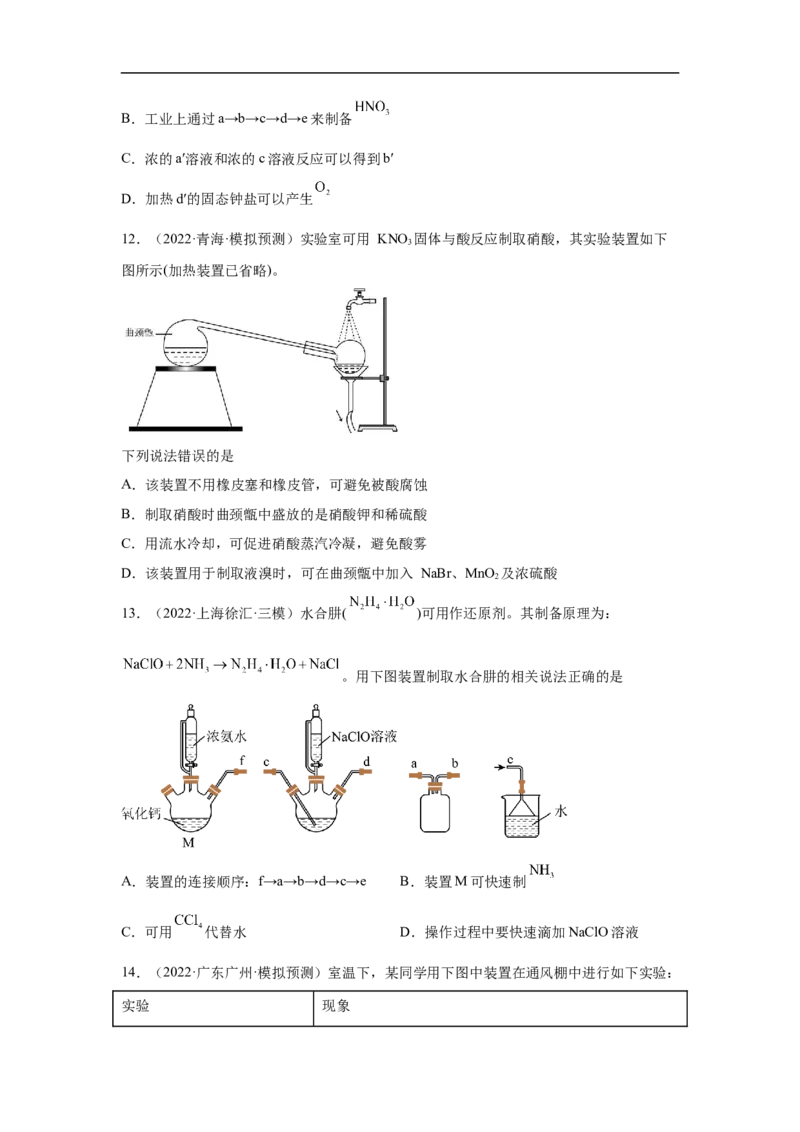
12.(2022·青海·模拟预测)实验室可用 KNO 固体与酸反应制取硝酸,其实验装置如下
3
图所示(加热装置已省略)。
下列说法错误的是
A.该装置不用橡皮塞和橡皮管,可避免被酸腐蚀
B.制取硝酸时曲颈甑中盛放的是硝酸钾和稀硫酸
C.用流水冷却,可促进硝酸蒸汽冷凝,避免酸雾
D.该装置用于制取液溴时,可在曲颈甑中加入 NaBr、MnO 及浓硫酸
2
13.(2022·上海徐汇·三模)水合肼( )可用作还原剂。其制备原理为:
。用下图装置制取水合肼的相关说法正确的是
A.装置的连接顺序:f→a→b→d→c→e B.装置M可快速制
C.可用 代替水 D.操作过程中要快速滴加NaClO溶液
14.(2022·广东广州·模拟预测)室温下,某同学用下图中装置在通风棚中进行如下实验:
实验 现象试管Ⅰ中开始无明显现象,后逐渐有微小气泡生成,反应
越来越剧烈,试管口上方出现红棕色气体,溶液呈蓝色。
试管Ⅱ中剧烈反应,迅速生成大量红棕色气体,溶液呈绿
色:之后向溶液中持续通入 ,溶液又变为蓝色。
下列说法不正确的是A.试管Ⅰ中浅红棕色气体为 ,由铜还原硝酸生成
B.等质量的Cu完全溶解时,Ⅰ中消耗的 更少
C.试管Ⅱ中反应后溶液颜色与试管Ⅰ中的不同,可能是由于溶有
D.蓝色的 呈平面四边形结构,中心离子不可能为 杂化
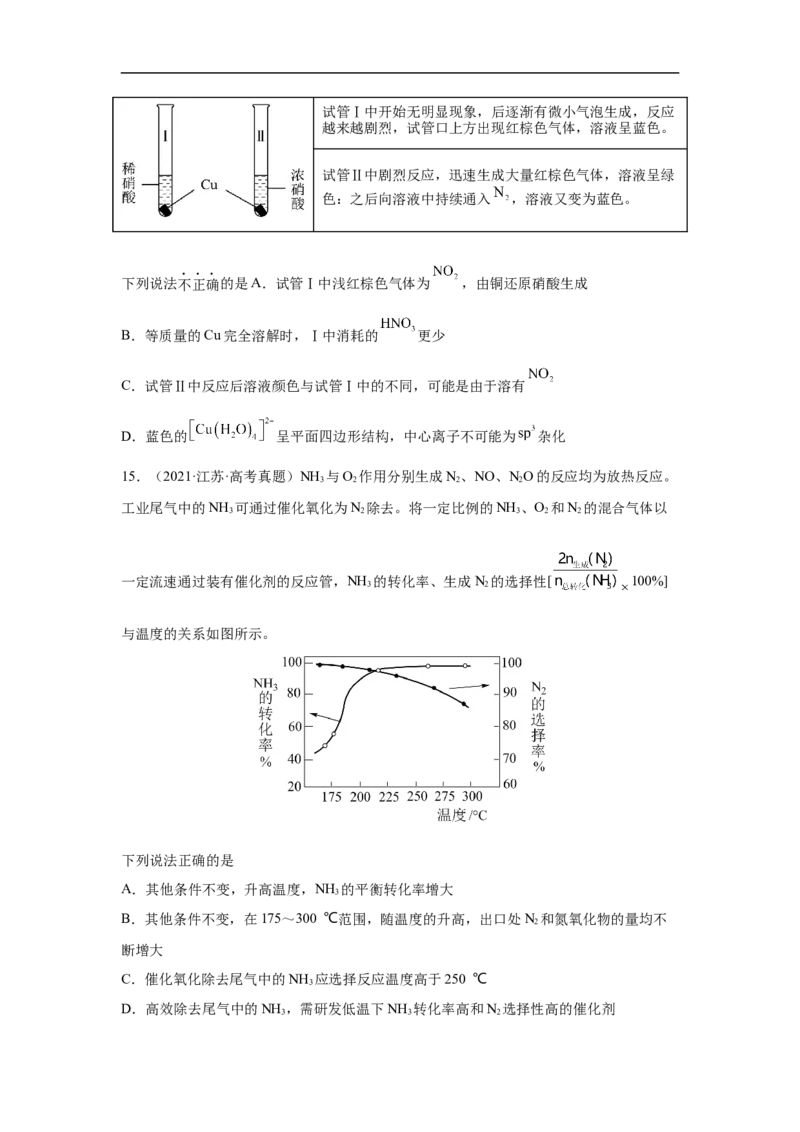
15.(2021·江苏·高考真题)NH 与O 作用分别生成N、NO、NO的反应均为放热反应。
3 2 2 2
工业尾气中的NH 可通过催化氧化为N 除去。将一定比例的NH 、O 和N 的混合气体以
3 2 3 2 2
一定流速通过装有催化剂的反应管,NH 的转化率、生成N 的选择性[ 100%]
3 2
与温度的关系如图所示。
下列说法正确的是
A.其他条件不变,升高温度,NH 的平衡转化率增大
3
B.其他条件不变,在175~300 ℃范围,随温度的升高,出口处N 和氮氧化物的量均不
2
断增大
C.催化氧化除去尾气中的NH 应选择反应温度高于250 ℃
3
D.高效除去尾气中的NH ,需研发低温下NH 转化率高和N 选择性高的催化剂
3 3 216.(2022·海南·高考真题)磷酸氢二铵[ ]常用于干粉灭火剂。某研究小组用
磷酸吸收氨气制备 ,装置如图所示(夹持和搅拌装置已省略)。
回答问题:
(1)实验室用 和 制备氨气的化学方程式为_______。
(2)现有浓 质量分数为85%,密度为1.7g/mL。若实验需100mL1.7mol/L的 溶
液,则需浓 _______mL(保留一位小数)。
(3)装置中活塞 的作用为_______。实验过程中,当出现_______现象时,应及时关闭 ,
打开 。
(4)当溶液pH为8.0~9.0时,停止通 ,即可制得 溶液。若继续通入 ,
当 时,溶液中 、_______和_______(填离子符号)浓度明显增加。
(5)若本实验不选用pH传感器,还可选用_______作指示剂,当溶液颜色由_______变为
_______时,停止通 。
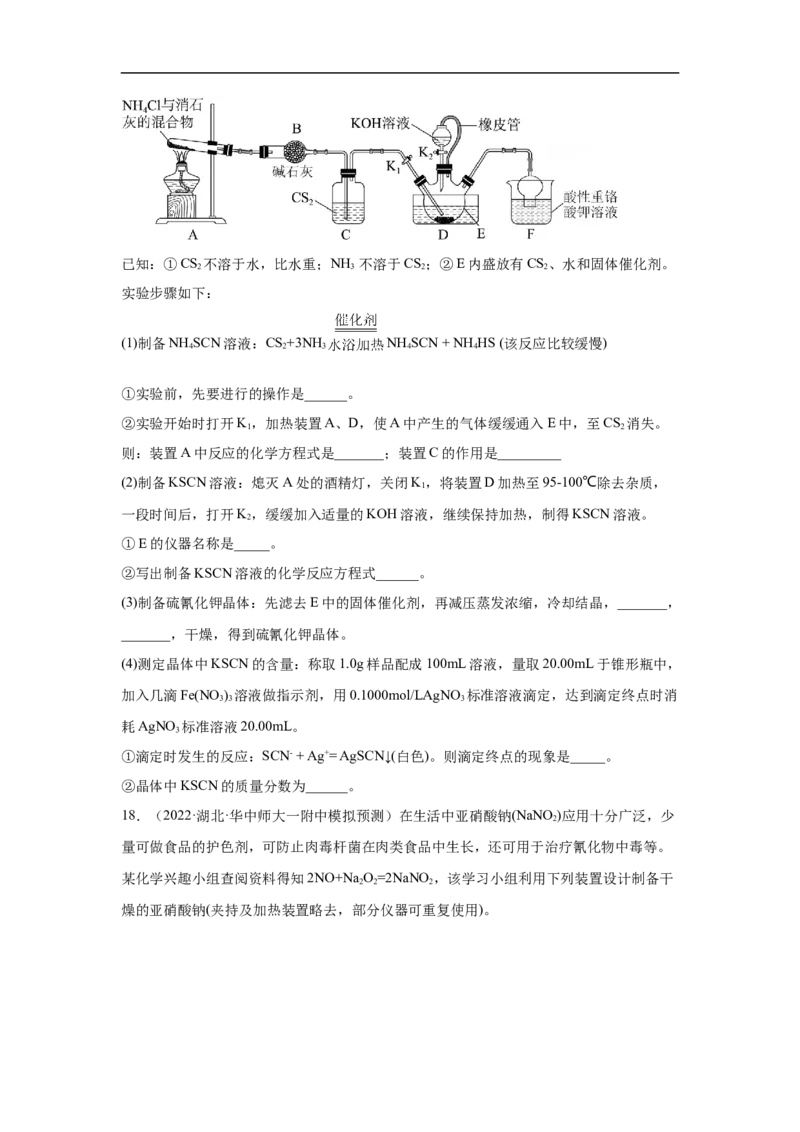
17.(2022·广东惠州·二模)某学习小组在实验室模拟工业制备硫氰化钾(KSCN),装置如
图:已知:①CS 不溶于水,比水重;NH 不溶于CS;②E内盛放有CS、水和固体催化剂。
2 3 2 2
实验步骤如下:
(1)制备NH SCN溶液:CS+3NH NH SCN + NH HS (该反应比较缓慢)
4 2 3 4 4
①实验前,先要进行的操作是______。
②实验开始时打开K,加热装置A、D,使A中产生的气体缓缓通入E中,至CS 消失。
1 2
则:装置A中反应的化学方程式是_______;装置C的作用是_________
(2)制备KSCN溶液:熄灭A处的酒精灯,关闭K,将装置D加热至95-100℃除去杂质,
1
一段时间后,打开K,缓缓加入适量的KOH溶液,继续保持加热,制得KSCN溶液。
2
①E的仪器名称是_____。
②写出制备KSCN溶液的化学反应方程式______。
(3)制备硫氰化钾晶体:先滤去E中的固体催化剂,再减压蒸发浓缩,冷却结晶,_______,
_______,干燥,得到硫氰化钾晶体。
(4)测定晶体中KSCN的含量:称取1.0g样品配成100mL溶液,量取20.00mL于锥形瓶中,
加入几滴Fe(NO ) 溶液做指示剂,用0.1000mol/LAgNO 标准溶液滴定,达到滴定终点时消
3 3 3
耗AgNO 标准溶液20.00mL。
3
①滴定时发生的反应:SCN- + Ag+= AgSCN↓(白色)。则滴定终点的现象是_____。
②晶体中KSCN的质量分数为______。
18.(2022·湖北·华中师大一附中模拟预测)在生活中亚硝酸钠(NaNO )应用十分广泛,少
2
量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长,还可用于治疗氰化物中毒等。
某化学兴趣小组查阅资料得知2NO+Na O=2NaNO ,该学习小组利用下列装置设计制备干
2 2 2
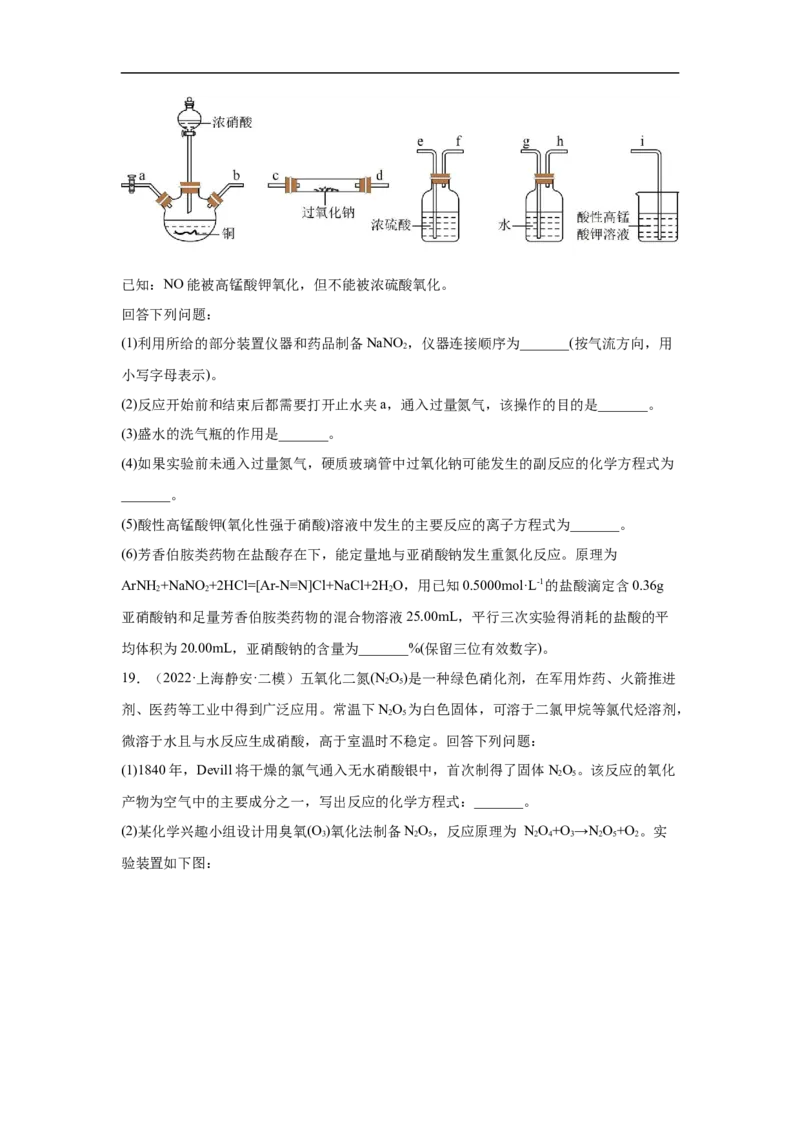
燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。已知:NO能被高锰酸钾氧化,但不能被浓硫酸氧化。
回答下列问题:
(1)利用所给的部分装置仪器和药品制备NaNO ,仪器连接顺序为_______(按气流方向,用
2
小写字母表示)。
(2)反应开始前和结束后都需要打开止水夹a,通入过量氮气,该操作的目的是_______。
(3)盛水的洗气瓶的作用是_______。
(4)如果实验前未通入过量氮气,硬质玻璃管中过氧化钠可能发生的副反应的化学方程式为
_______。
(5)酸性高锰酸钾(氧化性强于硝酸)溶液中发生的主要反应的离子方程式为_______。
(6)芳香伯胺类药物在盐酸存在下,能定量地与亚硝酸钠发生重氮化反应。原理为
ArNH+NaNO +2HCl=[Ar-N≡N]Cl+NaCl+2H O,用已知0.5000mol·L-1的盐酸滴定含0.36g
2 2 2
亚硝酸钠和足量芳香伯胺类药物的混合物溶液25.00mL,平行三次实验得消耗的盐酸的平
均体积为20.00mL,亚硝酸钠的含量为_______%(保留三位有效数字)。
19.(2022·上海静安·二模)五氧化二氮(N O)是一种绿色硝化剂,在军用炸药、火箭推进
2 5
剂、医药等工业中得到广泛应用。常温下NO 为白色固体,可溶于二氯甲烷等氯代烃溶剂,
2 5
微溶于水且与水反应生成硝酸,高于室温时不稳定。回答下列问题:
(1)1840年,Devill将干燥的氯气通入无水硝酸银中,首次制得了固体NO。该反应的氧化
2 5
产物为空气中的主要成分之一,写出反应的化学方程式:_______。
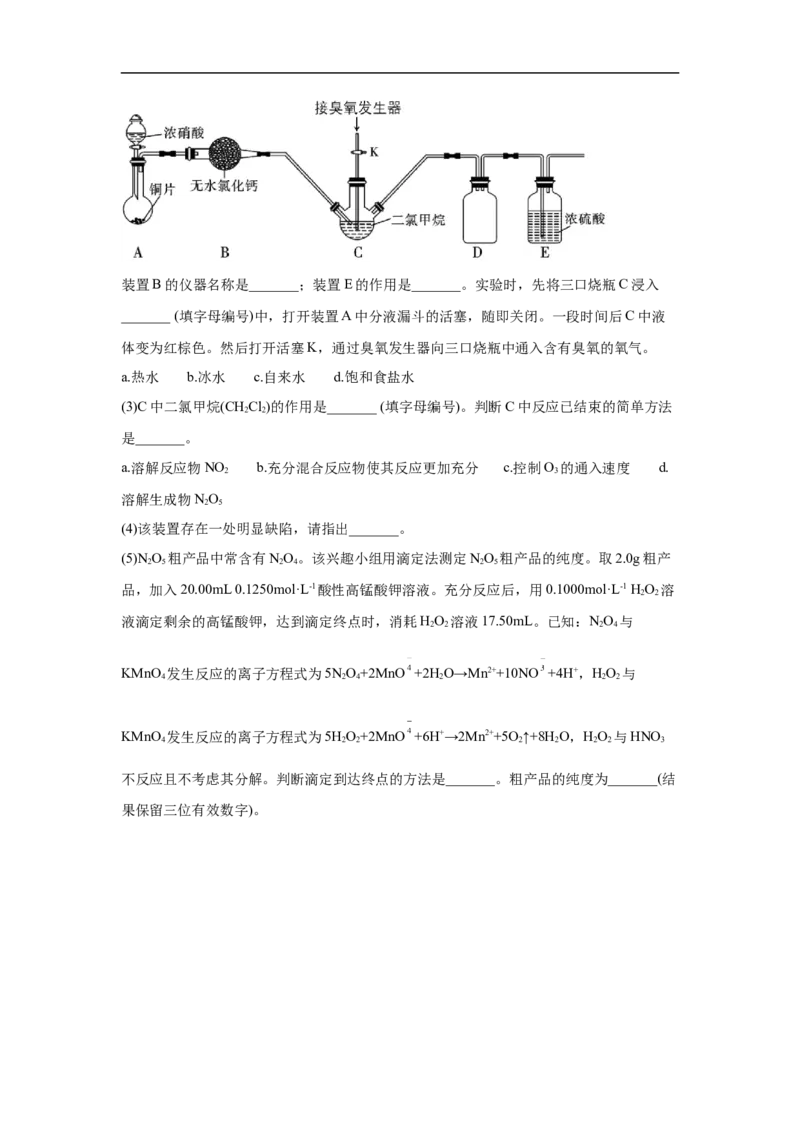
(2)某化学兴趣小组设计用臭氧(O )氧化法制备NO,反应原理为 NO+O →NO+O 。实
3 2 5 2 4 3 2 5 2
验装置如下图:装置B的仪器名称是_______;装置E的作用是_______。实验时,先将三口烧瓶C浸入
_______ (填字母编号)中,打开装置A中分液漏斗的活塞,随即关闭。一段时间后C中液
体变为红棕色。然后打开活塞K,通过臭氧发生器向三口烧瓶中通入含有臭氧的氧气。
a.热水 b.冰水 c.自来水 d.饱和食盐水
(3)C中二氯甲烷(CHCl)的作用是_______ (填字母编号)。判断C中反应已结束的简单方法
2 2
是_______。
a.溶解反应物NO b.充分混合反应物使其反应更加充分 c.控制O 的通入速度 d.
2 3
溶解生成物NO
2 5
(4)该装置存在一处明显缺陷,请指出_______。
(5)N O 粗产品中常含有NO。该兴趣小组用滴定法测定NO 粗产品的纯度。取2.0g粗产
2 5 2 4 2 5
品,加入20.00mL 0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1 HO 溶
2 2
液滴定剩余的高锰酸钾,达到滴定终点时,消耗HO 溶液17.50mL。已知:NO 与
2 2 2 4
KMnO 发生反应的离子方程式为5NO+2MnO +2H O→Mn2++10NO +4H+,HO 与
4 2 4 2 2 2
KMnO 发生反应的离子方程式为5HO+2MnO +6H+→2Mn2++5O ↑+8H O,HO 与HNO
4 2 2 2 2 2 2 3
不反应且不考虑其分解。判断滴定到达终点的方法是_______。粗产品的纯度为_______(结
果保留三位有效数字)。