文档内容
晋江二中 鹏峰中学 广海中学 泉港五中2022-2023学年
上学期十月高三联考
化学试卷
满分100分 考试时间75分钟
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.3 K 39 S 32
一、选择题:本题共10小题,每小题4分,共40分。每小题只有一个选项符合题目要求。
1、我国在探索太空、开发深海、建设高铁、5G技术等方面取得举世瞩目的成就,这些成就与化学
有着密切联系。下列说法正确的是
A.火箭箭体采用铝合金,工业上常采用电解熔融氯化铝冶炼铝
B.5G手机电池工作时,电池中化学能完全转化为电能
C.华为5G手机芯片的主要成分是二氧化硅
D.中国天眼FAST用到的高性能碳化硅是一种新型的无机非金属材料
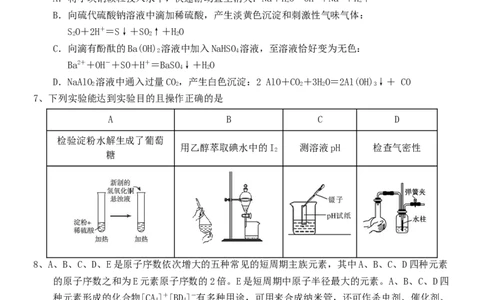
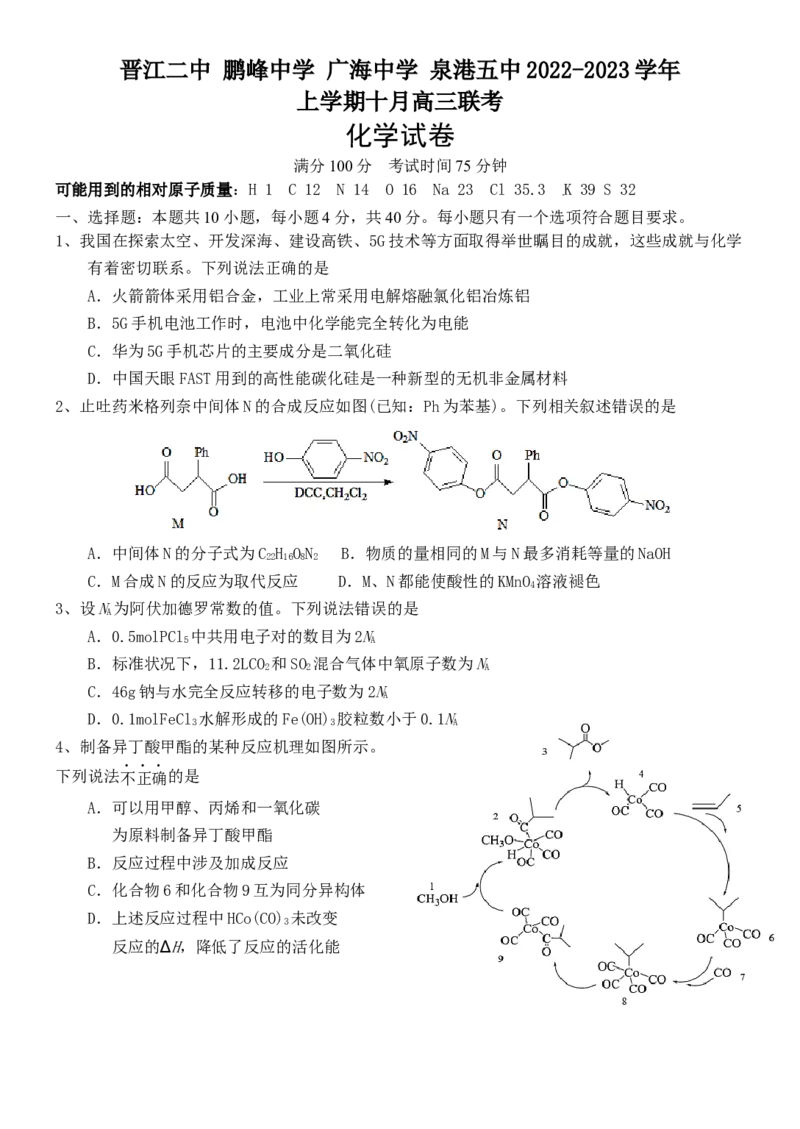
2、止吐药米格列奈中间体N的合成反应如图(已知:Ph为苯基)。下列相关叙述错误的是
A.中间体N的分子式为C H ON B.物质的量相同的M与N最多消耗等量的NaOH
22 16 8 2
C.M合成N的反应为取代反应 D.M、N都能使酸性的KMnO 溶液褪色
4
3、设N为阿伏加德罗常数的值。下列说法错误的是
A
A.0.5molPCl 中共用电子对的数目为2N
5 A
B.标准状况下,11.2LCO 和SO 混合气体中氧原子数为N
2 2 A
C.46g钠与水完全反应转移的电子数为2N
A
D.0.1molFeCl 水解形成的Fe(OH) 胶粒数小于0.1N
3 3 A
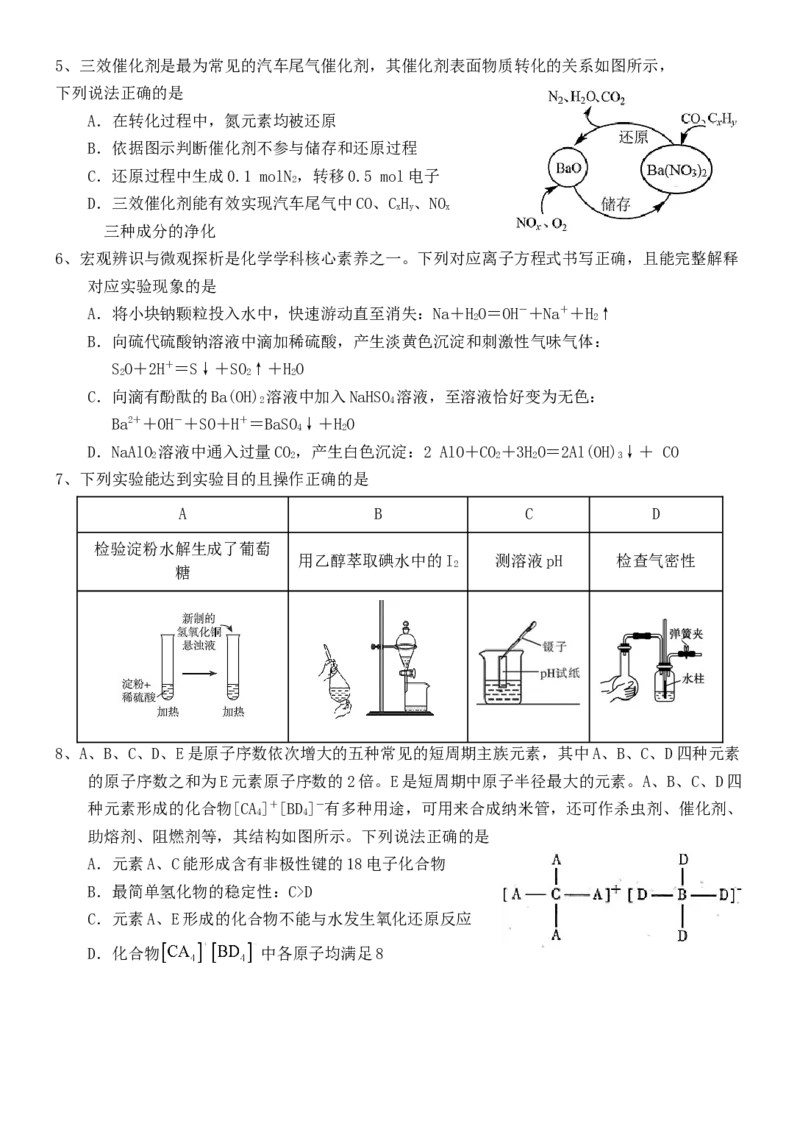
4、制备异丁酸甲酯的某种反应机理如图所示。
下列说法不正确的是
A.可以用甲醇、丙烯和一氧化碳
为原料制备异丁酸甲酯
B.反应过程中涉及加成反应
C.化合物6和化合物9互为同分异构体
D.上述反应过程中HCo(CO) 未改变
3
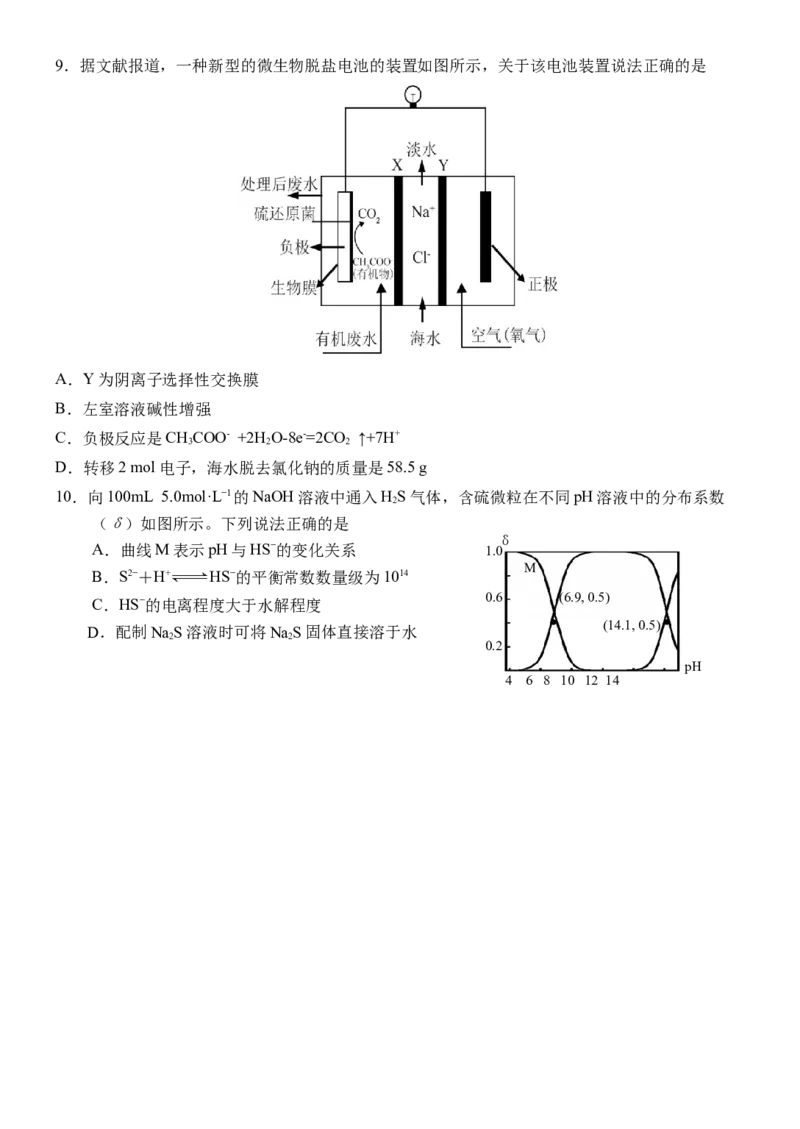
反应的∆H,降低了反应的活化能5、三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图所示,
下列说法正确的是
A.在转化过程中,氮元素均被还原
B.依据图示判断催化剂不参与储存和还原过程
C.还原过程中生成0.1 molN,转移0.5 mol电子
2
D.三效催化剂能有效实现汽车尾气中CO、CH、NO
x y x
三种成分的净化
6、宏观辨识与微观探析是化学学科核心素养之一。下列对应离子方程式书写正确,且能完整解释
对应实验现象的是
A.将小块钠颗粒投入水中,快速游动直至消失:Na+HO=OH-+Na++H↑
2 2
B.向硫代硫酸钠溶液中滴加稀硫酸,产生淡黄色沉淀和刺激性气味气体:
SO+2H+=S↓+SO↑+HO
2 2 2
C.向滴有酚酞的Ba(OH) 溶液中加入NaHSO 溶液,至溶液恰好变为无色:
2 4
Ba2++OH-+SO+H+=BaSO↓+HO
4 2
D.NaAlO 溶液中通入过量CO,产生白色沉淀:2 AlO+CO+3HO=2Al(OH)↓+ CO
2 2 2 2 3
7、下列实验能达到实验目的且操作正确的是
A B C D
检验淀粉水解生成了葡萄
用乙醇萃取碘水中的I 测溶液pH 检查气密性
2
糖
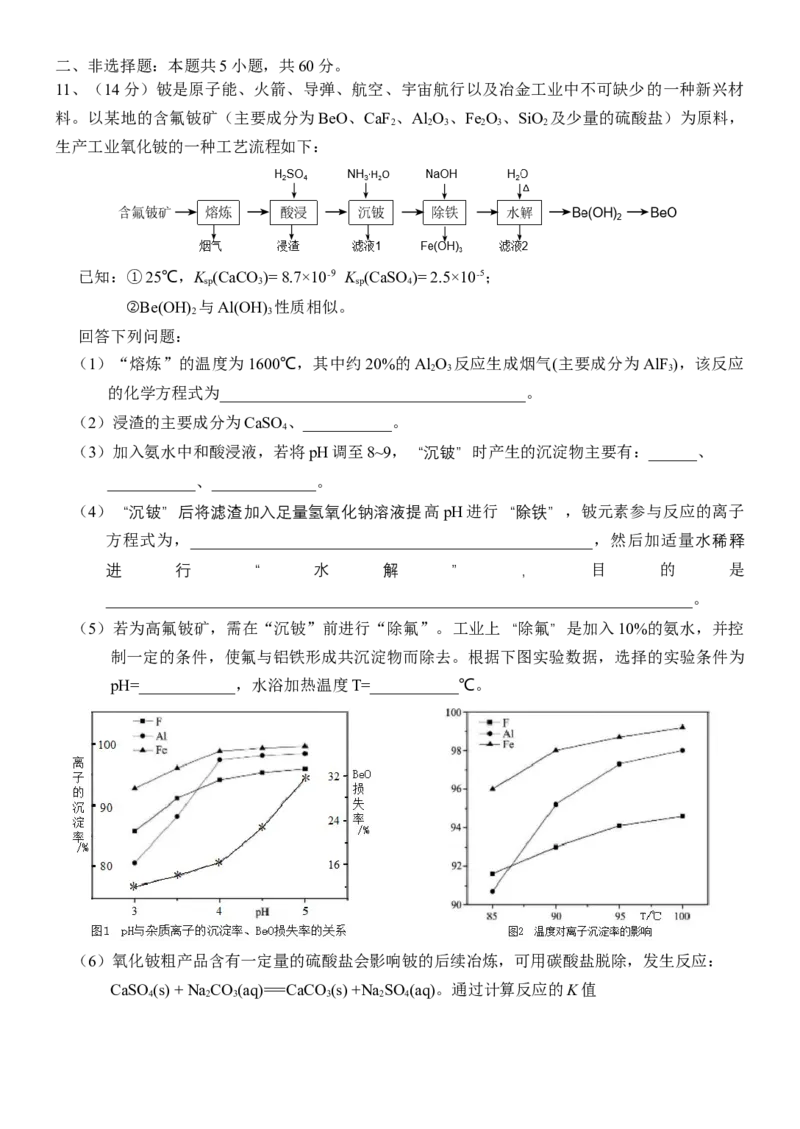
8、A、B、C、D、E是原子序数依次增大的五种常见的短周期主族元素,其中A、B、C、D四种元素
的原子序数之和为E元素原子序数的2倍。E是短周期中原子半径最大的元素。A、B、C、D四
种元素形成的化合物[CA]+[BD]-有多种用途,可用来合成纳米管,还可作杀虫剂、催化剂、
4 4
助熔剂、阻燃剂等,其结构如图所示。下列说法正确的是
A.元素A、C能形成含有非极性键的18电子化合物
B.最简单氢化物的稳定性:C>D
C.元素A、E形成的化合物不能与水发生氧化还原反应
D.化合物 中各原子均满足89.据文献报道,一种新型的微生物脱盐电池的装置如图所示,关于该电池装置说法正确的是
A.Y为阴离子选择性交换膜
B.左室溶液碱性增强
C.负极反应是CHCOO- +2H O-8e-=2CO ↑+7H+
3 2 2
D.转移2 mol电子,海水脱去氯化钠的质量是58.5 g
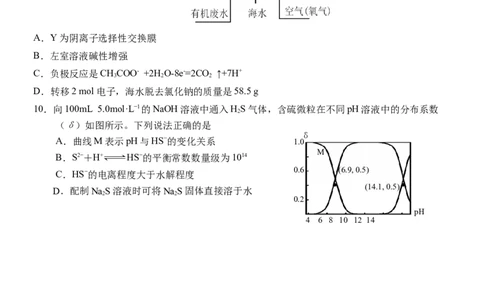
10.向100mL 5.0mol·L−1的NaOH溶液中通入HS气体,含硫微粒在不同pH溶液中的分布系数
2
(δ)如图所示。下列说法正确的是
δ
A.曲线M表示pH与HS−的变化关系 1.0
M
B.S2−+H+ HS−的平衡常数数量级为1014
0.6 (6.9, 0.5)
C.HS−的电离程度大于水解程度
· ·
(14.1, 0.5)
D.配制NaS溶液时可将NaS固体直接溶于水
2 2
0.2
pH
4 6 8 10 12 14二、非选择题:本题共5小题,共60分。
11、(14分)铍是原子能、火箭、导弹、航空、宇宙航行以及冶金工业中不可缺少的一种新兴材
料。以某地的含氟铍矿(主要成分为BeO、CaF 、Al O 、Fe O 、SiO 及少量的硫酸盐)为原料,
2 2 3 2 3 2
生产工业氧化铍的一种工艺流程如下:
已知:①25℃,K (CaCO )= 8.7×10-9 K (CaSO)= 2.5×10-5;
sp 3 sp 4
②Be(OH) 与Al(OH) 性质相似。
2 3
回答下列问题:
(1)“熔炼”的温度为1600℃,其中约20%的Al O 反应生成烟气(主要成分为AlF),该反应
2 3 3
的化学方程式为______________________________________。
(2)浸渣的主要成分为CaSO、___________。
4
(3)加入氨水中和酸浸液,若将pH调至8~9,“沉铍”时产生的沉淀物主要有:______、
___________、_____________。
(4)“沉铍”后将滤渣加入足量氢氧化钠溶液提高pH进行“除铁”,铍元素参与反应的离子
方程式为,__________________________________________________,然后加适量水稀释
进 行 “ 水 解 ” , 目 的 是
_________________________________________________________________________。
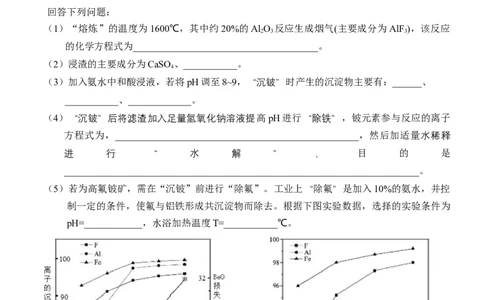
(5)若为高氟铍矿,需在“沉铍”前进行“除氟”。工业上“除氟”是加入10%的氨水,并控
制一定的条件,使氟与铝铁形成共沉淀物而除去。根据下图实验数据,选择的实验条件为
pH=____________,水浴加热温度T=___________℃。
(6)氧化铍粗产品含有一定量的硫酸盐会影响铍的后续冶炼,可用碳酸盐脱除,发生反应:
CaSO(s) + Na CO(aq)=CaCO (s) +Na SO (aq)。通过计算反应的K值
4 2 3 3 2 4说明用碳酸钠脱硫酸根反应的程度大小:_________________________
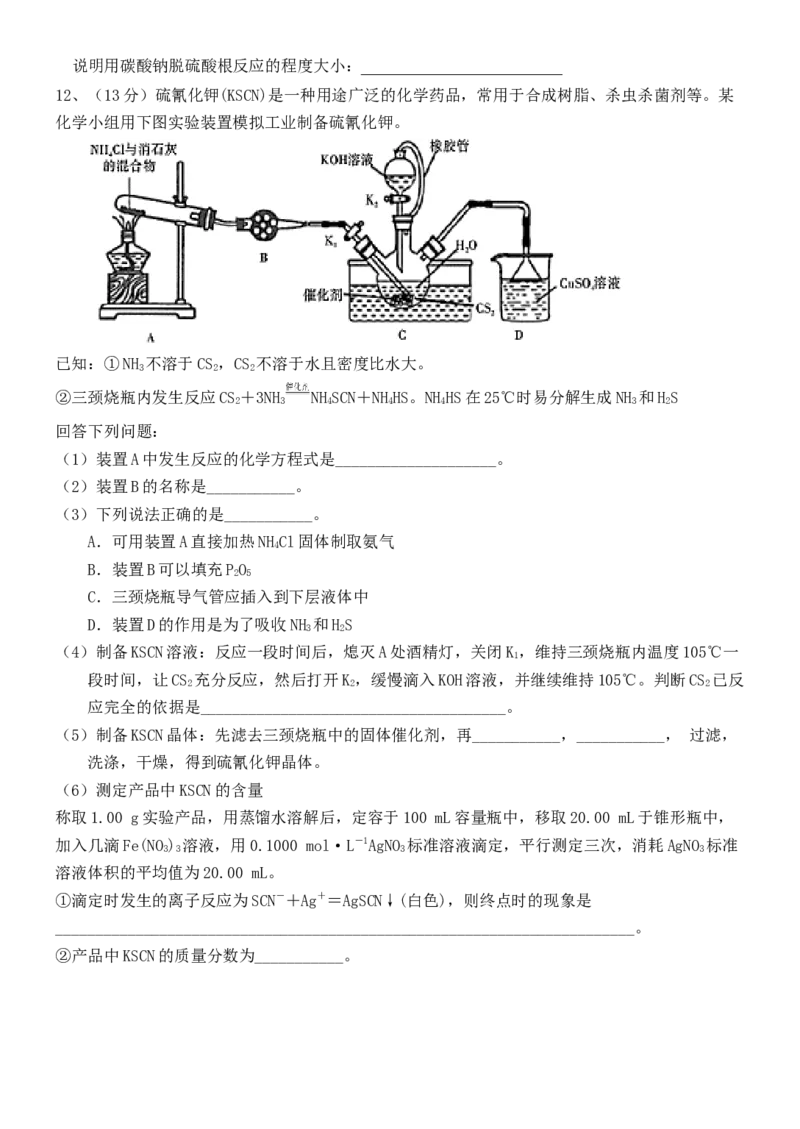
12、(13分)硫氰化钾(KSCN)是一种用途广泛的化学药品,常用于合成树脂、杀虫杀菌剂等。某
化学小组用下图实验装置模拟工业制备硫氰化钾。
已知:①NH 不溶于CS,CS 不溶于水且密度比水大。
3 2 2
②三颈烧瓶内发生反应CS+3NH NHSCN+NHHS。NHHS在25℃时易分解生成NH 和HS
2 3 4 4 4 3 2
回答下列问题:
(1)装置A中发生反应的化学方程式是____________________。
(2)装置B的名称是___________。
(3)下列说法正确的是___________。
A.可用装置A直接加热NHCl固体制取氨气
4
B.装置B可以填充PO
2 5
C.三颈烧瓶导气管应插入到下层液体中
D.装置D的作用是为了吸收NH 和HS
3 2
(4)制备KSCN溶液:反应一段时间后,熄灭A处酒精灯,关闭K,维持三颈烧瓶内温度105℃一
1
段时间,让CS 充分反应,然后打开K,缓慢滴入KOH溶液,并继续维持105℃。判断CS 已反
2 2 2
应完全的依据是______________________________________。
(5)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再___________,___________, 过滤,
洗涤,干燥,得到硫氰化钾晶体。
(6)测定产品中KSCN的含量
称取1.00 g实验产品,用蒸馏水溶解后,定容于100 mL容量瓶中,移取20.00 mL于锥形瓶中,
加入几滴Fe(NO) 溶液,用0.1000 mol·L-1AgNO 标准溶液滴定,平行测定三次,消耗AgNO 标准
3 3 3 3
溶液体积的平均值为20.00 mL。
①滴定时发生的离子反应为SCN-+Ag+=AgSCN↓(白色),则终点时的现象是
________________________________________________________________________。
②产品中KSCN的质量分数为___________。13、(13分)甲烷催化裂解是工业上制备乙炔的方法之一。回答下列问题:
(1)已知:CH(g)+2O(g)=CO (g)+2HO(l) H=-885 kJ/mol
4 2 2 2 1
2C H(g)+5O(8)=4CO (g)+2HO(l) H= -2600 kJ/mol
2 2 2 2 2 2 △
2H(g)+O(g)=2HO(l) H =-572 kJ/mol
2 2 2 3 △
则2CH(g)=C H(g)+3H(g) H=_______kJ/mol
4 2 2 △2
(2)某科研小组尝试利用固体表面催化工艺进行CH 的裂解。
△ 4
①若用 分别表示CH、C H、H 和固体催化剂,在固体催化剂
4 2 2 2
表面CH 的裂解过程如图所示,从吸附到解吸的过程中,能量状态最高的是_______(填标号),其
4
理由是___________________________________________________________________________。
②在恒容密闭容器中充入a mol甲烷,测得单位时间内在固体催化剂表面CH 的转化率[ɑ(CH )]与
4 4
温度(t °C)的关系如图所示,t℃后CH 的转化率突减的原因可能是
0 0 4
_________________________________________________。
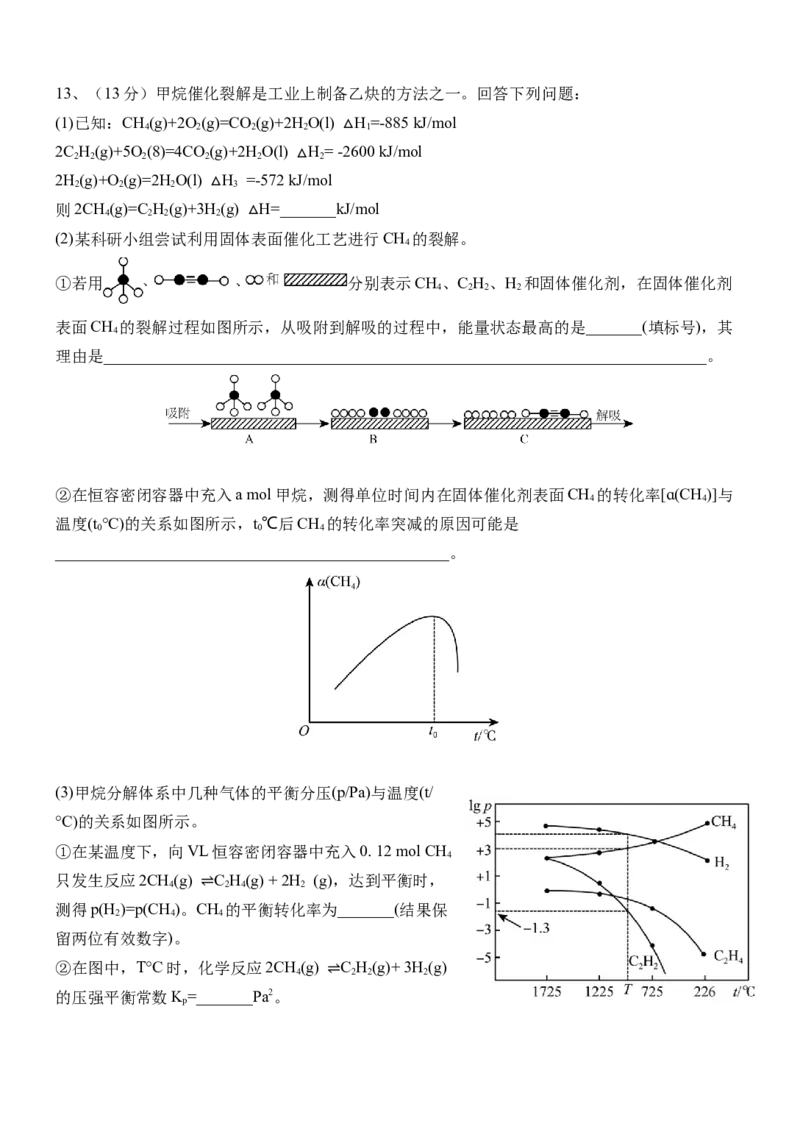
(3)甲烷分解体系中几种气体的平衡分压(p/Pa)与温度(t/
°C)的关系如图所示。
①在某温度下,向VL恒容密闭容器中充入0. 12 mol CH
4
只发生反应2CH(g) C H(g) + 2H (g),达到平衡时,
4 2 4 2
测得p(H )=p(CH )。CH 的平衡转化率为_______(结果保
2 4 ⇌ 4
留两位有效数字)。
②在图中,T°C时,化学反应2CH(g) C H(g)+ 3H (g)
4 2 2 2
的压强平衡常数K=_______Pa2。
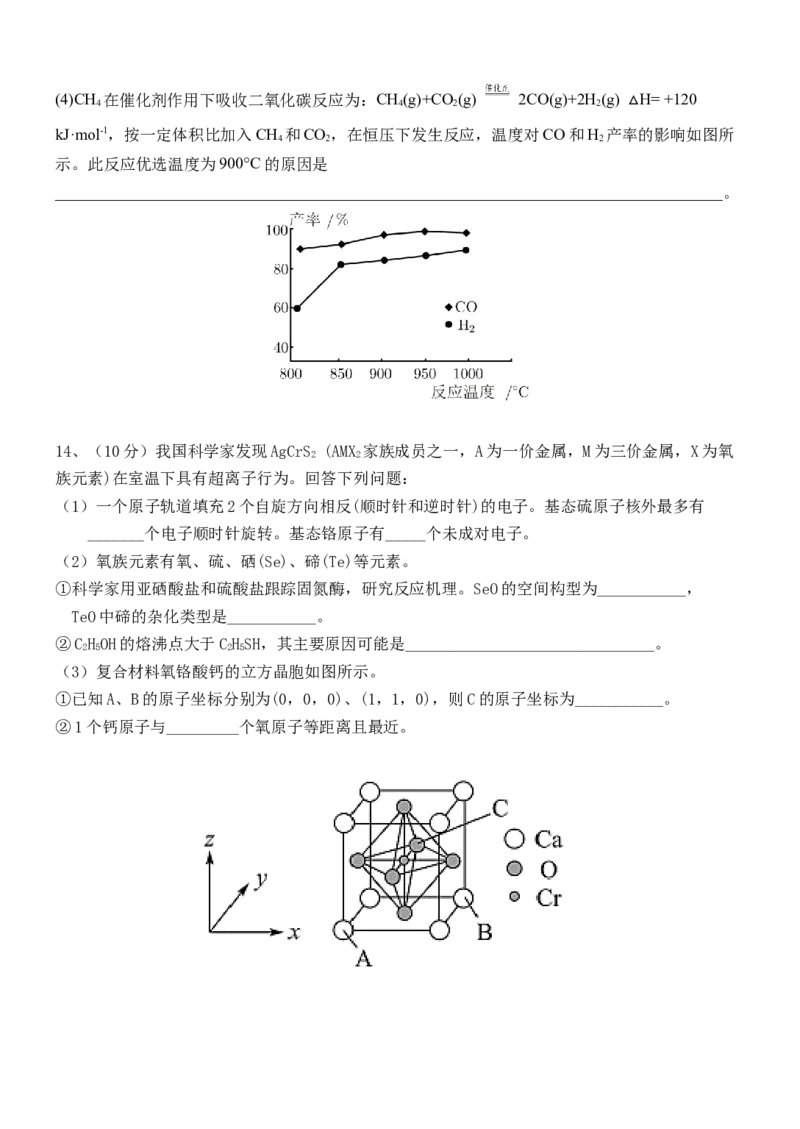
p ⇌(4)CH 在催化剂作用下吸收二氧化碳反应为:CH(g)+CO (g) 2CO(g)+2H (g) H= +120
4 4 2 2
kJ·mol-1,按一定体积比加入CH 和CO,在恒压下发生反应, 温度对CO和H 产率△的影响如图所
4 2 2
示。此反应优选温度为900°C的原因是
___________________________________________________________________________________。
14、(10分)我国科学家发现AgCrS (AMX 家族成员之一,A为一价金属,M为三价金属,X为氧
2 2
族元素)在室温下具有超离子行为。回答下列问题:
(1)一个原子轨道填充2个自旋方向相反(顺时针和逆时针)的电子。基态硫原子核外最多有
_______个电子顺时针旋转。基态铬原子有_____个未成对电子。
(2)氧族元素有氧、硫、硒(Se)、碲(Te)等元素。
①科学家用亚硒酸盐和硫酸盐跟踪固氮酶,研究反应机理。SeO的空间构型为___________,
TeO中碲的杂化类型是___________。
②CHOH的熔沸点大于CHSH,其主要原因可能是_______________________________。
2 5 2 5
(3)复合材料氧铬酸钙的立方晶胞如图所示。
①已知A、B的原子坐标分别为(0,0,0)、(1,1,0),则C的原子坐标为___________。
②1个钙原子与_________个氧原子等距离且最近。15、(10分)化合物I是一种非常有效的肾上腺素β-2受体激动剂,临床上广泛用于治疗支气管哮
喘等呼吸道疾病。其合成路线如下:
O
Br SOCl
H C CH C H O C H O 2 C H BrO 2 Br
2 2 2 6 2 4 2 P 2 3 2 Cl
A B C D E
OH
CHO
F
OH OH OH
CH OH CHO CHO
2 X
NHC(CH ) NHC(CH ) Br
HO 3 3 O 3 3 O
I H G
已知:
回答下列问题:
(1)下列说法正确的是______(填序号)。
A.A→B的反应类型为加成反应
B.B→C的反应条件可为:Cu,O,Δ
2
C.C能与B发生反应,该反应的原子利用率达100%
D.1molD最多可与2molNaOH溶液发生反应
(2)G的含氧官能团名称为___________________________。
( 3 ) E→G 的 反 应 方 程 式 为 为
________________________________________________________。
(4)已知:G+X→H+HBr,X的结构简式为_______________。
(5)H→I的反应类型为___________________。
(6)J(分子式为C HO)为F的同系物,同时满足下列条件的J的同分异构体有______种。
8 8 2
①能发生银镜反应;②在NaOH溶液中能反应生成两种有机物。
写出其中核磁共振氢谱图显示五组峰,且峰面积比为1:1:2:2:2的异构体的结构简
式
_______________________________。