文档内容
模板 02 化学反应机理图像分析
本节导航
识·题型解读 考情分析+命题预测/技巧解读
明 ·模板构建 答题模板 + 技巧点拨
技法01 基元反应和过渡态理论 技法02 反应历程能垒图
技法03 反应机理图
通·模板运用 真题示例+模板答题+变式训练
练 ·模板演练 最新模拟、预测考向
新高考强调素养为本的情境化命题,高考通过真实情境的创设,考查学生的信息获取能力和创新思维。
近几年高考中,化学反应机理(反应历程)试题频繁出现,主要以选择题的形式出现,题目主要以图
示的形式来描述某一化学变化所经由的全部反应,就是把一个复杂反应分解成若干个反应,然后按照
一定规律组合起来,从而达到阐述复杂反应的内在联系的目的。由于陌生度高,思维转化大,且命题
视角在不断地创新和发展,成为大多数考生的失分点。所以,很有必要对这两类题型的解题模型进行
掌握。
第一步:仔细审题 阅读题目获取对解题有价值的信息,排除无效信息,并作标记。
第二步:明确类型 判断图像类型是反应历程能垒图、反应机理循环图。
第三步:提取信息 提取图像关键信息,结合选项,分析判断。
①反应历程能垒图:分析随反应历程发生的能量变化与物质变化;
②反应机理图:分析机理图上物质的进出及转化关系。
技法01 基元反应和过渡态理论
1.基元反应(1)大多数的化学反应往往经过多个反应步骤才能实现,其中每一步反应都称为基元反应。
(2)基元反应速率方程
对于基元反应aA+bB===gG+hH,其速率方程可写为v=k·ca(A)·cb(B)(其中k称为速率常数,恒温下,
k不因反应物浓度的改变而变化),这种关系可以表述为基元反应的化学反应速率与反应物浓度以其化学计
量数为指数的幂的乘积成正比。
2.反应机理
基元反应构成的反应序列称为反应历程(又称反应机理),基元反应的总和称为总反应。由几个基元反
应组成的总反应也称复杂反应。
例如H(g)+I(g)===2HI(g),它的反应历程有如下两步基元反应:
2 2
II·+I·(快)
2
H+2I·===2HI(慢)
① 2
其中慢反应为整个反应的决速步骤。
②
3.过渡态理论
(1)化学反应并不是通过反应物分子的简单碰撞就能完成的,而是在反应物到生成物的过程中经过一个
高能的过渡态,处于过渡态的分子叫做活化络合物。活化络合物是一种高能量的不稳定的反应物原子组合
体,它能较快地分解为新的能量较低的较稳定的生成物。
(2)活化能(E)是处在过渡态的活化络合物分子平均能量与反应物分子平均能量的差值。
a
4.催化剂与反应历程
(1)催化剂对反应速率的影响
催化剂是通过降低化学反应所需的活化能来增大化学反应速率的。有催化剂参与的反应,活化能(E )
a1
较小,反应速率较大;没有催化剂参与的反应,活化能(E ')较大,反应速率较小。
a1
使用催化剂同时降低了正反应和逆反应的活化能,但反应的ΔH不变。
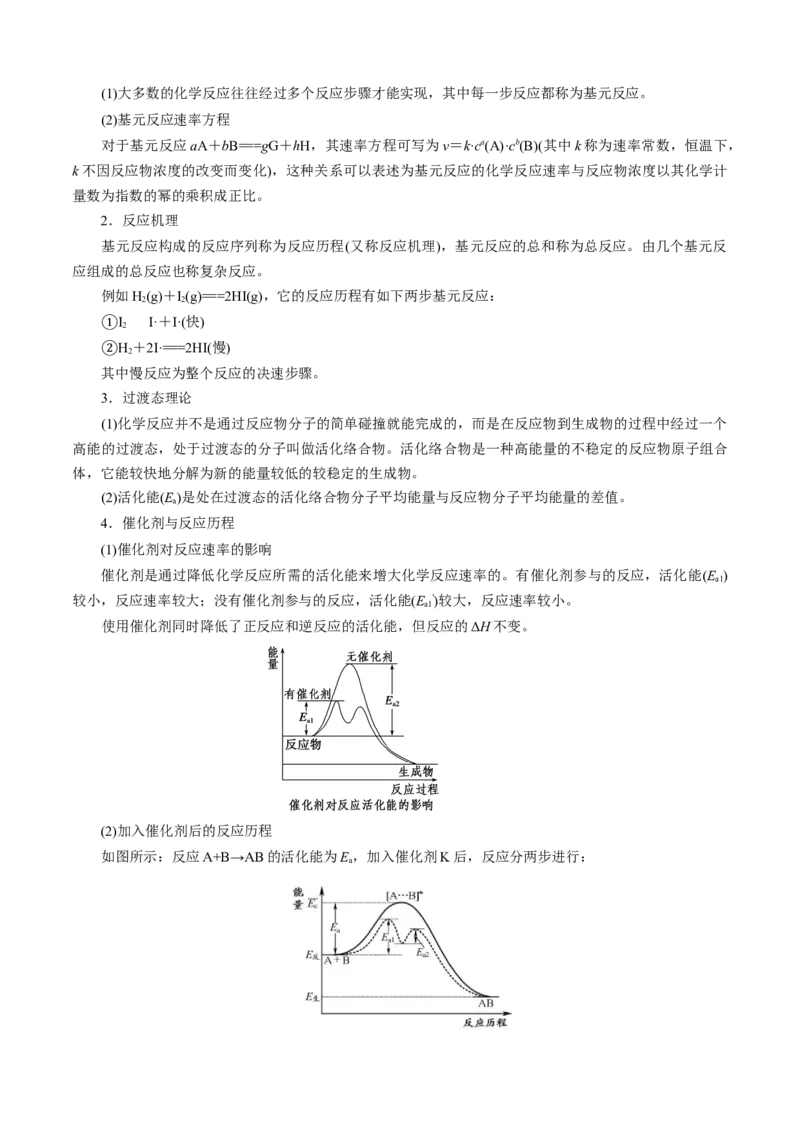
(2)加入催化剂后的反应历程
如图所示:反应A+B→AB的活化能为E,加入催化剂K后,反应分两步进行:
a①A+K→AK 活化能为E (慢反应)
a1
②AK+B→AB+K 活化能为E (快反应)
a2
总反应:A+B――→AB 活化能为E
a1
加入催化剂K后,两步反应的活化能E 和E 均小于原反应的活化能E,因此反应速率加快。
a1 a2 a
由于E >E ,第1步反应是慢反应,是决定整个反应快慢的步骤,称为“定速步骤”或“决速步骤”,
a1 a2
第1步反应越快,则整体反应速率就越快。因此对总反应来说,第一步反应的活化能E 就是在催化条件下
a1
总反应的活化能。
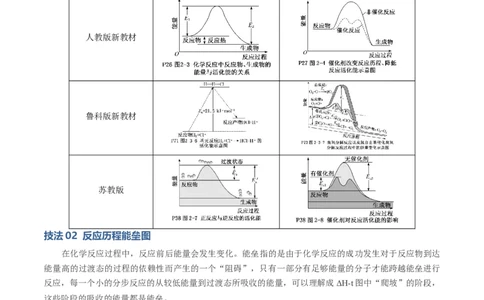
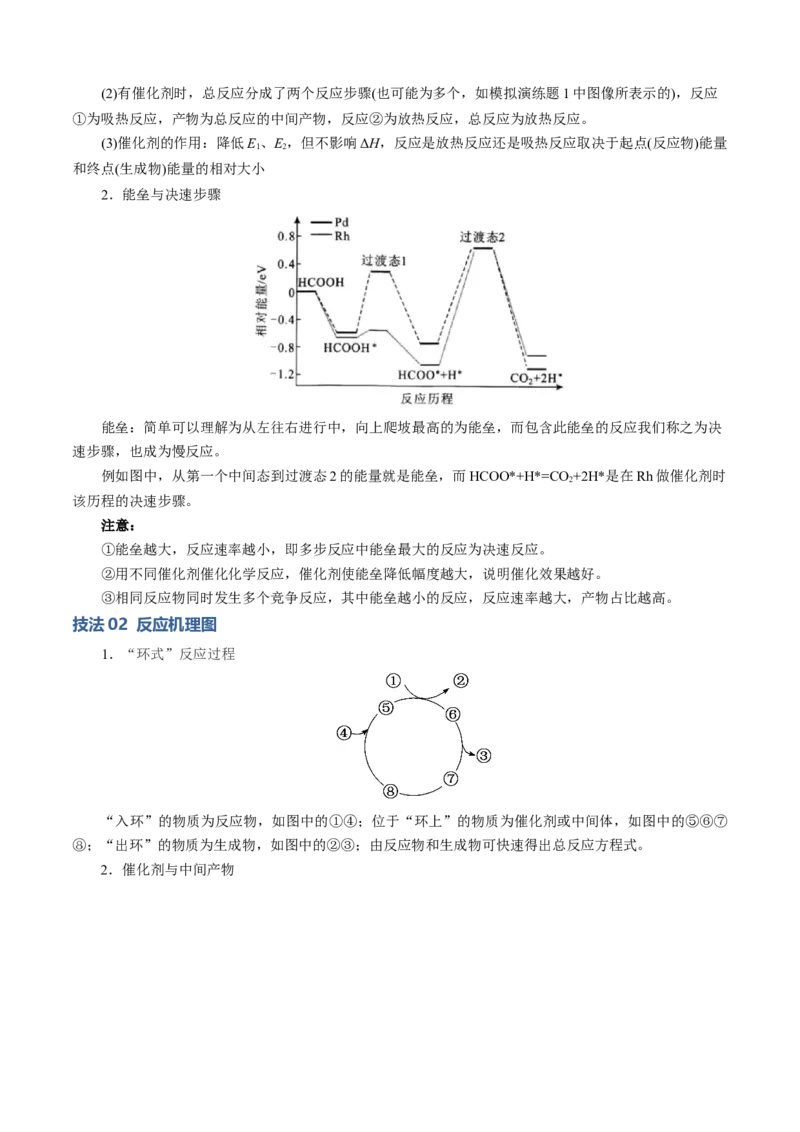
5.教材中的能量变化图示如下:
反应历程与活化能 催化剂对反应历程与活化能影响
人教版新教材
鲁科版新教材
苏教版
技法02 反应历程能垒图
在化学反应过程中,反应前后能量会发生变化。能垒指的是由于化学反应的成功发生对于反应物到达
能量高的过渡态的过程的依赖性而产生的一个“阻碍”,只有一部分有足够能量的分子才能跨越能垒进行
反应,每一个小的分步反应的从较低能量到过渡态所吸收的能量,可以理解成ΔH-t图中“爬坡”的阶段,
这些阶段的吸收的能量都是能垒。
1.催化剂与化学反应
(1)在无催化剂的情况下:E 为正反应的活化能;E 为逆反应的活化能;E-E 为此反应的焓变(ΔH)。
1 2 1 2(2)有催化剂时,总反应分成了两个反应步骤(也可能为多个,如模拟演练题1中图像所表示的),反应
①为吸热反应,产物为总反应的中间产物,反应②为放热反应,总反应为放热反应。
(3)催化剂的作用:降低E、E,但不影响ΔH,反应是放热反应还是吸热反应取决于起点(反应物)能量
1 2
和终点(生成物)能量的相对大小
2.能垒与决速步骤
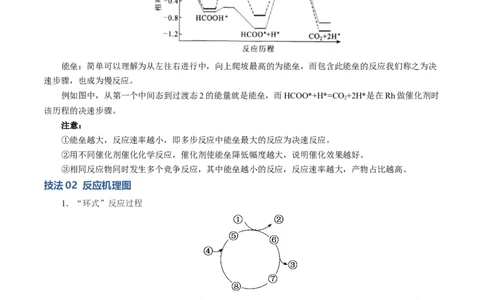
能垒:简单可以理解为从左往右进行中,向上爬坡最高的为能垒,而包含此能垒的反应我们称之为决
速步骤,也成为慢反应。
例如图中,从第一个中间态到过渡态2的能量就是能垒,而HCOO*+H*=CO +2H*是在Rh做催化剂时
2
该历程的决速步骤。
注意:
①能垒越大,反应速率越小,即多步反应中能垒最大的反应为决速反应。
②用不同催化剂催化化学反应,催化剂使能垒降低幅度越大,说明催化效果越好。
③相同反应物同时发生多个竞争反应,其中能垒越小的反应,反应速率越大,产物占比越高。
技法02 反应机理图
1.“环式”反应过程
“入环”的物质为反应物,如图中的①④;位于“环上”的物质为催化剂或中间体,如图中的⑤⑥⑦
⑧;“出环”的物质为生成物,如图中的②③;由反应物和生成物可快速得出总反应方程式。
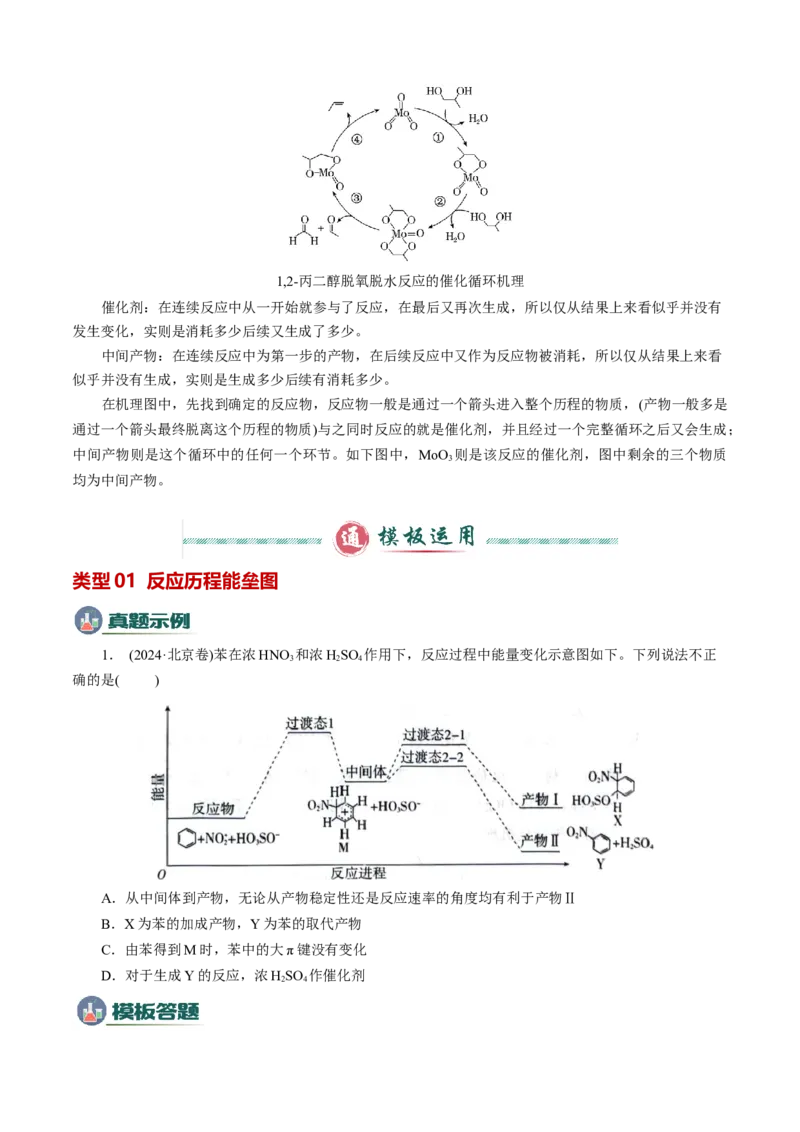
2.催化剂与中间产物1,2-丙二醇脱氧脱水反应的催化循环机理
催化剂:在连续反应中从一开始就参与了反应,在最后又再次生成,所以仅从结果上来看似乎并没有
发生变化,实则是消耗多少后续又生成了多少。
中间产物:在连续反应中为第一步的产物,在后续反应中又作为反应物被消耗,所以仅从结果上来看
似乎并没有生成,实则是生成多少后续有消耗多少。
在机理图中,先找到确定的反应物,反应物一般是通过一个箭头进入整个历程的物质,(产物一般多是
通过一个箭头最终脱离这个历程的物质)与之同时反应的就是催化剂,并且经过一个完整循环之后又会生成;
中间产物则是这个循环中的任何一个环节。如下图中,MoO 则是该反应的催化剂,图中剩余的三个物质
3
均为中间产物。
类型01 反应历程能垒图
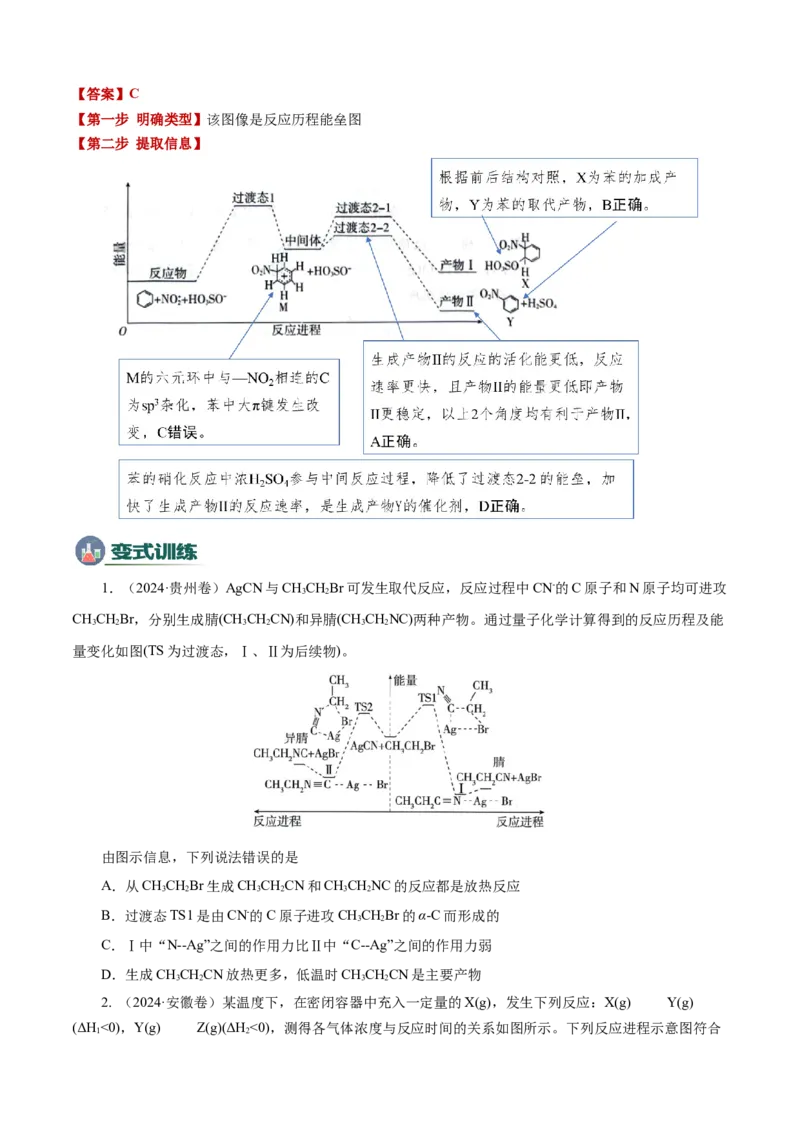
1. (2024·北京卷)苯在浓HNO 和浓HSO 作用下,反应过程中能量变化示意图如下。下列说法不正
3 2 4
确的是( )
A.从中间体到产物,无论从产物稳定性还是反应速率的角度均有利于产物Ⅱ
B.X为苯的加成产物,Y为苯的取代产物
C.由苯得到M时,苯中的大π键没有变化
D.对于生成Y的反应,浓HSO 作催化剂
2 4【答案】C
【第一步 明确类型】该图像是反应历程能垒图
【第二步 提取信息】
1.(2024·贵州卷)AgCN与CHCHBr可发生取代反应,反应过程中CN-的C原子和N原子均可进攻
3 2
CHCHBr,分别生成腈(CHCHCN)和异腈(CHCHNC)两种产物。通过量子化学计算得到的反应历程及能
3 2 3 2 3 2
量变化如图(TS为过渡态,Ⅰ、Ⅱ为后续物)。
由图示信息,下列说法错误的是
A.从CHCHBr生成CHCHCN和CHCHNC的反应都是放热反应
3 2 3 2 3 2
B.过渡态TS1是由CN-的C原子进攻CHCHBr的α-C而形成的
3 2
C.Ⅰ中“N--Ag”之间的作用力比Ⅱ中“C--Ag”之间的作用力弱
D.生成CHCHCN放热更多,低温时CHCHCN是主要产物
3 2 3 2
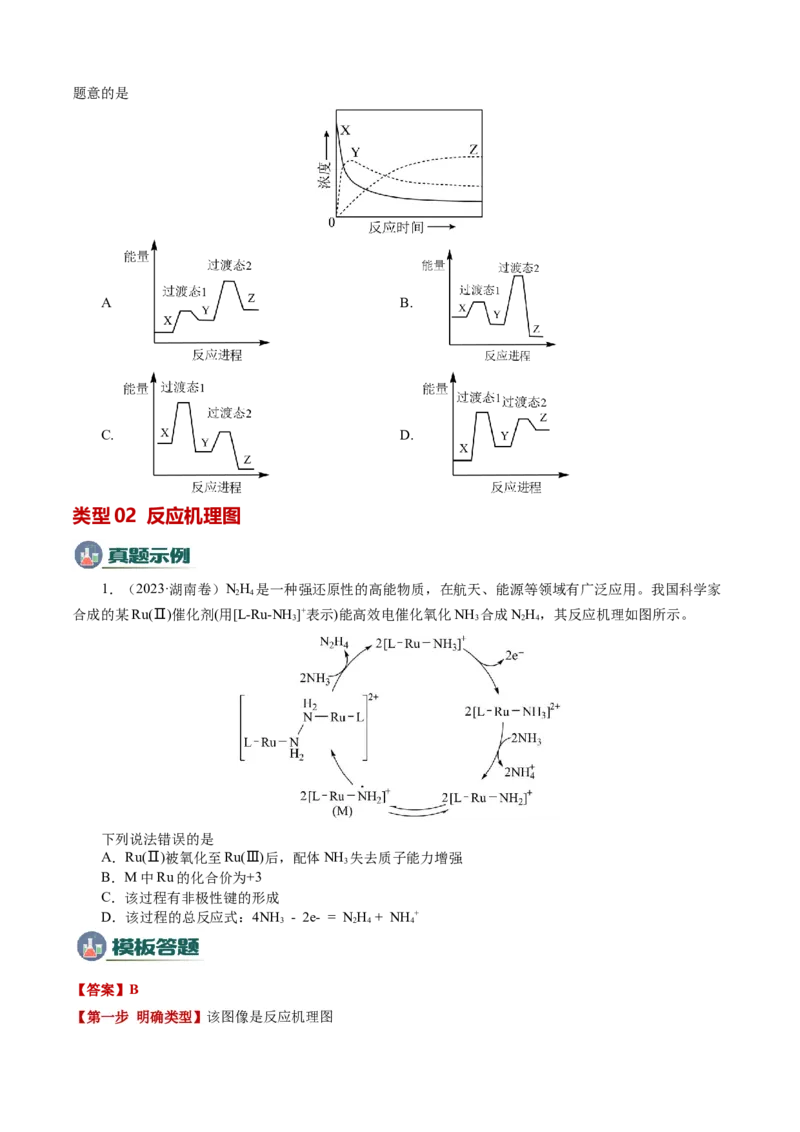
2. (2024·安徽卷)某温度下,在密闭容器中充入一定量的X(g),发生下列反应:X(g) Y(g)
(ΔH <0),Y(g) Z(g)(ΔH<0),测得各气体浓度与反应时间的关系如图所示。下列反应进程示意图符合
1 2题意的是
A B.
.
C. D.
类型02 反应机理图
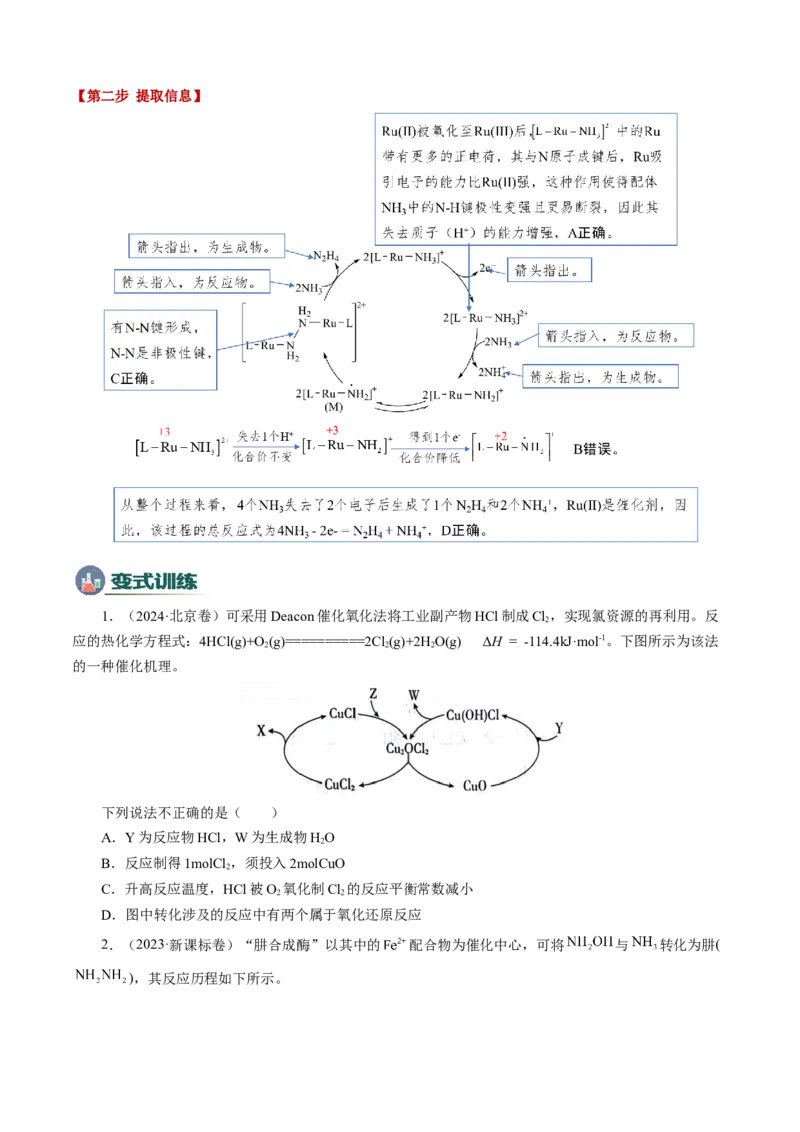
1.(2023·湖南卷)NH 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家
2 4
合成的某Ru(Ⅱ)催化剂(用[L-Ru-NH ]+表示)能高效电催化氧化NH 合成NH,其反应机理如图所示。
3 3 2 4
下列说法错误的是
A.Ru(Ⅱ)被氧化至Ru(Ⅲ)后,配体NH 失去质子能力增强
3
B.M中Ru的化合价为+3
C.该过程有非极性键的形成
D.该过程的总反应式:4NH - 2e- = NH + NH +
3 2 4 4
【答案】B
【第一步 明确类型】该图像是反应机理图【第二步 提取信息】
1.(2024·北京卷)可采用Deacon催化氧化法将工业副产物HCl制成Cl,实现氯资源的再利用。反
2
应的热化学方程式:4HCl(g)+O (g)==========2Cl(g)+2HO(g) ΔH = -114.4kJ·mol-1。下图所示为该法
2 2 2
的一种催化机理。
下列说法不正确的是( )
A.Y为反应物HCl,W为生成物HO
2
B.反应制得1molCl ,须投入2molCuO
2
C.升高反应温度,HCl被O 氧化制Cl 的反应平衡常数减小
2 2
D.图中转化涉及的反应中有两个属于氧化还原反应
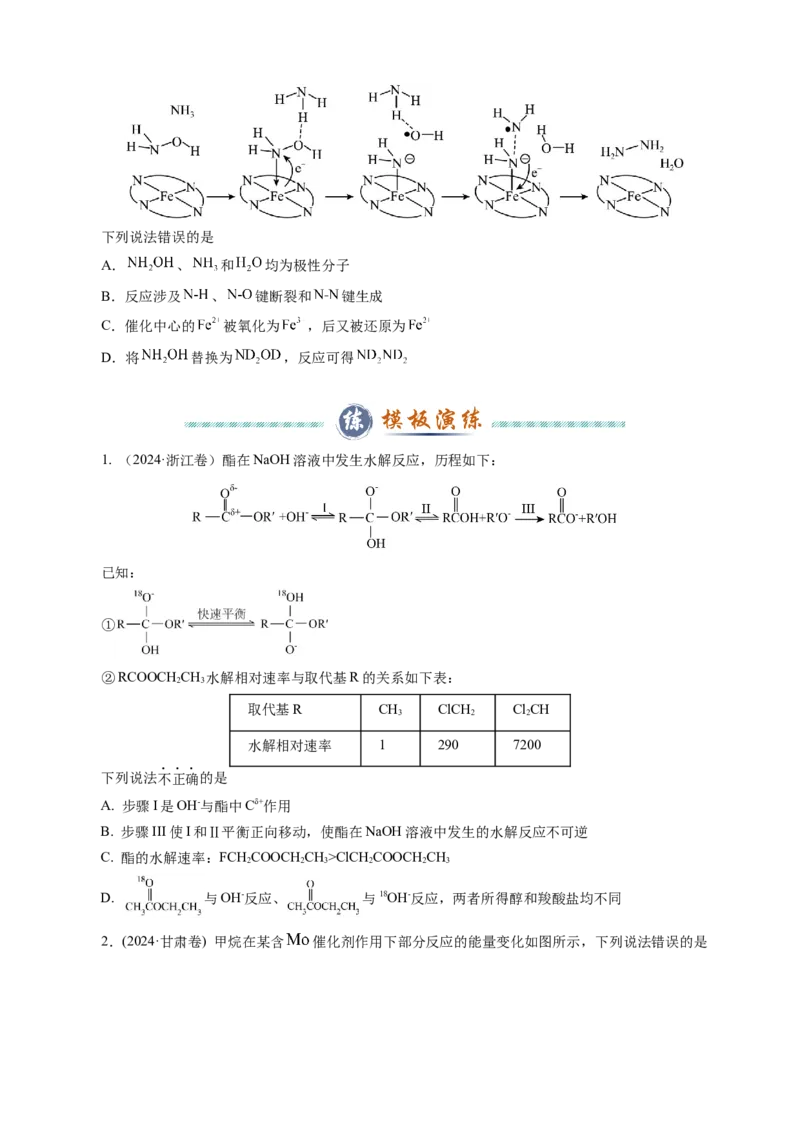
2.(2023·新课标卷)“肼合成酶”以其中的 配合物为催化中心,可将 与 转化为肼(
),其反应历程如下所示。下列说法错误的是
A. 、 和 均为极性分子
B.反应涉及 、 键断裂和 键生成
C.催化中心的 被氧化为 ,后又被还原为
D.将 替换为 ,反应可得
1. (2024·浙江卷)酯在NaOH溶液中发生水解反应,历程如下:
已知:
①
②RCOOCH CH 水解相对速率与取代基R的关系如下表:
2 3
取代基R CH ClCH ClCH
3 2 2
水解相对速率 1 290 7200
下列说法不正确的是
A. 步骤I是OH-与酯中Cδ+作用
B. 步骤III使I和Ⅱ平衡正向移动,使酯在NaOH溶液中发生的水解反应不可逆
C. 酯的水解速率:FCH COOCH CH>ClCH COOCH CH
2 2 3 2 2 3
D. 与OH-反应、 与18OH-反应,两者所得醇和羧酸盐均不同
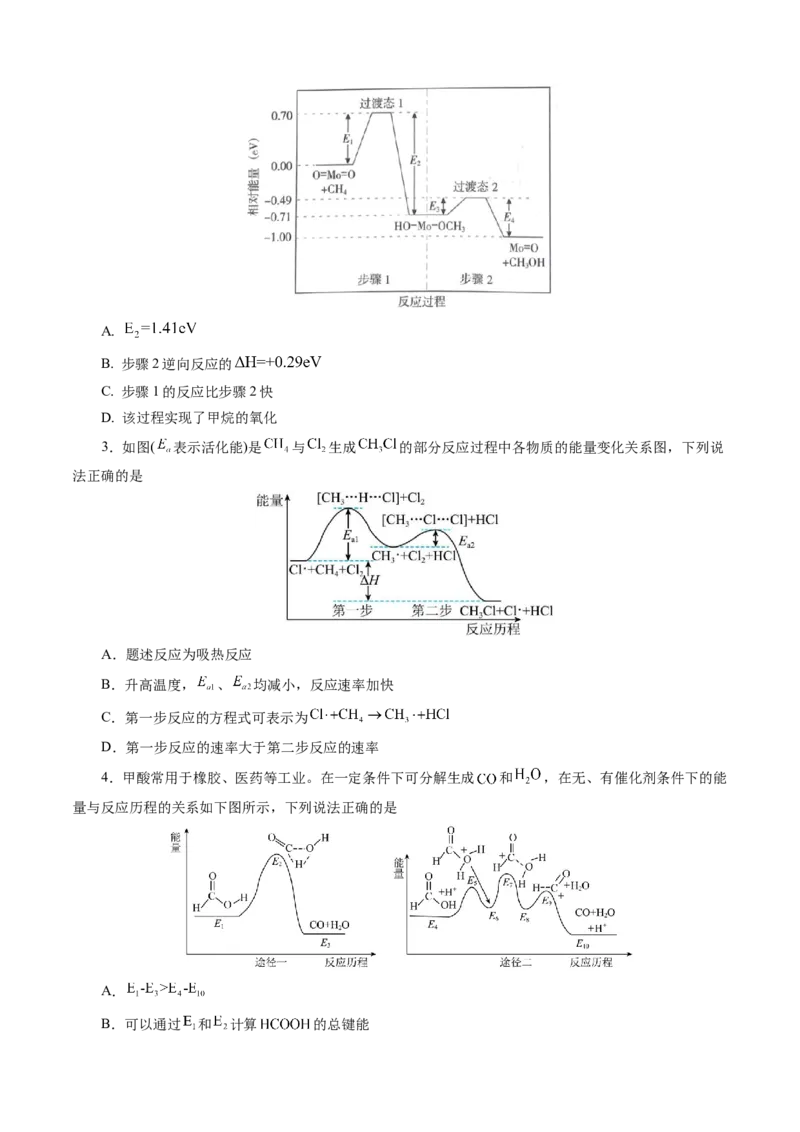
2.(2024·甘肃卷) 甲烷在某含 催化剂作用下部分反应的能量变化如图所示,下列说法错误的是A.
B. 步骤2逆向反应的
C. 步骤1的反应比步骤2快
D. 该过程实现了甲烷的氧化
3.如图( 表示活化能)是 与 生成 的部分反应过程中各物质的能量变化关系图,下列说
法正确的是
A.题述反应为吸热反应
B.升高温度, 、 均减小,反应速率加快
C.第一步反应的方程式可表示为
D.第一步反应的速率大于第二步反应的速率
4.甲酸常用于橡胶、医药等工业。在一定条件下可分解生成 和 ,在无、有催化剂条件下的能
量与反应历程的关系如下图所示,下列说法正确的是
A.
B.可以通过 和 计算 的总键能C.途径二中 参与反应,是该反应过程的中间产物
D.途径二中反应的快慢由生成 的速率决定
5.已知 催化反应 历程如下图所示,催化历程中有 参
与。下列有关该反应的说法正确的是
A.步骤①的速率常数大于步骤②
B.反应历程中存在非极性键的断裂和形成
C.催化历程中,仅氧元素的化合价未发生变化
D.步骤②的热化学方程为:
6.标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下(已知O 和Cl 的相对能量为
2 2
0),下列说法错误的是
A.
B.可计算 键能为
C.相同条件下,O 的平衡转化率:历程Ⅱ=历程Ⅰ
3
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
ClO(g)+O(g)=O (g)+Cl(g) ΔH=(E-E )kJ∙mol−1
2 4 5
7.利用计算机技术测得乙炔( )在 催化作用下生成 的反应历程及相对能量变化
如图所示。下列说法正确的是A. 的
B.反应历程中能量最高的物质中含有两种官能团
C.升高反应体系的温度可以提高乙炔的平衡转化率
D.决速步骤的反应为
8.某酮和甲胺的反应机理及能量图像如图所示:
下列说法错误的是
A.该历程中 为催化剂,故 浓度越大,反应速率越快
B.该历程中发生了加成反应和消去反应
C.反应过程中有极性键的断裂和生成
D.该历程中制约反应速率的反应为反应②
9.一定条件下,丙烯与 反应生成 和 的反应历程如图所示。【已知
Arrhenius经验公式为 ( 为活化能,k为速率常数,R和C为常数)】,下列说法正确的是A.反应 的 为
B.丙烯与 的加成反应为放热反应,所以该反应一定能自发进行
C.其他条件不变,适当升高温度可以提高加成产物 的比例
D.根据该反应推测,丙烯与 加成的主要产物为2-溴丙烷
10.如果在反应体系中只有底物和溶剂,没有另加试剂,那么底物就将与溶剂发生反应,溶剂就成了
试剂,这样的反应称为溶剂解反应。如三级溴丁烷在乙醇中可以发生溶剂解反应,反应的机理和能量进程
图如下所示:
下列说法不正确的是
A.三级溴丁烷在乙醇中的溶剂解反应属于取代反应
B.不同卤代烃在乙醇中发生溶剂解反应的速率取决于相应碳卤键的键能
C.该反应机理中的中间产物 中的碳原子有两种杂化方式
D.卤代烃在发生消去反应时可能会有醚生成
11.为早日实现“碳中和碳达峰”目标,科学家提出用钌(Ru)基催化剂催化 和 反应生成
HCOOH.反应机理如图所示,已知当生成46g液态HCOOH时放出31.2kJ的热量。下列说法正确的是A.反应历程中存在极性键、非极性键的断裂与形成
B.物质Ⅰ为该反应的催化剂,物质Ⅱ、Ⅲ为中间产物
C.催化剂能降低活化能,加快反应速率,改变反应热,从而提高转化率
D.通过 和 反应制备液态HCOOH,每转移1mol ,放出31.2kJ的热量
12.氢能是一种重要的清洁能源,由 可以制得 。在催化剂作用下, 催化释放氢的
反应机理和相对能量的变化情况分别如图1和图2所示。下列叙述正确的是
A. 催化释放氢的过程中有非极性键的断裂与形成
B. 催化释放氢反应除生成 外,还生成
C.在催化剂表面解离 键比解离 键难
D. 催化释放氢的热化学方程式为:
13.我国科研团队研究 电催化合成氨反应[ ]时,发现不同电
解质溶液对催化历程的影响如图所示,其中吸附在催化剂表面的物种用*标注。下列说法错误的是
A.反应放热是合成氨反应自发进行的主要助力B.选用 作电解质的反应速率比选用 的快
C. 先吸附于催化剂表面再参加合成氨反应
D.形成 键合作用时,合成氨反应的 的绝对值更大
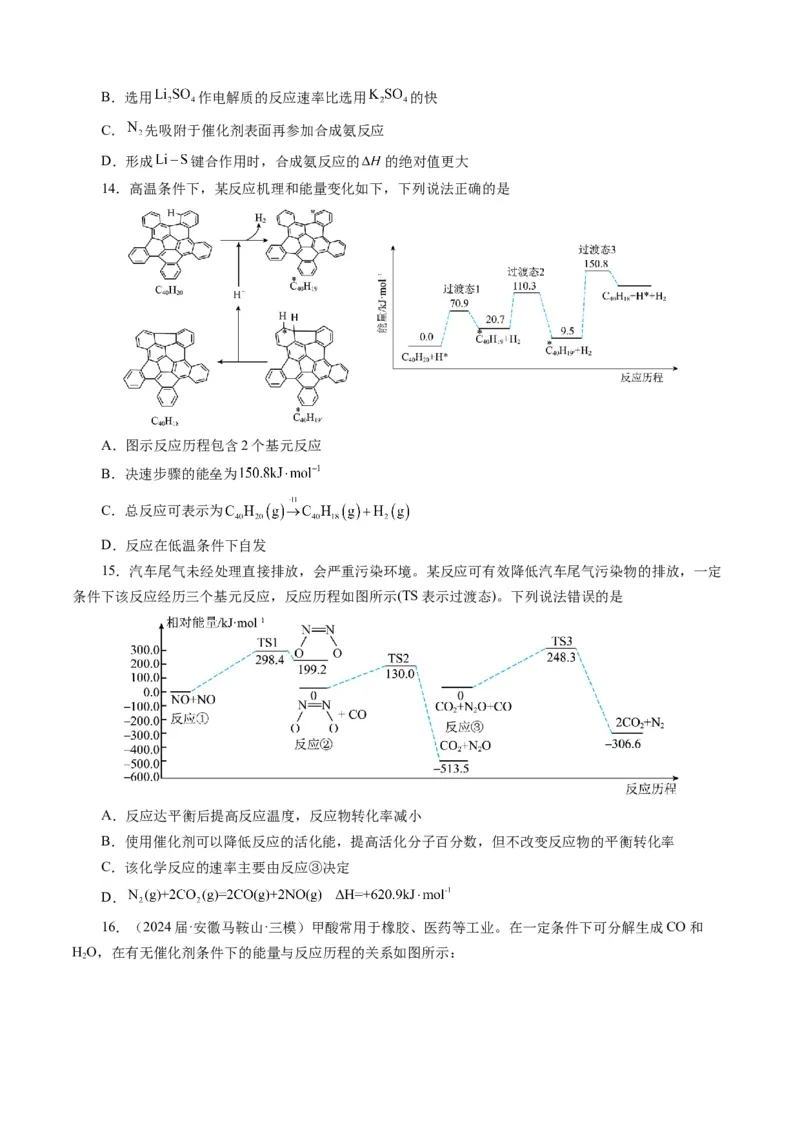
14.高温条件下,某反应机理和能量变化如下,下列说法正确的是
A.图示反应历程包含2个基元反应
B.决速步骤的能垒为
C.总反应可表示为
D.反应在低温条件下自发
15.汽车尾气未经处理直接排放,会严重污染环境。某反应可有效降低汽车尾气污染物的排放,一定
条件下该反应经历三个基元反应,反应历程如图所示(TS表示过渡态)。下列说法错误的是
A.反应达平衡后提高反应温度,反应物转化率减小
B.使用催化剂可以降低反应的活化能,提高活化分子百分数,但不改变反应物的平衡转化率
C.该化学反应的速率主要由反应③决定
D.
16.(2024届·安徽马鞍山·三模)甲酸常用于橡胶、医药等工业。在一定条件下可分解生成CO和
HO,在有无催化剂条件下的能量与反应历程的关系如图所示:
2下列说法错误的是
A.该反应为放热反应
B.若用D(氘)标记甲酸中的羧基氢,最终产物中可能存在DHO
C.途径Ⅱ的反应历程中,存在3种中间产物
D.由途径Ⅱ可知氢离子可以作为甲酸分解生成CO和HO的催化剂
2
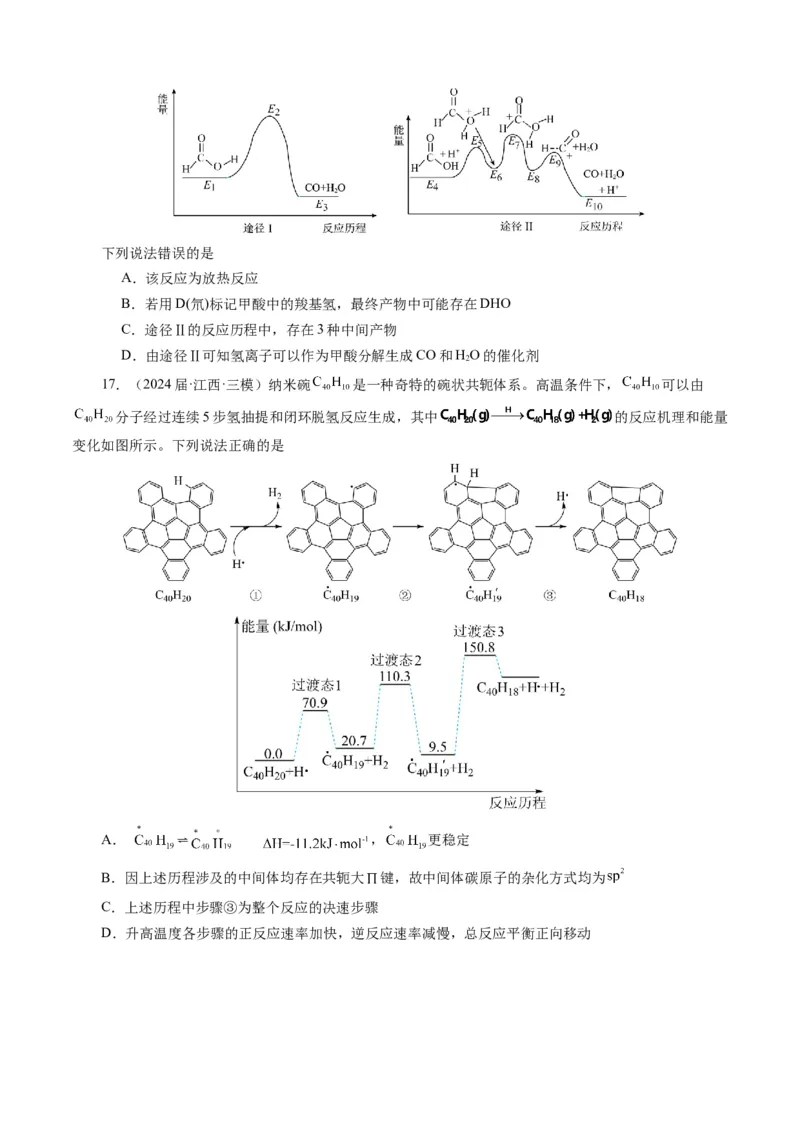
17.(2024届·江西·三模)纳米碗 是一种奇特的碗状共轭体系。高温条件下, 可以由
分子经过连续5步氢抽提和闭环脱氢反应生成,其中 的反应机理和能量
变化如图所示。下列说法正确的是
A. ⇌ , 更稳定
B.因上述历程涉及的中间体均存在共轭大 键,故中间体碳原子的杂化方式均为
C.上述历程中步骤③为整个反应的决速步骤
D.升高温度各步骤的正反应速率加快,逆反应速率减慢,总反应平衡正向移动