文档内容
专项训练 滴定前指示剂的选择(解析版)
1.(2023春·重庆沙坪坝·高三重庆一中校考阶段练习)用0.1000 mol-1的NaOH溶液
分别滴定0.1000 mol/L、20.00mLHX、HY、HZ三种酸溶液。溶液pH与加入NaOH体
积之间的关系如图所示,下列说法错误的是
A.HX为一元强酸,电离常数K(HY)>K(HZ)
a a
B.a、b、c三点中,b点所对应的水溶液里阴离子的物质的量浓度最大
C.d点所对应的水溶液里,c(OH-)约为0.02 mol/L
D.滴定时使用酚酞作指示剂,会产生系统误差,但可通过空白对照实验消除
【答案】B
【分析】如图,0.1000mol/L的HX、HY、HZ的pH分别为1、2,4左右,根据酸性越
强电离程度越大,所以酸性:HX>HY>HZ,因为0.1000mol/L的HX溶液,pH=1,所
以HX为一元强酸,依此解题;
【详解】A.综上所述,HX为一元强酸,HY和HZ为弱酸,且酸性HY>HZ,所以
K (HY)>K (HZ),故A正确;
a a
B.HX为强酸,HY和HZ为弱酸,且a、b点时HY、HZ酸尚未完全中和,故溶液中
阴离子浓度最大的为c点,故B错误;
C.d点时,加入NaOH溶液体积为30mL,过量10mL,此时溶液总体积为50mL,溶
0.1mol/L×0.01L
液中c(OH-)约为 =0.02mol/L,故C正确;
0.05L
D.酚酞的变色范围(pH)为8.2~10,由题图中的滴定终点附近各溶液的pH突变范围可
知,用强碱滴定HX、HY、HZ溶液时,可以使用酚酞作为指示剂,产生的系统误差,
可通过空白对照实验消除,故D正确;
故选B。
试卷第1页,共30页
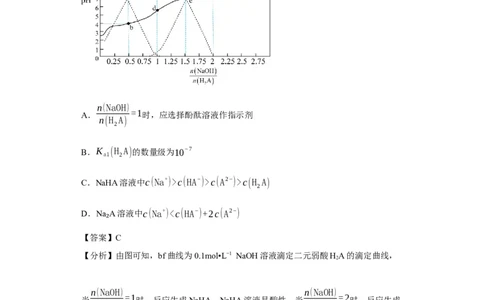
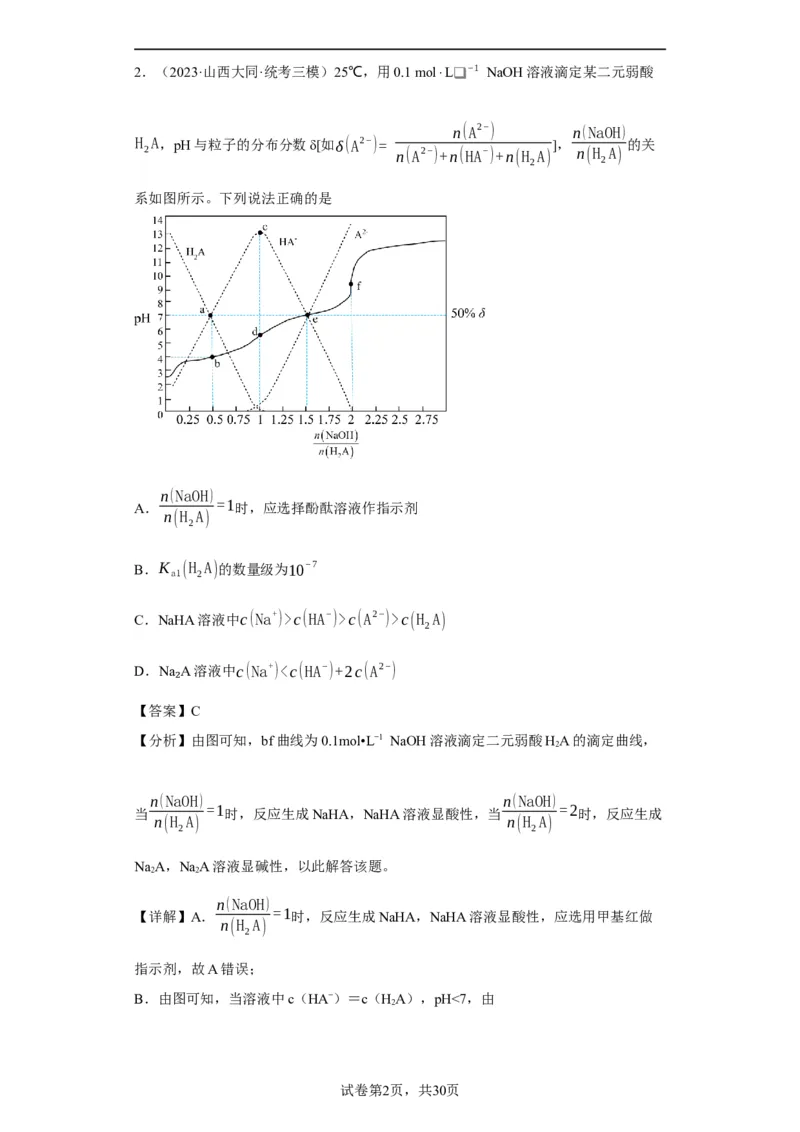
学科网(北京)股份有限公司2.(2023·山西大同·统考三模)25℃,用0.1 mol⋅L❑ −1 NaOH溶液滴定某二元弱酸
n(A2−) n(NaOH)
H A,pH与粒子的分布分数δ[如δ(A2−)= ], 的关
2 n(A2−)+n(HA−)+n(H A) n(H A)
2 2
系如图所示。下列说法正确的是
n(NaOH)
A.
=1时,应选择酚酞溶液作指示剂
n(H A)
2
B.K (H A)的数量级为10−7
a1 2
C.NaHA溶液中c(Na+)>c(HA−)>c(A2−)>c(H A)
2
D.Na A溶液中c(Na+)1×10−7,故B错误;
a1 c(H A)
2
¿
C.由分析可知,NaHA溶液显酸性,HA-电离程度大于水解程度;所以溶液中
c(Na+)>c(HA−)>c(A2−)>c(H A),故C正确;
2
D.NaA溶液中存在元素质量守恒关系:c(Na+)=2c(HA−)+2c(A2−)+2c(HA),所以
2 2
c(Na+)>c(HA−)+2c(A2−),故D错误;
故答案选C。
3.(2023·山东济宁·统考二模)实验室测定反应Ag++Fe2+
⇌
Fe3++Ag↓的平衡常数K
的过程为:
①一定温度下,将0.0100mol⋅L−1Ag SO 溶液与0.0400mol⋅L−1FeSO 溶液(pH=1)
2 4 4
等体积混合,产生灰黑色沉淀;
②待步骤①中反应达到平衡时,取v mL上层清液,用c mol⋅L−1KSCN标准溶液滴定
1
Ag+,至出现稳定的浅红色时消耗KSCN标准溶液v mL。
1
资料:Ag++SCN− ⇌ AgSCN↓(白色) K=1012,Fe3++SCN− ⇌ FeSCN2+ (红
色) K=102.3
下列说法正确的是
A.Ag SO 溶液可替换为AgNO 溶液
2 4 3
B.过程①中产生的灰黑色沉淀为Fe或Ag元素的氧化物
C.可用KCl标准溶液代替KSCN的标准溶液滴定Ag+
D.步骤②中不待溶液澄清,直接用浊液做滴定实验测定c(Ag+),则所测K值偏小
【答案】D
【详解】A.AgNO 溶液中的NO❑ −具有强氧化性能够将Fe2+氧化为Fe3+,影响反应
3 3
Ag++Fe2+
⇌
Fe3++Ag↓的平衡常数K测定,故A错误;
B.由方程式可知过程①中产生的灰黑色沉淀为Ag,故B错误;
C.硫氰化钾和铁离子形成红色溶液,氯化钾和铁离子不反应,故不能用KCl标准溶
液代替KSCN的标准溶液滴定Ag+,故C错误;
D.实验①所得浊液中还含有Ag,因存在平衡Ag++Fe2+
⇌
Fe3++Ag↓,且随着反应
Ag++SCN−
⇌
AgSCN↓的进行,使得Ag++Fe2+
⇌
Fe3++Ag↓平衡逆向移动,则测定平
试卷第3页,共30页
学科网(北京)股份有限公司c V
0.01- 1 1
c V V
衡体系中的c(Ag+)偏高, 1 1偏高,所得到的K= 偏小,故D正确;
V c 1 V 1( 0.01+ c 1 V 1)
V V
故选D。
4.(2023·山东德州·统考二模)电流滴定法(电压10-100 mV)是根据电流情况判断滴定
终点,如图所示,仅I 、I-同时存在时才能产生电流。可用此法来测定Na S O 溶液的
2 2 2 3
浓度。已知:2S O2-+I =S O2+2I- 。下列说法正确的是
2 3 2 4 6
A.a为滴定终点
B.ab段电流减小是因为离子浓度降低
C.应选用淀粉溶液做指示剂
D.若碘液中含有38.1 g的I ,硫代硫酸钠溶液的浓度为0.5mol⋅L-1
2
【答案】D
【详解】A.滴定终点时无I ,电流为0,a点电流最大,不是滴定终点,故A错误;
2
B.根据2S O2-+I =S O2+2I-,该反应生成的离子的物质的量增加,电流减少是因为
2 3 2 4 6
I 浓度的减少,故B错误;
2
C.不需要淀粉指示剂,电流就可以判断滴定情况,故C错误;
38.1g
D.若碘液中含有38.1 g的I ,n(I )= =0.15mol,
2 2 254g/mol
n(Na❑S❑ O❑)=2n(I )=0.3mol,V=600mL,所以硫代硫酸钠溶液的浓度为0.5
2 2 3 2
mol⋅L-1;故D正确;
故答案选D。
5.(2023·天津和平·统考二模)常温时,用0.100 0 mol⋅L−1的NaOH溶液滴定二元
酸H A溶液。溶液中,pH、分布系数δ随滴加V(NaOH)的变化关系如图所示。[比如
2
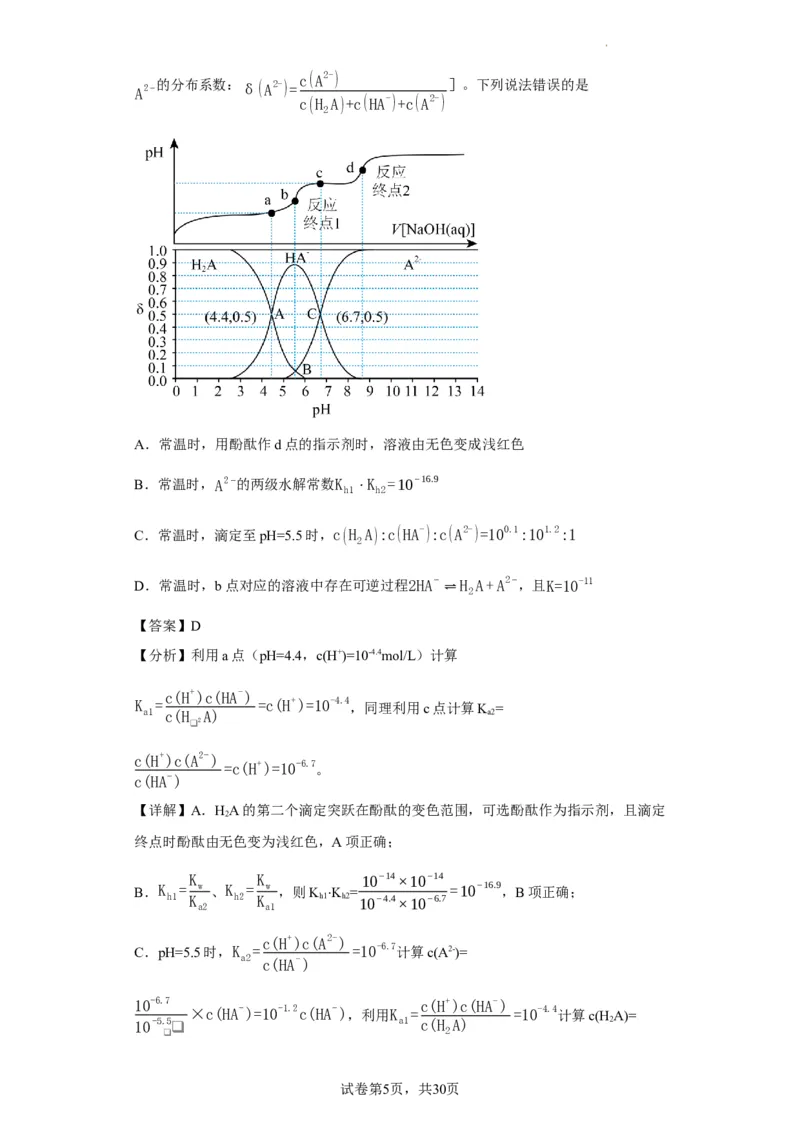
试卷第4页,共30页c(A2-)
A2−
的分布系数:δ(A2-)= ]。下列说法错误的是
c(H A)+c(HA-)+c(A2-)
2
A.常温时,用酚酞作d点的指示剂时,溶液由无色变成浅红色
B.常温时,A2−的两级水解常数K ⋅K =10−16.9
h1 h2
C.常温时,滴定至pH=5.5时,c(H A):c(HA-):c(A2-)=100.1:101.2:1
2
D.常温时,b点对应的溶液中存在可逆过程2HA−
⇌
H A+A2−,且K=10-11
2
【答案】D
【分析】利用a点(pH=4.4,c(H+)=10-4.4mol/L)计算
c(H+)c(HA-)
K = =c(H+)=10-4.4 ,同理利用c点计算K =
a1 c(H A) a2
❑2
c(H+)c(A2-)
=c(H+)=10-6.7
。
c(HA-)
【详解】A.HA的第二个滴定突跃在酚酞的变色范围,可选酚酞作为指示剂,且滴定
2
终点时酚酞由无色变为浅红色,A项正确;
K K 10−14×10−14
B.K = w 、K = w ,则K K = =10−16.9 ,B项正确;
h1 K h2 K h1 h2 10−4.4×10−6.7
a2 a1
⋅
c(H+)c(A2-)
C.pH=5.5时,K = =10-6.7 计算c(A2-)=
a2 c(HA-)
10-6.7 c(H+)c(HA-)
×c(HA-)=10-1.2c(HA-),利用K = =10-4.4 计算c(HA)=
10-5.5
❑
a1 c(H A) 2
❑ 2
试卷第5页,共30页
学科网(北京)股份有限公司10-5.5
×c(HA-)=10-1.1c(HA-),所以c(HA):c(HA-):c(A2-)=10-1.1:1:10-
10-4.4
❑
2
❑
1.2=100.1:101.2:1,C项正确;
c(A2-)c(H A) c(A2-)c(H+)c(H A) K
D.2HA− HA+A2−,且K= 2 = 2 = a2=10−2.3,D
2 c2(HA-) c(HA-)c(H+)c(HA-) K
a1
⇌
项错误;
故选D。
6.(2022秋·河南·高二校联考期中)为了更好地表示溶液的酸碱性,科学家提出了酸
c(H+)
度的概念:AG=lg 。常温下,用0.1mol/L的NaOH溶液滴定20mL0.1mol/
c(OH-)
LHCN溶液,溶液的酸度AG随滴入的NaOH溶液体积的变化如图所示(滴定过程中温
度的变化忽略不计),已知100.8=6.3,下列说法正确的是
A.该过程可以用甲基橙作指示剂
B.常温下,HCN的电离常数K ≈6.3×10-10
a
c(CN-)
C.滴定过程中 的值逐渐减小
c(HCN)⋅c(OH-)
D.当V=10mL时,溶液中存在:c(H+)+c(HCN)=c(OH-)+c(CN-)
【答案】B
【详解】A.滴定终点时溶液显碱性,应用酚酞作指示剂,A项错误;
c(H+
)
B.未加NaOH溶液时,AG=3.8, =103.8 ,结合K =10-14,可得
c(OH-
)
w
c2 (H+ )=103.8×10-14 ,K =
c2 (H+
) =
103.8×10-14
=6.3×10-10,B项正确;
a c(HCN) 0.1
试卷第6页,共30页c(CN-
)
C. 的分子,分母同时乘以c(H+ )得到
c(HCN)×c(OH-
)
c(H+ )×c(CN- ) K
= a ,温度不变,平衡常数不变,C项错误;
c(HCN)×c(OH- )×c(H+
)
K
w
D.当V=10mL时,溶液中的n(NaCN)=n(HCN),利用电荷守恒和物料守恒可得
2c(H+ )+c(HCN)=2c(OH- )+c(CN-
),D项错误。
故选B。
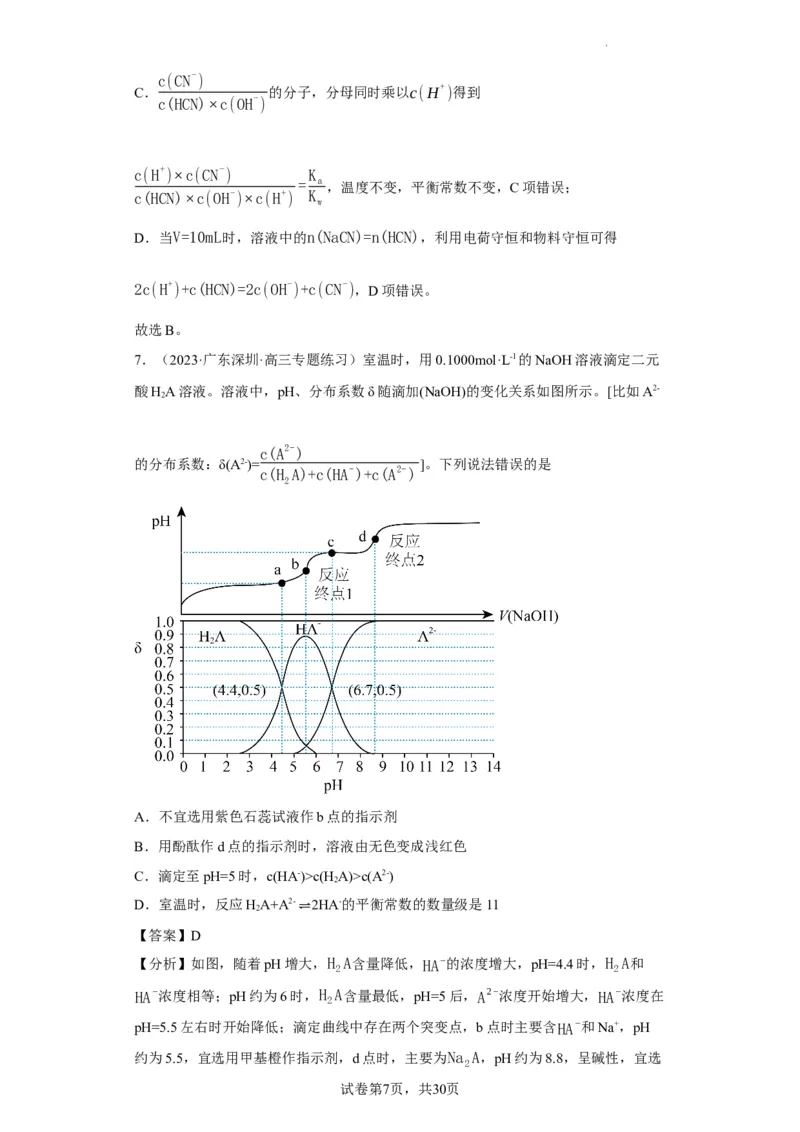
7.(2023·广东深圳·高三专题练习)室温时,用0.1000mol·L-1的NaOH溶液滴定二元
酸HA溶液。溶液中,pH、分布系数δ随滴加(NaOH)的变化关系如图所示。[比如A2-
2
c(A2-)
的分布系数:δ(A2-)= ]。下列说法错误的是
c(H A)+c(HA-)+c(A2-)
2
A.不宜选用紫色石蕊试液作b点的指示剂
B.用酚酞作d点的指示剂时,溶液由无色变成浅红色
C.滴定至pH=5时,c(HA-)>c(H A)>c(A2-)
2
D.室温时,反应H
2
A+A2- ⇌2HA-的平衡常数的数量级是11
【答案】D
【分析】如图,随着pH增大,H A含量降低,HA−的浓度增大,pH=4.4时,H A和
2 2
HA−浓度相等;pH约为6时,H A含量最低,pH=5后,A2−浓度开始增大,HA−浓度在
2
pH=5.5左右时开始降低;滴定曲线中存在两个突变点,b点时主要含HA−和Na+,pH
约为5.5,宜选用甲基橙作指示剂,d点时,主要为Na A,pH约为8.8,呈碱性,宜选
2
试卷第7页,共30页
学科网(北京)股份有限公司用酚酞作指示剂;
【详解】A.b点突变的pH范围为4.4~6.7,而紫色石蕊的变色的pH范围是5~8过
于宽泛,不可作指示剂,故A正确;
B.d点突变的pH范围为8~9,酚酞变色的pH范围为8.2~10.0,可以作为指示剂,
且溶液是由无色变为浅红色,故B正确;
C.由图中分布曲线可知,在pH=5时,c(HA−)>c(H A)>c(A2−),故C正确;
2
D.由图中分布曲线可知,①H
2
A
⇌
HA−+H+ K
a1
=10−4.4,②HA−
⇌
A2−+H+
K 10−4.4
K =10−6.7,①-②可得H A+A2− ⇌2HA−,此时K= a1 = =102.3,故D错误;
a2 2 K 10−6.7
a2
故选D。
8.(2023·广东深圳·深圳市高级中学校考模拟预测)室温下,用浓度为0.1000mol/L
的NaOH溶液分别滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定
曲线如图所示。下列说法正确的是
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ c(Y−) > c(OH−) > c(H+ )
K (HY)⋅c(HY)
D.将HY和HZ溶液混合后,溶液中存在:c(H+) = a +c(Z−)
c(H+)
【答案】B
【分析】等浓度的酸,酸性越强其电能能力越强pH越小,即酸性强弱:
HZ>HY>HX,且0.1mol/LHZ的pH为1,则它为强酸而HY、HX为弱酸。
【详解】A.从图起点看,相同浓度的三种酸,离子浓度HZ>HY>HX,所以导电能力
试卷第8页,共30页HZ>HY>HX,A项错误;
B.甲基橙的显色反应为3.1~4.4,滴定终点显酸性时用甲基橙,终点为碱性时选酚酞,
B项正确;
C.恰好中和的混合溶液成分为NaX、NaY,强碱弱酸盐呈碱性即c(OH-)>c(H+),同时
酸性越弱水解程度越强,即NaX水解强,c(X-)1,可用酚酞指示滴定终点c
0.05+10−x−10x−14
C.c点pH=x,HA的电离常数K =
a 102x−14−1
D.d点时,c(Na+)>c(A−)+c(OH−)
【答案】D
【详解】A.b点溶液中溶质为HA、NaA,溶液中OH-均来自于水的电离,溶液
pH=3,溶液中c(H+)=10−3mol/L,
K 10−14
c(OH−) =c(OH−)= W = mol/L=10−11mol/L,d点溶液中溶质为NaA、
水 c(H+) 10−3
试卷第9页,共30页
学科网(北京)股份有限公司NaOH,溶液中H+均来自于水的电离,溶液pH≈11,溶液中
c(H+) =c(H+)=10−11mol/L,因此水的电离程度:b点和d点近似相同,故A项正确;
水
B.由于HA为弱酸,因此HA溶液中溶质HA发生部分电离,0.1mol/L HA溶液中
c(H+)<0.1mol/L,溶液pH=a>1,HA溶液与NaOH溶液浓度相同,因此滴入10mL
NaOH溶液时,二者恰好完全反应,达到滴定终点,滴定终点溶质为NaA,溶液呈碱
性,因此滴定过程中可用酚酞指示滴定终点,故B项正确;
C.c点溶液体积为20mL,溶液中溶质为NaA,溶液中
0.1mol/L×10mL
c(Na+)= =0.05mol/L,溶液pH=x,则c(H+)=10−xmol/L,
20mL
K 10−14
c(OH−)= W = mol/L=10x−14mol/L,由溶液中电荷守恒
c(H+) 10−x
c(H+)+c(Na+)=c(OH−)+c(A−)可知,溶液中c(A−)=(0.05+10−x−10x−14)mol/L,由
溶液中物料守恒c(Na+)=c(HA)+c(A−)可知,溶液中
c(HA)=0.05mol/L−(0.05+10−x−10x−14)mol/L=(10x−14−10−x)mol/L,因此HA的
c(A−)×c(H+) (0.05+10−x−10x−14)×10−x 0.05+10−x−10x−14
电离常数K = = = ,故
a c(HA) 10x−14−10−x 102x−14−1
C项正确;
D.d点溶液中溶质为NaA、NaOH,由图可知溶液呈碱性,由溶液中电荷守恒
c(H+)+c(Na+)=c(OH−)+c(A−)可知,c(Na+) n (NaOH),
HX过量,由此可知HX为弱酸,则达到滴定终点时溶液呈碱性,宜选择酚酞做指示剂,
故A错误;
B.室温下,N点时溶液显中性即c(OH-)=c(H+)=10-7mol/L,故c(Na+)=c(X-),根据
0.10mol/L×0.01L 1
钠元素守恒可知: c(Na+)=c(X-)= = mol/L,根据c(HX)=c(HX) -
0.01L+0.011L 21 总
0.10mol/L×0.011L 1 1
c(X-)可知,c(HX)= - mol/L= mol/L,则
0.01L+0.011L 21 210
1
10-7×
c(H+)×c(X-) 210
K (HX)= = =1.0×10-6 ,故B错误;
a c(HX) 1
21
C.室温下,N点时溶液显中性,故c(Na+)=c(X-),根据钠元素守恒可知: c(Na+)=c(X-)=
0.10mol/L×0.01L 1
= mol/L,根据c(HX)=c(HX) -c(X-)可知,c(HX)=
0.01L+0.011L 21 总
0.10mol/L×0.011L 1 1
- mol/L= mol/L,故c(X-)是c(HX)的10倍,故C正确;
0.01L+0.011L 21 210
D.P点n(HX) = 2n (NaOH),二者发生中和反应后,溶液为等物质的量的NaX、HX的
混合溶液,溶液pH < 7,溶液显酸性,说明HX的电离作用大于X-的水解作用,故微
粒浓度c(X- ) > c (HX),故D错误;
试卷第11页,共30页
学科网(北京)股份有限公司答案选C。
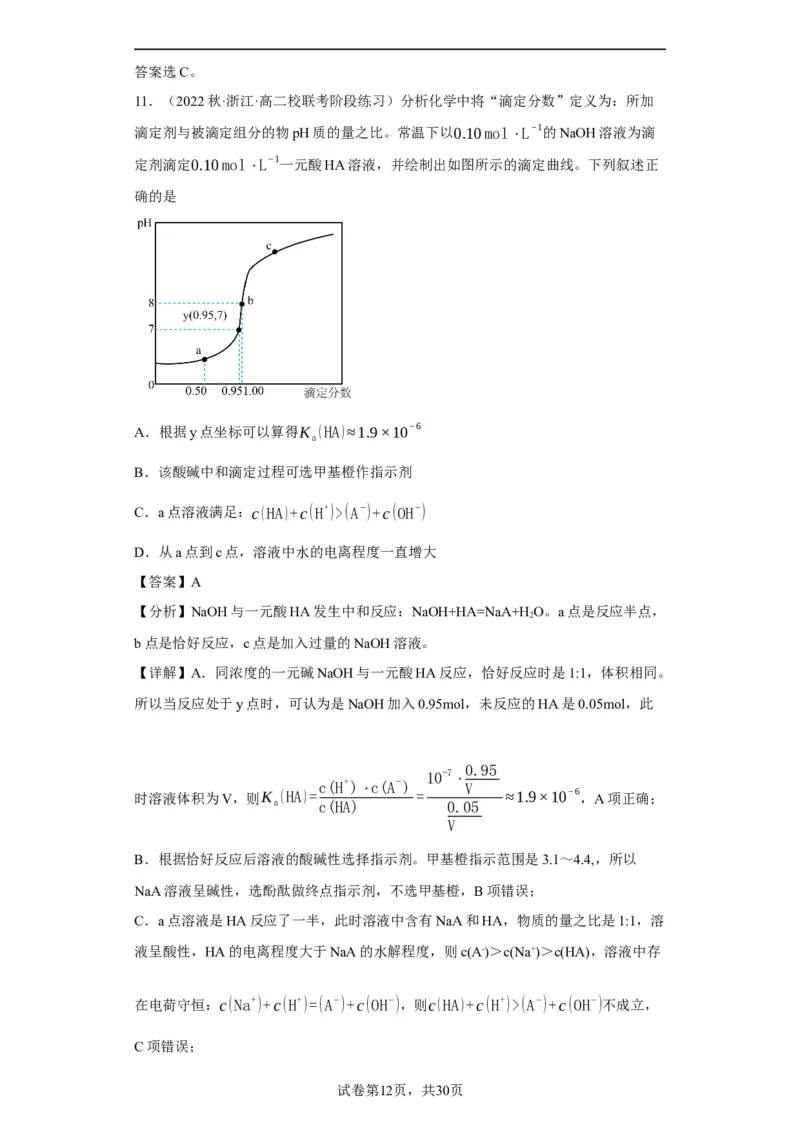
11.(2022秋·浙江·高二校联考阶段练习)分析化学中将“滴定分数”定义为:所加
滴定剂与被滴定组分的物pH质的量之比。常温下以0.10mol⋅L−1的NaOH溶液为滴
定剂滴定0.10mol⋅L−1一元酸HA溶液,并绘制出如图所示的滴定曲线。下列叙述正
确的是
A.根据y点坐标可以算得K (HA)≈1.9×10−6
a
B.该酸碱中和滴定过程可选甲基橙作指示剂
C.a点溶液满足:c(HA)+c(H+)>(A−)+c(OH−)
D.从a点到c点,溶液中水的电离程度一直增大
【答案】A
【分析】NaOH与一元酸HA发生中和反应:NaOH+HA=NaA+H O。a点是反应半点,
2
b点是恰好反应,c点是加入过量的NaOH溶液。
【详解】A.同浓度的一元碱NaOH与一元酸HA反应,恰好反应时是1:1,体积相同。
所以当反应处于y点时,可认为是NaOH加入0.95mol,未反应的HA是0.05mol,此
0.95
10-7
⋅
c(H+)⋅c(A-) V
时溶液体积为V,则K (HA)= = ≈1.9×10−6 ,A项正确;
a c(HA) 0.05
V
B.根据恰好反应后溶液的酸碱性选择指示剂。甲基橙指示范围是3.1~4.4,,所以
NaA溶液呈碱性,选酚酞做终点指示剂,不选甲基橙,B项错误;
C.a点溶液是HA反应了一半,此时溶液中含有NaA和HA,物质的量之比是1:1,溶
液呈酸性,HA的电离程度大于NaA的水解程度,则c(A-)>c(Na+)>c(HA),溶液中存
在电荷守恒:c(Na+)+c(H+)=(A−)+c(OH−),则c(HA)+c(H+)>(A−)+c(OH−)不成立,
C项错误;
试卷第12页,共30页D.溶液中存在酸或碱抑制水的电离,只存在可水解的盐的时促进水的电离。从a点到
c点,溶液中溶质由NaA和HA→NaA→NaA和NaOH,故溶液中水的电离程度先变大
后减小,D项错误;
故答案选A。
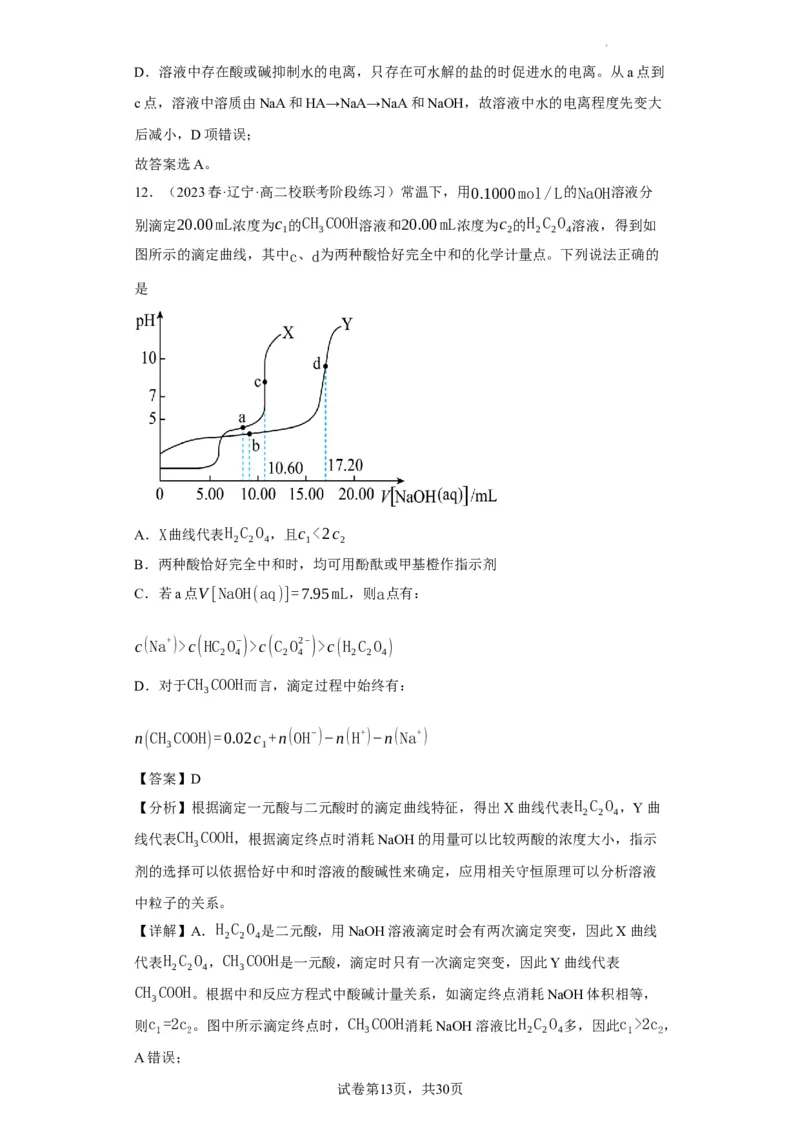
12.(2023春·辽宁·高二校联考阶段练习)常温下,用0.1000mol/L的NaOH溶液分
别滴定20.00mL浓度为c 的CH COOH溶液和20.00mL浓度为c 的H C O 溶液,得到如
1 3 2 2 2 4
图所示的滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点。下列说法正确的
是
A.X曲线代表H C O ,且c <2c
2 2 4 1 2
B.两种酸恰好完全中和时,均可用酚酞或甲基橙作指示剂
C.若a点V[NaOH(aq)]=7.95mL,则a点有:
c(Na+)>c(HC O−)>c(C O2−)>c(H C O )
2 4 2 4 2 2 4
D.对于CH COOH而言,滴定过程中始终有:
3
n(CH COOH)=0.02c +n(OH−)−n(H+)−n(Na+)
3 1
【答案】D
【分析】根据滴定一元酸与二元酸时的滴定曲线特征,得出X曲线代表H C O ,Y曲
2 2 4
线代表CH COOH,根据滴定终点时消耗NaOH的用量可以比较两酸的浓度大小,指示
3
剂的选择可以依据恰好中和时溶液的酸碱性来确定,应用相关守恒原理可以分析溶液
中粒子的关系。
【详解】A.H C O 是二元酸,用NaOH溶液滴定时会有两次滴定突变,因此X曲线
2 2 4
代表H C O ,CH COOH是一元酸,滴定时只有一次滴定突变,因此Y曲线代表
2 2 4 3
CH COOH。根据中和反应方程式中酸碱计量关系,如滴定终点消耗NaOH体积相等,
3
则c =2c 。图中所示滴定终点时,CH COOH消耗NaOH溶液比H C O 多,因此c >2c ,
1 2 3 2 2 4 1 2
A错误;
试卷第13页,共30页
学科网(北京)股份有限公司B.两种酸均是弱酸,恰好被中和时,生成的盐为强碱弱酸盐,溶液呈碱性,因此应选
用酚酞作指示剂,B错误;
C.H C O 恰好被中和时消耗NaOH溶液10.60mL。a点时消耗NaOH溶液7.95mL,
2 2 4
此时溶质为NaHC O 和Na C O 且两者浓度相等,溶液中钠离子浓度最大,a点时
2 4 2 2 4
pH<7,溶液呈酸性,说明HC O−电离程度大于C O2−水解程度,因此
2 4 2 4
c(C O2− )>c(HC O− ),C错误;
2 4 2 4
D.根据C原子守恒得:n(CH COOH)=0.02c -n(CH COO−),滴定过程中存在电荷
3 1 3
守恒:c(Na+)+c(H+)=c(CH COO−)+c(OH−),即
3
n(Na+)+n(H+)=n(CH COO−)+n(OH−),把n(CH COO−)=n(Na+)+n(H+)-n(OH−)代
3 3
入C原子守恒式得:n(CH COOH)=0.02c +n(OH−)-n(H+)-n(Na+),D正确;
3 1
故选D。
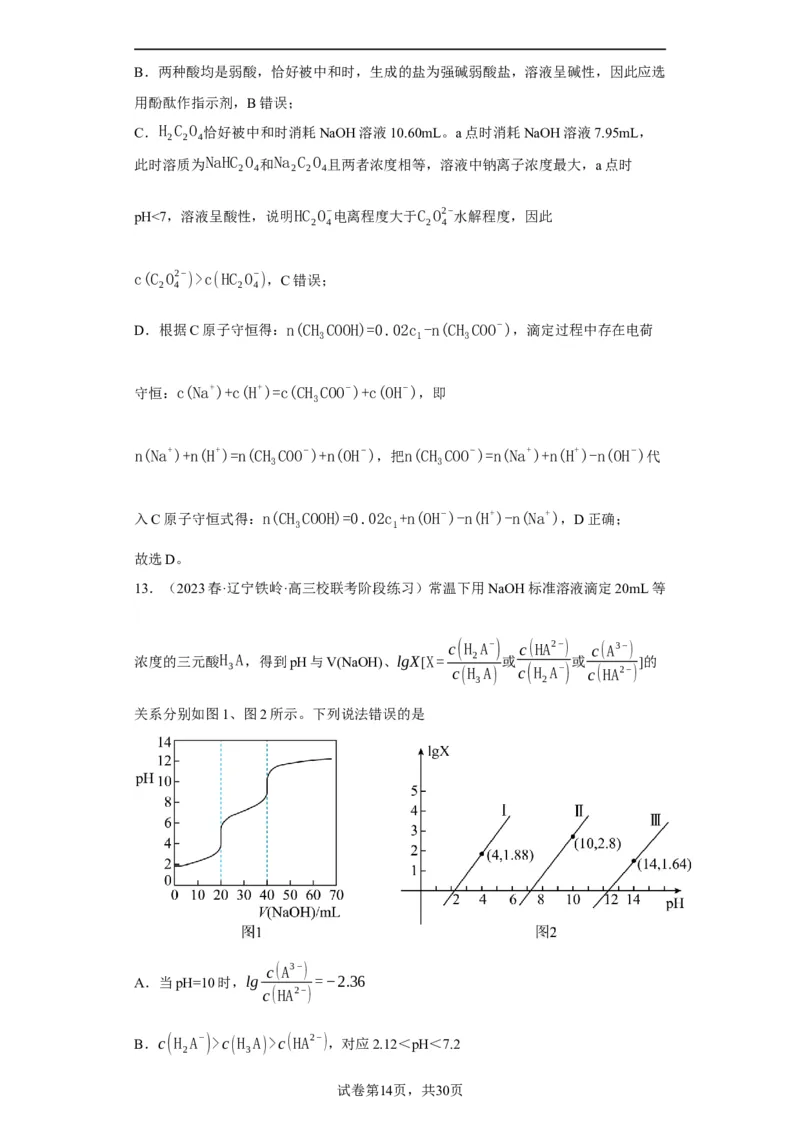
13.(2023春·辽宁铁岭·高三校联考阶段练习)常温下用NaOH标准溶液滴定20mL等
c(H A−) c(HA2−) c(A3−)
浓度的三元酸H A,得到pH与V(NaOH)、lgX[X= 2 或 或 ]的
3 c(H A) c(H A−) c(HA2−)
3 2
关系分别如图1、图2所示。下列说法错误的是
c(A3−)
A.当pH=10时,lg =−2.36
c(HA2−)
B.c(H A−)>c(H A)>c(HA2−),对应2.12<pH<7.2
2 3
试卷第14页,共30页C.20mL到40mL滴定过程中,水的电离程度逐渐增大
D.用NaOH标准液滴定NaH A溶液时,可选用酚酞做指示剂
2
【答案】B
【分析】随NaOH加入,依次发生:H A+NaOH=NaH A+H O,
3 2 2
NaH A+NaOH=Na HA+H O,Na HA+NaOH=Na A+H O,由图2知,当lgX=0时,,
2 2 2 2 3 2
c(H A−) c(HA2−) c(A3−)
2 = = =1则曲线Ⅰ、Ⅱ、Ⅲ依次表示的pH与
c(H A) c(H A−) c(HA2−)
3 2
c(H A−) c(HA2−) c(A3−)
lg 2 、lg 、lg ,由Ⅰ(4,1.88)、Ⅱ(10,2.8)、Ⅲ
c(H A) c(H A−) c(HA2−)
3 2
c(H+)c(H A−)
(14,1.64)知,K = 2 =10−4×101.88 =10-2.12,
a1 c(H A)
3
c(H+)c(HA2−) c(H+)c(A3−)
K
a2
=
c(H A−)
=10−10×102.8 =10-7.2,K
a3
=
c(HA2−)
=10−14×101.64 =10-
2
12.36。
c(H+)c(A3−) c(A3−) c(A3−)
【详解】A.K = =10−10× =10-12.36,则lg =−2.36,
a3 c(HA2−) c(HA2−) c(HA2−)
故A正确;
B.NaH A溶液中c(H A−)>c(H A)>c(HA2−),由图1知,pH>2.12,但pH不一定小
2 2 3
于7.2,故B错误;
C.20mL到40mL滴定过程中,H+抑制水电离的作用逐渐减弱,则水的电离程度逐渐
增大,故C正确;
D.酚酞指示剂的变色范围为8.2~10.0,由图1第2个pH突变可知,NaOH标准液滴
定NaH A溶液时,可选用酚酞做指示剂,故D正确;
2
故答案选B。
14.(2022·广东广州·高三统考专题练习)常温下,用如图1所示装置,分别向
25mL0.3mol•L-1NaCO 溶液和25mL0.3mol•L-1NaHCO 溶液中逐滴滴加0.3mol•L-1的稀
2 3 3
盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。下列说法正确的是
试卷第15页,共30页
学科网(北京)股份有限公司A.X曲线为NaCO 溶液的滴定曲线
2 3
B.b点的溶液中:2c(Na+)=3c(CO❑ 2− )+3c(HCO❑ − )+3c(H CO)
3 3 2 3
K
w
C.用pH试纸测得c点的pH约为8,可知:K (H CO)<
a2 2 3 K (H CO )
a2 2 3
D.a、d两点水的电离程度:ac(Na+)>c(H+)>c(OH−)
D.其他相同,HNO 替代HR,曲线位于图中曲线下方
2
【答案】B
【分析】本题关键是求丙酸浓度,代入x点和y点数据计算:
16c−0.8 16c−1.6
4.27=pK −lg ,4.75=pK −lg ,解得:c=0.2。进而计算
a 0.8 a 1.6
pK =4.75,K =10−4.75。
a a
【详解】A.依题意,c(HR)=c(R−)时缓冲能力最强,即y点溶液,pH为4.75,A项正
确;
16c
B.由上分析y点为反应一半的点,即 =0.1×16得到c=0.2mol/L,B项错误;
2
C.y点溶液中,电荷守恒式有c(Na+)+c(H+)=c(OH−)+c(R−),溶液呈酸性,
c(R−)>c(Na+)>c(H+)>c(OH−),C项正确;
D.HNO 的电离常数大于丙酸,故pK (HNO )较小,故曲线位于图中曲线下方,D项正
2 a 2
试卷第17页,共30页
学科网(北京)股份有限公司确;
故选B。
16.(2023秋·湖北黄冈·高二湖北省红安县第一中学校考阶段练习)某同学在两个相
同的特制容器中分别加入20mL0.4mol⋅L−1Na CO 溶液和40mL0.2mol⋅L−1
2 3
NaHCO 溶液,再分别用0.4mol⋅L−1盐酸滴定,利用pH计和压力传感器检测,得到如
3
图曲线:
下列说法不正确的是
A.图中甲、丁线表示向Na CO 溶液中滴加盐酸,乙、丙线表示向NaHCO 溶液中滴加
2 3 3
盐酸
B.当滴加盐酸的体积为V mL时(a点、b点),所发生的反应用离子方程式表示为:
1
HCO−+H+=H CO
3 2 3
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴
定终点
D.Na CO 和NaHCO 溶液中均满足:c(H CO )−c(CO2−)=c(OH−)−c(H+)
2 3 3 2 3 3
【答案】D
【分析】NaCO 的水解程度大于NaHCO ,则0.4mol•L-1NaCO 溶液的碱性强于
2 3 3 2 3
40mL0.2mol•L-1NaHCO 溶液,NaCO 与HCl反应先生成NaHCO ,NaHCO 再与盐酸
3 2 3 3 3
反应生成CO 气体,NaHCO 直接与HCl反应生成CO 气体,并且
2 3 2
n(Na CO)=n(NaHCO )=0.008mol,分别加入20mL0.4mol•L-1HCl时NaCO 恰好转化为
2 3 3 2 3
NaHCO ,容器中压强不变,随着HCl的加入,容器中压强逐渐增大,加入40mLHCl
3
时容器的压强达到最大值,NaHCO 直接与HCl反应生成CO 气体,容器中压强增大,
3 2
并且加入20mLHCl时容器的压强达到最大值、一直保持不变,所以图中甲、丁线表示
试卷第18页,共30页向NaCO 溶液中滴加盐酸,乙、丙线表示向NaHCO 溶液中滴加盐酸,据此分析解答。
2 3 3
【详解】A.由上述分析可知,图中甲、丁线表示向NaCO 溶液中滴加盐酸,乙、丙
2 3
线表示向NaHCO 溶液中滴加盐酸,A正确;
3
B.在加入20mL盐酸时NaCO 转化为了NaHCO ,从20mL以后发生NaHCO 与HCl
2 3 3 3
反应,开始时生成的碳酸由于浓度低而没有分解为CO 气体,故当滴加盐酸的体积为
2
VmL时(a点、b点),所发生反应的离子方程式为HCO- +H+═H CO❑,B正确;
1 3 2 3
C.由图可知,滴定分析时,c点的pH在9左右,在酚酞的变色范围内,可选择酚酞
作指示剂;d点的pH在4左右,在甲基橙的变色范围内,可选择甲基橙作指示剂,C
正确;
D.NaCO 溶液中的质子守恒:2c(H CO )+c(HCO−)+c(H+)=c(OH−)和NaHCO 溶液
2 3 2 3 3 3
中的质子守恒:c(H CO )−c(CO2−)=c(OH−)−c(H+), D错误;
2 3 3
综上所述,选D。
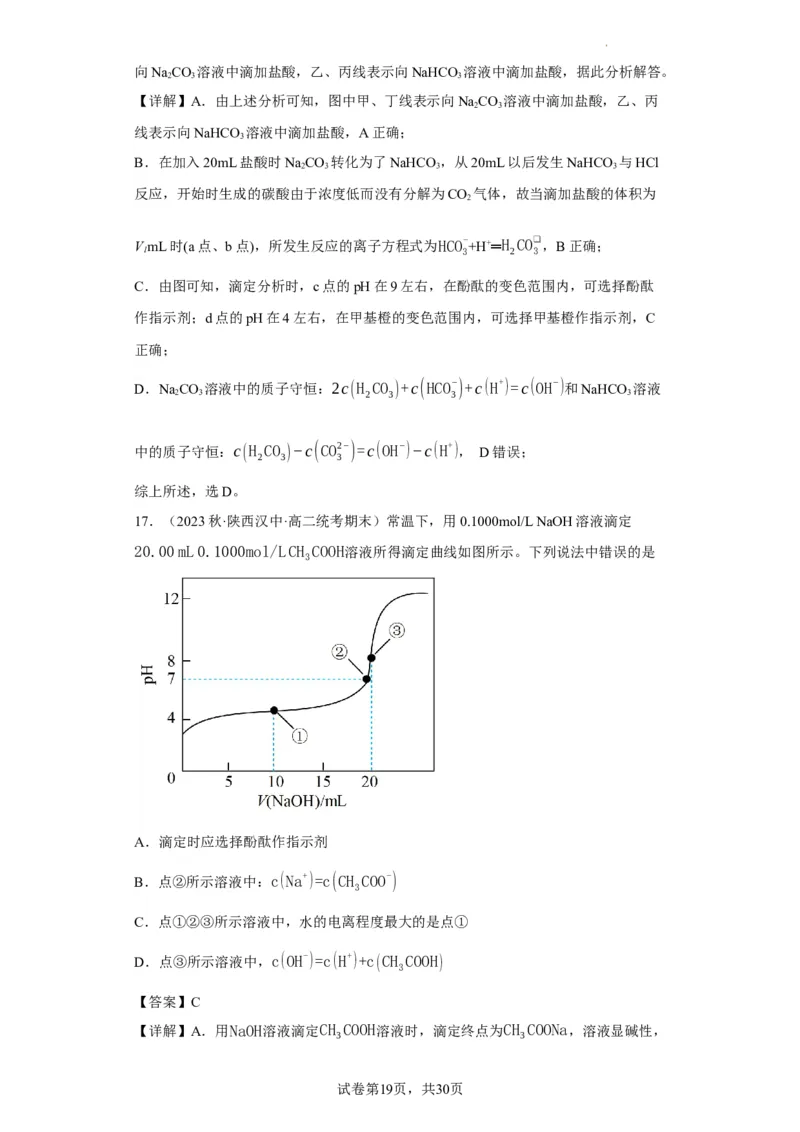
17.(2023秋·陕西汉中·高二统考期末)常温下,用0.1000mol/L NaOH溶液滴定
20.00 mL 0.1000mol/LCH COOH溶液所得滴定曲线如图所示。下列说法中错误的是
3
A.滴定时应选择酚酞作指示剂
B.点②所示溶液中:c(Na+)=c(CH COO-)
3
C.点①②③所示溶液中,水的电离程度最大的是点①
D.点③所示溶液中,c(OH-)=c(H+)+c(CH COOH)
3
【答案】C
【详解】A.用NaOH溶液滴定CH COOH溶液时,滴定终点为CH COONa,溶液显碱性,
3 3
试卷第19页,共30页
学科网(北京)股份有限公司可选择酚酞作指示剂,故A正确;
B.②点处的溶液中pH=7,即c(H+)=c(OH-),根据电荷守恒可得:
c(Na+)=c(CH COO−),故B正确;
3
C.①→③过程中,溶液中的溶质CH COOH逐渐减少,CH COONa逐渐增多,水的电离
3 3
程度逐渐增大,故C错误;
D.点③所示溶液中,NaOH与CH COOH恰好完全反应生成CH COONa,根据
3 3
CH COONa溶液的质子守恒为c(OH-)=c(H+)+c(CH COOH),故D正确;
3 3
故答案选C。
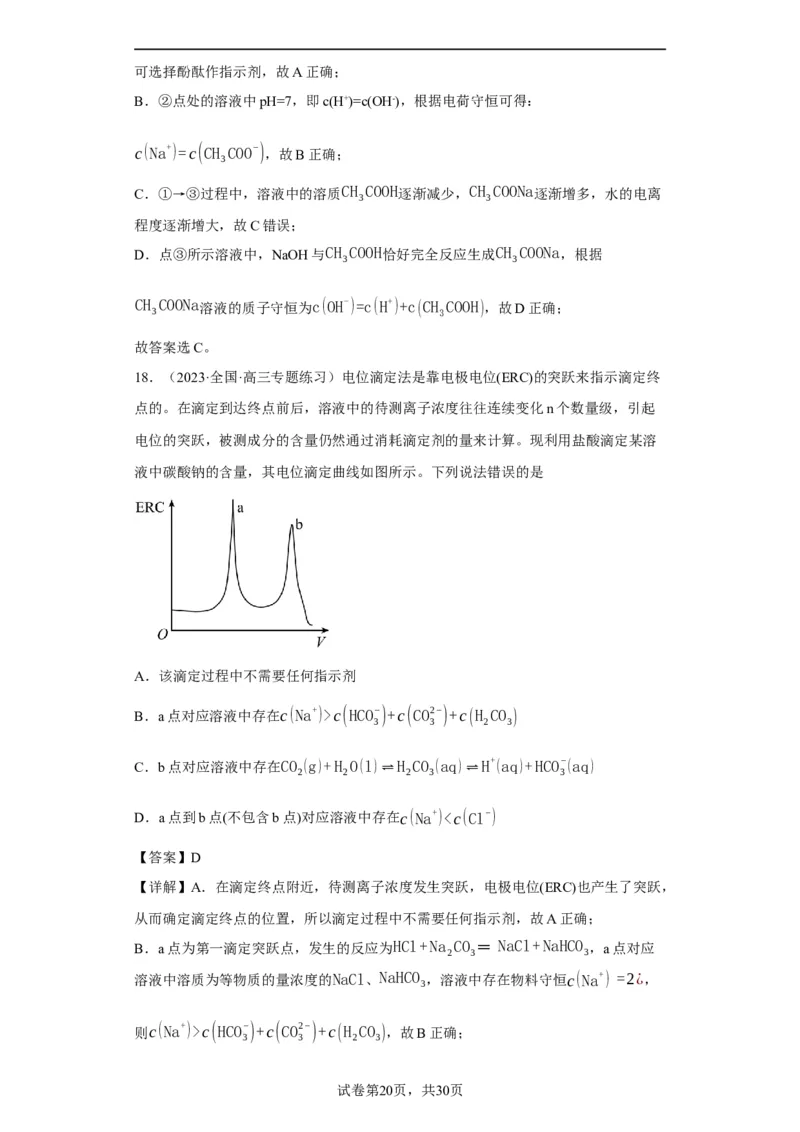
18.(2023·全国·高三专题练习)电位滴定法是靠电极电位(ERC)的突跃来指示滴定终
点的。在滴定到达终点前后,溶液中的待测离子浓度往往连续变化n个数量级,引起
电位的突跃,被测成分的含量仍然通过消耗滴定剂的量来计算。现利用盐酸滴定某溶
液中碳酸钠的含量,其电位滴定曲线如图所示。下列说法错误的是
A.该滴定过程中不需要任何指示剂
B.a点对应溶液中存在c(Na+)>c(HCO−)+c(CO2−)+c(H CO )
3 3 2 3
C.b点对应溶液中存在CO (g)+H O(l)⇌ H CO (aq)⇌ H+ (aq)+HCO− (aq)
2 2 2 3 3
D.a点到b点(不包含b点)对应溶液中存在c(Na+)c(HCO−)+c(CO2−)+c(H CO ),故B正确;
3 3 2 3
试卷第20页,共30页C.b点为第二滴定突跃点,HCl恰好与Na CO 反应生成NaCl、CO 和H O,因少量CO
2 3 2 2 2
溶解生成的H CO 电离使溶液呈弱酸性,即溶液中存在题给的平衡,C正确;
2 3
D.a点到b点(不包括b点)对应溶液中NaHCO 未反应完,盐酸不足,所以溶液中始终
3
存在c(Na+)>c(Cl−),故D错误;
故选D。
19.(2023春·重庆沙坪坝·高二重庆南开中学校考开学考试)常温下,用
0.1000mol/L的NaOH溶液滴定20.00mL浓度分别为c 、c 的一元酸(HA)、二元酸( H B
1 2 2
)溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点。忽略溶液
混合时体积变化。下列叙述正确的是
A.X曲线代表H B,Y曲线代表HA,c c ,A正确;
2 1 2
B.H B、HA恰好完全中和时,产物为强碱弱酸盐,均呈碱性,可使用酚酞做指示剂,
2
不可使用甲基橙做指示剂,B错误;
C.完全中和时消耗V (NaOH) = 10.60mL, a点V (NaOH) = 7.95mL时,占消耗氢氧
化钠总体积的四分之三,则溶质为NaHB与NaB,且二者的浓度比为:1 : 1形成的溶
2
液,则a点物料守恒和电荷守恒有关系式:c(Na+)+c(H+)=c(HB−)+2c(B2−)+c(OH-)
①,2c(Na+)=3c(HB−)+3c(B2−)+3c(H B)②,用②-①,
2
试卷第21页,共30页
学科网(北京)股份有限公司得c(Na+)+c(OH-)=2c(HB−)+c(B2−)+3c(H B)+c(H+)由于酸性环境,c(H+) >
2
c(OH-),故c(Na+)>2c(HB−)+c(B2−)+3c(H B),C错误;
2
D.溶液中的质子守恒:c(H+)+c(HA)=c(OH-)①,物料守恒:②c(A−)
+c(HA)=0.05mol⋅L-1②,②×2-①得:c(HA)+2c(A−)+c(OH−)=c(H+)+c1,D正确;
故本题选D。
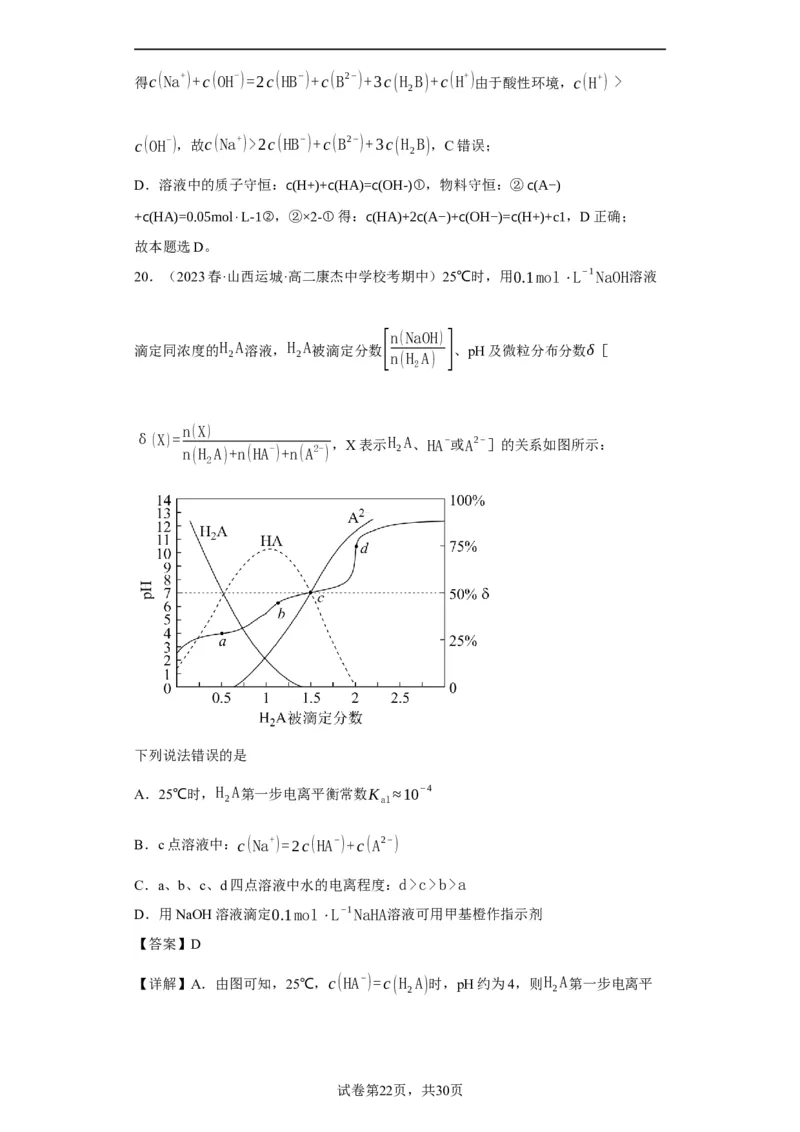
20.(2023春·山西运城·高二康杰中学校考期中)25℃时,用0.1mol⋅L−1NaOH溶液
[n(NaOH) ]
滴定同浓度的H A溶液,H A被滴定分数 、pH及微粒分布分数δ[
2 2 n(H A)
2
n(X)
δ(X)= ,X表示H A、HA−或A2−]的关系如图所示:
n(H A)+n(HA-)+n(A2-) 2
2
下列说法错误的是
A.25℃时,H A第一步电离平衡常数K ≈10−4
2 al
B.c点溶液中:c(Na+)=2c(HA−)+c(A2−)
C.a、b、c、d四点溶液中水的电离程度:d>c>b>a
D.用NaOH溶液滴定0.1mol⋅L−1NaHA溶液可用甲基橙作指示剂
【答案】D
【详解】A.由图可知,25℃,c(HA−)=c(H A)时,pH约为4,则H A第一步电离平
2 2
试卷第22页,共30页衡常数K =
c(HA−)⋅c(H+)
=c(H+)≈10−4 ,故A正确;
al c(H A)
2
B.c点溶液中溶质为NaHA和Na A,且c(HA−)=c(A2−),由电荷守恒可知
2
c(Na+)+c(H+)=c(HA−)+c(OH−)+2c(A2−),pH=7,c(H+)=c(OH−),故
c(Na+)=c(HA−)+2c(A2−)=3c(HA−)=3c(A2−)=2c(HA−)+c(A2−),故B正确:
C.未加NaOH溶液时,H A电离出H+,抑制水的电离,加入NaOH溶液,酸逐渐被中
2
和生成盐,对水的抑制程度减弱,生成的NaHA、Na A能水解,促进水的电离,当酸
2
碱恰好中和为Na A,即d点附近(pH突变),对水的电离促进程度最大,故a、b、c、d
2
四点溶液中水的电离程度:d>c>b>a,故C正确;
D.滴定后溶液呈碱性,应选择酚酞作指示剂,故D错误;
故选D。
21.(2023·全国·模拟预测)常温下,用0.10mol⋅L−1盐酸滴定0.10mol⋅L−1Na CO
2 3
溶液时,溶液pH随滴定百分率的变化如图所示。已知:b点溶液中
c(H CO )≈c(CO2−),K (H CO )=5×10−7 ,K (H CO )=5×10−11 ,lg5≈0.7。下
2 3 3 a1 2 3 a2 2 3
列说法错误的是
A.a点的溶液中:c(H CO )−c(CO2−)>c(OH−)−c(Cl−)
2 3 3
B.b点溶液的pH约为8.3
C.煮沸的目的是除去溶解的CO ,使突跃变大,冷却后继续滴定到终点
2
D.滴定过程可选用酚酞、甲基橙双指示剂
【答案】A
试卷第23页,共30页
学科网(北京)股份有限公司【分析】常温下,用0.10mol⋅L−1盐酸滴定0.10mol⋅L−1Na CO 溶液时,a点滴定百
2 3
分率为25%,故溶液中溶质Na CO 、NaHCO 、NaCl的物质的量之比为1:1:1,b点
2 3 3
滴定百分率为50%,恰好反应得到碳酸氢钠、氯化钠溶液;c点滴定百分率为100%,
碳酸钠与盐酸恰好反应生成氯化钠、二氧化碳和水。
【详解】A.由思路分析可知,a点溶液中溶质Na CO 、NaHCO 、NaCl的物质的量之
2 3 3
比为1:1:1,根据电荷守恒可知,
c(Na+)+c(H+)=c(OH−)+c(Cl−)+c(HCO−)+2c(CO2−),根据物料守恒可知,
3 3
c(Na+)=2c(HCO−)+2c(CO2−)+2c(H CO ),把物料守恒代入电荷守恒有①:
3 3 2 3
2c(H CO )+c(HCO−)+c(H+)=c(OH−)+c(Cl−),根据氯、碳物料守恒可知,
2 3 3
1
2c(Cl−)= c(Na+)=c(HCO−)+c(CO2−)+c(H CO ),则有②:
2 3 3 2 3
c(HCO−)=2c(Cl−)−c(CO2−)−c(H CO ),把②代入①得
3 3 2 3
c(H CO )−c(CO2−)+c(H+)=c(OH−)−c(Cl−),故
2 3 3
c(H CO )−c(CO2−)K
h2
,A2−存在水解平衡:A2−+H
2
O
⇌
HA−+OH−
a1
K
K = w =10−8.17 ,K >K ,溶液中HA−的电离程度大于A2−、HA−的水解程度,即
h1 K a2 h1
a
c(A2−)>c(H A),C项错误;
2
D.第一次滴定终点时,溶液呈酸性,可用甲基橙作指示剂,第二次滴定终点时溶液
的pH在8-10之间,可用酚酞作指示剂,D项正确。
答案选C。
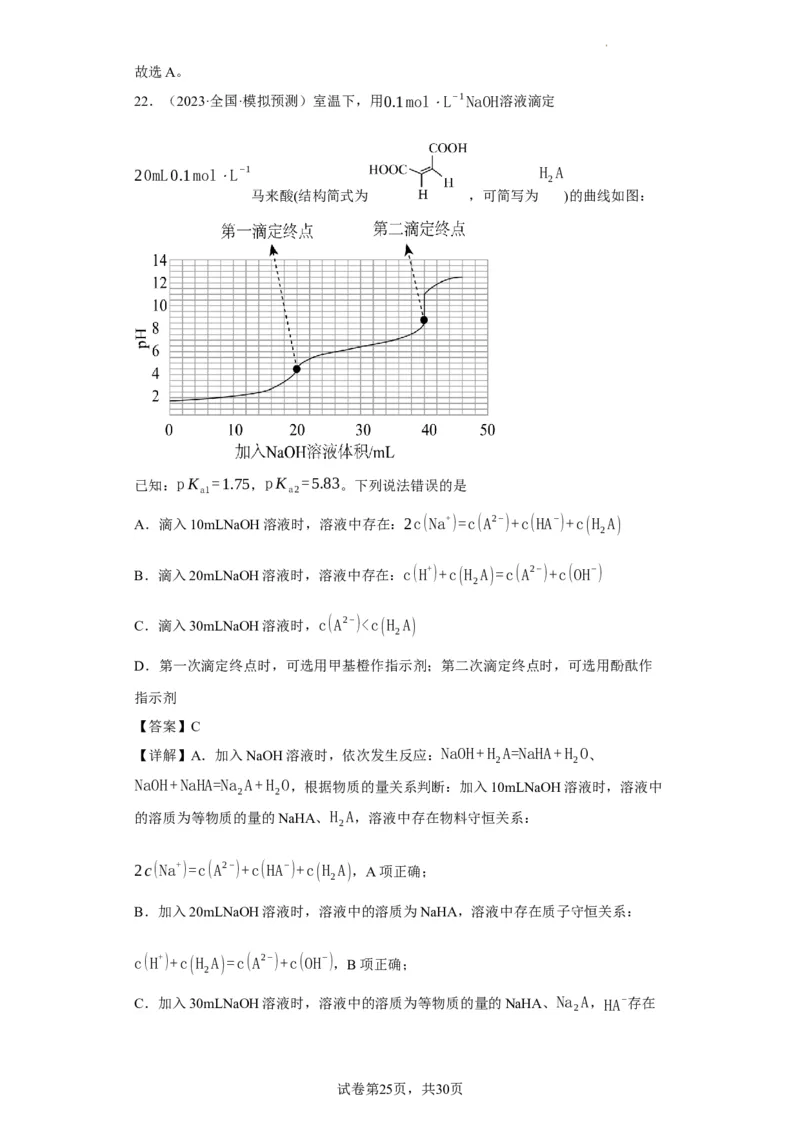
23.(2023春·安徽池州·高二池州市第一中学校联考期中)常温下,用0.1000mol/L
的NaOH溶液分别滴定0.1000mol/L的HCl溶液和0.1000mol/L的醋酸溶液,滴定曲线
如下图。下列有关说法正确的是
A.实线表示滴定盐酸的曲线
B.酸的强弱是影响突跃范围大小的重要因素
C.ab段的离子反应式是H++OH−=H O
2
D.两个体系滴定终点的确定都可用甲基橙作指示剂
【答案】B
【详解】A.从起点的pH可看出,实线表示醋酸的曲线,故A错误;
B.同浓度时,酸弱pH大起点高,酸强pH小起点低,故B正确;
C.根据图像可以判断a点是醋酸溶液,所以ab段的离子反应式是
CH COOH+OH−=CH COO−+H O,故C错误;
3 3 2
D.CH COOH最终生成CH COONa,溶液呈碱性,应用酚酞做指示剂,故D错误;
3 3
试卷第26页,共30页故答案选B。
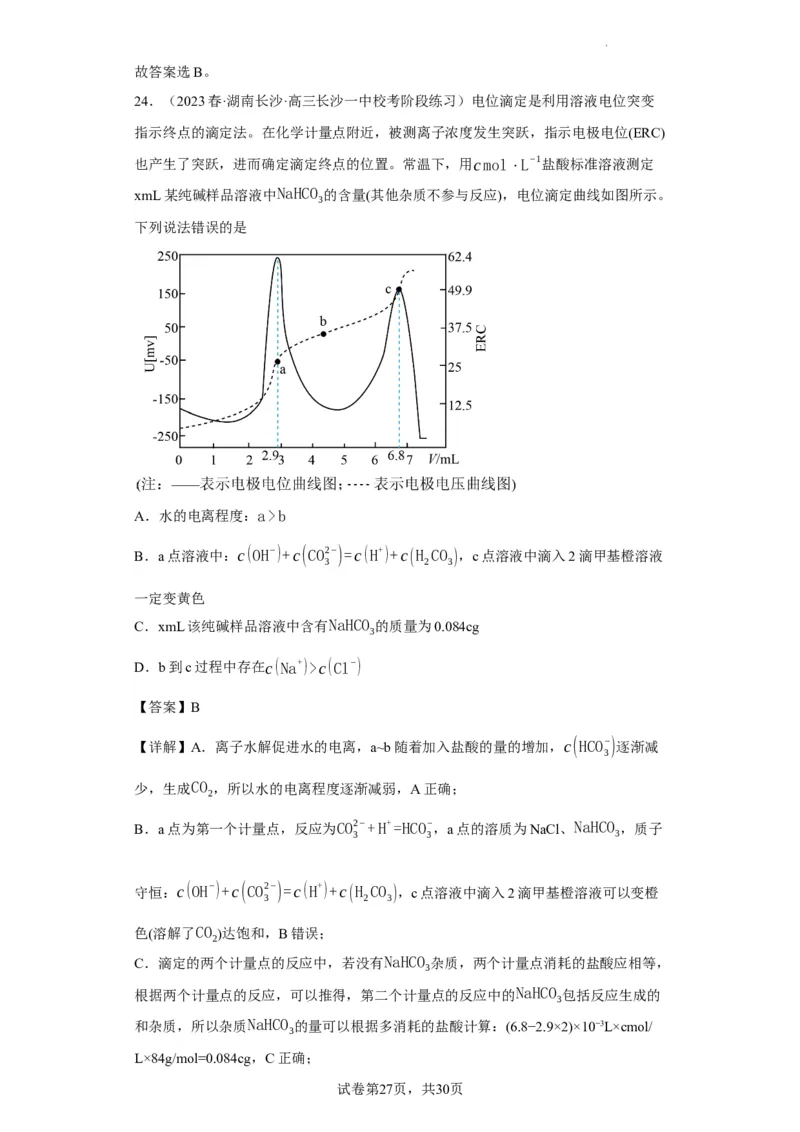
24.(2023春·湖南长沙·高三长沙一中校考阶段练习)电位滴定是利用溶液电位突变
指示终点的滴定法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)
也产生了突跃,进而确定滴定终点的位置。常温下,用cmol⋅L−1盐酸标准溶液测定
xmL某纯碱样品溶液中NaHCO 的含量(其他杂质不参与反应),电位滴定曲线如图所示。
3
下列说法错误的是
A.水的电离程度:a>b
B.a点溶液中:c(OH−)+c(CO2−)=c(H+)+c(H CO ),c点溶液中滴入2滴甲基橙溶液
3 2 3
一定变黄色
C.xmL该纯碱样品溶液中含有NaHCO 的质量为0.084cg
3
D.b到c过程中存在c(Na+)>c(Cl−)
【答案】B
【详解】A.离子水解促进水的电离,a~b随着加入盐酸的量的增加,c(HCO−)逐渐减
3
少,生成CO ,所以水的电离程度逐渐减弱,A正确;
2
B.a点为第一个计量点,反应为CO2−+H+=HCO−,a点的溶质为NaCl、NaHCO
,质子
3 3 3
守恒:c(OH−)+c(CO2−)=c(H+)+c(H CO ),c点溶液中滴入2滴甲基橙溶液可以变橙
3 2 3
色(溶解了CO )达饱和,B错误;
2
C.滴定的两个计量点的反应中,若没有NaHCO 杂质,两个计量点消耗的盐酸应相等,
3
根据两个计量点的反应,可以推得,第二个计量点的反应中的NaHCO 包括反应生成的
3
和杂质,所以杂质NaHCO 的量可以根据多消耗的盐酸计算:(6.8−2.9×2)×10−3L×cmol/
3
L×84g/mol=0.084cg,C正确;
试卷第27页,共30页
学科网(北京)股份有限公司D.在整个滴定过程中,参加反应的离子是CO2−、HCO−、H+,溶液中的Na+不参加反
3 3
应,守恒不变,c点是第二个滴定终点,消耗盐酸最多的点,所以在c点之前盐酸不足,
则c(Na+)>c(Cl−),D正确;
故选B。
25.(2023·全国·高三统考专题练习)已知:常温下K (H SO )=1.4×10-2,
a1 2 3
K (H SO )=6.0×10-8,通过下列实验探究含硫化合物的性质。
a2 2 3
实验1:测得0.1mol·L-1HSO 溶液pH=2.1。
2 3
实验2:向10mL0.1mol·L-1NaHSO 溶液中逐滴加入5mL水,用pH计监测过程中pH变
3
化。
实验3:用0.1mol·L-1NaOH溶液滴定10mL0.1mol·L-1HSO 溶液。
2 3
实验4:向10mL0.1mol·L-1NaS溶液中加入10mL0.1mol·L-1MnSO 溶液,充分混合,产
2 4
生粉色沉淀,再加几滴0.1mol·L-1CuSO 溶液,产生黑色沉淀。
4
下列说法不正确的是
A.由实验1可知:0.1mol·L-1HSO
溶液中c(SO2-
)K (CuS)
sp sp
【答案】A
【详解】A.由实验1可知:0.1mol·L-1HSO 溶液pH=2.1,溶液呈酸性,则溶液中离
2 3
子浓度大小的顺序为c(H+)>c(HSO- )>c(SO2-
)>c(OH-),A不正确;
3 3
B.实验2中逐滴加入5mL水,溶液中HSO−的水解平衡正向移动,水解程度不断增大,
3
c(OH-)增大,pH增大,B正确;
C.实验3随着NaOH的加入,先生成HSO−,再生成SO2−,所以可出现两次突跃,
3 3
HSO− 的电离大于水解,溶液呈酸性,应选用甲基橙作指示剂,SO2−
水解呈碱性,应选
3 3
用酚酞作指示剂,C正确;
D.实验4可知,白色沉淀转化为黑色沉淀是MnS转化为CuS,说明
K (MnS)>K (CuS),D正确;
sp sp
试卷第28页,共30页故选A。
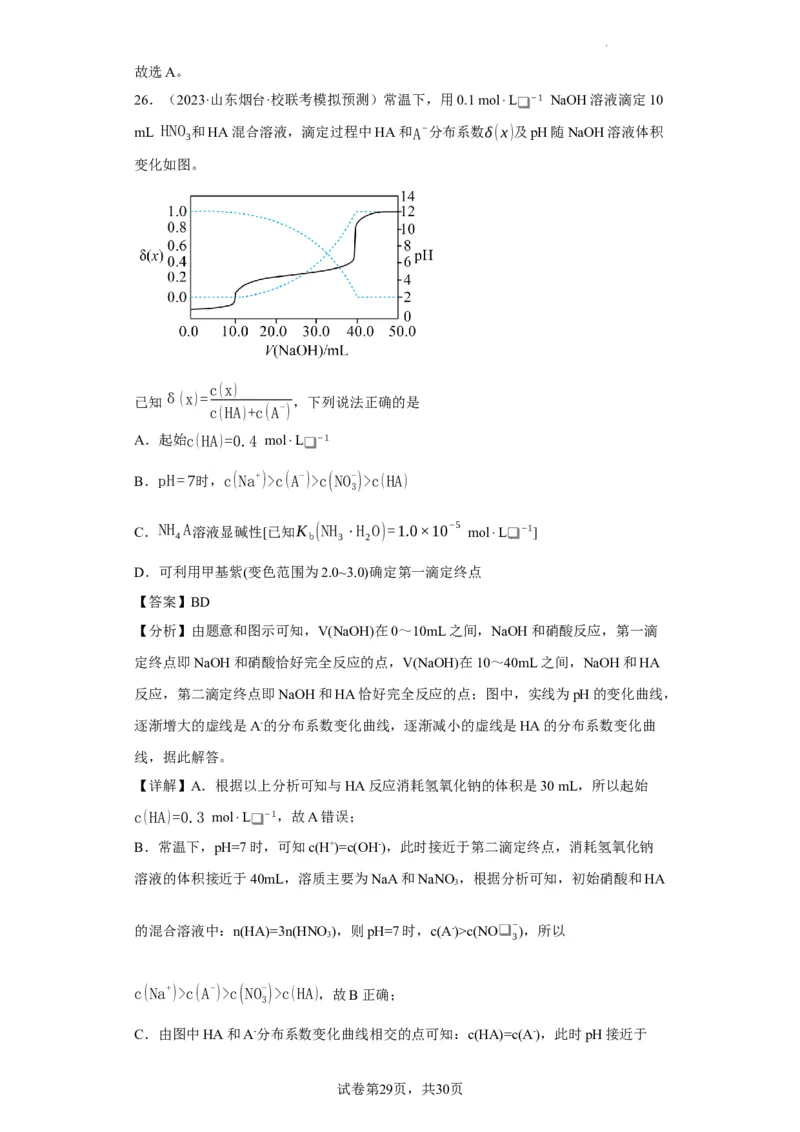
26.(2023·山东烟台·校联考模拟预测)常温下,用0.1 mol⋅L❑ −1 NaOH溶液滴定10
mL HNO 和HA混合溶液,滴定过程中HA和A−分布系数δ(x)及pH随NaOH溶液体积
3
变化如图。
c(x)
已知
δ(x)=
,下列说法正确的是
c(HA)+c(A-)
A.起始c(HA)=0.4 mol⋅L❑ −1
B.pH=7时,c(Na+)>c(A-)>c(NO-)>c(HA)
3
C.NH
4
A溶液显碱性[已知K
b
(NH
3
⋅H
2
O)=1.0×10−5 mol⋅L❑ −1]
D.可利用甲基紫(变色范围为2.0~3.0)确定第一滴定终点
【答案】BD
【分析】由题意和图示可知,V(NaOH)在0~10mL之间,NaOH和硝酸反应,第一滴
定终点即NaOH和硝酸恰好完全反应的点,V(NaOH)在10~40mL之间,NaOH和HA
反应,第二滴定终点即NaOH和HA恰好完全反应的点;图中,实线为pH的变化曲线,
逐渐增大的虚线是A-的分布系数变化曲线,逐渐减小的虚线是HA的分布系数变化曲
线,据此解答。
【详解】A.根据以上分析可知与HA反应消耗氢氧化钠的体积是30 mL,所以起始
c(HA)=0.3 mol⋅L❑ −1,故A错误;
B.常温下,pH=7时,可知c(H+)=c(OH-),此时接近于第二滴定终点,消耗氢氧化钠
溶液的体积接近于40mL,溶质主要为NaA和NaNO ,根据分析可知,初始硝酸和HA
3
的混合溶液中:n(HA)=3n(HNO ),则pH=7时,c(A-)>c(NO❑ − ),所以
3 3
c(Na+)>c(A-)>c(NO-)>c(HA),故B正确;
3
C.由图中HA和A-分布系数变化曲线相交的点可知:c(HA)=c(A-),此时pH接近于
试卷第29页,共30页
学科网(北京)股份有限公司c(H+)c(A−)
5,K(HA)= =c(H+)=10-5,由于K (NH ⋅H O)=1.0×10−5 ,这说明NH A
a b 3 2 4
c(HA)
溶液中A-的水解程度等于铵根离子的水解程度,因此显中性,故C错误;
D.根据图像可知第一滴定终点时溶液pH介于2~3之间,所以可利用甲基紫(变色范
围为2.0~3.0)确定第一滴定终点,故D正确;
故选BD。
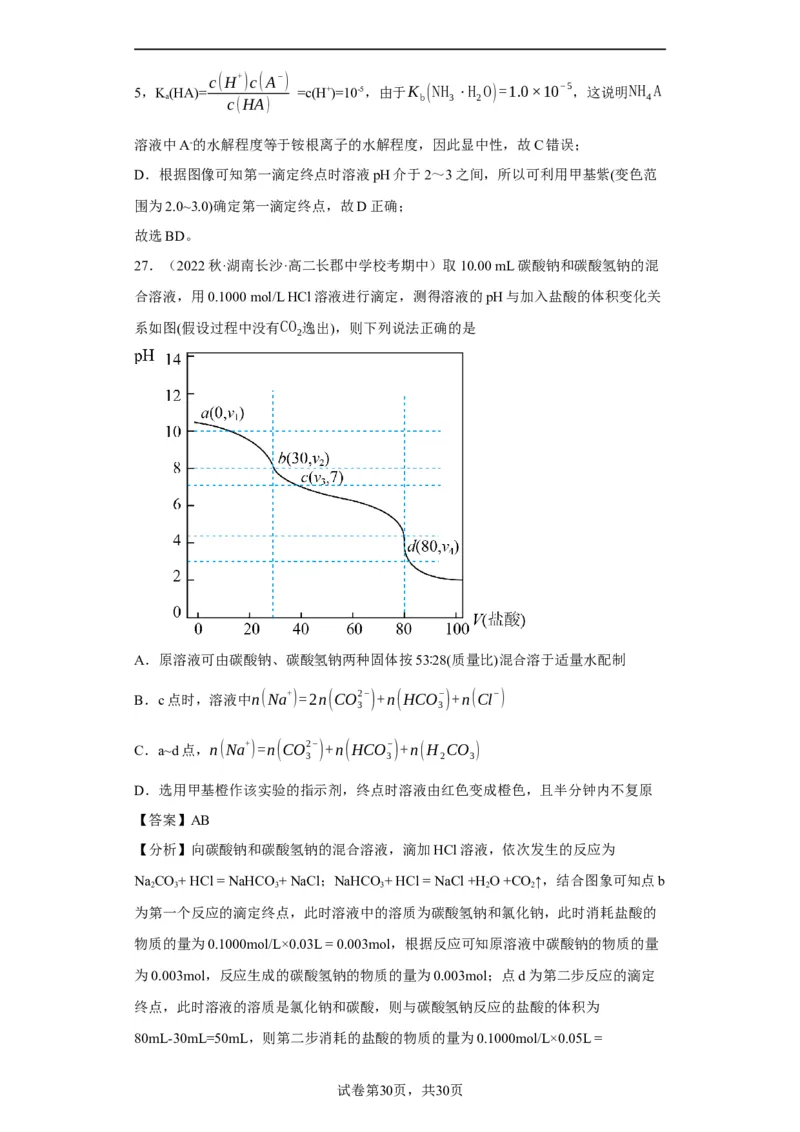
27.(2022秋·湖南长沙·高二长郡中学校考期中)取10.00 mL碳酸钠和碳酸氢钠的混
合溶液,用0.1000 mol/L HCl溶液进行滴定,测得溶液的pH与加入盐酸的体积变化关
系如图(假设过程中没有CO 逸出),则下列说法正确的是
2
A.原溶液可由碳酸钠、碳酸氢钠两种固体按53∶28(质量比)混合溶于适量水配制
B.c点时,溶液中n(Na+)=2n(CO2−)+n(HCO−)+n(Cl−)
3 3
C.a~d点,n(Na+)=n(CO2−)+n(HCO−)+n(H CO )
3 3 2 3
D.选用甲基橙作该实验的指示剂,终点时溶液由红色变成橙色,且半分钟内不复原
【答案】AB
【分析】向碳酸钠和碳酸氢钠的混合溶液,滴加HCl溶液,依次发生的反应为
NaCO+ HCl = NaHCO + NaCl;NaHCO + HCl = NaCl +H O +CO ↑,结合图象可知点b
2 3 3 3 2 2
为第一个反应的滴定终点,此时溶液中的溶质为碳酸氢钠和氯化钠,此时消耗盐酸的
物质的量为0.1000mol/L×0.03L = 0.003mol,根据反应可知原溶液中碳酸钠的物质的量
为0.003mol,反应生成的碳酸氢钠的物质的量为0.003mol;点d为第二步反应的滴定
终点,此时溶液的溶质是氯化钠和碳酸,则与碳酸氢钠反应的盐酸的体积为
80mL-30mL=50mL,则第二步消耗的盐酸的物质的量为0.1000mol/L×0.05L =
试卷第30页,共30页0.005mol,原溶液中碳酸氢钠的物质的量为0.005mol - 0.003 mol = 0.002 mol;点c的
pH等于7,此时溶液的溶质为碳酸氢钠、氯化钠和碳酸。
【详解】A.由分析可知原溶液中碳酸钠的质量为0.003mol×106g/mol = 0.318g,碳酸
0.318g 53
氢钠的质量为0.002mol×84g/mol = 0.168g,二者的质量比为 = ,A项正确;
0.168g 28
B.c点时溶液呈中性,根据电荷守恒可知n(Na+)=2n(CO2−)+n(HCO−)+n(Cl−),
3 3
B项正确;
C.经分析可知溶液中碳酸钠和碳酸氢钠的物质的量之比为3:2,则溶液中Na:C=8:
5,由此可知a~d点,根据物料守恒可知
5n(Na+)=8[n(CO2−)+n(HCO−)+n(H CO )],C项错误;
3 3 2 3
D.结合图象可知整个滴定过程中溶液的pH由大到小变化,选用甲基橙作该实验的指
示剂,终点时溶液由橙色变成红色,且半分钟内不复原,D项错误;
故选AB。
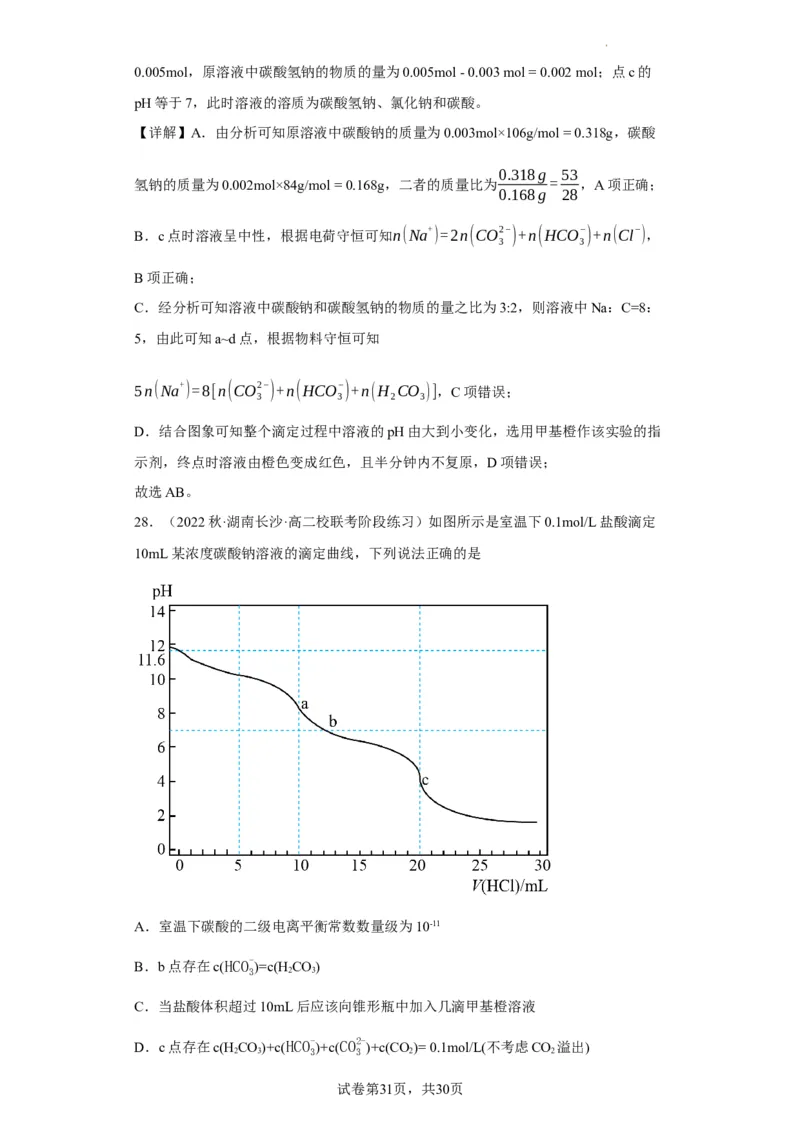
28.(2022秋·湖南长沙·高二校联考阶段练习)如图所示是室温下0.1mol/L盐酸滴定
10mL某浓度碳酸钠溶液的滴定曲线,下列说法正确的是
A.室温下碳酸的二级电离平衡常数数量级为10-11
B.b点存在c(HCO-
)=c(H CO)
3 2 3
C.当盐酸体积超过10mL后应该向锥形瓶中加入几滴甲基橙溶液
D.c点存在c(HCO)+c(HCO- )+c(CO2- )+c(CO )= 0.1mol/L(不考虑CO 溢出)
2 3 3 3 2 2
试卷第31页,共30页
学科网(北京)股份有限公司【答案】AC
【分析】起点至a点发生反应H++CO2-=HCO-,a点溶质为NaHCO ,b点溶液呈中性,
3 3 3
c点为盐酸与碳酸钠恰好反应生成NaCl和水和二氧化碳;
【详解】A.根据图像在a点和c点附近均出现滴定突跃可知,碳酸钠溶液浓度等于盐
酸浓度,则碳酸钠溶液的浓度为0.1mol⋅L−1,0.1mol⋅L−1碳酸钠溶液pH=11.6,溶
10−14 10−2.4×10−2.4
液中c(OH-)= =10−2.4mol/L,求碳酸根水解常数为K = =10−3.8,
10−11.6 ℎ 0.1
10−14
则碳酸的二级电离平衡常数K = =10−10.2 ,数量级为10-11,A正确;
a2 10−3.8
B.a点完成了H++CO2-=HCO-,该点c(HCO- )>c(H CO),当横坐标为15mL时,若不考
3 3 3 2 3
虑电离和水解,则c(HCO- )=c(H CO),由图像可知,此时溶液为酸性,说明HCO 电
3 2 3 2 3
离是主要的,则c(HCO- )>c(H CO),b点在二者中间,则应存在c(HCO- )>c(H CO),B
3 2 3 3 2 3
错误;
C.当盐酸体积超过10mL后溶液为酸性,所以使用甲基橙作为指示剂,C正确;
D.c点溶液体积为30mL,根据物料守恒有c(HCO)+c(HCO- )+c(CO2-
)+c(CO )=
2 3 3 3 2
0.03333mol/L,D错误;
故选AC。
29.(2023秋·湖南·高三校联考阶段练习)常温下,用0.1000mol/L的NaOH溶液滴
定20.00mL浓度分别为c 、c 的一元酸(HA)、二元酸(H B)溶液,得到如图滴定曲线,
1 2 2
其中c、d为两种酸恰好完全中和的化学计量点。忽略溶液混合时体积变化。下列叙述
正确的是。
试卷第32页,共30页A.X曲线代表H B,Y曲线代表HA,c >c
2 1 2
B.两种酸恰好完全中和时,均可用酚酞或甲基橙作指示剂
C.若c =0.1000mol/L,对于HA而言,滴定过程中有
1
c(HA)+2c(A−)+c(OH−)=c(H+)+0.1000mol/L
D.若a点V(NaOH)=7.95mL,则a点c(Na+)<2c(HB−)+c(B2−)+3c(H B)
2
【答案】AC
【分析】二元弱酸,有两次滴定突变,一元酸有一次滴定突变,故X曲线代表H B,Y
2
曲线代表HA,据此分析。
【详解】A.HA消耗的V (NaOH)小于H B消耗V (NaOH)的二倍,则c >c ,A正确;
2 1 2
B.H B、HA恰好完全中和时,产物为强碱弱酸盐,均呈碱性,可使用酚酞做指示剂,
2
不可使用甲基橙做指示剂,B错误;
C.溶液中的质子守恒:c(H+)+c(HA)=c(OH-)①,物料守恒:②
c(A−)+c(HA)=0.05mol⋅L-1②,②×2-①得:
c(HA)+2c(A−)+c(OH−)=c(H+)+0.1000mol/L,C正确;
D.完全中和时消耗V (NaOH) = 10.60mL, a点V (NaOH) = 7.95mL时,占消耗氢氧
化钠总体积的四分之三,则溶质为NaHB与NaB,且二者的浓度比为:1 : 1形成的溶
2
液,则a点物料守恒和电荷守恒有关系式:c(Na+)+c(H+)=c(HB−)+2c(B2−)+c(OH-)
①,2c(Na+)=3c(HB−)+3c(B2−)+3c(H B)②,用②-①,
2
得c(Na+)+c(OH-)=2c(HB−)+c(B2−)+3c(H B)+c(H+)由于酸性环境,c(H+) >
2
c(OH-),故c(Na+)>2c(HB−)+c(B2−)+3c(H B),D错误;
2
试卷第33页,共30页
学科网(北京)股份有限公司故本题选AC。
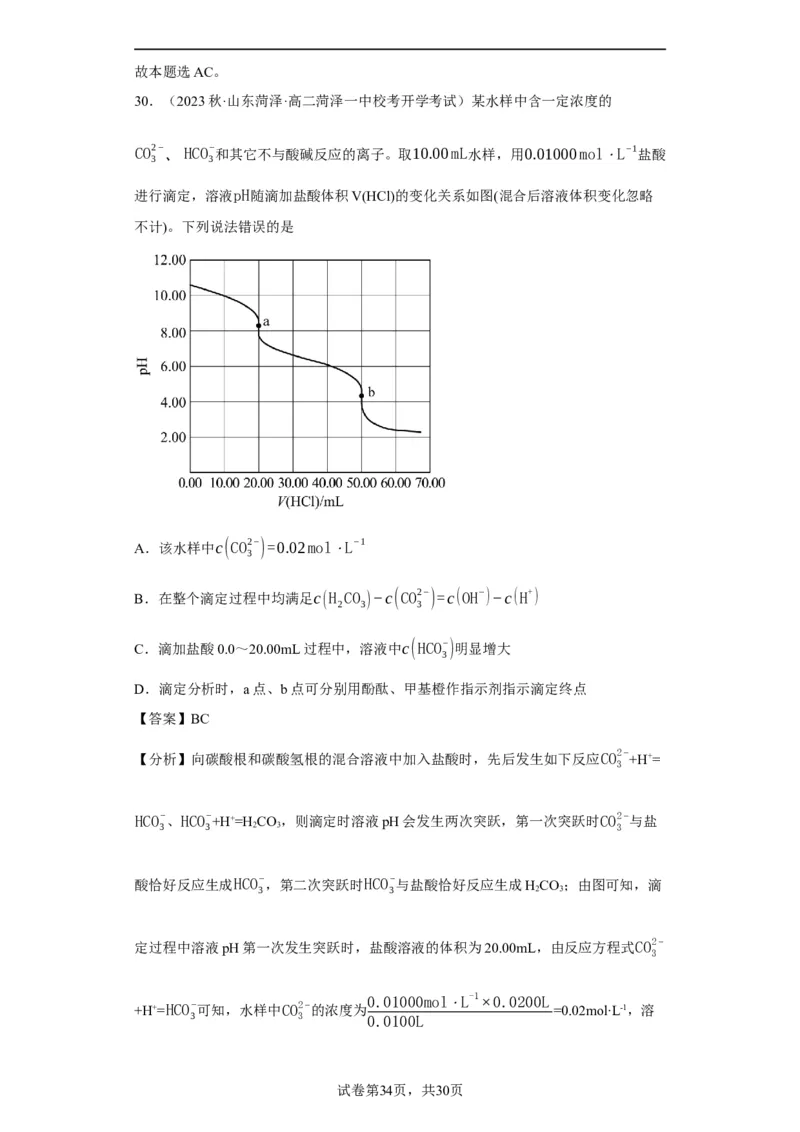
30.(2023秋·山东菏泽·高二菏泽一中校考开学考试)某水样中含一定浓度的
CO2−、HCO− 和其它不与酸碱反应的离子。取10.00mL水样,用0.01000mol⋅L−1盐酸
3 3
进行滴定,溶液pH随滴加盐酸体积V(HCl)的变化关系如图(混合后溶液体积变化忽略
不计)。下列说法错误的是
A.该水样中c(CO2−)=0.02mol⋅L−1
3
B.在整个滴定过程中均满足c(H CO )−c(CO2−)=c(OH−)−c(H+)
2 3 3
C.滴加盐酸0.0~20.00mL过程中,溶液中c(HCO−)明显增大
3
D.滴定分析时,a点、b点可分别用酚酞、甲基橙作指示剂指示滴定终点
【答案】BC
【分析】向碳酸根和碳酸氢根的混合溶液中加入盐酸时,先后发生如下反应CO2−
+H+=
3
HCO−、HCO− +H+=H CO,则滴定时溶液pH会发生两次突跃,第一次突跃时CO2−与盐
3 3 2 3 3
酸恰好反应生成HCO− ,第二次突跃时HCO−
与盐酸恰好反应生成HCO;由图可知,滴
3 3 2 3
定过程中溶液pH第一次发生突跃时,盐酸溶液的体积为20.00mL,由反应方程式CO2−
3
+H+=HCO−可知,水样中CO2−的浓度为
0.01000mol⋅L-1×0.0200L
=0.02mol∙L-1,溶
3 3 0.0100L
试卷第34页,共30页液pH第二次发生突跃时,盐酸溶液的体积为50.00mL,则水样中HCO−的浓度为
3
0.01000mol⋅L-1×(0.0500L-0.0200L-0.0200L)
=0.01mol∙L-1。
0.0100L
【详解】A.由分析可知,水样中CO2−的浓度为0.02mol∙L-1,A正确;
3
B.由图可知,a点发生的反应为CO2− +H+=HCO−,可溶性碳酸氢盐溶液中质子守恒关
3 3
系为c(H CO)+c(H+)=c(OH-)+c(CO2− ),即c(H CO)-c(CO2− )=c(OH-)-c(H+),但在其它点
2 3 3 2 3 3
不存在此质子守恒关系,B错误;
C.由分析可知,水样中HCO−的浓度为0.01mol/L,当盐酸溶液体积V(HCl)≤20.00mL
3
时,只发生反应CO2− +H+=HCO−,滴定时溶液中HCO−浓度为
3 3 3
0.01000mol/L×0.0100L+0.01000mol/L×V(HCl)
=0.01mol/L,则滴定时溶液中
0.0100L+V(HCl)
HCO−
的浓度不变,C错误;
3
D.由图可知,a点突跃点在8-10之间,可以会用酚酞做指示剂,b点突跃点在4左右,
可使用甲基橙做指示剂,D正确;
故选BC。
试卷第35页,共30页
学科网(北京)股份有限公司