文档内容
热点专项 溶液中粒子浓度大小比较
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.单一溶液中粒子浓度的关系.............................................................................................................................
2.混合溶液(缓冲溶液)中粒子浓度的关系判断..................................................................................................
3.混合溶液中离子浓度的比较.............................................................................................................................
【命题预测】...........................................................................................................................................................
考向1溶液混合型粒子浓度关系...........................................................................................................................
考向2 化工流程中粒子浓度关系..........................................................................................................................
考点要求 考题统计 考情分析
2024· 重庆卷,11,3分;2024·江
苏卷,12,3分;2024·安徽卷, 溶液中离子浓度的大小比较是主流试题,
文字陈述 13,3分;2023•浙江省6月选考, 难度在选择题中最大,往往是压轴题。此
15,3分;2022•重庆卷,11,3 类试题信息量大,且都隐藏于题目或图象
分;2022·浙江省6月卷,23,2分 中,主要通过酸碱中和滴定、电离平衡、
水解平衡和沉淀溶解平衡的情境,利用三
大守恒进行离子浓度大小比较、离子浓
2024·湖南卷,13,3分;2023•湖
度、电离平衡常数、水解平衡常数和溶度
南卷,12,3分;2023•江苏卷,
图象分析 积常数的计算等。预计2025年此类题仍活
12,3分;2022•福建卷,10;
跃在卷面上。
2022•江苏卷,12,3分;1.(2024· 重庆卷,11,3分)某兴趣小组探究[Cu(NH )](NO ) 的生成过程。若向
3 4 3 2
3mL0.1mol·L-1Cu(NO ) 溶液中逐滴加入 氨水,则下列说法正确的是( )
3 2
A.产生少量沉淀时(pH =4.8),溶液中c(NH +)c(NO -)
4 3
C.沉淀部分溶解时,溶液中c(Cu2+) < c(NH +)
4
D.沉淀完全溶解时,溶液中2c([Cu(NH )]2+) >c(NO -)
3 4 3
2.(2024·江苏卷,12,3分)室温下,通过下列实验探究SO 的性质。已知K (H SO )=1.3×10-2,
2 a1 2 3
K (H SO )=6.2×10-8.。
a2 2 3
实验1:将SO 气体通入水中,测得溶液pH=3。
2
实验2:将SO 气体通入0.1mol·L-1NaOH溶液中,当溶液pH=4时停止通气。
2
实验3:将SO 气体通入0.1mol·L-1酸性KMnO 溶液中,当溶液恰好褪色时停止通气。
2 4
下列说法正确的是( )
A.实验1所得溶液中:cSO 2-+cHSO ->c(H+)
3 3
B.实验2所得溶液中:cSO 2->cHSO -
3 3
C.实验2所得溶液经蒸干、灼烧制得NaHSO 固体
3
D.实验3所得溶液中:cSO 2->cMn2+
43.(2024·安徽卷,13,3分)环境保护工程师研究利用NaS、FeS和HS处理水样中的Cd2+。已知
2 2
时,HS饱和溶液浓度约为0.1mol·L-1,K (H S)=10-6.97,K (H S)=10-12.90,K (FeS)=10-17.20,K (CdS)=10-
2 a1 2 a2 2 sp sp
26.10。下列说法错误的是( )
A.NaS溶液中:cNa++cH+=cOH-+cHS-+2cS2-
2
B.0.01mol·L-1NaS溶液中:cNa+>cS2->cOH->cHS-
2
C.向cCd2+=0.01mol·L-1的溶液中加入FeS,可使
D.向cCd2+=0.01mol·L-1的溶液中通入HS气体至饱和,所得溶液中:cH+>cCd2+
2
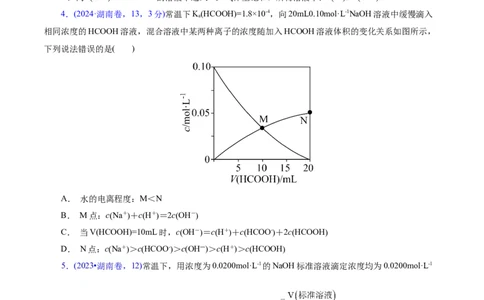
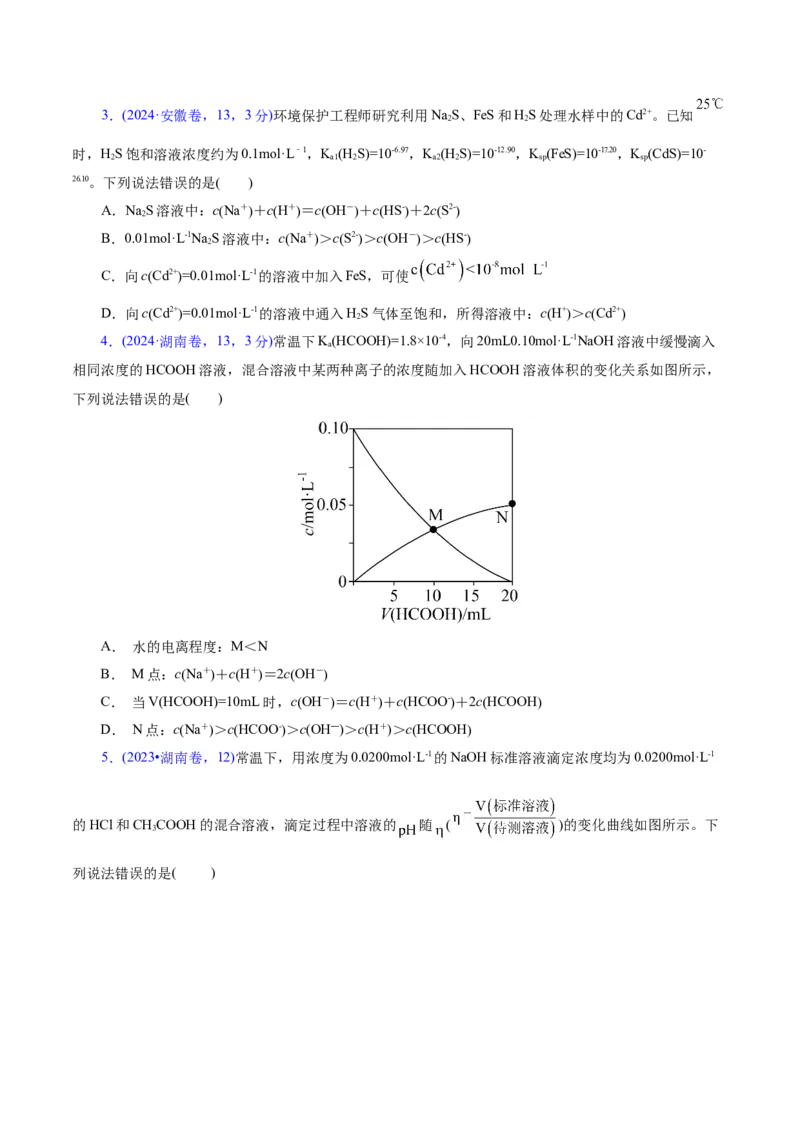
4.(2024·湖南卷,13,3分)常温下K(HCOOH)=1.8×10-4,向20mL0.10mol·L-1NaOH溶液中缓慢滴入
a
相同浓度的HCOOH溶液,混合溶液中某两种离子的浓度随加入HCOOH溶液体积的变化关系如图所示,
下列说法错误的是( )
A. 水的电离程度:M<N
B. M点:cNa++cH+=2cOH-
C. 当V(HCOOH)=10mL时,cOH-=cH++cHCOO-+2cHCOOH
D. N点:cNa+>cHCOO->c(OH―)>c(H+)>cHCOOH
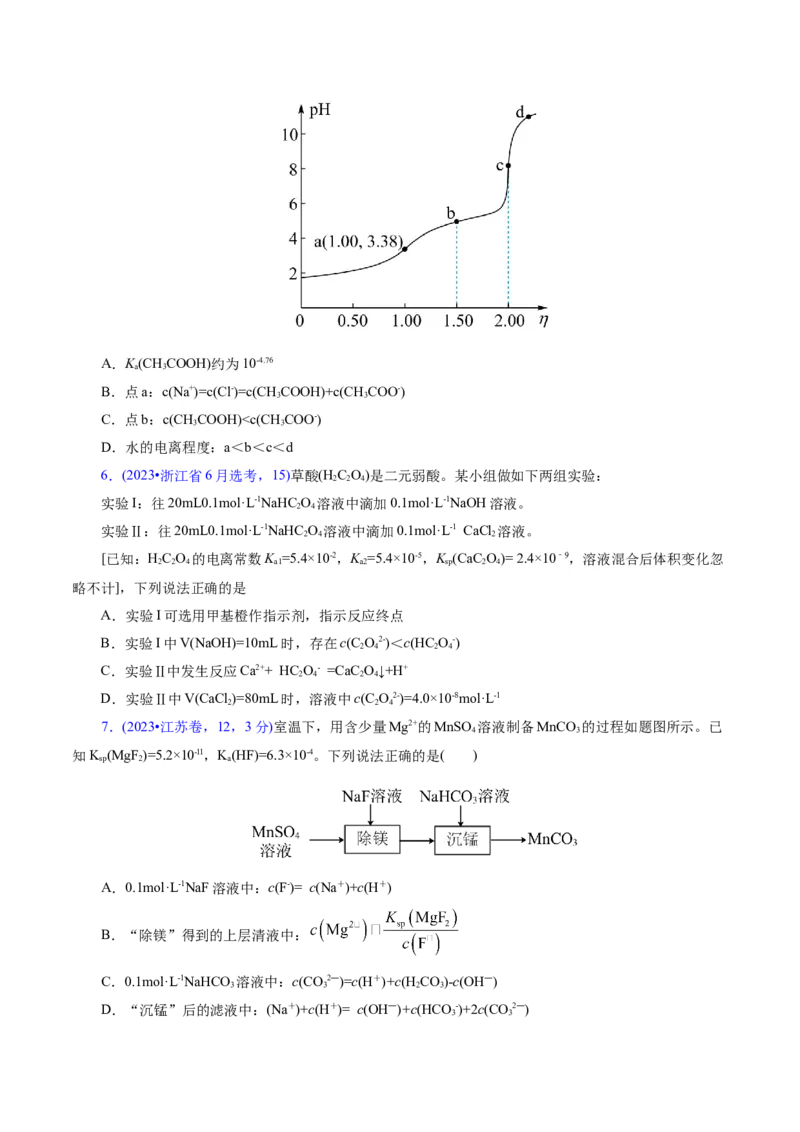
5.(2023•湖南卷,12)常温下,用浓度为0.0200mol·L-1的NaOH标准溶液滴定浓度均为0.0200mol·L-1
的HCl和CHCOOH的混合溶液,滴定过程中溶液的 随 ( )的变化曲线如图所示。下
3
列说法错误的是( )A.K(CHCOOH)约为10-4.76
a 3
B.点a:c(Na+)=c(Cl-)=c(CH COOH)+c(CH COO-)
3 3
C.点b:c(CHCOOH)c(HSO -)>c(H SO )
2 3 3 2 3
B.NaOH完全转化为NaHSO 时,溶液中:c(H+)+c(SO 2-)=c(OH—)+c(H SO )
3 3 2 3
C.NaOH完全转化为NaSO 时,溶液中:c(Na+)>c(SO 2-)>c(OH—)>c(HSO -)
2 3 3 3
D.NaOH溶液吸收SO ,c =0.1mol•L-1溶液中:c(H SO )>c(SO 2-)
2 总 2 3 3
3.室温下,通过下列实验探究NaHSO、NaSO 溶液的性质。
3 2 3
实验1:用pH试纸测量0.1mol·L-1NaHSO 溶液的pH,测得pH约为5
3
实验2:0.1mol·L-1NaHSO 溶液中加入等体积0.1mol·L-1NaOH溶液,没有明显现象
3
实验3:0.1mol·L-1NaSO 溶液中滴加新制饱和氯水,氯水颜色褪去
2 3
实验4:将0.1mol·L-1NaSO 溶液与0.1mol·L-1CaCl 溶液等体积混合,产白色沉淀
2 3 2
下列说法正确的是( )
A.由实验1可得出: >K (H SO )
a2 2 3
B.实验2所得的溶液中c(HSO -)>c(SO 2-)
3 3
C.实验3中发生反应的离子方程式为HO+Cl + SO 2-=SO2-+2H++2Cl-
2 2 3 4
D.实验4中两溶液混合时有:c(Ca2+)·c(SO 2-)<K (CaSO)
3 sp 3
4.(2025· 江浙皖高中发展共同体高三联考)草酸钠(Na C O)可用作抗凝血剂。室温下,通过下列实验
2 2 4
探究NaC O 溶液的性质。
2 2 4
实验 实验操作和现象
1 测得0.1mol·L-1NaC O 溶液的pH=8.4
2 2 4
2 向0.2mol·L-1NaC O 溶液中加入等体积 盐酸,测得混合后溶液的pH=5.5
2 2 4
3 向0.1mol·L-1NaC O 溶液中滴加几滴酸性KMnO 溶液,振荡,溶液仍为无色
2 2 4 4
4 向0.1mol·L-1NaC O 溶液中加入等体积0.1mol·L-1CaCl 溶液,产生白色沉淀
2 2 4 2
下列有关说法正确的是( )
A.0.1mol·L-1NaC O 溶液中存在:cNa++cH+=cOH-+cHC O-+cC O2-
2 2 4 2 4 2 4
B.实验2得到的溶液中:c(Cl-)>cHC O>cC O2-
2 2 4 2 4
C.实验3中 被还原成 ,则反应的离子方程式:C O2-+2MnO-+16H+=10CO ↑+Mn2++8H O
2 4 4 2 2
D.依据实验4可得:K (CaC O) >2.5×10-3
sp 2 4
5.(2022·江苏省百校大联考高三第二次考试)室温下,通过下列实验探究亚硫酸盐的性质。已知:K (H SO )=1.54×10-2、K (H SO )=1.02×10-7
a1 2 3 a2 2 3
实验 实验操作和现象
1 向10mL0.10mol·L-1NaOH溶液通入11.2mL(标准状况)SO ,测得pH约为9
2
2 向10mL0.10mol·L-1NaOH溶液通入SO 至溶液pH=7
2
3 向10mL0.1mol·L-1NaOH溶液通入22.4mL(标准状况)SO ,测得pH约为3
2
4 取实验3所得溶液1mL,加入1mL0.01mol·L-1Ba(OH) 溶液,产生白色沉淀
2
下列说法正确的是( )
A.实验1得到的溶液中有:c(SO 2-)+c(HSO -)+c(H+)7
3 向NaClO溶液中通入少量的CO,测得pH降低
2
4 向0.01mol•L-1NaCO 溶液中加入等体积0.02mol•L-1CaCl 溶液,产生白色沉淀
2 3 2
下列所得结论正确的是( )
A.实验1溶液中存在:c(Na+)+c(H+)= c(OH-)+c(CO 2-)+c(HCO-)
3 3
B.由实验2可得
C.实验3反应的离子方程式:CO+H O+2 = CO2-+2HClO
2 2 3
D.实验4所得上层清液中的
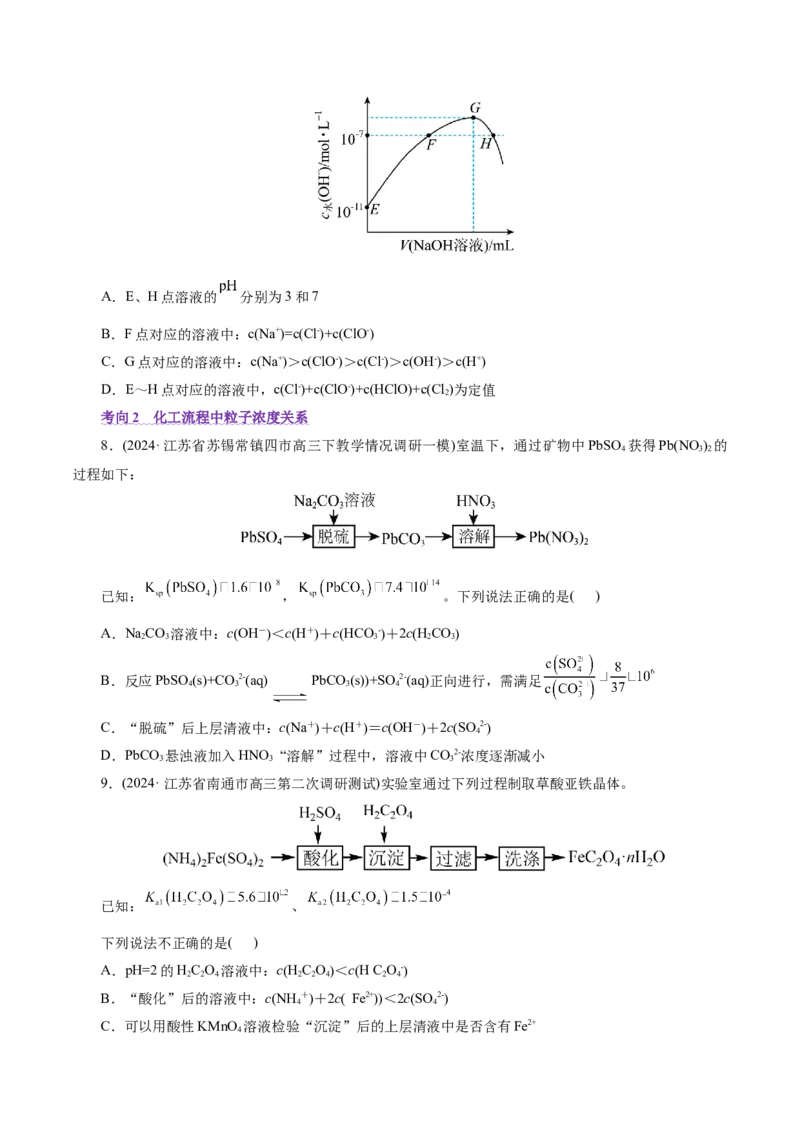
7.常温下,向新制氯水中滴加 溶液,溶液中水电离出的OH-浓度与 溶液体积之间的关系
如图所示。下列推断正确的是( )A.E、H点溶液的 分别为3和7
B.F点对应的溶液中:c(Na+)=c(Cl-)+c(ClO-)
C.G点对应的溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(OH-)>c(H+)
D.E~H点对应的溶液中,c(Cl-)+c(ClO-)+c(HClO)+c(Cl )为定值
2
考向 2 化工流程中粒子浓度关系
8.(2024·江苏省苏锡常镇四市高三下教学情况调研一模)室温下,通过矿物中PbSO 获得Pb(NO ) 的
4 3 2
过程如下:
已知: , 。下列说法正确的是( )
A.NaCO 溶液中:cOH-<cH++cHCO -+2cHCO
2 3 3 2 3
B.反应PbSO (s)+CO2-(aq) PbCO (s))+SO 2-(aq)正向进行,需满足
4 3 3 4
C.“脱硫”后上层清液中:cNa++cH+=cOH-+2cSO 2-
4
D.PbCO 悬浊液加入HNO “溶解”过程中,溶液中CO2-浓度逐渐减小
3 3 3
9.(2024· 江苏省南通市高三第二次调研测试)实验室通过下列过程制取草酸亚铁晶体。
已知: 、
下列说法不正确的是( )
A.pH=2的HC O 溶液中:cHC O<cH C O-
2 2 4 2 2 4 2 4
B.“酸化”后的溶液中:cNH ++2c Fe2+<2cSO 2-
4 4
C.可以用酸性KMnO 溶液检验“沉淀”后的上层清液中是否含有Fe2+
4D.水洗后,再用乙醇洗涤有利于晶体快速干燥
10.[真题改编](2023•江苏卷,12)室温下,用含少量Mg2+的MnSO 溶液制备MnCO 的过程如题图所
4 3
示:
已知:K (MgF )=5.2×10-11,K (MnCO )=8.0×10-11,K [Mn(OH) ]=1.9×10-13;K (H CO)=4.5×10-7,
sp 2 sp 3 sp 2 a1 2 3
K (H CO)=4.7×10-11。下列说法正确的是( )
a2 2 3
A.MgF 饱和溶液中:cF-+cHF=2cMg2+
2
B.为提高MnCO 的产率,使用NaCO 溶液“沉锰”效果更好
3 2 3
C.0.1mol·L-1NaHCO 溶液中,cNa+>cHCO ->cCO2->cHCO
3 3 3 2 3
D.反应Mn2++2HCO-=MnCO↓+HCO 的平衡常数为
3 3 2 3
11.(2024· 江苏省南通市海门高三第一次调研考试)室温下,用 溶液吸收SO
2
的过程如图所示。已知 , ,下列说法正确的是( )
A. 溶液中:
B. 溶液中:
C.吸收烟气后的溶液中:
D.“沉淀”得到的上层清液中:
12.(2024· 江苏省南通市如皋市高三下适应性考试)室温下,用含少量ZnSO 杂质的1mol·L-1 MnSO
4 4
溶液制备MnCO 的过程如下图所示。下列说法正确的是( )
3已知:
A.“除锌”后所得上层清液中, 一定小于
B.0.1mol·L-1NH HCO 溶液中存在:
4 3
C.氨水、NH HCO 溶液中存在:
4 3
D.“沉锰”后的滤液中存在:
13.(2024·江苏省盐城市高三一模考试)室温下,用含少量 的FeSO 溶液制备FeCO 的过程如图所
4 3
示。已知: 。下
列说法正确的是( )
A. 溶液中:
B.“除钙”得到的上层清液中:
C. 的氨水−NH HCO 溶液:
4 3
D.“沉铁”反应的离子方程式:
14.(2024·江苏省南京市、盐城市高三第一次模拟考试)室温下,用含少量 的粗NiSO 溶液
4
制备NiSO·6H O晶体的流程如下图所示。
4 2已知 。下列说法正确的是( )
A.粗 溶液中:
B.“沉铁”反应为:
C. 溶液中:
D.“沉镁”后的滤液中:
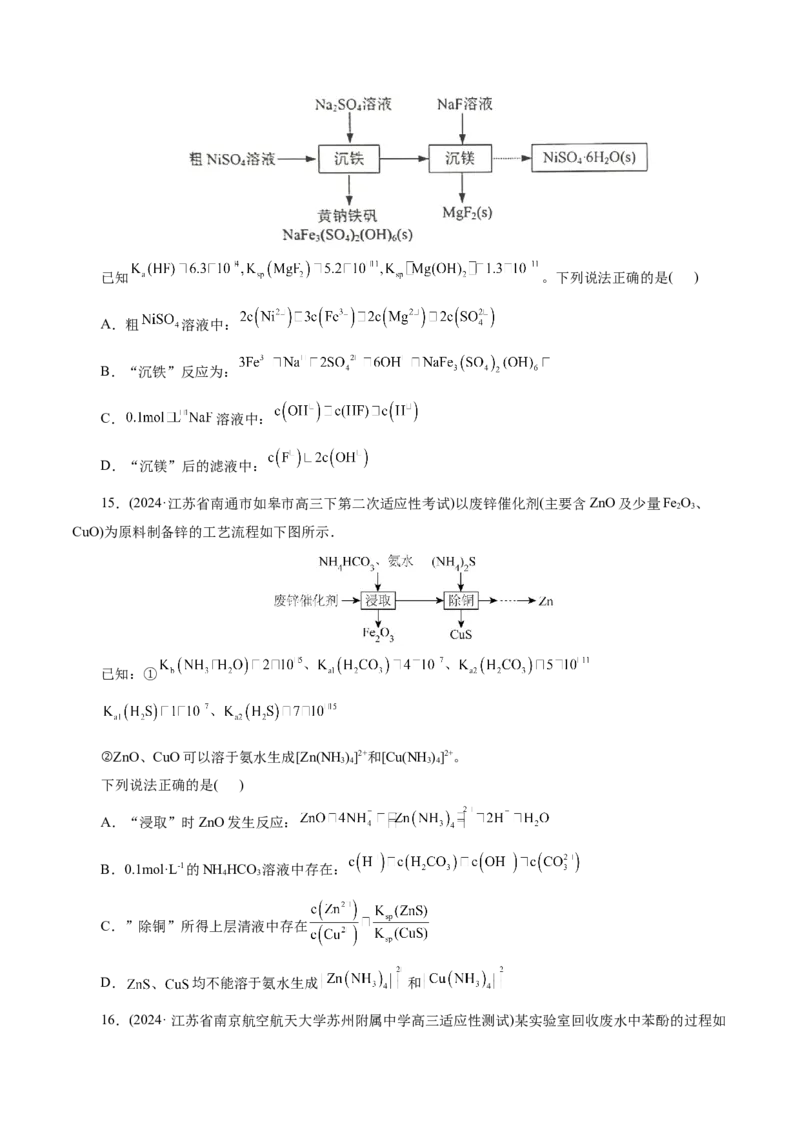
15.(2024·江苏省南通市如皋市高三下第二次适应性考试)以废锌催化剂(主要含ZnO及少量Fe O、
2 3
CuO)为原料制备锌的工艺流程如下图所示.
已知:①
②ZnO、CuO可以溶于氨水生成[Zn(NH )]2+和[Cu(NH )]2+。
3 4 3 4
下列说法正确的是( )
A.“浸取”时ZnO发生反应:
B.0.1mol·L-1的NH HCO 溶液中存在:
4 3
C.”除铜”所得上层清液中存在
D. 均不能溶于氨水生成 和
16.(2024· 江苏省南京航空航天大学苏州附属中学高三适应性测试)某实验室回收废水中苯酚的过程如下图所示。已知:苯酚的电离常数K=1.0×10-10,HCO 的电离常数K =4.5×10-7,K =4.7×10-11。
a 2 3 a1 a2
下列有关说法不正确的是( )
A.操作1、操作2 均为分液
B. NaHCO 溶液中存在:c(HCO)+c(H+)=c(OH-)+c(CO 2-)
3 2 3 3
C.若反应1后溶液中存在c(Na+)=2 c(C HO-)+2 c(C HOH),此时c(C HO-)>c(HCO-)
6 5 6 5 6 5 3
D.反应2 中通入CO 至溶液 pH=10时, 此时溶液中存在: c(C HO-)= c(C HOH)
2 6 5 6 5
17.(2024·江苏省连云港市高三第一次调研考试)室温下,用含少量Co2+和Ni2+的FeSO 溶液制备
4
FeC O·2H O的过程如下。
2 4 2
已知: , ; ,
下列说法正确的是( )
A.0.01mol·L-1NaS溶液中:c(HS―)>c(S2-)
2
B.“除钴镍”后得到的上层清液中c(Co2+)为6.0×10-2mol·L-1,则c(Ni2+)为1.0×10-6mol·L-1
C.0.1mol·L-1NaHC O 溶液中:cOH-=cH++ c C O2-+cHC O
2 4 2 4 2 2 4
D.“沉铁”后的滤液中:cNa++ cH+=cOH-+2c C O2-+cH C O-
2 4 2 4
18.燃煤烟气脱硫的一种方法如图所示。室温下以150mL 0.2 氨水吸收 ,若通入 所引
起的溶液体积变化和 、 挥发可忽略,溶液中含硫物种的浓度 。
的电离平衡常数分别为: , ; 的电离平衡常数为:
。下列说法正确的是( )
A.NH ·H O吸收 所得到的溶液中:
3 2
B.NH ·H O吸收 , 溶液:
3 2C.NH ·H O吸收标况下0.448L ,所得溶液中:
3 2
D.题图所示“吸收”“氧化”后的溶液pH增大