文档内容
热点强化练 10 新型电源工作原理
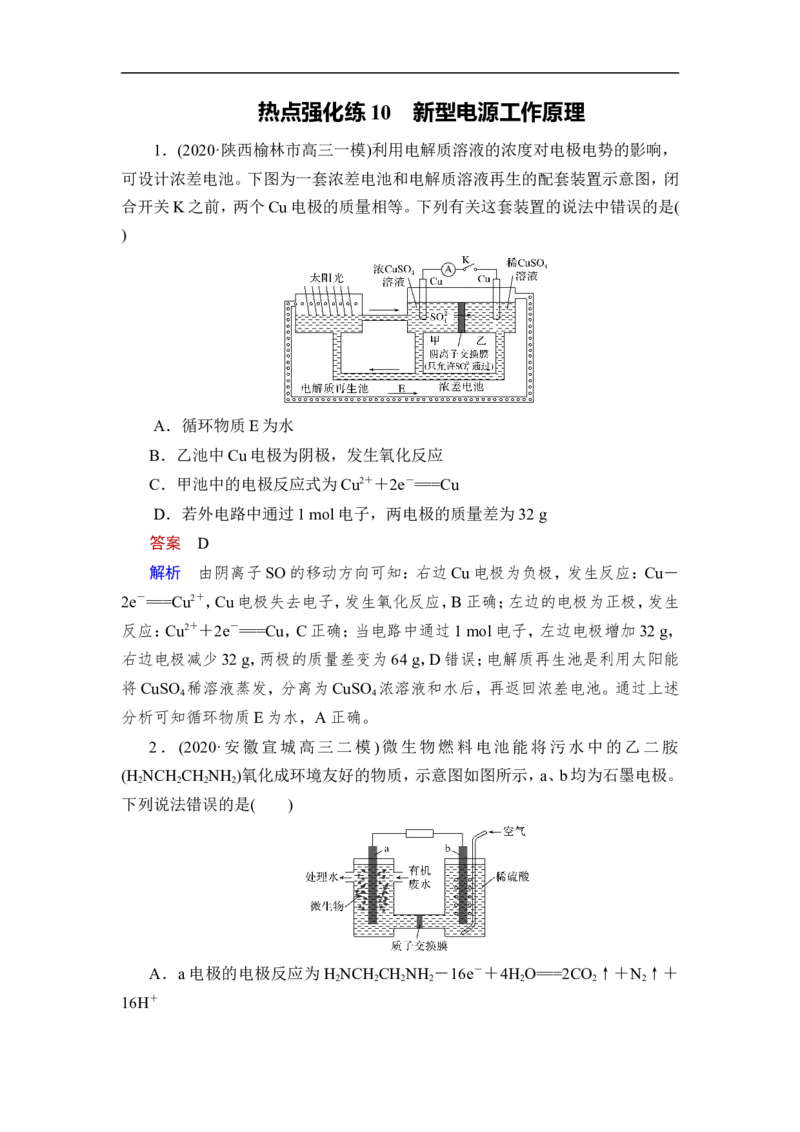
1.(2020·陕西榆林市高三一模)利用电解质溶液的浓度对电极电势的影响,
可设计浓差电池。下图为一套浓差电池和电解质溶液再生的配套装置示意图,闭
合开关K之前,两个Cu电极的质量相等。下列有关这套装置的说法中错误的是(
)
A.循环物质E为水
B.乙池中Cu电极为阴极,发生氧化反应
C.甲池中的电极反应式为Cu2++2e-===Cu
D.若外电路中通过1 mol电子,两电极的质量差为32 g
答案 D
解析 由阴离子SO的移动方向可知:右边Cu电极为负极,发生反应:Cu-
2e-===Cu2+,Cu电极失去电子,发生氧化反应,B正确;左边的电极为正极,发生
反应:Cu2++2e-===Cu,C正确;当电路中通过1 mol电子,左边电极增加32 g,
右边电极减少32 g,两极的质量差变为64 g,D错误;电解质再生池是利用太阳能
将CuSO 稀溶液蒸发,分离为CuSO 浓溶液和水后,再返回浓差电池。通过上述
4 4
分析可知循环物质E为水,A正确。
2.(2020·安徽宣城高三二模)微生物燃料电池能将污水中的乙二胺
(H NCH CH NH )氧化成环境友好的物质,示意图如图所示,a、b均为石墨电极。
2 2 2 2
下列说法错误的是( )
A.a电极的电极反应为H NCH CH NH -16e-+4H O===2CO ↑+N ↑+
2 2 2 2 2 2 2
16H+B.电池工作时质子通过交换膜由负极区向正极区移动
C.a电极上的电势比b电极上的电势低
D.开始放电时b电极附近溶液的pH保持不变
答案 D
解析 根据原电池装置图分析,H N(CH ) NH 在a电极上失电子发生氧化反
2 2 2 2
应,生成氮气、二氧化碳和水,则a为负极,电极反应式为H N(CH ) NH +4H O
2 2 2 2 2
-16e-===2CO ↑+N ↑+16H+,氧气在正极b上得电子发生还原反应,电极反
2 2
应式为:O +4e-+4H+===2H O,A选项正确;原电池中,阳离子向正极移动,阴
2 2
离子向负极移动,因此,电池工作时质子(H+)通过质子交换膜由负极区向正极区
移动,B选项正确;由上述分析可知,a电极为负极,b电极为正极,故a电极上的
电势比b电极上的电势低,C选项正确;开始放电时,氧气在正极b上得电子发生
还原反应,发生的电极反应式为O +4e-+4H+===2H O,H+浓度减小,故b电极
2 2
附近溶液的pH增大,D选项错误。
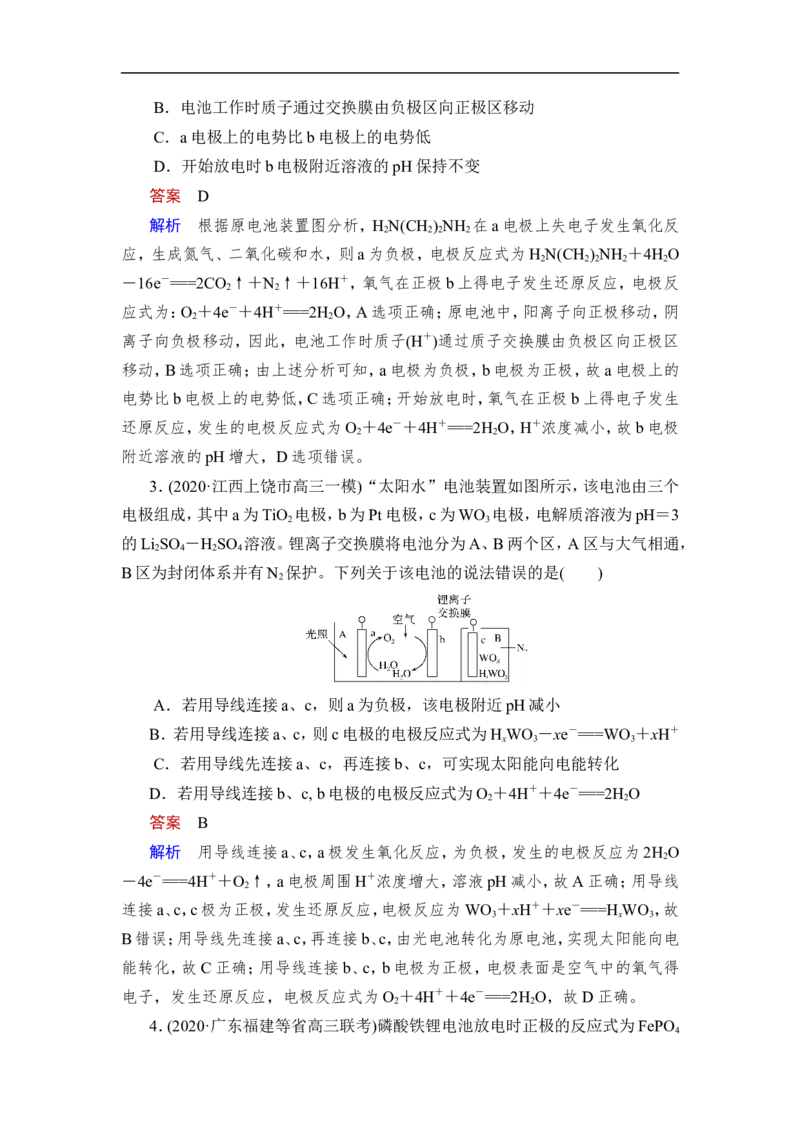
3.(2020·江西上饶市高三一模)“太阳水”电池装置如图所示,该电池由三个
电极组成,其中a为TiO 电极,b为Pt电极,c为WO 电极,电解质溶液为pH=3
2 3
的Li SO -H SO 溶液。锂离子交换膜将电池分为A、B两个区,A区与大气相通,
2 4 2 4
B区为封闭体系并有N 保护。下列关于该电池的说法错误的是( )
2
A.若用导线连接a、c,则a为负极,该电极附近pH减小
B.若用导线连接a、c,则c电极的电极反应式为H WO -xe-===WO +xH+
x 3 3
C.若用导线先连接a、c,再连接b、c,可实现太阳能向电能转化
D.若用导线连接b、c, b电极的电极反应式为O +4H++4e-===2H O
2 2
答案 B
解析 用导线连接a、c,a极发生氧化反应,为负极,发生的电极反应为2H O
2
-4e-===4H++O ↑,a电极周围H+浓度增大,溶液pH减小,故A正确;用导线
2
连接a、c,c极为正极,发生还原反应,电极反应为WO +xH++xe-===H WO ,故
3 x 3
B错误;用导线先连接a、c,再连接b、c,由光电池转化为原电池,实现太阳能向电
能转化,故C正确;用导线连接b、c,b电极为正极,电极表面是空气中的氧气得
电子,发生还原反应,电极反应式为O +4H++4e-===2H O,故D正确。
2 2
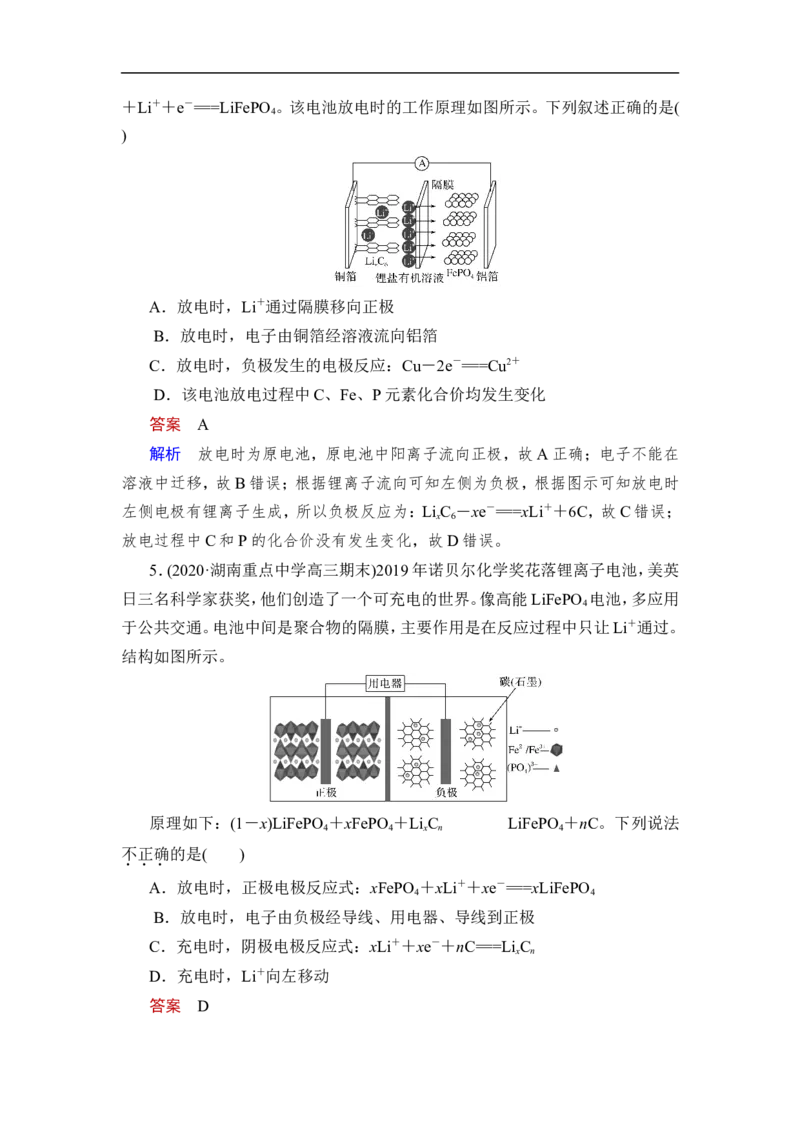
4.(2020·广东福建等省高三联考)磷酸铁锂电池放电时正极的反应式为FePO
4+Li++e-===LiFePO 。该电池放电时的工作原理如图所示。下列叙述正确的是(
4
)
A.放电时,Li+通过隔膜移向正极
B.放电时,电子由铜箔经溶液流向铝箔
C.放电时,负极发生的电极反应:Cu-2e-===Cu2+
D.该电池放电过程中C、Fe、P元素化合价均发生变化
答案 A
解析 放电时为原电池,原电池中阳离子流向正极,故A正确;电子不能在
溶液中迁移,故B错误;根据锂离子流向可知左侧为负极,根据图示可知放电时
左侧电极有锂离子生成,所以负极反应为:Li C -xe-===xLi++6C,故C错误;
x 6
放电过程中C和P的化合价没有发生变化,故D错误。
5.(2020·湖南重点中学高三期末)2019年诺贝尔化学奖花落锂离子电池,美英
日三名科学家获奖,他们创造了一个可充电的世界。像高能LiFePO 电池,多应用
4
于公共交通。电池中间是聚合物的隔膜,主要作用是在反应过程中只让Li+通过。
结构如图所示。
原理如下:(1-x)LiFePO +xFePO +Li C LiFePO +nC。下列说法
4 4 x n 4
不正确的是( )
A.放电时,正极电极反应式:xFePO +xLi++xe-===xLiFePO
4 4
B.放电时,电子由负极经导线、用电器、导线到正极
C.充电时,阴极电极反应式:xLi++xe-+nC===Li C
x n
D.充电时,Li+向左移动
答案 D解 析 放 电 为 原 电 池 原 理 , 从 (1 - x)LiFePO + xFePO +
4 4
Li C LiFePO +nC可知,Li C 失电子,作负极,那么负极反应为:Li C -
x n 4 x n x n
xe-===xLi++nC,LiFePO 作正极,正极反应为:xFePO +xLi++xe-
4 4
===xLiFePO ,充电为电解池工作原理,反应为放电的逆过程。由以上分析可知,
4
放电正极上FePO 得到电子,发生还原反应生成 LiFePO ,正极电极反应式:
4 4
xFePO +xLi++xe-===xLiFePO ,A正确;原电池中电子流向是负极-导线-用
4 4
电器-导线-正极,B正确;充电时,阴极为放电时负极的逆过程,Li+变化为
Li C ,电极反应式:xLi++xe-+nC===Li C ,C正确;充电时,作为电解池,阳离
x n x n
子向阴极移动,Li+向右移动,D错误。
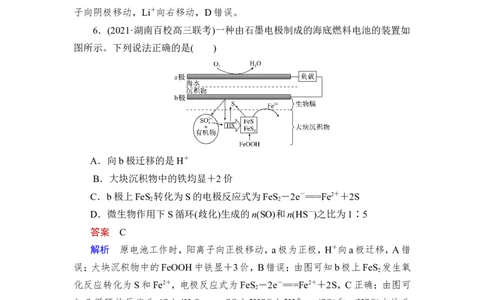
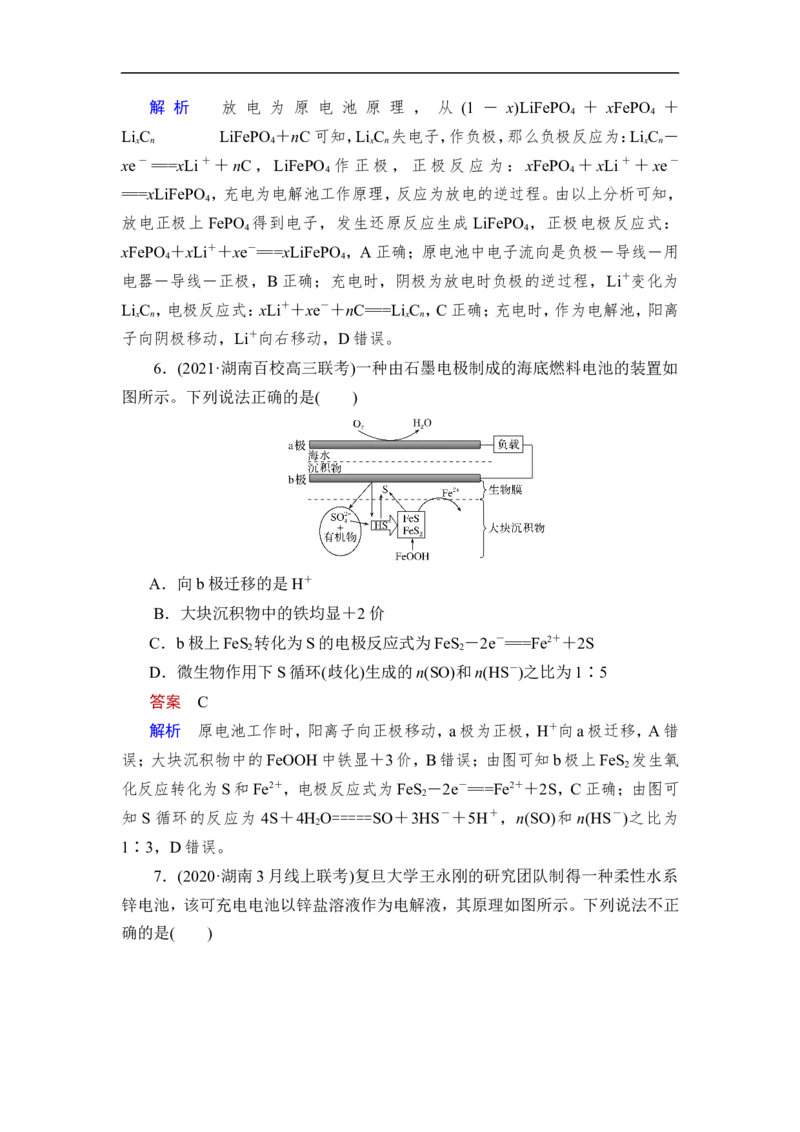
6.(2021·湖南百校高三联考)一种由石墨电极制成的海底燃料电池的装置如
图所示。下列说法正确的是( )
A.向b极迁移的是H+
B.大块沉积物中的铁均显+2价
C.b极上FeS 转化为S的电极反应式为FeS -2e-===Fe2++2S
2 2
D.微生物作用下S循环(歧化)生成的n(SO)和n(HS-)之比为1∶5
答案 C
解析 原电池工作时,阳离子向正极移动,a极为正极,H+向a极迁移,A错
误;大块沉积物中的FeOOH中铁显+3价,B错误;由图可知b极上FeS 发生氧
2
化反应转化为S和Fe2+,电极反应式为FeS -2e-===Fe2++2S,C正确;由图可
2
知 S 循环的反应为 4S+4H O=====SO+3HS-+5H+,n(SO)和 n(HS-)之比为
2
1∶3,D错误。
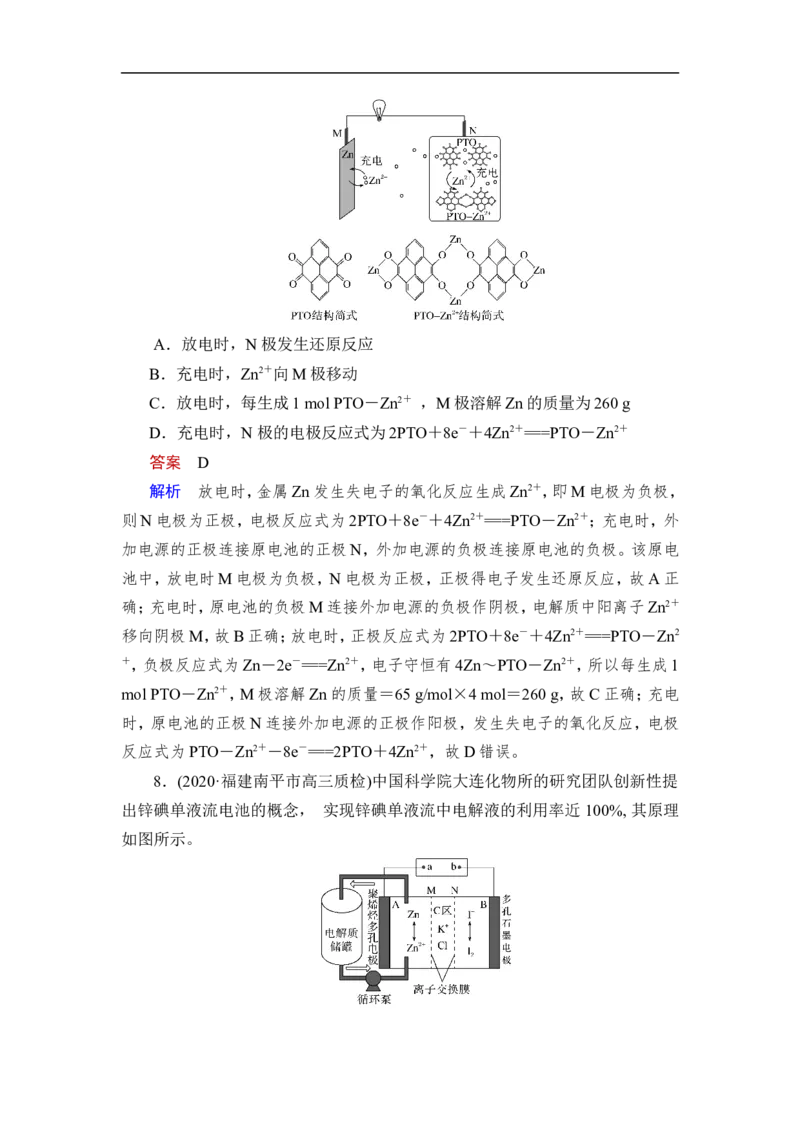
7.(2020·湖南3月线上联考)复旦大学王永刚的研究团队制得一种柔性水系
锌电池,该可充电电池以锌盐溶液作为电解液,其原理如图所示。下列说法不正
确的是( )A.放电时,N极发生还原反应
B.充电时,Zn2+向M极移动
C.放电时,每生成1 mol PTO-Zn2+ ,M极溶解Zn的质量为260 g
D.充电时,N极的电极反应式为2PTO+8e-+4Zn2+===PTO-Zn2+
答案 D
解析 放电时,金属Zn发生失电子的氧化反应生成Zn2+,即M电极为负极,
则N电极为正极,电极反应式为2PTO+8e-+4Zn2+===PTO-Zn2+;充电时,外
加电源的正极连接原电池的正极N,外加电源的负极连接原电池的负极。该原电
池中,放电时M电极为负极,N电极为正极,正极得电子发生还原反应,故A正
确;充电时,原电池的负极M连接外加电源的负极作阴极,电解质中阳离子Zn2+
移向阴极M,故B正确;放电时,正极反应式为2PTO+8e-+4Zn2+===PTO-Zn2
+,负极反应式为Zn-2e-===Zn2+,电子守恒有4Zn~PTO-Zn2+,所以每生成1
mol PTO-Zn2+,M极溶解Zn的质量=65 g/mol×4 mol=260 g,故C正确;充电
时,原电池的正极N连接外加电源的正极作阳极,发生失电子的氧化反应,电极
反应式为PTO-Zn2+-8e-===2PTO+4Zn2+,故D错误。
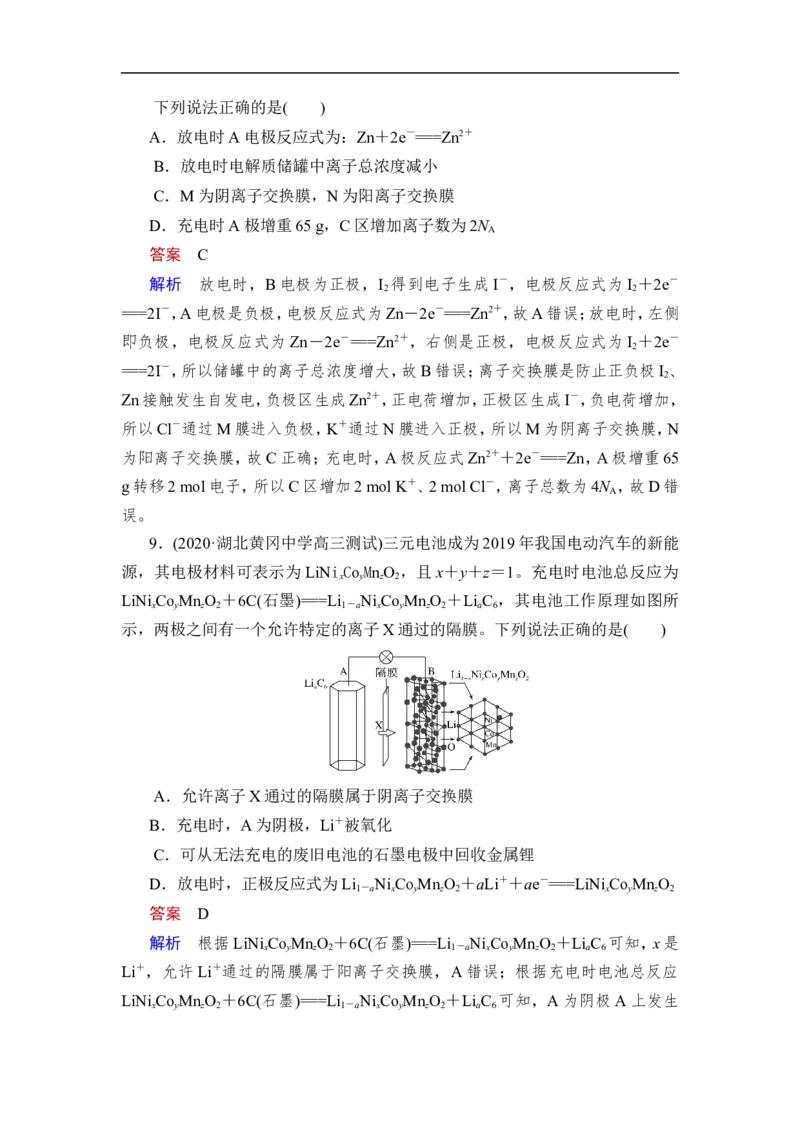
8.(2020·福建南平市高三质检)中国科学院大连化物所的研究团队创新性提
出锌碘单液流电池的概念, 实现锌碘单液流中电解液的利用率近 100%, 其原理
如图所示。下列说法正确的是( )
A.放电时A电极反应式为:Zn+2e-===Zn2+
B.放电时电解质储罐中离子总浓度减小
C.M为阴离子交换膜,N为阳离子交换膜
D.充电时A极增重65 g,C区增加离子数为2N
A
答案 C
解析 放电时,B电极为正极,I 得到电子生成I-,电极反应式为 I +2e-
2 2
===2I-,A电极是负极,电极反应式为Zn-2e-===Zn2+,故A错误;放电时,左侧
即负极,电极反应式为Zn-2e-===Zn2+,右侧是正极,电极反应式为 I +2e-
2
===2I-,所以储罐中的离子总浓度增大,故B错误;离子交换膜是防止正负极I 、
2
Zn接触发生自发电,负极区生成Zn2+,正电荷增加,正极区生成I-,负电荷增加,
所以Cl-通过M膜进入负极,K+通过N膜进入正极,所以M为阴离子交换膜,N
为阳离子交换膜,故C正确;充电时,A极反应式Zn2++2e-===Zn,A极增重65
g转移2 mol电子,所以C区增加2 mol K+、2 mol Cl-,离子总数为4N ,故D错
A
误。
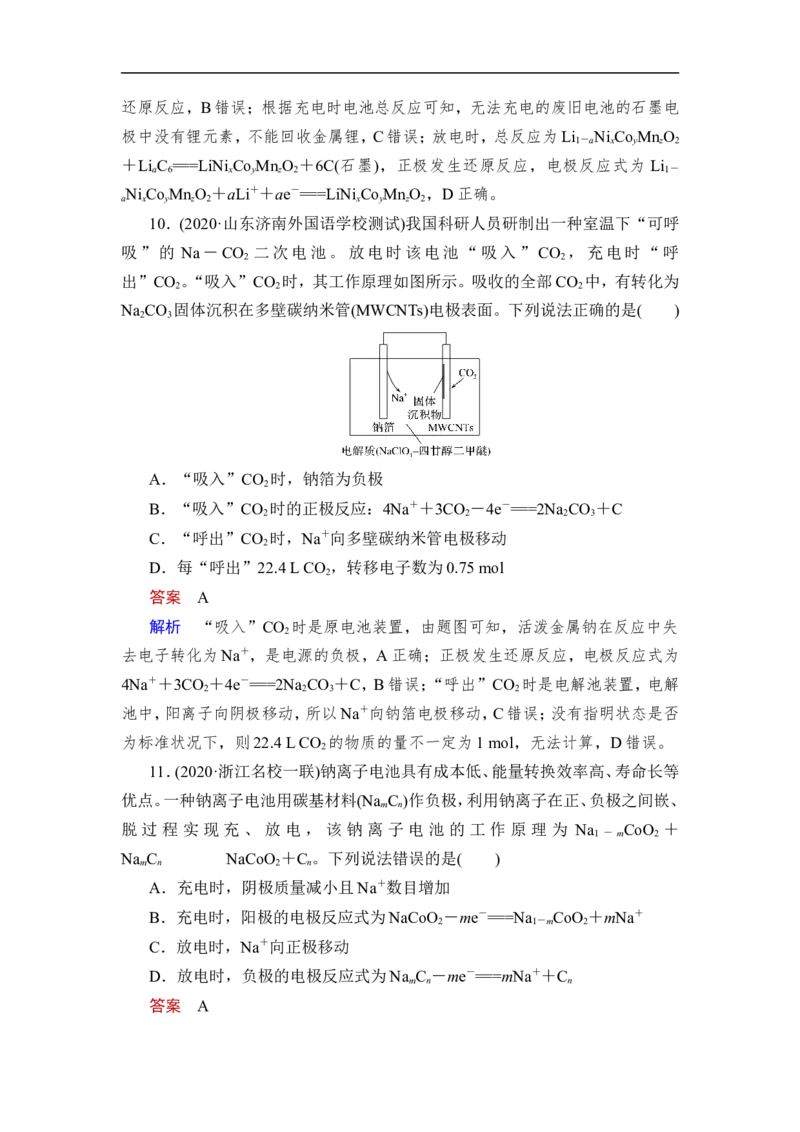
9.(2020·湖北黄冈中学高三测试)三元电池成为2019年我国电动汽车的新能
源,其电极材料可表示为 LiNi Co MnO ,且x+y+z=1。充电时电池总反应为
x y z 2
LiNi Co MnO +6C(石墨)===Li Ni Co MnO +Li C ,其电池工作原理如图所
x y z 2 1-a x y z 2 a 6
示,两极之间有一个允许特定的离子X通过的隔膜。下列说法正确的是( )
A.允许离子X通过的隔膜属于阴离子交换膜
B.充电时,A为阴极,Li+被氧化
C.可从无法充电的废旧电池的石墨电极中回收金属锂
D.放电时,正极反应式为Li Ni Co MnO +aLi++ae-===LiNi Co MnO
1-a x y z 2 x y z 2
答案 D
解析 根据LiNi Co MnO +6C(石墨)===Li Ni Co MnO +Li C 可知,x是
x y z 2 1-a x y z 2 a 6
Li+,允许Li+通过的隔膜属于阳离子交换膜,A错误;根据充电时电池总反应
LiNi Co MnO +6C(石墨)===Li Ni Co MnO +Li C 可知,A为阴极A上发生
x y z 2 1-a x y z 2 a 6还原反应,B错误;根据充电时电池总反应可知,无法充电的废旧电池的石墨电
极中没有锂元素,不能回收金属锂,C错误;放电时,总反应为Li Ni Co MnO
1-a x y z 2
+Li C ===LiNi Co MnO +6C(石墨),正极发生还原反应,电极反应式为 Li
a 6 x y z 2 1-
Ni Co MnO +aLi++ae-===LiNi Co MnO ,D正确。
a x y z 2 x y z 2
10.(2020·山东济南外国语学校测试)我国科研人员研制出一种室温下“可呼
吸”的 Na-CO 二次电池。放电时该电池“吸入”CO ,充电时“呼
2 2
出”CO 。“吸入”CO 时,其工作原理如图所示。吸收的全部CO 中,有转化为
2 2 2
Na CO 固体沉积在多壁碳纳米管(MWCNTs)电极表面。下列说法正确的是( )
2 3
A.“吸入”CO 时,钠箔为负极
2
B.“吸入”CO 时的正极反应:4Na++3CO -4e-===2Na CO +C
2 2 2 3
C.“呼出”CO 时,Na+向多壁碳纳米管电极移动
2
D.每“呼出”22.4 L CO ,转移电子数为0.75 mol
2
答案 A
解析 “吸入”CO 时是原电池装置,由题图可知,活泼金属钠在反应中失
2
去电子转化为Na+,是电源的负极,A正确;正极发生还原反应,电极反应式为
4Na++3CO +4e-===2Na CO +C,B错误;“呼出”CO 时是电解池装置,电解
2 2 3 2
池中,阳离子向阴极移动,所以Na+向钠箔电极移动,C错误;没有指明状态是否
为标准状况下,则22.4 L CO 的物质的量不一定为1 mol,无法计算,D错误。
2
11.(2020·浙江名校一联)钠离子电池具有成本低、能量转换效率高、寿命长等
优点。一种钠离子电池用碳基材料(Na C )作负极,利用钠离子在正、负极之间嵌、
m n
脱 过 程 实 现 充 、 放 电 , 该 钠 离 子 电 池 的 工 作 原 理 为 Na CoO +
1 - m 2
Na C NaCoO +C 。下列说法错误的是( )
m n 2 n
A.充电时,阴极质量减小且Na+数目增加
B.充电时,阳极的电极反应式为NaCoO -me-===Na CoO +mNa+
2 1-m 2
C.放电时,Na+向正极移动
D.放电时,负极的电极反应式为Na C -me-===mNa++C
m n n
答案 A解析 充电时,阴极上发生还原反应,电极反应式为 mNa++C +me-
n
===Na C ,阴极质量增大,A项错误;充电时,阳极上发生氧化反应,电极反应式
m n
为NaCoO -me-===Na CoO +mNa+,B项正确;放电时,阳离子向正极移动,
2 1-m 2
C项正确;放电时,负极发生氧化反应,电极反应式为 Na C -me-===mNa++
m n
C ,D项正确。
n