文档内容
热点强化练 4 工艺流程中的热点金属
1.(2020·湖北武汉市高三模拟)三氯化钌是一种重要的贵金属化合物,广泛
应用于氯碱工业中金属阳极钌涂层及加氢催化剂。
Ⅰ.三氯化钌的制备
将金属钌粉与氯化钠混合后,加入微量还原性淀粉,将温度升高到 800~1
000 ℃,再往熔融的熔体中通入氯气,大部分钌粉转化为氯钌酸钠(Na RuCl ),再
2 6
经过一系列化学工艺制备出三氯化钌。
(1)生成氯钌酸钠的化学方程式为____________________________________
___________________________________________________________________。
(2)升温阶段加入还原性淀粉的作用是________________________________
___________________________________________________________________。
Ⅱ.三氯化钌的回收
从废弃催化剂回收三氯化钌的一种工艺流程如下图所示:
回答下列问题:
(3)“氧化”时加H SO 的目的_______________________________________
2 4
___________________________________________________________________。
(4)“吸收”过程中加入乙醇的作用是________________________________
___________________________________________________________________。
(5)可用氢还原重量法测定产品的纯度,其原理为 2RuCl +3H ===2Ru+
3 2
6HCl。某同学对产品纯度进行测定,所得数据记录如下:
实验序号 产品质量/g 固体Ru质量/g
① 1.250 0 0.490 0
② 1.250 0 0.510 0
③ 1.250 0 0.500 0
则产品的纯度为________(用百分数表示,保留两位有效数字)。
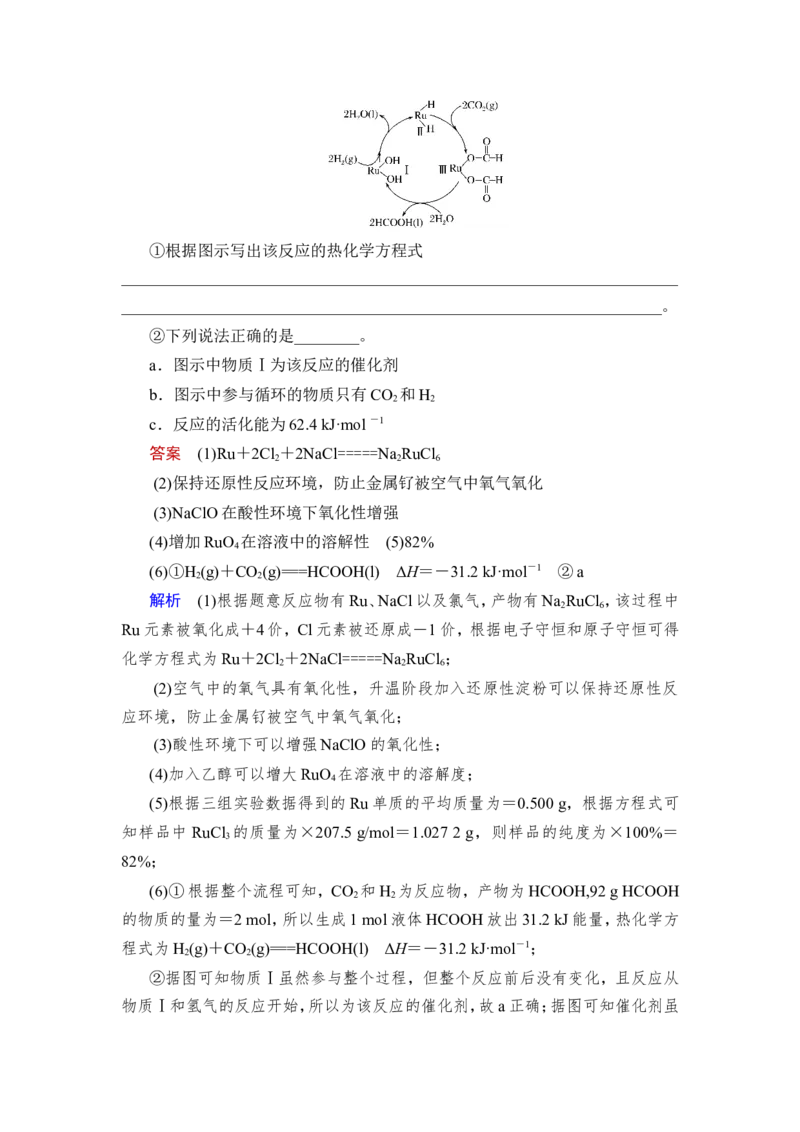
(6)钌及其化合物在合成工业上有广泛用途,下图是用钌(Ru)基催化剂催化合
成甲酸的过程。每生成92 g液态HCOOH放出62.4 kJ的热量。①根据图示写出该反应的热化学方程式
_____________________________________________________________________
___________________________________________________________________。
②下列说法正确的是________。
a.图示中物质Ⅰ为该反应的催化剂
b.图示中参与循环的物质只有CO 和H
2 2
c.反应的活化能为62.4 kJ·mol -1
答案 (1)Ru+2Cl +2NaCl=====Na RuCl
2 2 6
(2)保持还原性反应环境,防止金属钌被空气中氧气氧化
(3)NaClO在酸性环境下氧化性增强
(4)增加RuO 在溶液中的溶解性 (5)82%
4
(6)①H (g)+CO (g)===HCOOH(l) ΔH=-31.2 kJ·mol-1 ②a
2 2
解析 (1)根据题意反应物有Ru、NaCl以及氯气,产物有Na RuCl ,该过程中
2 6
Ru元素被氧化成+4价,Cl元素被还原成-1价,根据电子守恒和原子守恒可得
化学方程式为Ru+2Cl +2NaCl=====Na RuCl ;
2 2 6
(2)空气中的氧气具有氧化性,升温阶段加入还原性淀粉可以保持还原性反
应环境,防止金属钌被空气中氧气氧化;
(3)酸性环境下可以增强NaClO的氧化性;
(4)加入乙醇可以增大RuO 在溶液中的溶解度;
4
(5)根据三组实验数据得到的Ru单质的平均质量为=0.500 g,根据方程式可
知样品中 RuCl 的质量为×207.5 g/mol=1.027 2 g,则样品的纯度为×100%=
3
82%;
(6)①根据整个流程可知,CO 和H 为反应物,产物为HCOOH,92 g HCOOH
2 2
的物质的量为=2 mol,所以生成1 mol液体HCOOH放出31.2 kJ能量,热化学方
程式为H (g)+CO (g)===HCOOH(l) ΔH=-31.2 kJ·mol-1;
2 2
②据图可知物质Ⅰ虽然参与整个过程,但整个反应前后没有变化,且反应从
物质Ⅰ和氢气的反应开始,所以为该反应的催化剂,故a正确;据图可知催化剂虽然整个过程前后质量和化学性质没有变化,但也参与了整个循环,故b错误;每
生成2 mol HCOOH放出62.4 kJ的能量,据此可知反应物和生成物的能量之差,
不能确定反应的活化能,故c错误;综上所述选a。
2.(2020·湖北黄冈高三测试)氧化铬绿(Cr O )的性质独特,在冶金、颜料等领
2 3
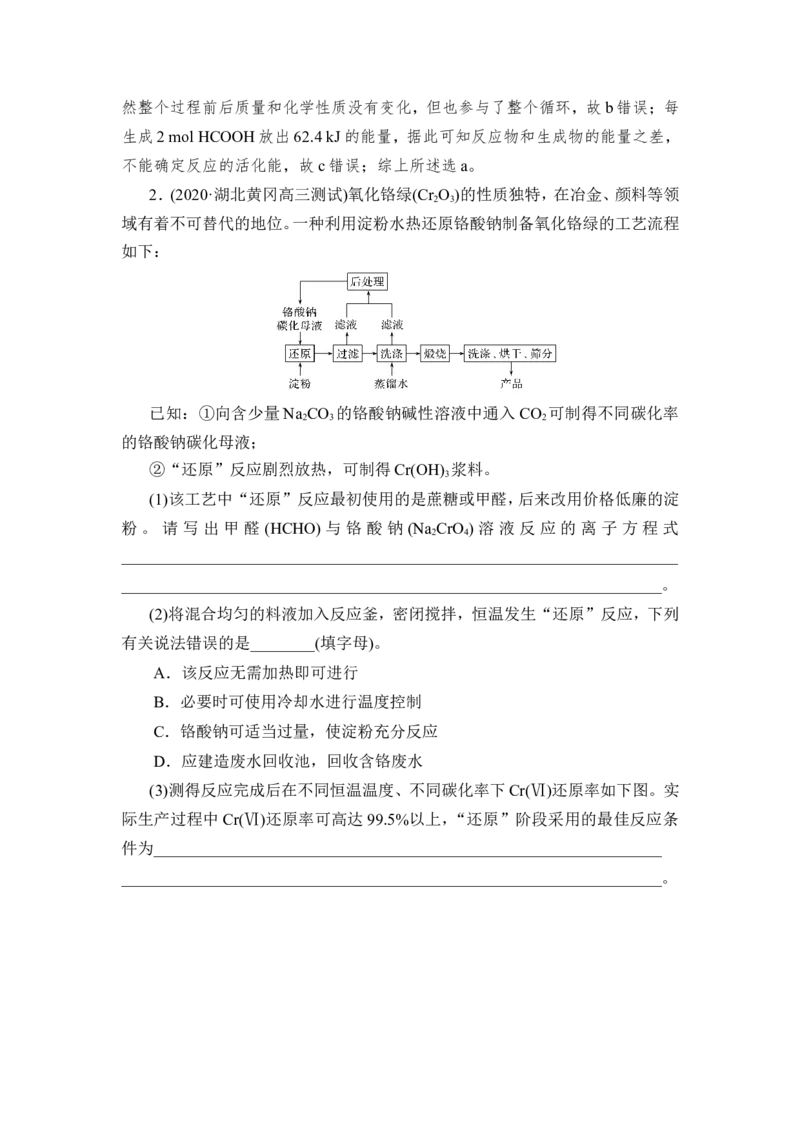
域有着不可替代的地位。一种利用淀粉水热还原铬酸钠制备氧化铬绿的工艺流程
如下:
已知:①向含少量Na CO 的铬酸钠碱性溶液中通入 CO 可制得不同碳化率
2 3 2
的铬酸钠碳化母液;
②“还原”反应剧烈放热,可制得Cr(OH) 浆料。
3
(1)该工艺中“还原”反应最初使用的是蔗糖或甲醛,后来改用价格低廉的淀
粉 。 请 写 出 甲 醛 (HCHO) 与 铬 酸 钠 (Na CrO ) 溶 液 反 应 的 离 子 方 程 式
2 4
_____________________________________________________________________
___________________________________________________________________。
(2)将混合均匀的料液加入反应釜,密闭搅拌,恒温发生“还原”反应,下列
有关说法错误的是________(填字母)。
A.该反应无需加热即可进行
B.必要时可使用冷却水进行温度控制
C.铬酸钠可适当过量,使淀粉充分反应
D.应建造废水回收池,回收含铬废水
(3)测得反应完成后在不同恒温温度、不同碳化率下Cr(Ⅵ)还原率如下图。实
际生产过程中Cr(Ⅵ)还原率可高达99.5%以上,“还原”阶段采用的最佳反应条
件为_______________________________________________________________
___________________________________________________________________。(4)滤液中所含溶质为____________________________________________。
该水热法制备氧化铬绿工艺的优点有______________________________
_____________________________________、_______________________________
_______________________(请写出两条)。
(5)由水热法制备的氢氧化铬为无定型氢氧化铬[Cr(OH) ·nH O]。将洗涤并干
3 2
燥后的氢氧化铬滤饼充分煅烧,质量损失与固体残留质量比为9∶19,经计算得
出n=________。
(6)重铬酸钠(Na Cr O ·H O)与硫酸铵热分解法也是一种生产氧化铬绿的方法
2 2 7 2
生 产 过 程 中 产 生 的 气 体 对 环 境 无 害 , 其 反 应 的 化 学 方 程 式 为
_____________________________________________________________________
___________________________________________________________________。
答案 (1)4CrO+3HCHO+4H O===4Cr(OH) ↓+2OH-+3CO
2 3
(2)AC (3)碳化率40%、恒温240 ℃
(4)Na CO (或NaHCO 或Na CO 、NaHCO ) 工艺清洁、原料价格低廉、设备
2 3 3 2 3 3
要求低、副产物碳酸盐可用于铬酸钠碳化母液的制备 无废气废渣排放、废水可
回收利用、流程短等 (5)0.5
(6)Na Cr O ·H O+(NH ) SO =====Cr O +Na SO +5H O+N ↑
2 2 7 2 4 2 4 2 3 2 4 2 2
解析 (1)HCHO中碳元素化合价为0价,该反应在碱性环境下进行,最终生
成为有碳酸钠、Cr(OH) 等,根据化合价升降守恒、电荷守恒以及原子守恒可知其
3
反应的离子方程式为:4CrO+3HCHO+4H O===4Cr(OH) ↓+2OH-+3CO;(2)
2 3
该反应虽然为放热反应,但不一定全过程都不需要加热,如燃烧反应为放热反应
反应开始需要加热,故A说法错误;因该反应放热剧烈,若温度过高,Cr(OH) 可
3
能会发生分解,会影响最终产品质量,因此可在必要时可使用冷却水进行温度控
制,故B说法正确;为保证原料的充分利用,淀粉应适当过量,使铬酸钠充分反应,
故C说法错误;铬为重金属元素,直接排放至环境中会污染水资源,因此应建造
废水回收池,回收含铬废水,故D说法正确;(3)由图可知,在碳化率为40%时,还
原率较高,在温度为240 ℃时,还原率达到接近100%,再升高温度对于还原率的影响不大,故最佳反应条件为:碳化率40%、恒温240 ℃;(4)HCHO的氧化产物为
+4价碳的化合物,因在碱性条件下,则溶质为:Na CO (或NaHCO 或Na CO 、
2 3 3 2 3
NaHCO );水热法制备工艺的优点有:工艺清洁、原料价格低廉、设备要求低、副
3
产物碳酸盐可用于铬酸钠碳化母液的制备、无废气废渣排放、废水可回收利用、
流程短等;(5)加热过程中相关物质的转化关系式为:
2Cr(OH) ·nH O~Cr O ~(3+2n)H O
3 2 2 3 2
152 18×(3+2n)
19 9
=,解得n=0.5;
(6)重铬酸钠具有强氧化性,硫酸铵具有还原性,生产过程中产生的气体对环
境无害,故N元素转化为N ,二者发生氧化还原反应生成Cr O 、N 、Na SO 、
2 2 3 2 2 4
H O,根据氧化还原反应得失电子守恒和原子守恒可知该反应方程式为:
2
Na Cr O ·H O+(NH ) SO =====Cr O +Na SO +5H O+N ↑。
2 2 7 2 4 2 4 2 3 2 4 2 2
3.(2020·河北保定市高三二模)金属铋在自然界中的量极少,用途非常广泛,
通常以辉铋矿为原料提取金属铋,工艺流程如图所示:
已知:①辉铋矿主要成分是Bi S ,还含少量Bi O 、SiO 、铁的氧化物和硫化
2 3 2 3 2
物等。
②Bi O 能溶于酸,NaBiO 不溶于水。
2 3 3
③常温下,K [Fe(OH) ]=4×10-38,K [Bi(OH) ]=4×10-30;K [Fe(OH) ]=
sp 3 sp 3 sp 2
8.0×10-16;
回答下列问题:
(1)写出酸浸氧化时Bi S 被氧化成硫单质的化学方程式
2 3
_______________________________________________________________。
(2)滤渣1的成分为________。
(3)除杂剂的作用a.调节溶液pH,b________,写出一种能提高产物产量的除
杂剂________。
(4)滤液2还可用来制备NaBiO ,可向滤液2中加入NaOH和NaClO溶液制
3
取NaBiO ,写出该反应的离子方程式
3___________________________________________________________________。
答案 (1)Bi S +6HCl+NaClO ===2BiCl +NaCl+3S↓+3H O
2 3 3 3 2
(2)S和SiO (3)除去杂质Fe3+ Bi O 或Bi(OH)
2 2 3 3
(4)Na++Bi3++ClO-+4OH-===NaBiO ↓+Cl-+2H O
3 2
解析 辉铋矿酸浸氧化后过滤,得到滤渣 1为不溶于酸的二氧化硅和Bi S
2 3
被氧化后生成的硫单质,滤液1中含有BiCl 、NaCl,FeCl 等,为了避免引入新杂
3 3
质,则加入的除杂试剂可以是Bi O 或Bi(OH) ,目的是调节pH使铁离子转化成
2 3 3
氢氧化铁除去,滤液2中的主要成分为氯化钠和BiCl ,经电解得到铋单质。
3
(1)酸浸氧化时 Bi S 被氧化成硫单质的化学方程式为 Bi S +6HCl+
2 3 2 3
NaClO ===2BiCl +NaCl+3S↓+3H O;(2)滤渣1的成分为S和SiO ;(3)可用
3 3 2 2
Bi O 或Bi(OH) 调节pH使铁离子转化成氢氧化铁沉淀除去;(4)滤液2中的主要
2 3 3
成分为氯化钠和BiCl ,加入NaOH和NaClO溶液制取NaBiO 时发生反应的离
3 3
子方程式为Na++Bi3++ClO-+4OH-===NaBiO ↓+Cl-+2H O。
3 2
4.(2021·1月重庆市学业水平选择考适应性测试,15)碳酸锶(SrCO )是一种重要的
3
工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90% SrCO ,
3
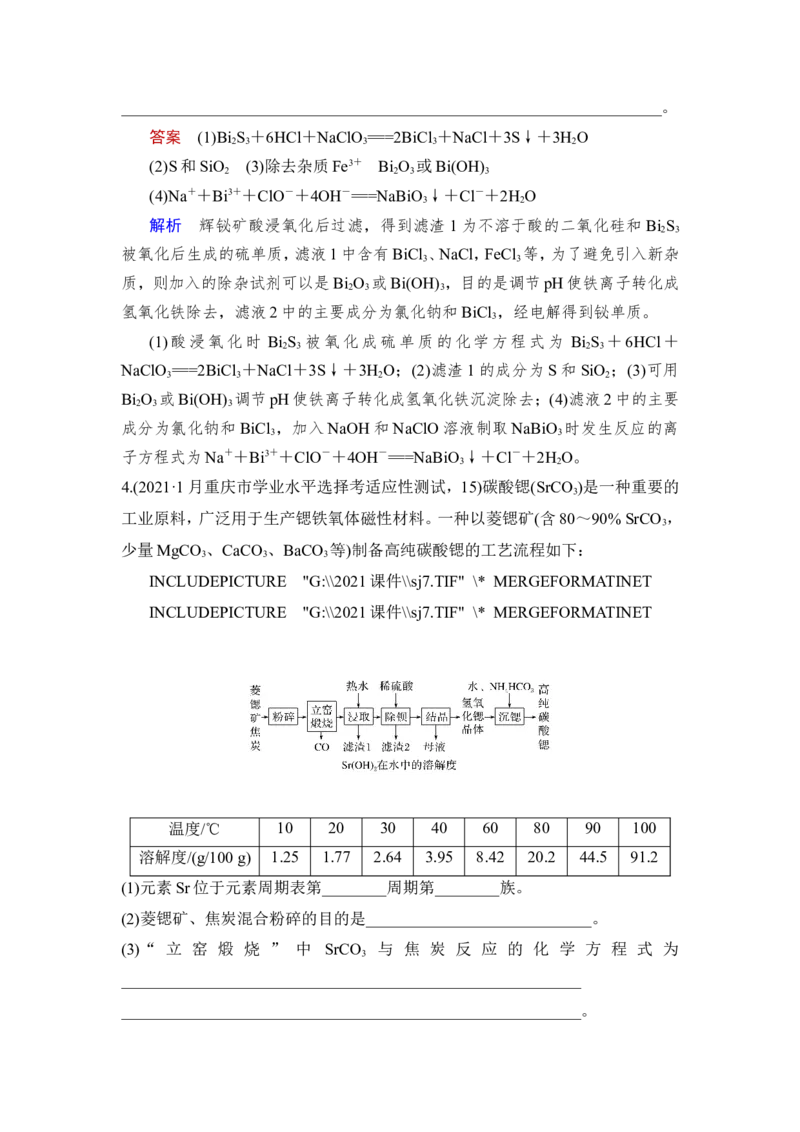
少量MgCO 、CaCO 、BaCO 等)制备高纯碳酸锶的工艺流程如下:
3 3 3
INCLUDEPICTURE "G:\\2021课件\\sj7.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\sj7.TIF" \* MERGEFORMATINET
温度/℃ 10 20 30 40 60 80 90 100
溶解度/(g/100 g) 1.25 1.77 2.64 3.95 8.42 20.2 44.5 91.2
(1)元素Sr位于元素周期表第________周期第________族。
(2)菱锶矿、焦炭混合粉碎的目的是____________________________。
(3)“ 立 窑 煅 烧 ” 中 SrCO 与 焦 炭 反 应 的 化 学 方 程 式 为
3
_________________________________________________________
_________________________________________________________。进行煅烧反应的立窑衬里应选择________(填“石英砂砖”或“碱性耐火砖”)。
(4)“浸取”中用热水浸取而不用冷水的原因是______________________
____________________________________________________________;
滤渣1含有焦炭、Ca(OH) 和________。
2
(5)“沉锶”中反应的化学方程式为____________________________
__________________________________________________________。
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体
(xSrO·yFe O )中Sr与Fe的质量比为0.13,则为________(取整数)。
2 3
答案 (1)五 ⅡA (2)增大反应物接触面积,加快反应速率,提高原料利用率
(3)SrCO +C=====SrO+2CO↑ 碱性耐火砖
3
(4)Sr(OH) 的溶解度随温度升高而增大,提高SrO的浸出率 MgO
2
(5)Sr(OH) +NH HCO ===SrCO ↓+NH ·H O+H O
2 4 3 3 3 2 2
(6) 6
解析 (1)Sr位于周期表第五周期第ⅡA族。(2)粉碎是为了增大反应物的接
触面积,加快反应速率,提高原料利用率。(3)SrCO 与C反应,相当于SrCO 分解
3 3
生成SrO和CO ,C与CO 反应,有利于SrCO 的分解。煅烧应选择碱性耐火砖,
2 2 3
因为石英砂砖中含有SiO ,在高温下能与SrO反应生成SrSiO 。(4)煅烧后得到
2 3
MgO、CaO、SrO、BaO,用热水溶解,由Sr(OH) 溶解度可知,热水浸取有利于
2
Sr(OH) 的溶解,提高浸出率,同时减小了Ca(OH) 的溶解度,所以滤渣1中有
2 2
Ca(OH) ,MgO不溶于水,滤渣1中还有MgO。(5)Sr(OH) 和NH HCO 反应生成
2 2 4 3
SrCO ,相当于 HCO 与 OH-反应,Sr(OH) 中另一个 OH-正好与 NH 反应。
3 2
(6)n(Fe O )∶n(SrO) =∶≈6。
2 3
5.(2020·河南等省五岳4月联考)金属钛在航天、潜海和医疗方面应用广泛。
以钛铁矿[主要成分为钛酸亚铁(FeTiO ),含少量Fe O ]为原料制备钛的工艺流程
3 2 3
如图所示。
(1)步骤②、③、④中,均需进行的操作是________(填操作名称)。
(2)滤液1中钛元素以TiO2+形式存在,步骤①中生成TiO2+的化学方程式为_____________________________________________________________________
___________________________________________________________________,
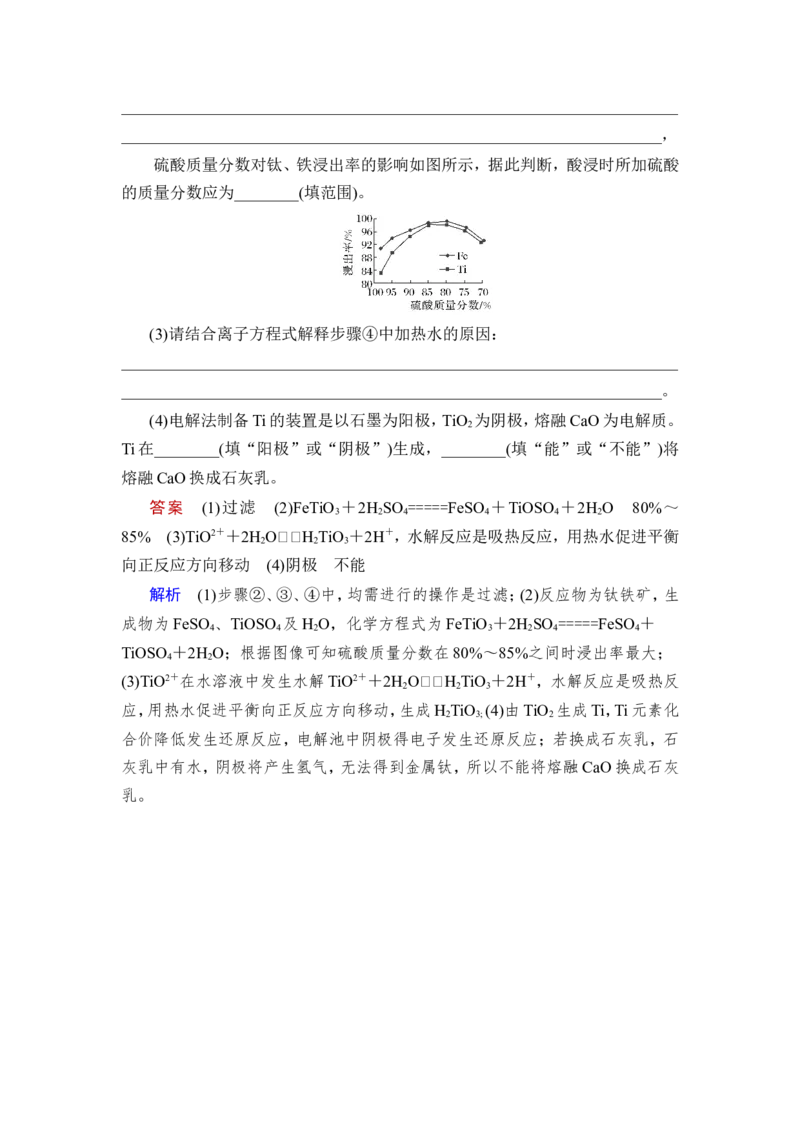
硫酸质量分数对钛、铁浸出率的影响如图所示,据此判断,酸浸时所加硫酸
的质量分数应为________(填范围)。
(3)请结合离子方程式解释步骤④中加热水的原因:
_____________________________________________________________________
___________________________________________________________________。
(4)电解法制备Ti的装置是以石墨为阳极,TiO 为阴极,熔融CaO为电解质。
2
Ti在________(填“阳极”或“阴极”)生成,________(填“能”或“不能”)将
熔融CaO换成石灰乳。
答案 (1)过滤 (2)FeTiO +2H SO =====FeSO +TiOSO +2H O 80%~
3 2 4 4 4 2
85% (3)TiO2++2H OH TiO +2H+,水解反应是吸热反应,用热水促进平衡
2 2 3
向正反应方向移动 (4)阴极 不能
解析 (1)步骤②、③、④中,均需进行的操作是过滤;(2)反应物为钛铁矿,生
成物为FeSO 、TiOSO 及H O,化学方程式为FeTiO +2H SO =====FeSO +
4 4 2 3 2 4 4
TiOSO +2H O;根据图像可知硫酸质量分数在80%~85%之间时浸出率最大;
4 2
(3)TiO2+在水溶液中发生水解TiO2++2H OH TiO +2H+,水解反应是吸热反
2 2 3
应,用热水促进平衡向正反应方向移动,生成H TiO (4)由TiO 生成Ti,Ti元素化
2 3; 2
合价降低发生还原反应,电解池中阴极得电子发生还原反应;若换成石灰乳,石
灰乳中有水,阴极将产生氢气,无法得到金属钛,所以不能将熔融CaO换成石灰
乳。