文档内容
第二章 化学物质及其变化
第05讲 离子共存 离子的检验和推断(精练)
完卷时间:50分钟
可能用到的相对原子质量:O16 S32 Ba 137
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·广东肇庆市·高三三模)下列有关离子共存的叙述或离子方程式的书写正确的是
A.常温pH=7的溶液中,K+、 、Fe3+可以大量共存
B.通入HS至饱和的溶液中,Cl-、 、Cu2+可以大量共存
2
C.泡沫灭火器是利用水解原理:
D.Zn溶于过量的浓硝酸中:
2.(2021·广东珠海市·高三一模)在酸性溶液中能大量共存且为无色透明溶液的是
A.
B.
C.
D.
3.(2020·四川成都市·成都七中高三一模)下列有关NaClO和NaCl混合溶液的叙述正确的是
A.该溶液中,Ag+、K+、NO 、CHOH(CHOH)CHO可以大量共存
3 4
B.向该溶液中滴入少量FeSO 溶液,反应的离子方程式2Fe2++ClO-+2H+=Cl-+2Fe3++HO
4 2
C.用玻璃棒蘸取该溶液滴在pH试纸上,pH试纸变蓝但不褪色
D.向该溶液中加入浓盐酸,会产生Cl
2
4.(2020·江苏南通市·启东中学高三月考)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明的溶液中:H+、Fe2+、SO2-、NO-
4 3
B.使甲基橙变红的溶液中:Ca2+、NH+、CHCOO-、Cl-
4 3
C.0.1 mol·L-1 BaCl 溶液中:K+、Na+、OH-、NO-
2 3
D.由水电离出的c(H+)=10-12 mol·L-1的溶液中:Mg2+、K+、Br-、HCO-
3
5.(2021·吉林长春市·高三三模)某工业废水仅含有表中离子中的4种(少量存在的离子不考虑):阳离子 K+ Cu2+ Fe3+
Cl-
阴离子
某同学欲探究废水的组成,进行了如下实验:
Ⅰ.取废水少许加入足量稀盐酸,有气体生成,无沉淀生成;Ⅱ.向Ⅰ中所得的溶液中加入BaCl 溶液,有
2
白色沉淀生成。
下列推断错误的是
A.该废水为无色溶液 B.II中沉淀一定不是BaCO
3
C.整个实验过程无氧化还原反应发生 D.溶液中一定含有Cl-
6.(2021·上海金山区·高三二模)某溶液中可能含有物质的量浓度相等的
和 。取少量溶液,加入过量的 溶液并加热,产生使
湿润的红色石蕊试纸变蓝的气体,同时生成白色沉淀。则原溶液中
A.可能有 、 B.可能有4种离子
C.可能无 D.一定有 、 、
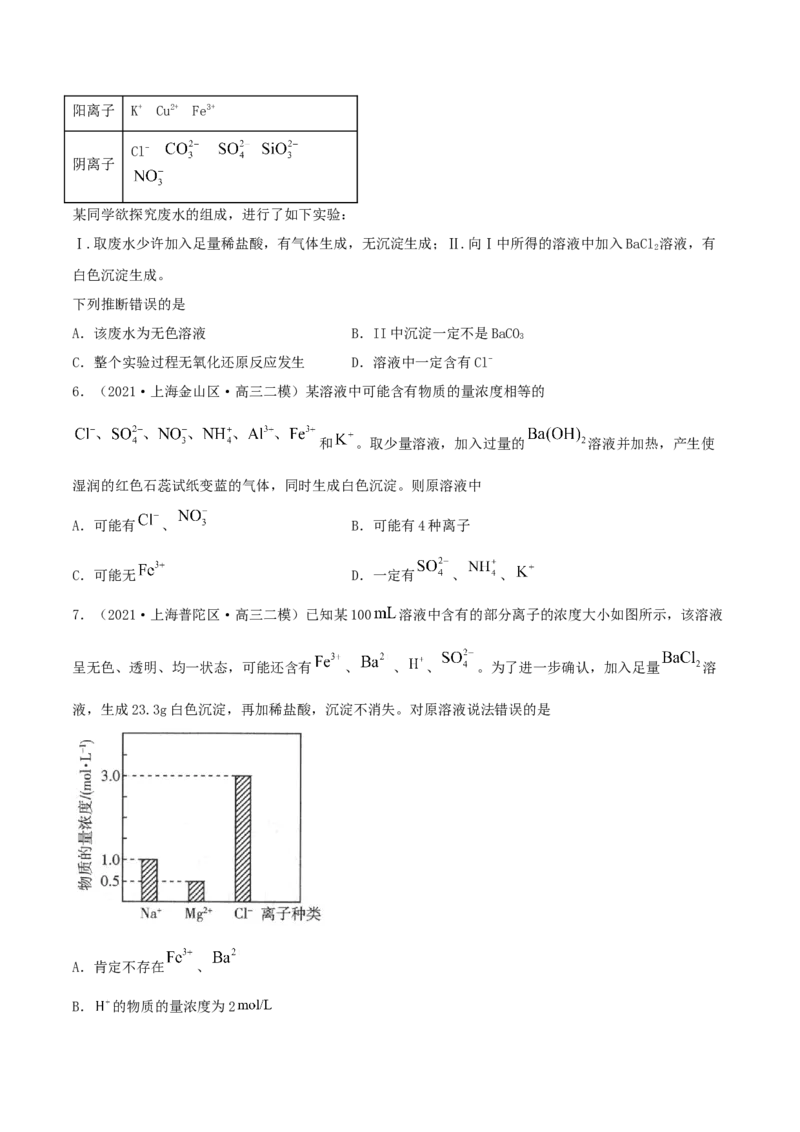
7.(2021·上海普陀区·高三二模)已知某100 溶液中含有的部分离子的浓度大小如图所示,该溶液
呈无色、透明、均一状态,可能还含有 、 、 、 。为了进一步确认,加入足量 溶
液,生成23.3g白色沉淀,再加稀盐酸,沉淀不消失。对原溶液说法错误的是
A.肯定不存在 、
B. 的物质的量浓度为2C.加入含0.2 的溶液时,沉淀质量达到最大量
D.加入少量 溶液,反应的离子方程式为
8.(2020·永济市涑北中学校高三月考)下列各组离子中,能大量共存且加入(或通入)X试剂后发生反应
的离子方程式对应正确的是
选项 离子组 试剂X 离子方程式
过量的盐
A Fe3+、Al3+、 、 +2H+═HO+SO↑
酸 2 2
过量的铜
B 透明溶液中:Fe3+、 、 、Cl- 2Fe3++Cu═2Fe2++Cu2+
粉
C Na+、Ba2+、 、Cl- NaHSO 溶液 H++ ═CO↑+HO
4 2 2
pH=1的溶液中:Mg2+、Fe2+、 、 2Fe2++HO+2H+═2Fe3+
D 双氧水 2 2
+2HO
2
A.A B.B C.C D.D
9.(2021·云南高三二模)某样品含有Al3+、NH 、Fe2+、CO 、SO 、Cl-中的几种离子,将该样品溶于
水后,取少量溶液做如图实验:
下列说法错误的是
A.该样品溶液pH<7
B.该样品不含有CO
C.该样品溶液中一定存在:3c(Al3+)+c(NH )+c(H+)+2c(Fe2+)=2c(SO )+c(Cl-)+c(OH-)
D.溶液A与过量CO 反应的离子方程式为CO+AlO +2HO=Al(OH)↓+HCO
2 2 2 3
10.(2021·浙江宁波市·高三一模)某固体混合物中可能含有:K+、 、Al3+、 Br-、 、、 等离子,某同学为了确认其成分进行了实验探究,实验及现象如下(所加试剂均足量):
下列说法正确的是
A.气体A中可能含有SO
2
B.固体混合物中一定含有Br-、 和
C.固体混合物中一定不含Al3+
D.为确定固体混合物中是否含K+,需进行焰色反应实验
11.(2020·浙江高三期中)某混合物X中可能含有FeSO、NaAlO、CuSO、NaO、(NH)SO 中的几种或
4 2 4 2 2 4 2 4
全部。将X与足量水作用,得到气体Q、固体Y和碱性溶液Z。下列结论不正确的是
A.混合物X中NaO、NaAlO 至少有一种
2 2 2
B.生成的气体Q可能含有二种成分
C.将固体Y充分灼烧,其质量一定减少
D.溶液Z一定无色,加入适量硫酸可能生成沉淀
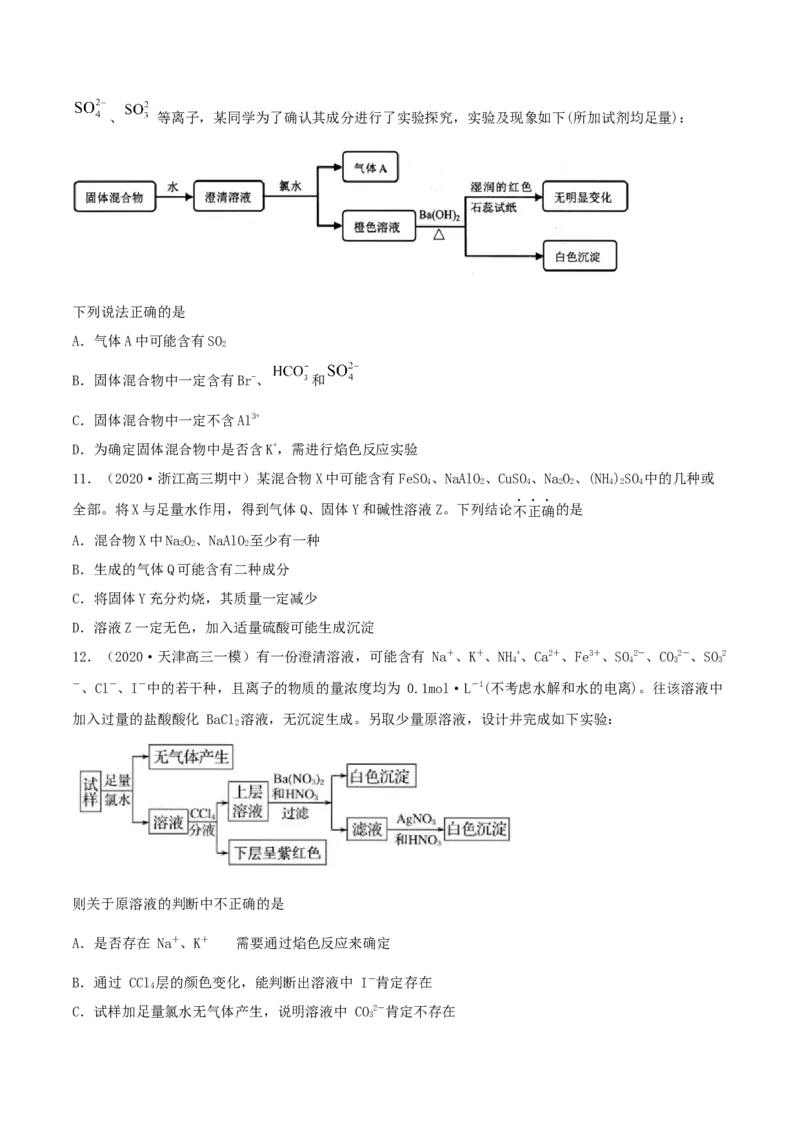
12.(2020·天津高三一模)有一份澄清溶液,可能含有 Na+、K+、NH+、Ca2+、Fe3+、SO2-、CO2-、SO2
4 4 3 3
-、Cl-、I-中的若干种,且离子的物质的量浓度均为 0.1mol·L-1(不考虑水解和水的电离)。往该溶液中
加入过量的盐酸酸化 BaCl 溶液,无沉淀生成。另取少量原溶液,设计并完成如下实验:
2
则关于原溶液的判断中不正确的是
A.是否存在 Na+、K+ 需要通过焰色反应来确定
B.通过 CCl 层的颜色变化,能判断出溶液中 I-肯定存在
4
C.试样加足量氯水无气体产生,说明溶液中 CO2-肯定不存在
3D.肯定不存在的离子是 Ca2+、Fe3+、SO2-、CO2-、Cl-
4 3
二、主观题(共2小题,共40分)
13.(2021·新疆高三模拟)(20分)现有四种溶液m,n,p、q,分别含阴阳离于 、 、 、
、 、 、 、 中的各一种,为了确定组成,进行了以下实验:将四种溶液两两混
合,发现m、n能剧烈反应,产生白色沉淀和无色气体,p、q能产生无色有刺激性气味的气体,p与m,n
均有沉淀产生,且在m中逐滴滴入p时,沉淀增多,后减少但没有完全消失。回答下列问题。
(1)p是________,q是_________(均填化学式)。
(2)写出在m中逐滴滴入p,沉淀减少时发生反应的离子方程式__________。
(3)实验室检验q中阳离子需要的试剂或试纸是___________。
(4)经分析, 存在于_________(填m、n、p、q)溶液中,实验室常用重量法检验该溶液中 离子
的浓度,步骤如下:Ⅰ用量筒取该溶液8.0mL并转移至小烧杯中;Ⅱ加入盐酸酸化,然后加入足量的
溶液(沉淀反应在接近沸腾的温度下进行);Ⅲ过滤所得沉淀;洗涤,烘干后得到ag固体。
①所用量简的规格为___________。
A.10mL B.50mL C.100mL D.500mL
②过滤时,沉淀物颗粒的大小会影响过滤速度,从利于过滤的角度分析,沉淀反应需要在接近沸腾的温度
下进行的原因可能是__________。
③检验沉淀洗涤干净的方法是___________。
④计算,硫酸根的浓度为___________mol/L(用含a的式子表示)。
14.(2021·上海青浦区·高三二模)(20分)食盐是日常生活的必需品,也是重要的化工原料。试剂级
NaCl可用海盐(含泥沙、海藻、K+、Ca2+、Mg2+、Fe3+、SO 等杂质)为原料制备。实验室提纯NaCl的流程如
图:
提供的试剂:饱和NaCO 溶液、饱和KCO 溶液、NaOH溶液、BaCl 溶液、Ba(NO) 溶液、75%乙醇、四氯化
2 3 2 3 2 3 2
碳(1)欲除去溶液I中的Ca2+、Mg2+、Fe3+、 ,在提供的试剂中,选出m所代表的试剂,按滴加顺序依次
为_______、NaOH、_______(只填化学式);洗涤除去NaCl晶体表面附带的少量KCl,在提供的试剂中,选
用的试剂为_______。
(2)操作X为用提纯的NaCl配制500mL 4.00mol/L NaCl溶液,所用的玻璃仪器除烧杯、玻璃棒外还有
_______(填仪器名称)
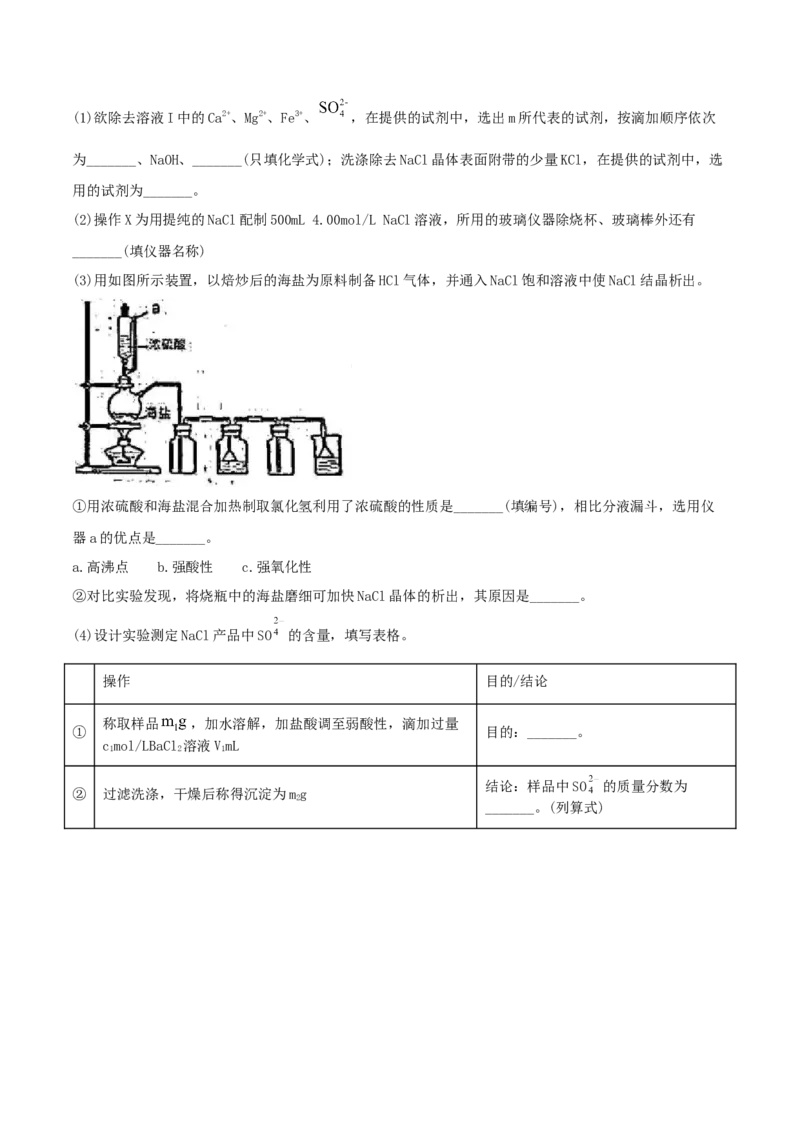
(3)用如图所示装置,以焙炒后的海盐为原料制备HCl气体,并通入NaCl饱和溶液中使NaCl结晶析出。
①用浓硫酸和海盐混合加热制取氯化氢利用了浓硫酸的性质是_______(填编号),相比分液漏斗,选用仪
器a的优点是_______。
a.高沸点 b.强酸性 c.强氧化性
②对比实验发现,将烧瓶中的海盐磨细可加快NaCl晶体的析出,其原因是_______。
(4)设计实验测定NaCl产品中SO 的含量,填写表格。
操作 目的/结论
称取样品 ,加水溶解,加盐酸调至弱酸性,滴加过量
① 目的:_______。
cmol/LBaCl 溶液VmL
1 2 1
结论:样品中SO 的质量分数为
② 过滤洗涤,干燥后称得沉淀为mg
2
_______。(列算式)