文档内容
第二章 化学物质及其变化
第05讲 离子共存 离子的检验和推断(精练)
完卷时间:50分钟
可能用到的相对原子质量:O16 S32 Ba 137
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·广东肇庆市·高三三模)下列有关离子共存的叙述或离子方程式的书写正确的是
A.常温pH=7的溶液中,K+、 、Fe3+可以大量共存
B.通入HS至饱和的溶液中,Cl-、 、Cu2+可以大量共存
2
C.泡沫灭火器是利用水解原理:
D.Zn溶于过量的浓硝酸中:
【答案】C
【解析】A.pH=7的溶液中Fe3+不会大量存在,Fe3+在pH约2.7开始沉淀,在pH为3.7时沉淀完全,A项错
误;B.HS在溶液中可以发生电离,电离出的S2-与Cu2+在溶液中生成沉淀不能共存,B项错误;C.泡沫灭
2
火器中两种溶液混合反应过程是硫酸铝与碳酸氢钠发生互促程度大的双水解,C项正确;D.浓硝酸具有氧
化性,Zn与浓硝酸反应生成NO,D项错误;故答案选C。
2
2.(2021·广东珠海市·高三一模)在酸性溶液中能大量共存且为无色透明溶液的是
A.
B.
C.
D.
【答案】B
【解析】A. 在溶液中显紫色,不符合限定条件,故A不符合题意;B. 都
大量共存,故B符合题意;C. 在酸性条件下发生氧化还原反应,故C不符合题意;D.
在酸性条件下反应生成二氧化硫和水,故D不符合题意。
综上所述,答案为B。3.(2020·四川成都市·成都七中高三一模)下列有关NaClO和NaCl混合溶液的叙述正确的是
A.该溶液中,Ag+、K+、NO 、CHOH(CHOH)CHO可以大量共存
3 4
B.向该溶液中滴入少量FeSO 溶液,反应的离子方程式2Fe2++ClO-+2H+=Cl-+2Fe3++HO
4 2
C.用玻璃棒蘸取该溶液滴在pH试纸上,pH试纸变蓝但不褪色
D.向该溶液中加入浓盐酸,会产生Cl
2
【答案】D
【解析】A.该溶液中,Ag+与Cl-反应生成沉淀,ClO-与CHOH(CHOH)CHO发生氧化还原反应,故A错误;
3 4
B.向该溶液中滴入少量FeSO 溶液,该反应是在碱性环境中,因此离子方程式中不会出现氢离子参与反应,
4
故B错误;C.NaClO具有强氧化性,最终pH试纸褪色,故C错误;D.向该溶液中加入浓盐酸,NaClO与
浓盐酸反应生成Cl,Cl-+ClO-+2H+= Cl↑+ HO,故D正确。
2 2 2
综上所述,答案为D。
4.(2020·江苏南通市·启东中学高三月考)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明的溶液中:H+、Fe2+、SO2-、NO-
4 3
B.使甲基橙变红的溶液中:Ca2+、NH+、CHCOO-、Cl-
4 3
C.0.1 mol·L-1 BaCl 溶液中:K+、Na+、OH-、NO-
2 3
D.由水电离出的c(H+)=10-12 mol·L-1的溶液中:Mg2+、K+、Br-、HCO-
3
【答案】C
【解析】A项H+、NO-与Fe2+发生氧化还原反应不能大量共存;B项溶液呈酸性,CHCOO-不能大量共存;D
3 3
项溶液呈酸性或碱性,Mg2+、HCO-等不能大量共存。
3
5.(2021·吉林长春市·高三三模)某工业废水仅含有表中离子中的4种(少量存在的离子不考虑):
阳离子 K+ Cu2+ Fe3+
Cl-
阴离子
某同学欲探究废水的组成,进行了如下实验:
Ⅰ.取废水少许加入足量稀盐酸,有气体生成,无沉淀生成;Ⅱ.向Ⅰ中所得的溶液中加入BaCl 溶液,有
2
白色沉淀生成。
下列推断错误的是
A.该废水为无色溶液 B.II中沉淀一定不是BaCO
3
C.整个实验过程无氧化还原反应发生 D.溶液中一定含有Cl-
【答案】D【解析】Ⅰ.取废水少许加入足量盐酸,有气体生成,无沉淀生成,气体为二氧化碳,则一定含 ,
阴离子一定不含 ,阳离子一定不含Cu2+、Fe3+;Ⅱ.向Ⅰ中所得的溶液中加入BaCl 溶液,有白色沉
2
淀生成,因I中盐酸足量,白色沉淀可能为硫酸钡,则原溶液中一定含 ,由上述分析可知,一定含
、 ,由电荷守恒可知,阳离子一定含K+,溶液中不含Cu2+、Fe3+、 ,不能确定含Cl-、
中的哪一种,
A.因溶液含4种离子,则含有的离子是K+、 、 以及 Cl-、 中的一种,溶液为无色溶液,
选项A正确;B.Ⅱ中产生白色沉淀为硫酸钡,离子方程式是Ba2++ =BaSO↓,选项B正确;C.整个
4
实验过程中均发生复分解反应,无氧化还原反应发生,选项C正确;D.由分析可知,可能含有Cl-、
其中一种,不能确定是否含有Cl-,D错误;答案选D。
6.(2021·上海金山区·高三二模)某溶液中可能含有物质的量浓度相等的
和 。取少量溶液,加入过量的 溶液并加热,产生使
湿润的红色石蕊试纸变蓝的气体,同时生成白色沉淀。则原溶液中
A.可能有 、 B.可能有4种离子
C.可能无 D.一定有 、 、
【答案】A
【解析】取少量溶液,加入过量的 溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体NH,故
3
原溶液中含有 ,同时生成白色沉淀说明含有 ,由于Fe(OH) 是红褐色沉淀,故原溶液中一定没
3
有Fe3+,Al3+与过量的 溶液将转化为 ,故原溶液中可能含有Al3+,由题干信息可知,各离子的物质的量浓度相等,故若只含有 、 则溶液电荷不守恒,故肯定由K+或Al3+,当有Al3+时,则
还应该由Cl-和 ,当含有K+时,则电荷恰好守恒,则肯定没有Cl-和 ,据此分析解题:
A. 由分析可知,当有Al3+时,则还应该由Cl-和 ,当含有K+时,则电荷恰好守恒,则肯定没有Cl-和
,故可能有 、 ,A符合题意;B. 当有Al3+时,则还应该由Cl-和 ,原溶液中含有 、
、Al3+、Cl-和 五种离子,当含有K+时,则电荷恰好守恒,则肯定没有Cl-和 ,原溶液中只
有3种离子,故不可能有4种离子,B不合题意;C. 由分析可知,原溶液中一定不含 ,C不合题意;
D. 有分析可知,原溶液不一定含有 ,D不合题意;故答案为:A。
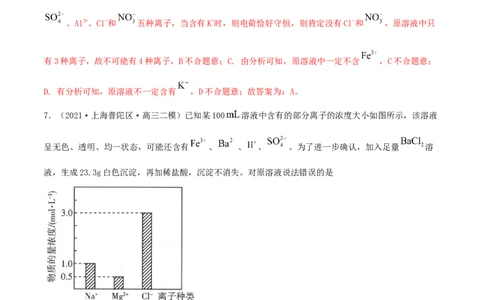
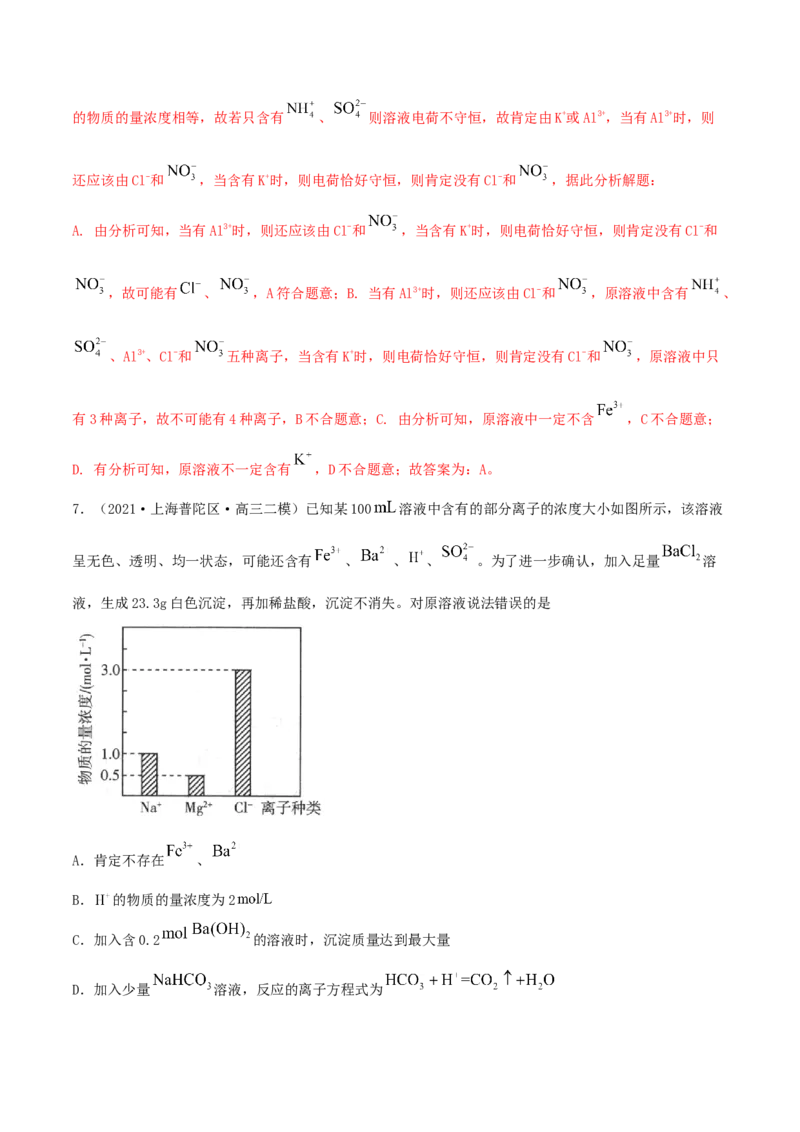
7.(2021·上海普陀区·高三二模)已知某100 溶液中含有的部分离子的浓度大小如图所示,该溶液
呈无色、透明、均一状态,可能还含有 、 、 、 。为了进一步确认,加入足量 溶
液,生成23.3g白色沉淀,再加稀盐酸,沉淀不消失。对原溶液说法错误的是
A.肯定不存在 、
B. 的物质的量浓度为2
C.加入含0.2 的溶液时,沉淀质量达到最大量
D.加入少量 溶液,反应的离子方程式为【答案】B
【解析】①该溶液呈无色、透明、均一状态,说明溶液中一定不含 ;②加入足量 溶液,生成
23.3g白色沉淀,再加稀盐酸,沉淀不消失,白色沉淀为硫酸钡,物质的量为0.1mol,原溶液中一定含有
,浓度为1mol/L,推出原溶液中一定不含 ;③已知的阳离子( 和 )所带正电荷浓度总
和为 ,阴离子(Cl-和 )所带负电荷浓度总和为
,根据溶液呈电中性,原溶液中一定含有H+,浓度为 ;
结论:原溶液中一定存在Na+、Mg2+、Cl-、H+、 ,一定不存在 、 。
A.原溶液中肯定不存在 、 ,故A正确;B.原溶液中H+的物质的量浓度为 ,故B错误;
C.原溶液中一定含有H+,浓度为 ,物质的量为0.1L×3mol∙L-1=0.3mol,镁离子的物质的量为
0.1L×0.5mol∙L-1=0.05mol,硫酸根离子物质的量为0.1mol,向100 原溶液中加入0.2 的
溶液时,钡离子过量,硫酸根全部沉淀,0.4mol氢氧根先与0.3mol氢离子反应生成水,余下0.1mol正好
将0.05mol镁离子沉淀完全,生成的成质量刚好最大,故C正确;D.溶液中含氢离子,向原溶液中加入
NaHCO 溶液,反应的离子方程式为 ,故D正确; 故选B。
3
8.(2020·永济市涑北中学校高三月考)下列各组离子中,能大量共存且加入(或通入)X试剂后发生反应
的离子方程式对应正确的是
选项 离子组 试剂X 离子方程式
过量的盐
A Fe3+、Al3+、 、 +2H+═HO+SO↑
酸 2 2
过量的铜
B 透明溶液中:Fe3+、 、 、Cl- 2Fe3++Cu═2Fe2++Cu2+
粉
C Na+、Ba2+、 、Cl- NaHSO 溶液 H++ ═CO↑+HO
4 2 2pH=1的溶液中:Mg2+、Fe2+、 、 2Fe2++HO+2H+═2Fe3+
D 双氧水 2 2
+2HO
2
A.A B.B C.C D.D
【答案】B
【解析】A.Fe3+、Al3+都与SO2-发生反应,在溶液中不能大量共存,故A错误;B.透明溶液可能是有色溶
3
液,在透明溶液中这四种离子能大量共存,加入铜粉,铜与铁离子反应,铜不能与亚铁离子反应,发生
2Fe3++Cu=2Fe2++Cu2+,故B正确;C.加入NaHSO 溶液后,Ba2+、与硫酸根离子生成硫酸钡沉淀,正确的离子
4
方程式为:H++SO2-+Ba2++HCO-=BaSO↓+CO↑+HO,故C错误;D.酸性环境下硝酸具有强的氧化性,所以
4 3 4 2 2
pH=1的溶液中,硝酸根离子与二价铁离子不共存,发生反应为3Fe2++NO-+4H+=3Fe3++NO↑+2HO,故D错误;
3 2
答案为B。
9.(2021·云南高三二模)某样品含有Al3+、NH 、Fe2+、CO 、SO 、Cl-中的几种离子,将该样品溶于
水后,取少量溶液做如图实验:
下列说法错误的是
A.该样品溶液pH<7
B.该样品不含有CO
C.该样品溶液中一定存在:3c(Al3+)+c(NH )+c(H+)+2c(Fe2+)=2c(SO )+c(Cl-)+c(OH-)
D.溶液A与过量CO 反应的离子方程式为CO+AlO +2HO=Al(OH)↓+HCO
2 2 2 3
【答案】C
【解析】某样品含有Al3+、NH 、Fe2+、CO 、SO 、Cl-中的几种离子,将该样品溶于水后,取少量溶液
加入过量的NaOH溶液、加热,得气体A为NH,溶液中含有NH ,沉淀A为Fe(OH),溶液中含有Fe2+,没有
3 3
CO ,溶液A中通入过量的CO,出现沉淀B为Al(OH),原溶液中含有Al3+,溶液B中肯定含有HCO ,原
2 3溶液中有SO 、Cl-中的一种或两种。
A. Al3+、NH 、Fe2+属于弱碱阳离子,水解后溶液呈酸性,该样品溶液pH<7,故A正确;B. 原溶液中含
有Al3+和Fe2+,不能与CO 共存,该样品不含有CO ,故B正确;C. 根据题中信息,不能确定溶液中SO
、Cl-同时存在,故C错误;D. 溶液A与过量CO 反应生成Al(OH) 和NaHCO,离子方程式为CO+AlO
2 3 3 2
+2HO=Al(OH)↓+HCO ,故D正确;故选C。
2 3
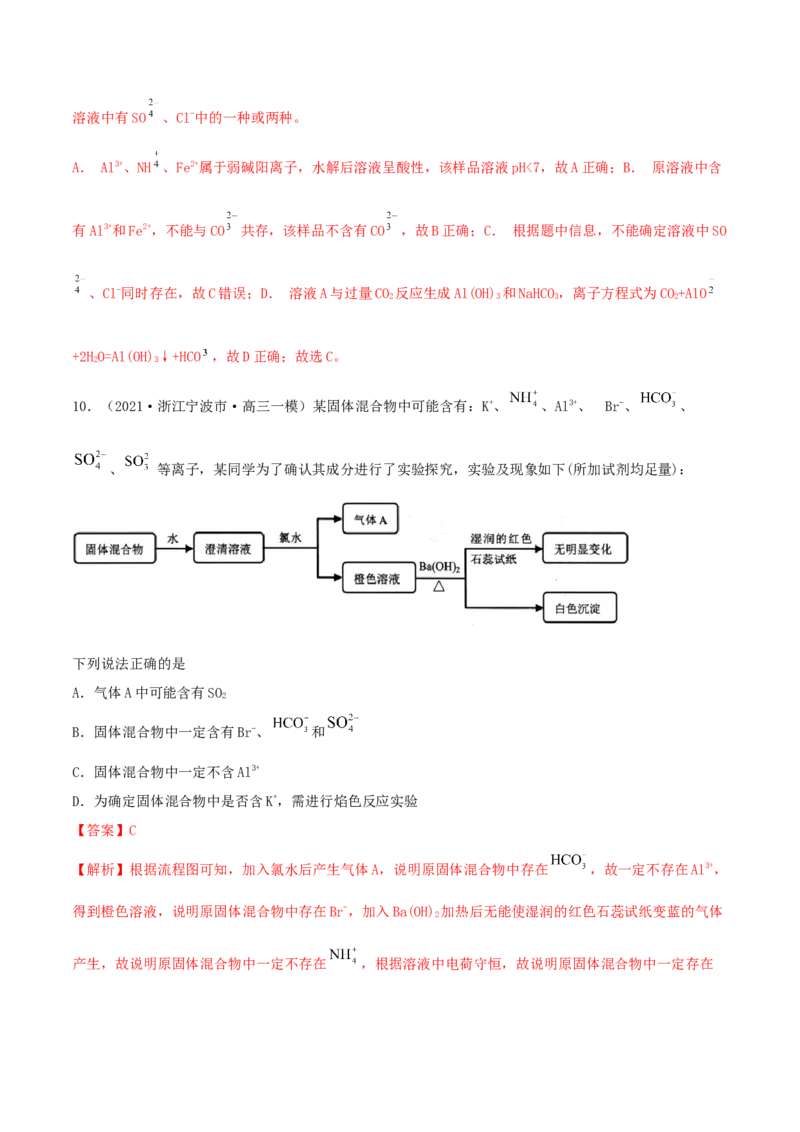
10.(2021·浙江宁波市·高三一模)某固体混合物中可能含有:K+、 、Al3+、 Br-、 、
、 等离子,某同学为了确认其成分进行了实验探究,实验及现象如下(所加试剂均足量):
下列说法正确的是
A.气体A中可能含有SO
2
B.固体混合物中一定含有Br-、 和
C.固体混合物中一定不含Al3+
D.为确定固体混合物中是否含K+,需进行焰色反应实验
【答案】C
【解析】根据流程图可知,加入氯水后产生气体A,说明原固体混合物中存在 ,故一定不存在Al3+,
得到橙色溶液,说明原固体混合物中存在Br-,加入Ba(OH) 加热后无能使湿润的红色石蕊试纸变蓝的气体
2
产生,故说明原固体混合物中一定不存在 ,根据溶液中电荷守恒,故说明原固体混合物中一定存在K+,由于氯水能将 氧化为 ,故加入Ba(OH) 后产生白色沉淀,不能说明原混合物是否含有 。
2
A.由于 +HO+Cl= +2H++2Cl-,故气体A中不可能含有SO,A错误;B.由分析可知,固体混合物
2 2 2
中无法确定是否含有 ,B错误;C.由分析可知,固体混合物中含有 ,由于3 +
Al3+=Al(OH)↓+3CO↑,故一定不含Al3+,C正确;D.由分析可知,根据电荷守恒即可确定固体混合物中
3 2
一定含有K+,无需进行焰色反应实验,D错误;故答案为:C。
11.(2020·浙江高三期中)某混合物X中可能含有FeSO、NaAlO、CuSO、NaO、(NH)SO 中的几种或
4 2 4 2 2 4 2 4
全部。将X与足量水作用,得到气体Q、固体Y和碱性溶液Z。下列结论不正确的是
A.混合物X中NaO、NaAlO 至少有一种
2 2 2
B.生成的气体Q可能含有二种成分
C.将固体Y充分灼烧,其质量一定减少
D.溶液Z一定无色,加入适量硫酸可能生成沉淀
【答案】D
【解析】若X中含有NaAlO 和(NH)SO,NaAlO 是强碱弱酸盐,溶液显碱性,(NH)SO 是强酸弱碱盐,溶
2 4 2 4 2 4 2 4
液显酸性,二者发生相互促进的双水解反应: + +HO=Al(OH) ↓+NH↑,若NaAlO 过量,则溶
2 3 3 2
液为碱性,则固体Y为Al(OH),如果X中还含有FeSO、CuSO,碱性溶液Z为NaSO、NaAlO、FeSO、
3 4 4 2 4 2 4
CuSO 的混合溶液,气体Q为氨气;
4
若X中含有过氧化钠,可与水反应生成氢氧化钠和氧气,反应生成的溶液显碱性,如果X中还含有FeSO、
4
CuSO,碱性条件下FeSO、CuSO 均可与氢氧根离子反应生成沉淀,亚铁离子易被氧化为三价铁离子,则固
4 4 4
体Y为Fe(OH) 或Cu(OH),碱性溶液Z为NaSO 和NaOH,气体Q为氧气;如果X中还含有(NH)SO,则生
3 2 2 4 4 2 4
成的氢氧化钠与(NH)SO 反应可生成氨气,则Q可能是氨气和氧气的混合气体;NaAlO 可存在于碱性溶液
4 2 4 2
中,则碱性溶液Z为NaSO、NaOH和NaAlO。
2 4 2
A.根据上述分析,混合物X中NaO、NaAlO 至少有一种,故A正确;B.根据上述分析,生成的气体Q可
2 2 2
能为氧气或者氨气,或者两种都有,故B正确;C.根据上述分析,将固体Y是氢氧化铁或者氢氧化铜或者
氢氧化铝,充分灼烧,质量都减少,故C正确;D.根据分析,溶液Z中可能含有NaAlO,加入适量硫酸可
2
能生成氢氧化铝沉淀;溶液Z中还可能含有硫酸铜或者硫酸亚铁,铜离子和亚铁离子在溶液中都有颜色,
故D错误;答案选D。
12.(2020·天津高三一模)有一份澄清溶液,可能含有 Na+、K+、NH+、Ca2+、Fe3+、SO2-、CO2-、SO2
4 4 3 3-、Cl-、I-中的若干种,且离子的物质的量浓度均为 0.1mol·L-1(不考虑水解和水的电离)。往该溶液中
加入过量的盐酸酸化 BaCl 溶液,无沉淀生成。另取少量原溶液,设计并完成如下实验:
2
则关于原溶液的判断中不正确的是
A.是否存在 Na+、K+ 需要通过焰色反应来确定
B.通过 CCl 层的颜色变化,能判断出溶液中 I-肯定存在
4
C.试样加足量氯水无气体产生,说明溶液中 CO2-肯定不存在
3
D.肯定不存在的离子是 Ca2+、Fe3+、SO2-、CO2-、Cl-
4 3
【答案】A
【解析】澄清溶液,往该溶液中加入过量的BaCl 和盐酸的混合溶液,无白色沉淀生成,无SO2-,加足量
2 4
氯水,无气体,则无CO2-,溶液加四氯化碳分液,下层紫红色,则有I-,上层加硝酸钡和稀硝酸有白色沉
3
淀,有SO2-,无Ca2+、Fe3+,溶液中一定含阳离子,且离子浓度都为0.1mol•L-1;根据电荷守恒,一定含有
3
NH+、Na+、K+,一定不存在Cl-;滤液中加硝酸酸化的硝酸银有白色沉淀,是过程中加氯水时引入的氯离,
4
结合溶液为电中性来解答。
A. 根据溶液中离子浓度均为0.1mol/L,且溶液呈电中性,溶液中一定存在 Na+、K+,不需要焰色反应来
确定,A项错误;B. 通过CCl 层的颜色变化,能判断出溶液中 I-肯定存在,B项正确;C. 试样加足量的
4
Cl 水,没有气体产生,说明无CO2-,C项正确;D. 由分析可知,肯定不存在的离子是Ca2+、Fe3+、SO2
2 3 4
-、CO2-、Cl-,D项正确;答案选A。
3
二、主观题(共2小题,共40分)
13.(2021·新疆高三模拟)(20分)现有四种溶液m,n,p、q,分别含阴阳离于 、 、 、
、 、 、 、 中的各一种,为了确定组成,进行了以下实验:将四种溶液两两混
合,发现m、n能剧烈反应,产生白色沉淀和无色气体,p、q能产生无色有刺激性气味的气体,p与m,n
均有沉淀产生,且在m中逐滴滴入p时,沉淀增多,后减少但没有完全消失。回答下列问题。
(1)p是________,q是_________(均填化学式)。
(2)写出在m中逐滴滴入p,沉淀减少时发生反应的离子方程式__________。(3)实验室检验q中阳离子需要的试剂或试纸是___________。
(4)经分析, 存在于_________(填m、n、p、q)溶液中,实验室常用重量法检验该溶液中 离子
的浓度,步骤如下:Ⅰ用量筒取该溶液8.0mL并转移至小烧杯中;Ⅱ加入盐酸酸化,然后加入足量的
溶液(沉淀反应在接近沸腾的温度下进行);Ⅲ过滤所得沉淀;洗涤,烘干后得到ag固体。
①所用量简的规格为___________。
A.10mL B.50mL C.100mL D.500mL
②过滤时,沉淀物颗粒的大小会影响过滤速度,从利于过滤的角度分析,沉淀反应需要在接近沸腾的温度
下进行的原因可能是__________。
③检验沉淀洗涤干净的方法是___________。
④计算,硫酸根的浓度为___________mol/L(用含a的式子表示)。
【答案】(除标注外,每空2分)(1)
(2) (3)NaOH溶液,红色石蕊试纸
(4)m ①A
②沸腾时,有利于产生颗粒较大的沉淀或有利于晶体生长
③用小试管取最后-次洗涤液少许,向其中加入少量的 溶液,如没有浑浊,说明沉淀洗涤干净,反
之,说明沉淀没有洗涤干净
④ (4分)
【解析】由m中逐滴滴入p时,沉淀增多,后减少但没有完全消失,可知在现有离子中,能满足先沉淀后
部分溶解现象的,一定是向铝盐溶液中逐滴滴入强碱溶液,故m为可溶性铝盐,p为强碱,再结合碱过量,
沉淀未溶解完全,说明强碱与铝盐混合,除了有氢氧化铝生成,还有其他沉淀生成,则可判断出m为
Al(SO),p为 ,则p、q能产生无色有刺激性气味的气体,q含 ,m、n能剧烈反应,产生
2 4 3
白色沉淀和无色气体,符合铝离子与 双水解生成氢氧化铝和二氧化碳的现象,则n含 ,由于
所剩离子仅为 和 ,溶液呈电中性,故q为 ,n为NaHCO。
3(1)根据上述分析,p为 ,q为 ,故答案依次为 , 。
(2)m为Al(SO),p为 ,沉淀为氢氧化铝,沉淀减少时的离子方程式为
2 4 3
,故答案为 。
(3)q为 ,则检验 的方法为:取待测液于试管中,加入浓氢氧化钠溶液,加热,用湿润的红
色石蕊试纸检验逸出的气体,若试纸变蓝,则原待测液中含 ,故需要的试剂或试纸为氢氧化钠溶液和
红色石蕊试纸,故答案为NaOH溶液,红色石蕊试纸。
(4) m为Al(SO),故 存在于m溶液中;故答案为:m。
2 4 3
①量筒量取液体时,所选规格遵循“近而大”的原则,故选规格为10mL的量筒;故答案选A。
②过滤时,沉淀物颗粒的大小会影响过滤速度,颗粒较大,有利于液体顺利滤出,故沉淀过程在接近沸腾
的温度下进行,是为了尽量使沉淀凝聚,即有利于产生颗粒较大的沉淀,或有利于晶体生长。
③检验沉淀是否洗涤干净,本质就是沉淀表面是否仍有可溶性离子残留,即是否有Cl-残留,故方法是,
取最后一次洗涤液少许于试管中,向其中加入少量的 溶液,如没有浑浊,说明沉淀洗涤干净,反
之,说明沉淀没有洗涤干净,故答案为:用小试管取最后-次洗涤液少许,向其中加入少量的 溶液,
如没有浑浊,说明沉淀洗涤干净,反之,说明沉淀没有洗涤干净。
④烘干后的固体成分仍为BaSO,硫元素守恒,故8.0mL溶液,n( )=n(BaSO)= mol,则c(
4 4
)= = mol/L;故答案为 。
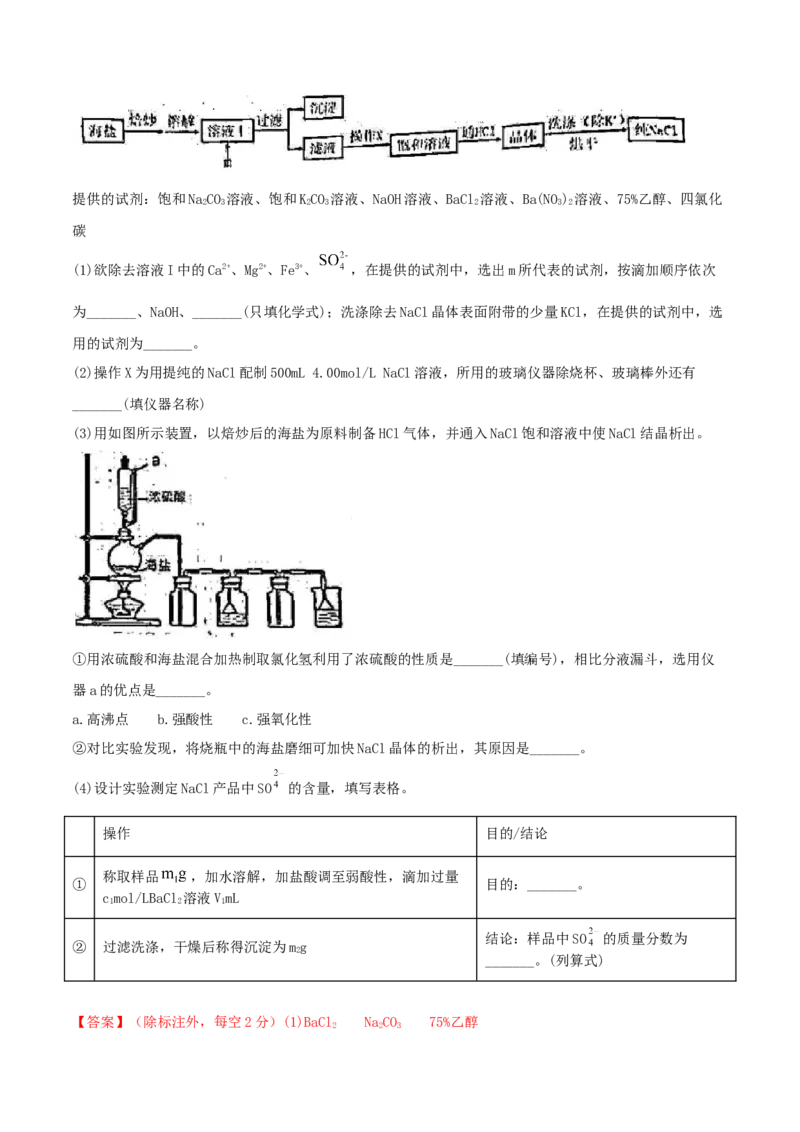
14.(2021·上海青浦区·高三二模)(20分)食盐是日常生活的必需品,也是重要的化工原料。试剂级
NaCl可用海盐(含泥沙、海藻、K+、Ca2+、Mg2+、Fe3+、SO 等杂质)为原料制备。实验室提纯NaCl的流程如
图:提供的试剂:饱和NaCO 溶液、饱和KCO 溶液、NaOH溶液、BaCl 溶液、Ba(NO) 溶液、75%乙醇、四氯化
2 3 2 3 2 3 2
碳
(1)欲除去溶液I中的Ca2+、Mg2+、Fe3+、 ,在提供的试剂中,选出m所代表的试剂,按滴加顺序依次
为_______、NaOH、_______(只填化学式);洗涤除去NaCl晶体表面附带的少量KCl,在提供的试剂中,选
用的试剂为_______。
(2)操作X为用提纯的NaCl配制500mL 4.00mol/L NaCl溶液,所用的玻璃仪器除烧杯、玻璃棒外还有
_______(填仪器名称)
(3)用如图所示装置,以焙炒后的海盐为原料制备HCl气体,并通入NaCl饱和溶液中使NaCl结晶析出。
①用浓硫酸和海盐混合加热制取氯化氢利用了浓硫酸的性质是_______(填编号),相比分液漏斗,选用仪
器a的优点是_______。
a.高沸点 b.强酸性 c.强氧化性
②对比实验发现,将烧瓶中的海盐磨细可加快NaCl晶体的析出,其原因是_______。
(4)设计实验测定NaCl产品中SO 的含量,填写表格。
操作 目的/结论
称取样品 ,加水溶解,加盐酸调至弱酸性,滴加过量
① 目的:_______。
cmol/LBaCl 溶液VmL
1 2 1
结论:样品中SO 的质量分数为
② 过滤洗涤,干燥后称得沉淀为mg
2
_______。(列算式)
【答案】(除标注外,每空2分)(1)BaCl NaCO 75%乙醇
2 2 3(2)500mL容量瓶、胶头滴管
(3)①a 平衡压强,使液体顺利滴下 ②增大与浓硫酸的接触面积,使产生HCl气体的速率加快
(4)使SO 完全沉淀 ×100% (4分)
【解析】(1)将海盐(含泥沙、海藻、K+、Ca2+、Mg2+、Fe3+、SO 等杂质)焙炒,除去海藻等有机杂质,并
使其颗粒变小,然后加水溶解,再依次加入过量BaCl 溶液除去SO 、过量NaOH溶液除去Mg2+和Fe3+、过
2
量碳酸钠除去过量的钡离子和钙离子,最后过滤,将滤液蒸发浓缩得到饱和溶液,再通入HCl气体酸化并
结晶,洗涤除去K+,烘干得到NaCl。
(1)为了不引入新的杂质,除去硫酸根应使用氯化钡溶液、除去Mg2+、Fe3+用NaOH溶液,除去Ca2+和过量的
Ba2+用NaCO 溶液,且NaCO 溶液需加在氯化钡之后,所以滴加顺序为BaCl、NaOH、NaCO;为了降低
2 3 2 3 2 2 3
NaCl的溶解度,同时使微量的KCl溶解,洗涤除去NaCl晶体表面附带的少量KCl应选用75%乙醇;
(2)配制500mL 4.00mol/L NaCl溶液,需要在烧杯溶解NaCl固体,溶解时需要玻璃棒搅拌,之后转移到
500mL容量瓶中进行定容,移液时需要玻璃棒引流,定容时需要胶头滴管滴加水,所用的玻璃仪器除烧杯、
玻璃棒外还有500mL容量瓶、胶头滴管;
(3)①氯化氢沸点低易挥发,而硫酸为高沸点酸不易挥发,所以将浓硫酸和NaCl混合加热可以挥发出HCl
气体,故选a;仪器a侧面导管可以平衡压强,使液体顺利滴下;
②将烧瓶海盐磨细可以增大与浓硫酸的接触面积,使产生HCl气体的速率加快,从而加快NaCl晶体的析出;
(4)步骤①中加入过量的BaCl 溶液,能使溶液中SO 完全沉淀,得到的沉淀为BaSO,质量为mg,则沉淀
2 4 2
中SO 的质量为 ,所以样品中硫酸根的质量分数为 ×100%= ×100%。