文档内容
第 09 讲 无机非金属材料
1.结合真实情境中的应用实例或通过实验探究,了解碳、硅及其重要化合物的主要性质,认识其在
生产中的应用和对生态环境的影响。
2.结合实例认识碳、硅及其化合物性质的多样性,了解通过化学反应可以探索物质性质、实现物质
转化,认识物质及其转化在自然资源综合利用和环境保护中的重要价值。
3.能借助国家关于安全生产、环境保护、食品安全、药物开发等方面的法律法规分析与化学有关的
社会热点问题。
4.能列举常见的大气、水体和土壤的污染物及其危害,能说明常见污染的成因和防治措施的化学原
理。
【核心素养分析】
1.变化观念与平衡思想:根据碳、硅的结构,预测在一定条件下碳、硅及其化合物可能发生的化学变
化。
2.科学态度与社会责任:关注与碳、硅有关的热点问题(如光导纤维、硅电池、半导体材料),形成
可持续发展的意识;知道碳、硅及其化合物对社会发展的重大贡献。
知识点一 碳及其重要化合物
1.碳单质
(1)结构、存在形态、物理性质和用途
存在形态 游离态和化合态
金刚石:空间网状结构;
结构
石墨:层状结构
同素异形体 金刚石、石墨、C 、C
60 70
金刚石:熔点高、硬度大;
物理性质
石墨:硬度小、电的良导体、有滑腻感
金刚石用作切割刀具,石墨用作电极、铅笔芯、高温润滑
用途
剂
(2)主要化学性质——还原性
可燃性 2C+O(不足)=====2CO、C+O(足量)=====CO
2 2 2CuO:2CuO+C=====2Cu+CO↑(冶炼金属)
2
与氧化
SiO:SiO+2C=====Si+2CO↑(制取粗硅)
2 2
物反应
HO:C+HO(g)=====CO+H(制取水煤气)
2 2 2
与强氧化 浓HSO :C+2HSO (浓)=====CO↑+2SO ↑+2HO
2 4 2 4 2 2 2
性酸反应 浓HNO:C+4HNO(浓)=====CO↑+4NO ↑+2HO
3 3 2 2 2
2.一氧化碳(CO)
(1)物理性质
无色气体,有毒,难溶于水。
(2)化学性质——还原性
①燃烧:2CO+O=====2CO,淡蓝色火焰;
2 2
②还原CuO:CuO+CO=====Cu+CO(冶炼金属)。
2
3.二氧化碳(CO)
2
(1)物理性质:CO 是一种无色、无味的气体,能溶于水,固态CO 俗称干冰。
2 2
(2)化学性质:与HO、NaO、Ca(OH) (足量、澄清)、Mg反应的方程式分别为CO+HOH CO、
2 2 2 2 2 2 3
NaO+CO===Na CO、CO+Ca(OH) ===CaCO ↓+HO 2Mg+CO=====2MgO+C。
2 2 2 3 2 2 3 2 2
(3)CO 在自然界中的循环
2
①CO 的主要来源:大量含碳燃料的燃烧。
2
②自然界消耗CO 的主要反应:
2
a.溶于江水、海水中:CO+HO HCO;
2 2 2 3
b.光合作用将CO 转化为O;
2 2
c.岩石的风化:CaCO +HO+CO===Ca(HCO)。
3 2 2 3 2
(4)CO、CO 气体的除杂方法
2
CO中混有CO 通过盛有NaOH溶液的洗气瓶,然后干燥气体
2
CO 中混有CO 通过盛有灼热CuO的硬质试管
2
通过盛有饱和NaHCO 溶液的洗气瓶,然后干
CO 中混有少量SO 或HCl 3
2 2 燥气体
①澄清石灰水只用于检验CO,不能用于除去混合气体中的CO,应用NaOH溶液除
2 2
去;
②CO、SO 通入CaCl 或BaCl 溶液均无沉淀产生
2 2 2 2
4.碳酸(H CO)
2 3
弱酸、不稳定。碳酸(H CO)只能在水中存在。HCO 在水中与CO 共存,因此常把CO+HO当碳酸
2 3 2 3 2 2 2
用。
5.碳酸的酸式盐和正盐的比较
(1)在水中的溶解性①含K+、Na+、NH的正盐易溶于水,其余一般不溶于水;酸式盐均能溶于水。
②一般来说,在相同温度下,难溶性正盐溶解度小于其酸式盐溶解度,如溶解度:
Ca(HCO )>CaCO ;可溶性正盐溶解度大于其酸式盐溶解度,如溶解度:NaCO>NaHCO。
3 2 3 2 3 3
(2)热稳定性
一般来说,热稳定性顺序为正盐>酸式盐>碳酸,如稳定性:NaCO>NaHCO>H CO。可溶性正盐>难
2 3 3 2 3
溶性正盐,如CaCO 高温分解,而KCO 不易分解。
3 2 3
(3)水溶液酸碱性
物质的量浓度相同时,正盐溶液的pH大于其酸式盐溶液,如pH:NaCO 溶液>NaHCO 溶液。
2 3 3
(4)与酸的反应
①CaCO 与盐酸反应的离子方程式:
3
CaCO +2H+===HO+CO↑+Ca2+。
3 2 2
②Ca(HCO ) 与盐酸反应的离子方程式:
3 2
HCO+H+===HO+CO↑。
2 2
(5)与碱的反应
①NaCO 与Ca(OH) 反应的离子方程式:
2 3 2
CO+Ca2+===CaCO ↓。
3
②NaHCO 与足量Ca(OH) 反应的离子方程式:
3 2
HCO+Ca2++OH-===CaCO ↓+HO。
3 2
Ca(OH) 与足量NaHCO 反应的离子方程式:
2 3
Ca2++2OH-+2HCO===CaCO ↓+CO+2HO。
3 2
知识点二 硅 无机非金属材料
一、硅单质
1.存在
硅单质主要有晶体和无定形两大类。
2.物理性质
带有金属光泽的灰黑色固体,熔点高,硬度大,有脆性。
3.化学性质
常温下与F、HF、NaOH反应;加热时能与H 化合生成不稳定的氢化物SiH,加热时还能与Cl、O
2 2 4 2 2
化合分别生成SiCl 、SiO。涉及的化学方程式如下:
4 2
①与非金属单质反应
②与氢氟酸反应:Si+4HF===SiF ↑+2H↑。
4 2
③与NaOH溶液反应:Si+2NaOH+HO===Na SiO+2H↑。
2 2 3 2
(4)制备方法
①制取粗硅:工业上,用焦炭在电炉中还原SiO 得到含有少量杂质的粗硅:SiO+2C=====Si+
2 2
2CO↑。
②粗硅提纯:Si+2Cl=====SiCl ,SiCl +2H=====Si+4HCl。
2 4 4 2
【特别提醒】①用焦炭还原SiO,产物是CO而不是CO。
2 2
②粗硅中含碳等杂质,与Cl 反应生成的SiCl 中含有CCl 等杂质,经过分馏提纯SiCl 后,再用H 还
2 4 4 4 2
原,得到高纯度硅。
(5)主要用途
①良好的半导体材料;②太阳能电池;③计算机芯片。
二、二氧化硅
1.存在
自然界中,碳元素既有游离态,又有化合态,而硅元素仅有化合态,主要以氧化物和硅酸盐的形式存
在。天然SiO 有晶体和无定形两种,统称硅石。
2
2.结构
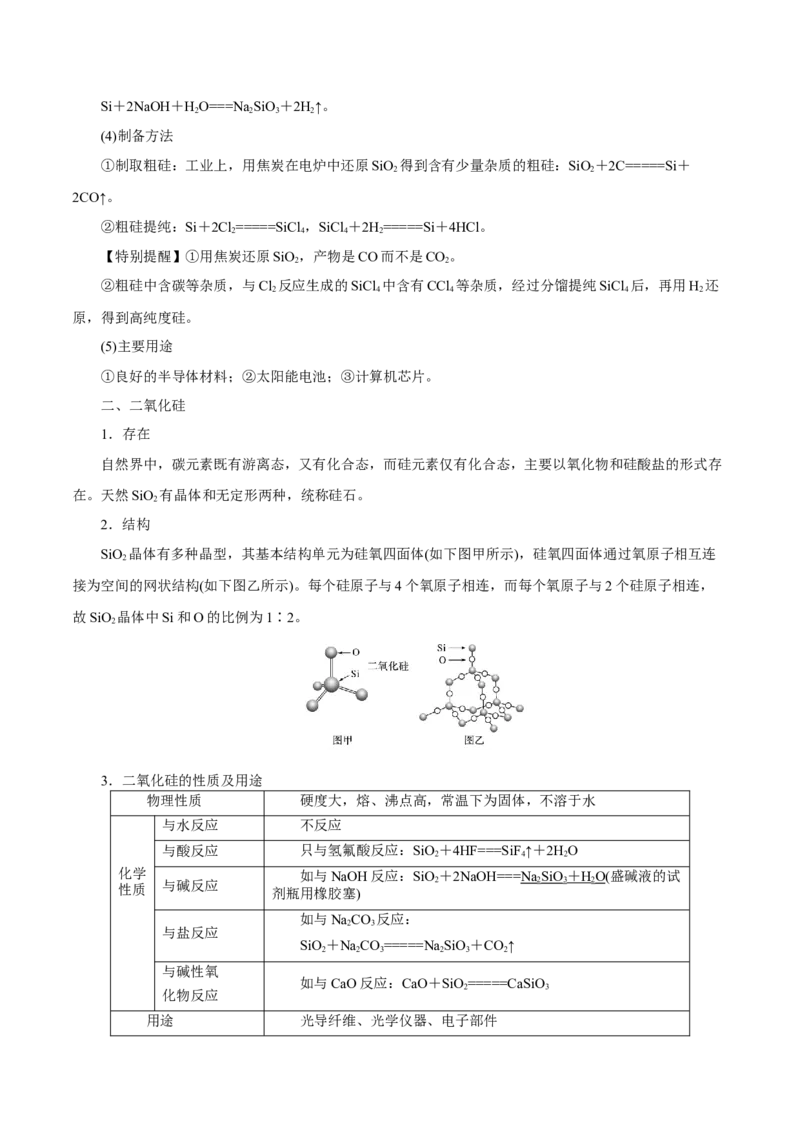
SiO 晶体有多种晶型,其基本结构单元为硅氧四面体(如下图甲所示),硅氧四面体通过氧原子相互连
2
接为空间的网状结构(如下图乙所示)。每个硅原子与4个氧原子相连,而每个氧原子与2个硅原子相连,
故SiO 晶体中Si和O的比例为1∶2。
2
3.二氧化硅的性质及用途
物理性质 硬度大,熔、沸点高,常温下为固体,不溶于水
与水反应 不反应
与酸反应 只与氢氟酸反应:SiO+4HF===SiF ↑+2HO
2 4 2
化学 如与NaOH反应:SiO+2NaOH===NaSiO + H O(盛碱液的试
性质 与碱反应 剂瓶用橡胶塞) 2 2 3 2
如与NaCO 反应:
2 3
与盐反应
SiO+NaCO=====NaSiO+CO↑
2 2 3 2 3 2
与碱性氧
如与CaO反应:CaO+SiO=====CaSiO
2 3
化物反应
用途 光导纤维、光学仪器、电子部件【特别提醒】
①SiO 是HSiO 的酸酐,但SiO 不与水反应,不能用SiO 直接与水作用制备HSiO。
2 2 3 2 2 2 3
②氢氟酸能与SiO 反应,故氢氟酸不能盛放在玻璃瓶中,而应存放在塑料瓶中。
2
三、硅酸、硅酸盐
1.硅酸
(1)物理性质
硅酸的溶解度小,新制备的硅酸为透明、胶冻状,干燥硅胶多孔,吸水性和吸附性强。
(2)化学性质
①弱酸性:酸性比碳酸弱,与NaOH溶液反应的化学方程式为HSiO+2NaOH===NaSiO+2HO。
2 3 2 3 2
②不稳定性:受热易分解,反应的化学方程式为
HSiO=====SiO+HO。
2 3 2 2
(3)制备:通过可溶性硅酸盐与其他酸反应制得,如NaSiO 溶液与盐酸反应:NaSiO+
2 3 2 3
2HCl===2NaCl+HSiO(胶体)。
2 3
(4)用途:硅胶可用作干燥剂、催化剂的载体等。
2.硅酸盐
①白色、可溶于水的粉末状固体,其水溶液俗称水玻璃,有黏性,水溶液显碱性。
②与酸性较硅酸强的酸反应:
a.与盐酸反应的化学方程式:
NaSiO+2HCl===2NaCl+HSiO↓。
2 3 2 3
b.与CO 水溶液反应的化学方程式:
2
NaSiO+HO+CO===Na CO+HSiO↓。
2 3 2 2 2 3 2 3
③用途:黏合剂(矿物胶),耐火阻燃材料。
(3)硅酸盐组成的表示
通常用二氧化硅和金属氧化物的组合形式表示硅酸盐的组成。如硅酸钠(Na SiO)可表示为
2 3
NaO·SiO ,石棉(CaMg Si O )可表示为CaO·3MgO·4SiO 。
2 2 3 4 12 2
推背图①NaSiO 的水溶液是一种黏合剂,是制备硅胶和木材防火剂等的原料;NaSiO 易与空气中的
2 3 2 3
CO、HO反应,要密封保存。
2 2
②可溶性碳酸盐、硅酸盐的水溶液呈碱性,保存该溶液的试剂瓶不能用玻璃塞,应用橡胶塞。
四、无机非金属材料
1.传统无机非金属材料,如水泥、玻璃、陶瓷等硅酸盐材料。
(1)常见硅酸盐材料比较水泥 玻璃 陶瓷
生产原料 石灰石、黏土 纯碱、石灰石、石英 黏土
主要设备 水泥回转窑 玻璃窑 陶瓷窑
(2)玻璃生产中的两个重要反应:NaCO+SiO=====NaSiO+CO↑;CaCO +SiO=====CaSiO +
2 3 2 2 3 2 3 2 3
CO↑。
2
2.新型无机非金属材料
材料类别 主要特性 示例 用途
高温结构 能承受高温,
氮化硅陶瓷 汽轮机叶片、轴承、永久性模具等
陶瓷 强度高
半导体陶瓷 具有电学特性 二氧化锡陶瓷 集成电路中的半导体
光学材料 具有光学特性 光导纤维 光缆通讯、医疗、照明等
生物陶瓷 具有生物功能 氧化铝陶瓷 人造骨骼、人造关节、接骨螺钉
高频考点一 硅和二氧化硅
例1.(2022·浙江卷)下列说法不正确的是
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
C.氧化铝熔点高,常用于制造耐高温材料
D.用石灰右-石膏法对燃煤烟气进行脱硫,同时可得到石膏
【变式探究】(2022·广东卷)陈述Ⅰ和Ⅱ均正确但不具有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 用焦炭和石英砂制取粗硅 SiO 可制作光导纤维
2
B 利用海水制取溴和镁单质 可被氧化,Mg2+可被还原
C 石油裂解气能使溴CCl 的溶液褪色 石油裂解可得到乙烯等不饱和烃
4
D FeCl 水解可生成Fe(OH) 胶体 FeCl 可用作净水剂
3 3 3
【变式探究】下列说法错误的是( )
A.(2019新课标Ⅲ)高纯硅可用于制作光感电池
B.(2019江苏)SiO 熔点高硬度大,可用于制光导纤维
2
C.(2019浙江)天然石英和水晶的主要成分都是二氧化硅
D.(2018天津)汉代烧制出“明如镜、声如磬”的瓷器,其主要原料为黏士高频考点二 硅酸盐及其应用
例3.(2021·浙江卷)下列说法不正确的是( )
A.硅酸钠是一种难溶于水的硅酸盐 B.镁在空气中燃烧可生成氧化镁和氮化镁
C.钠与水反应生成氢氧化钠和氢气 D.常温下,铝遇浓硝酸或浓硫酸时会发生钝化
【举一反三】(2020·浙江卷)Ca SiO 是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是(
3 5
)
A. 可发生反应:
B. 具有吸水性,需要密封保存
C. 能与SO ,反应生成新盐
2
D. 与足量盐酸作用,所得固体产物主要为SiO
2
高频考点三 无机非金属材料
例3.(2019·北京卷)下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料
的是
A.4.03米大口径碳化硅 B.2022年冬奥会 C.能屏蔽电磁波的碳包 D.“玉兔二号”钛
反射镜 聚氨酯速滑服 覆银纳米线 合金筛网轮
【变式探究】新材料的新秀——石墨烯和氧化石墨烯已成为物理、化学、材料科学研究的国际热点课
题。其结构模型如图所示:
下列有关说法正确的是( )
A.石墨烯是一种新型化合物
B.氧化石墨烯即石墨烯的氧化物
C.二者和石墨都是碳的同素异形体
D.氧化石墨烯具有一定的亲水性
高频考点四 与SiO 有关的无机化工流程题
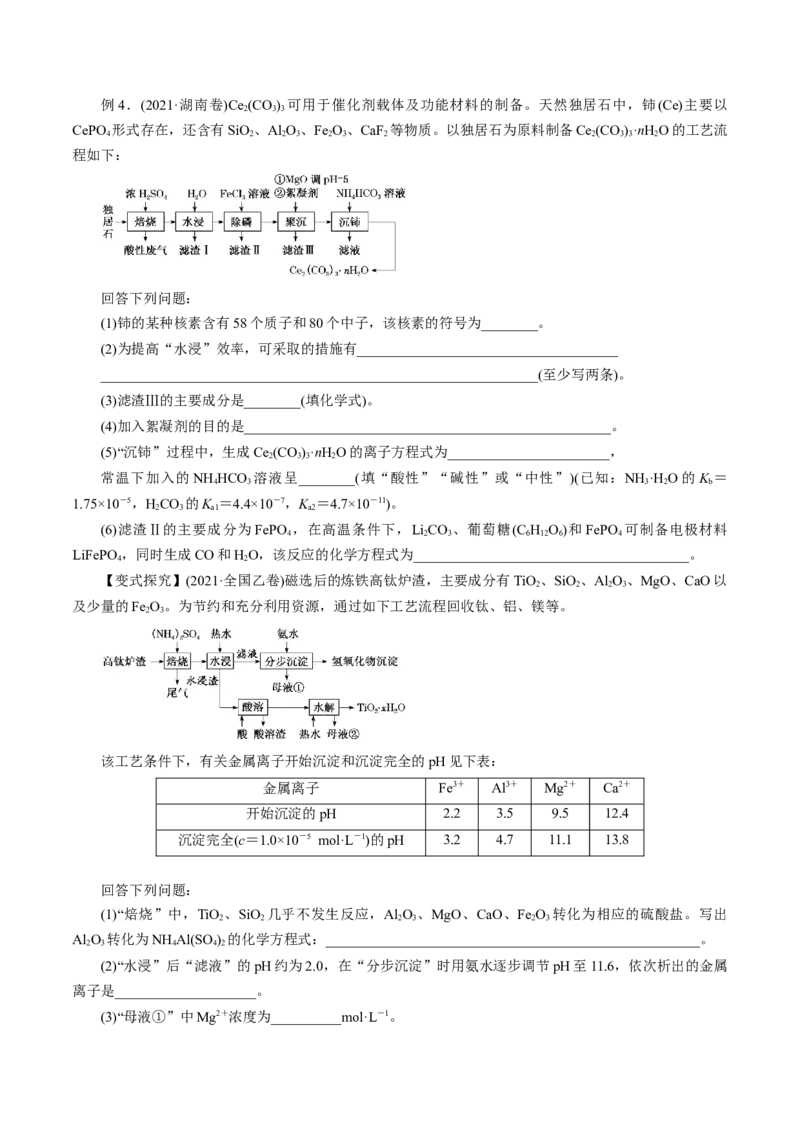
2例4.(2021·湖南卷)Ce (CO) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以
2 3 3
CePO 形式存在,还含有SiO、Al O、Fe O、CaF 等物质。以独居石为原料制备Ce (CO)·nHO的工艺流
4 2 2 3 2 3 2 2 3 3 2
程如下:
回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为________。
(2)为提高“水浸”效率,可采取的措施有_____________________________________
______________________________________________________________(至少写两条)。
(3)滤渣Ⅲ的主要成分是________(填化学式)。
(4)加入絮凝剂的目的是____________________________________________________。
(5)“沉铈”过程中,生成Ce (CO)·nHO的离子方程式为_______________________,
2 3 3 2
常温下加入的NH HCO 溶液呈________(填“酸性”“碱性”或“中性”)(已知:NH ·H O的K =
4 3 3 2 b
1.75×10-5,HCO 的K =4.4×10-7,K =4.7×10-11)。
2 3 a1 a2
(6)滤渣Ⅱ的主要成分为FePO ,在高温条件下,LiCO 、葡萄糖(C H O)和FePO 可制备电极材料
4 2 3 6 12 6 4
LiFePO ,同时生成CO和HO,该反应的化学方程式为_______________________________________。
4 2
【变式探究】(2021·全国乙卷)磁选后的炼铁高钛炉渣,主要成分有TiO、SiO、Al O、MgO、CaO以
2 2 2 3
及少量的Fe O。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
2 3
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表:
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×10-5 mol·L-1)的pH 3.2 4.7 11.1 13.8
回答下列问题:
(1)“焙烧”中,TiO 、SiO 几乎不发生反应,Al O 、MgO、CaO、Fe O 转化为相应的硫酸盐。写出
2 2 2 3 2 3
Al O 转化为NH Al(SO ) 的化学方程式:_____________________________________________________。
2 3 4 4 2
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,依次析出的金属
离子是____________________。
(3)“母液①”中Mg2+浓度为__________mol·L-1。(4)“水浸渣”在160 ℃“酸溶”,最适合的酸是________。“酸溶渣”的成分是________、________。
(5)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO·xHO沉淀,该反应的离子方程式是
2 2
________________________________________________________________________________________。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得________,循环利用。