文档内容
第三章 金属及其化合物
第09讲 铁及其重要化合物(精练)
完卷时间:50分钟
可能用到的相对原子质量:O 16 S 32 Ba 137
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·北京西城区·高三二模)下列事实与电化学无关的是
A.暖宝宝(含铁粉、 B.海沙比河沙混凝土更
C.家用铁锅生锈 D.铁罐运输浓硫酸
碳、氯化钠等)发热 易使钢筋生锈
A.A B.B C.C D.D
【答案】D
【解析】A.暖宝宝中铁粉、碳在氯化钠溶液中构成原电池,铁发生吸氧腐蚀放出热量,与电化学有关,
故A不符合题意;B.海沙中电解质的量大于河沙,钢筋在海沙中构成原电池时,由于电解质溶液浓度大,
腐蚀速率快,则海沙比河沙混凝土更易使钢筋生锈与电化学有关,故B不符合题意;C.家用铁锅生锈是因
为铁锅与锅中残留溶液构成原电池,发生吸氧腐蚀,则家用铁锅生锈与电化学有关,故C不符合题意;D.
铁在冷的浓硫酸中发生钝化,则铁罐运输浓硫酸与铁的钝化有关,与电化学有无关,故D符合题意;故选
D。
2.(2021·广东高三二模)一种利用 回收含铜废铁粉中的 的工艺如下:
下列说法错误的是
A.M是 , 与 在该条件下较难发生反应
B.“气化”过程的化学方程式为
C.“分解”过程需要适当降低反应体系的压强
D.“分解”过程可在空气气氛的密闭容器内进行
【答案】D【解析】A.Fe(CO) 分解得到5CO和Fe,故5M中的M代表CO,含铜废铁粉气化后仅得到Fe(CO),说明
5 5
与 在该条件下较难发生反应,故A正确;B.“气化”过程由CO与Fe生成Fe(CO),化学方程式为
5
,故B正确;C.“分解”过程发生反应, ,需要
适当降低反应体系的压强有利于平衡向右移动,提高分解率,故C正确;D.“分解”过程后CO还需要重
新回收利用,不能在空气气氛的密闭容器内进行,故D错误;故选D。
3.(2020·浙江绍兴市·高三一模)某同学为验证Fe3+的氧化性进行了如下实验:
序号 操作 现象
实验I 将2 mL 2 mol∙L−1Fe(NO) 溶液加入有银镜的试管中 银镜消失
3 3
实验II 将2 mL1 mol∙L−1 Fe(SO) 溶液加入有银镜的试管中 银镜减少,未消失
2 4 3
实验
将2mL2 mol∙L−1FeCl 溶液加入有银镜的试管中 银镜消失
III 3
将2mL 1 mol∙L−1 AgNO 溶液加入到1 mL 1 mol∙L−1 FeSO 产生白色沉淀,随
实验IV 3 4
溶液中 后有黑色固体产生
已知相同条件下AgCl的溶解度小于AgSO 下列说法不正确的是
2 4.
A.实验I不能说明Fe3+氧化了Ag
B.实验II和III说明溶液中存在平衡: Fe3++Ag Fe2++ Ag+
C.实验IV中产生白色沉淀,说明Ag+氧化了Fe2+
D.欲证明实验IV中产生了Fe3+,可以取上层清液滴加KSCN溶液
【答案】C
【解析】A.实验I中铁离子水解显酸性,含有硝酸根, (H+)的氧化性强于Fe3+,因此不能说明
Fe3+氧化了Ag,故A正确;B.实验II中银镜未消失,实验III银镜消失,说明实验II和III说明溶液中
存在平衡:Fe3++Ag Fe2++ Ag+,实验III生成的Ag+和Cl-反应得到AgCl沉淀,消耗Ag+,Ag+浓度减小,
致使平衡不断正向移动,故B正确;C.实验IV中产生白色沉淀,生成了AgSO 沉淀,Ag+具有强氧化性会
2 4
氧化Fe2+变为Fe3+,而自身变为黑色的Ag,故C错误;D.欲证明实验IV中产生了Fe3+,可以取上层清液滴
加KSCN溶液,若溶液变为血红色,说明含有Fe3+,若不变血红色,则说明不含有Fe3+,故D正确;综上所述,答案为C。
4.(2020·江西高三月考)压缩天然气汽车以天然气代替汽车用油,具有价格低、污染少、安全等优点。
未经处理的天然气含有HS,直接使用会造成大气污染,T.F菌在酸性溶液中可实现天然气的催化脱硫,其
2
原理如图所示。下列说法错误的是( )
A.Fe(SO) 可以视为该脱硫过程中的催化剂
2 4 3
B.该脱硫过程的总反应为:2HS+O=2S+2HO
2 2 2
C.该脱硫过程不能在高温下进行
D.该脱硫过程是将HS转化为FeSO
2 4
【答案】D
【解析】天然气中的脱硫原理是:Fe(SO) 氧化硫化氢,自身被还原成硫酸亚铁,硫酸亚铁被氧气氧化成
2 4 3
硫酸铁;A.T.F菌在酸性溶液中可实现天然气的催化脱硫,Fe(SO) 氧化硫化氢,自身被还原成硫酸亚铁,
2 4 3
硫酸亚铁被氧气氧化成硫酸铁,Fe(SO) 在整个过程中质量和化学性质不变,可以视为催化剂,故A正确;
2 4 3
B.脱硫过程:Fe(SO) 氧化硫化氢,自身被还原成硫酸亚铁,硫酸亚铁被氧气氧化成硫酸铁,Fe(SO)
2 4 3 2 4 3
视为催化剂,因此脱硫过程O 间接氧化HS,总反应为:2HS+O=2S+2HO,故B正确;C.T.F菌的主要成
2 2 2 2 2
分为蛋白质,高温下蛋白质会发生变性,因此该脱硫过程不能在高温下进行,故C正确;D.T.F菌在酸性
溶液中可实现天然气的催化脱硫,根据图示,Fe(SO) 氧化硫化氢生成硫,自身被还原成硫酸亚铁,硫酸
2 4 3
亚铁被氧气氧化成硫酸铁,故D错误;答案选D。
5.(2020·浙江嘉兴市·高三一模)高铁酸钠(NaFeO)是一种新型绿色消毒剂,其制备原理用化学方程
2 4
式表示为:3NaClO+2FeCl+10NaOH=2NaFeO+9NaCl+5HO。下列说法不正确的是
3 2 4 2
A.NaFeO 中Fe元素是+6价 B.还原产物是NaCl
2 4
C.FeCl 是还原剂 D.NaClO被氧化
3
【答案】D
【解析】A.根据化合物中各元素化合价之和为0可知,NaFeO 中Fe元素是+6价,A正确;B.NaClO被
2 4
FeCl 还原得到NaCl,因此NaCl是还原产物,B正确;C.FeCl 中Fe的化合价升高,失去电子,作还原剂,
3 3
C正确;D.NaClO中Cl的化合价降低,得到电子,作氧化剂,被还原,D错误;答案选D。
6.(2021·山东高三二模)利用反应2FeCO·2HO+HO+3KCO+HCO=2K[Fe(CO)]·3HO可制备光敏
2 4 2 2 2 2 2 4 2 2 4 3 2 4 3 2材料三草酸合铁酸钾晶体。下列说法正确的是
A.HO 是含有非极性键的极性分子
2 2
B.激发态的钾原子回到基态,会形成吸收光谱
C.向草酸亚铁溶液中滴加酸性KMnO 溶液,紫色褪去可证明溶液中含有Fe2+
4
D.HCO ( )与CHCOOH相比,可电离出的H+个数更多,所以酸性更强
2 2 4 3
【答案】A
【解析】A.HO 结构式为H-O-O-H,含有极性共价键H-O和非极性共价键O-O,极性不能抵消,是含有非
2 2
极性键的极性分子,A说法正确;B.激发态的钾原子回到基态,释放能量,会形成发射光谱,B说法错误;
C.向草酸亚铁溶液中滴加酸性KMnO 溶液,草酸根离子与亚铁离子均有还原性,则紫色褪去不能证明溶液
4
中含有Fe2+,C说法错误;D.酸的强弱与其电离出的H+个数无关,D说法错误;答案为A。
7.(2021·福建福州市·高三三模)硫铁矿烧渣是生产硫酸的固体废弃物,用其制备高效絮凝剂聚合氯
化硫酸铁铝,既能消除烧渣的危害,又能实现资源化。下列有关说法错误的是
A.离心沉降与过滤都能使实现固液分离
B.使用次氯酸钠氧化含铁溶液时发生:ClO-+2Fe2++2H+=2Fe3++Cl-+HO
2
C.水浴加热时应将温度计插入水浴锅液面下
D.聚合氯化硫酸铁铝可用于生活废水的杀菌消毒处理
【答案】D
【解析】A.硫铁矿烧渣用硫酸处理后,可溶性物质进入溶液,难溶性的物质仍以固体形式存在,可以通
过过滤的方法实现固液分离;也可以在离心力作用下,使分散在分散剂中的固相分散质分离出来,即采用
离心沉降方法实现固液分离,A正确;B.次氯酸钠具有强氧化性,会将Fe2+氧化为Fe3+,ClO-被还原为
Cl-,根据电子守恒、电荷守恒及原子守恒,可得反应的离子方程式为:ClO-+2Fe2++2H+=2Fe3++Cl-+HO,B正
2
确;C.水浴加热时要使用温度计测量水的温度,因此应将温度计插入水浴锅液面下,并且温度计不能接
触锅壁或锅底,C正确;D.聚合氯化硫酸铁铝在水中能够水解产生氢氧化铝胶体、氢氧化铁胶体,这些胶
体表面积大,吸附力强,能够吸附水中悬浮的固体小颗粒,使之形成沉淀而除去,因此可用于生活废水的
净化作用,但由于不具有强氧化性,因此不能起杀菌消毒作用,D错误;故合理选项是D。8.(2021·北京顺义区·高三二模)用废铁屑制备磁性氧化铁(FeO),制取过程如图:
3 4
下列说法不正确的是
A.浸泡过程中适当加热并搅拌效果更好
B.检验A中的Fe3+可以用KSCN溶液
C.加HO 时发生反应的离子方程式为:HO+2Fe2++2H+=2Fe3+ +2HO
2 2 2 2 2
D.制备FeO 的反应Fe2++2Fe3++8OH- FeO+4HO是氧化还原反应
3 4 3 4 2
【答案】D
【解析】A.浸泡过程中适当加热并搅拌可以提高反应速率和充分接触,效果更好,A正确;B.检验铁离
子可以用硫氰化钾,溶液显红色,B正确;C.过氧化氢能氧化亚铁离子,离子方程式为HO+2Fe2+
2 2
+2H+=2Fe3+ +2HO,C正确;D.制备FeO 的反应Fe2++2Fe3++8OH- FeO+4HO中没有元素化合价变化,
2 3 4 3 4 2
不是氧化还原反应,D错误;故选D。
9.(2021·广东高三一模)某学校化学社团为探究SO 与Fe3+是否发生氧化还原反应,按如图所示装置进
2
行实验(夹持、加热装置均省略),已知浓硫酸的沸点为338°C。下列说法错误的是
A.甲中生成SO 的同时还会有硫酸酸雾产生
2
B.试剂a为饱和NaHSO 溶液
3
C.丙中溶液pH降低,证明Fe3+氧化了SO
2
D.若Fe3+氧化了SO,则在丙中的溶液中滴加K[Fe(CN)]溶液,会出现蓝色沉淀
2 3 6
【答案】C
【解析】A.铜和浓硫酸反应需要加热,硫酸的沸点为338℃,所以甲中生成SO 的同时还会有硫酸酸雾产
2
生,故A正确;B.为了除去SO 中的硫酸酸雾,可以选择饱和NaHSO 溶液,故B正确;C.丙中溶液pH降
2 3低,也可能是SO 溶于水生成了亚硫酸,不能证明是Fe3+氧化了SO,故C错误;D.若Fe3+氧化了SO,则
2 2 2
生成了Fe2+,Fe2+和K[Fe(CN)]反应会出现蓝色沉淀,故D正确;故选C。
3 6
10.(2021·北京石景山区·高三一模)某小组对Fe2+和Ag+的反应进行了如下探究实验:
操作 现象 Ag+ 浓度变化曲线
实验 向1 mL 0.1 mol/L FeSO 溶液中加入1 mL 几分钟后,出现大量
4
Ⅰ 0.1 mol/L AgNO 溶液 灰黑色浑浊
3
实验 先向试管中加入几滴Fe(SO) 溶液,然后重
2 4 3 现象与实验Ⅰ相同
Ⅱ 复实验Ⅰ的操作
(已知:AgSO 为白色微溶物;反应过程中测得温度几乎无变化)
2 4
下列说法正确的是
A.实验Ⅰ只发生反应:Fe2++Ag+ Fe3++Ag,灰黑色浑浊是Ag
⇌
B.图中c(Ag+)由a→b急速变化的可能原因是反应放热
C.图中c(Ag+)由a→b急速变化的可能原因是生成的Ag起催化作用
D.图中c(Ag+)由a→b急速变化的可能原因是生成的Fe3+起催化作用
【答案】C
【解析】A.AgSO 为白色沉淀,故溶液中还可发生:2Ag++S =AgSO↓,灰黑色浑浊应是Ag和AgSO 的
2 4 2 4 2 4
混合物,故A错误;B.反应过程中测得温度几乎无变化,说明反应热效应不明显,故B错误;C.实验Ⅱ
中,先加入Fe(SO) 溶液,然后重复实验Ⅰ的操作,现象与实验Ⅰ相同,结合反应Fe2++Ag+ Fe3++Ag可
2 4 3 ⇌
知,应是生成的Ag起催化作用,故C正确;D.实验Ⅱ中,先加入Fe(SO) 溶液,然后重复实验Ⅰ的操作,
2 4 3
现象与实验Ⅰ相同,说明Fe3+没起催化作用,故D错误;答案选C。
11.(2021·河南郑州市·高三二模)某学习小组探究铁丝(含杂质碳)与浓硫酸的反应,反应装置如下图。
下列说法错误的是A.无法直接使用pH试纸来判断反应后硫酸是否剩余
B.可用KSCN和K[Fe(CN)]检验反应后溶液中铁元素的价态
3 6
C.将22.4mL(标准状况下)反应生成的气体通入足量氯水中,再滴加足量BaCl 溶液,最终得到0.233g沉
2
淀
D.生成的气体通入BaCl 溶液产生白色浑浊,可能是硫酸蒸气逸出或部分SO 被氧化所致
2 2
【答案】C
【解析】铁和浓硫酸在加热的条件下反应生成硫酸铁、二氧化硫、水,随着反应的进行,浓硫酸变稀,铁
和稀硫酸反应生成硫酸亚铁和氢气。
A.生成物中含有SO,SO 溶于水生成HSO,使溶液显酸性,因此不能直接使用pH试纸来判断反应后硫酸
2 2 2 3
是否剩余,A项正确;B.K[Fe(CN)]与Fe2+作用产生蓝色沉淀,K[Fe(CN)]可检验Fe2+,KSCN与Fe3+作用,
3 6 3 6
溶液变红色,KSCN可检验Fe3+,B项正确;C.反应生成的气体中含有SO、H,混合气体的总物质的量为
2 2
,若气体都为SO,根据S元素守恒,生成沉淀的物质的量为0.001mol,则产生沉
2
淀的质量为 ,但实际上,SO 物质的量小于0.001mol,则沉淀质量小于
2
0.233g,C项错误;D.生成的气体通入BaCl 溶液,由于硫酸蒸气逸出或部分SO 被氧化生成 ,会和
2 2
Ba2+反应生成BaSO 白色沉淀,D项正确;答案选C。
4
12.(2020·邵东市第一中学高三月考)黄铁矿(主要成分FeS),在空气中会被缓慢氧化,氧化过程如
2
图所示。下列说法不正确的是
A.发生反应a时,0.05mol FeS 被氧化时消耗标准状况下空气的体积大约19.6L
2
B.为了验证b过程反应后溶液中含Fe2+,可选用KSCN溶液和氯水
C.c发生反应的离子方程式为:14Fe3+ +FeS+8HO=15Fe2++2SO2-+16H+
2 2 4
D.已知25 ℃时,Ksp[Fe(OH)]=2.79×10-39,则该温度下d逆反应的平衡常数为K=2.79×103
3
【答案】B【解析】A.据图可知反应a中FeS 被氧化生成Fe2+和SO2-,Fe元素化合价不变,S元素化合价升高+7价,
2 4
所以0.05mol FeS 被氧化时转移电子0.7mol,消耗氧气0.175mol,氧气占空气体积 ,所以消耗空气
2
0.875mol,标况下体积为0.875mol×22.4L/mol=19.6L,故A正确;B.经反应b后溶液中一定存在Fe3+,
无论是否含有Fe2+,滴加KSCN溶液均会显红色,加入氯水后现象不变,无法检验Fe2+,故B错误;C.反应
c中反应物有FeS、Fe3+,产物有Fe2+和SO2-,说明该过程中铁离子将硫元素氧化,生成SO2-,结合电子守
2 4 4
恒和元素守恒可知离子方程式为14Fe3+ +FeS+8HO=15Fe2++2SO2-+16H+,故C正确;D.d的逆反应为
2 2 4
Fe(OH)+3H+ Fe3++3HO,该反应的平衡常数K=
3 2
=2.79×103,故D正确;故答案为B。
二、主观题(共3小题,共40分)
13.(2021·上海杨浦区·高三一模)(14分)(NH)Fe(SO)·6HO(硫酸亚铁铵)是一种重要的化工原料,
4 2 4 2 2
用途广泛。完成下列填空:
(1)铁在元素周期表的第ⅦB和第ⅠB之间。铁位于第___周期___族。
(2)写出Fe与水反应的化学方程式:___。
(3)将(NH)Fe(SO) 中非金属元素的简单阴离子按半径由小到大的顺序排列:___。
4 2 4 2
(4)同温度同浓度的FeSO 和(NH)Fe(SO) 溶液中,c(Fe2+)是否相等___?为什么?___。
4 4 2 4 2
(5)设计实验,证明(NH)Fe(SO)·6HO晶体中含有Fe2+___。
4 2 4 2 2
(6)已知:(NH)Fe(SO)·6HO在200℃失去全部结晶水。将一定质量的粉末状该晶体置于坩埚中,保持
4 2 4 2 2
200℃受热,经冷却、恒重等正确操作,计算得到的1mol晶体中结晶水含量总是偏低,偏低的可能原因是
___(写一条即可)。
【答案】(除标注外,每空2分)(1)四(或4)(1分) Ⅷ (1分)
(2)
(3) r(H-)<r(O2-)<r(N3-)<r(S2-)
(4)不相等 因为Fe2++2HO Fe(OH)+2H+、NH +HO NH·HO+H+, 的水解会抑制Fe2+水解,使
2 2 2 3 2
(NH)Fe(SO) 中c(Fe2+)偏大
4 2 4 2
(5)取样少许,加水(或稀硫酸)溶解,滴加KSCN溶液,无明显现象,滴加少量氯水,溶液变为血红色,说
明含Fe2+(6)(NH)Fe(SO)·6HO在坩埚中受热分解时,Fe2+可能会被空气中的氧气部分氧化,增加了氧元素的质量,
4 2 4 2 2
使结晶水含量的测定偏低
【解析】(1)位于第四周期,价电子共有8个,位于周期表的第8列,周期表中8、9、10三列合称第Ⅷ族,
即铁位于第四周期第Ⅷ族。
(2)Fe与水蒸气反应生成FeO 和H,反应方程式为: ;
3 4 2
(3)四种非金属元素简单阴离子分别为:H-、N3-、S2-、O2-,其中H-电子层为一层,半径最小,S2-电子层为
三层,半径最大,N3-、O2-电子层均为两层,但O的核电荷数大,对核外电子引力强,故半径小,所以四种
离子半径大小顺序为:r(H-)<r(O2-)<r(N3-)<r(S2-);
(4)(NH)Fe(SO) 中Fe2+水解与 水解相互抑制,水解程度比FeSO 中Fe2+水解程度小,故(NH)Fe(SO)
4 4 2 4 4 4 2
中Fe2+浓度大于FeSO 中Fe2+浓度;
4
(5)证明(NH)Fe(SO) 中含有Fe2+,可以通过将Fe2+氧化为Fe3+检验,但需排除原有Fe3+干扰,故应该先加
4 4 2
KSCN,再氧化Fe2+,具体方案为:取样少许,加水(或稀硫酸)溶解,滴加KSCN溶液,无明显现象,滴加少
量氯水,溶液变为血红色,说明含Fe2+;
(6)由于样品中铁元素为二价,易被氧化,题目操作未说明隔绝空气,故会产生误差,即
(NH)Fe(SO)·6HO在坩埚中受热分解时,Fe2+可能会被空气中的氧气部分氧化,增加了氧元素的质量,
4 2 4 2 2
使结晶水含量的测定偏低。
14.(2020·兰州市第七中学高三月考)(10分)以含钴废催化剂(主要成分为Co、Fe、SiO)为原料制取
2
复合氧化钴的流程如下:
(1)用HSO 溶解后过滤,得到的滤渣是____(填化学式)。将滤渣洗涤2~3次,再将洗液与滤液合并的目
2 4
的是____。
(2)在加热搅拌条件下加入NaClO,将Fe2+氧化成Fe3+,反应的离子方程式是____。
3
(3)已知:铁氰化钾的化学式为K[Fe(CN)];亚铁氰化钾的化学式为K[Fe(CN)]。
3 6 4 6
3Fe2++2[Fe(CN)]3− =Fe[Fe(CN)]↓(蓝色沉淀)
6 3 6 2
4Fe3++3[Fe(CN)]4− = Fe[Fe(CN)]↓(蓝色沉淀)
6 4 6 3
确定Fe2+是否氧化完全的方法是____。(仅供选择的试剂:铁氰化钾溶液、亚铁氰化钾溶液、铁粉、KSCN
溶液)
(4)向氧化后的溶液中加入适量的NaCO 调节酸度,使之生成黄钠铁矾[NaFe(SO)(OH) ]沉淀,写出该
2 3 2 6 4 4 12反应的离子方程式:____。
(5)已知CoCl 的溶解度曲线如图所示。向碱式碳酸钴沉淀中加入足量稀盐酸边加热边搅拌至完全溶解后,
2
需趁热过滤的原因是____。
【答案】(除标注外,每空2分)(1)SiO (1分)提高钴元素的利用率(或其他合理答案)(1分)
2
(2)6Fe2++6H++ClO- 6Fe3++Cl-+3HO
3 2
(3)取少许氧化后的溶液于试管中滴加几滴铁氰化钾溶液,若无蓝色沉淀生成,则说明Fe2+已全部被氧化
(4) 6Fe3++4SO2-+6HO+2Na++6CO2- =NaFe(SO)(OH) ↓+6CO↑
4 2 3 2 6 4 4 12 2
(5)防止因温度降低,CoCl 晶体析出
2
【解析】(1)含钴废催化剂中含有的Fe、Co均可溶于硫酸,而SiO 不溶,所以滤渣的是SiO ,洗涤滤
2 2
渣的洗涤液中含有钴的化合物,为了提高钴元素的利用率,将洗液与滤液合并;
本题答案为:SiO ,提高钴元素的利用率;
2
(2)在加热搅拌条件下加入NaClO,将Fe2+氧化成Fe3+,反应的离子方程式是:6Fe2++6H++ClO- 6Fe3+
3 3
+Cl-+3HO;
2
本题答案为:6Fe2++6H++ClO- 6Fe3++Cl-+3HO;
3 2
(3)依据所给信息,Fe2+和[Fe(CN)]3−反应,生成蓝色Fe[Fe(CN)] 沉淀,故确定Fe2+是否氧化完全的方
6 3 6 2
法是:取少许氧化后的溶液于试管中滴加几滴铁氰化钾溶液,若无蓝色沉淀生成,则说明Fe2+已全部被氧
化;
本题答案为:取少许氧化后的溶液于试管中滴加几滴铁氰化钾溶液,若无蓝色沉淀生成,则说明Fe2+已全
部被氧化;
(4)氧化后的溶液中,含有Fe3+,加入NaCO 后,生成[NaFe(SO)(OH) ]沉淀和CO 气体,离子方程式为:
2 3 2 6 4 4 12 2
6Fe3++4SO2-+6HO+2Na++6CO2- =NaFe(SO)(OH) ↓+6CO↑;
4 2 3 2 6 4 4 12 2
本题答案为:6Fe3++4SO2-+6HO+2Na++6CO2- =NaFe(SO)(OH) ↓+6CO↑;
4 2 3 2 6 4 4 12 2
(5)由CoCl 的溶解度曲线可知,随温度的升高,CoCl 的溶解度增大,所以趁热过滤,防止温度降低
2 2
CoCl 晶体析出;
2
本题答案为:防止因温度降低,CoCl 晶体析出。
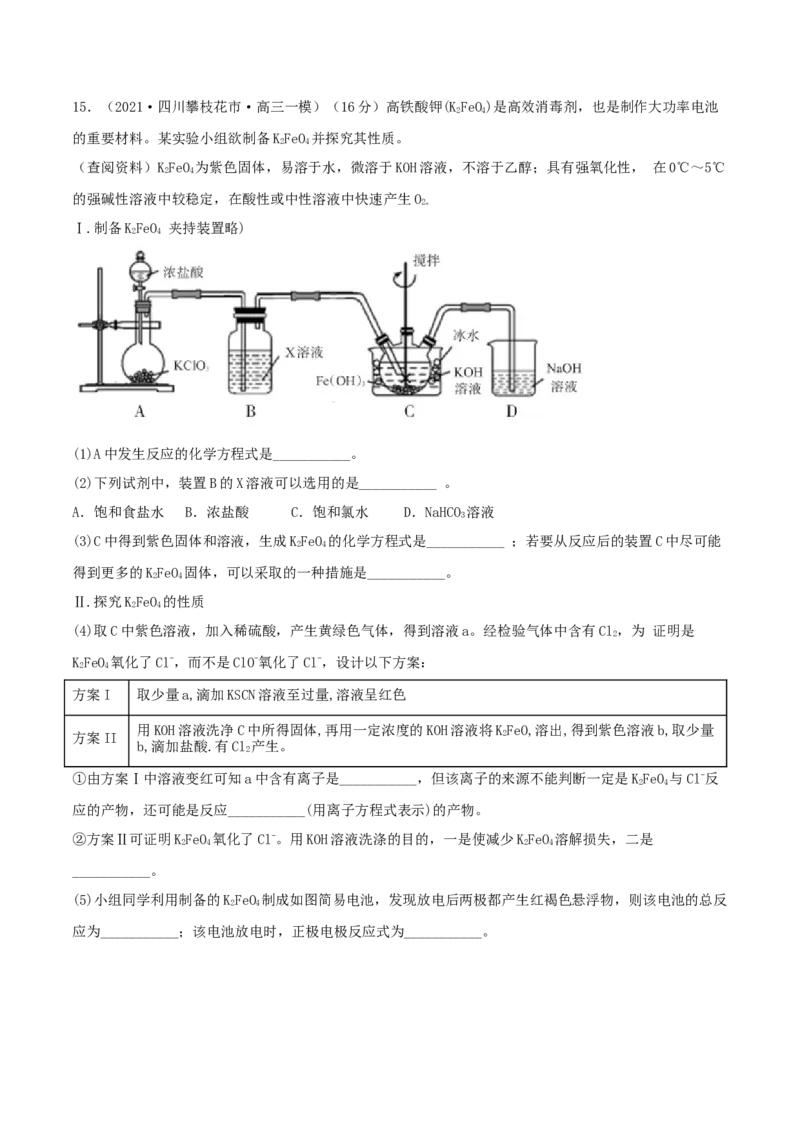
215.(2021·四川攀枝花市·高三一模)(16分)高铁酸钾(KFeO)是高效消毒剂,也是制作大功率电池
2 4
的重要材料。某实验小组欲制备KFeO 并探究其性质。
2 4
(查阅资料)KFeO 为紫色固体,易溶于水,微溶于KOH溶液,不溶于乙醇;具有强氧化性, 在0℃~5℃
2 4
的强碱性溶液中较稳定,在酸性或中性溶液中快速产生O
2。
Ⅰ.制备KFeO 夹持装置略)
2 4
(1)A中发生反应的化学方程式是___________。
(2)下列试剂中,装置B的X溶液可以选用的是___________ 。
A.饱和食盐水 B.浓盐酸 C.饱和氯水 D.NaHCO 溶液
3
(3)C中得到紫色固体和溶液,生成KFeO 的化学方程式是___________ ;若要从反应后的装置C中尽可能
2 4
得到更多的KFeO 固体,可以采取的一种措施是___________。
2 4
Ⅱ.探究KFeO 的性质
2 4
(4)取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得到溶液a。经检验气体中含有Cl,为 证明是
2
KFeO 氧化了Cl-,而不是ClO-氧化了Cl-,设计以下方案:
2 4
方案I 取少量a,滴加KSCN溶液至过量,溶液呈红色
用KOH溶液洗净C中所得固体,再用一定浓度的KOH溶液将KFeO,溶出,得到紫色溶液b,取少量
方案II 2
b,滴加盐酸.有Cl 产生。
2
①由方案Ⅰ中溶液变红可知a中含有离子是___________,但该离子的来源不能判断一定是KFeO 与Cl-反
2 4
应的产物,还可能是反应___________(用离子方程式表示)的产物。
②方案Ⅱ可证明KFeO 氧化了Cl-。用KOH溶液洗涤的目的,一是使减少KFeO 溶解损失,二是
2 4 2 4
___________。
(5)小组同学利用制备的KFeO 制成如图简易电池,发现放电后两极都产生红褐色悬浮物,则该电池的总反
2 4
应为___________;该电池放电时,正极电极反应式为___________。【答案】(除标注外,每空2分)(1)KClO + 6HCl(浓)=KCl +3Cl↑+ 3HO
3 2 2
(2) AC 3Cl + 2Fe(OH) +10KOH =2KFeO + 6KCl + 8HO
2 3 2 4 2
(3) 加入乙醇(1分)
(4)①Fe3+(1分)4FeO + 20H+=4Fe3++3O↑+10HO ②除尽KFeO 表面吸附的ClO﹣,防止ClO﹣与Cl﹣在酸
2 2 2 4
性条件下反应产生Cl,避免ClO﹣干扰实验
2
(5)Fe + KFeO + 4HO=2Fe(OH) + 2KOH FeO + 4HO +3e﹣= Fe(OH) + 5OH﹣
2 4 2 3 2 3
【解析】装置A是制取氯气,反应方程式;KClO + 6HCl(浓)=KCl +3Cl↑+ 3HO,得到的氯气中混有HCl
3 2 2
杂质气体,经装置B除杂,纯净的氯气通入装置C中发生反应:3Cl + 2Fe(OH) +10KOH =2KFeO + 6KCl +
2 3 2 4
8HO,用装置D来吸收过量的尾气中有毒的氯气。
2
(1)装置A中是氯元素发生归中反应,发生反应的化学方程式是:KClO + 6HCl(浓)=KCl +3Cl↑+ 3HO;
3 2 2
(2) 装置B是为了除去氯气中的HCl气体,A.饱和食盐水能溶解HCl,可选;B.浓盐酸有挥发性,氯气
中还混有HCl杂质,不选;C.饱和氯水能减小氯气的溶解,能溶解HCl,可选;D.NaHCO 溶液可与HCl反
3
应产生CO,氯气中混有杂质气体,不选;则X溶液可以选用的是:AC;
2
(3) C中得到紫色固体和溶液,C中通入氯气将氢氧化亚铁氧化,生成高铁酸钾(KFeO),化学方程式为:
2 4
3Cl + 2Fe(OH) +10KOH =2KFeO + 6KCl + 8HO;已知KFeO 不溶于乙醇,为了析出更多固体,措施是:
2 3 2 4 2 2 4
加入乙醇;
(4) ①i.Fe3+离子与SCN-发生络合反应,生成红色的络离子,由方案I中溶液变红可知溶液a中含有
Fe3+离子;但该离子的存在不能判断一定是KFeO,氧化了Cl,因为KFeO 在酸性溶液中不稳定,KFeO 在
2 4 2 2 4 2 4
酸性溶液中发生反应的离子方程式4FeO + 20H+=4Fe3++3O↑+10HO;
2 2
②方案Ⅱ可证明KFeO,氧化了Cl-,用KOH溶液洗涤的目的是确保KFeO 在碱性环境中的稳定性,同时除
2 4 2 4
尽KFeO 表面吸附的ClO﹣,防止ClO﹣与Cl﹣在酸性条件下反应产生Cl,避免ClO﹣干扰实验;
2 4 2
(5) 放电时为原电池原理,电池中Fe与KFeO 反应生成Fe(OH),该电池放电时的总反应为
2 4 3
Fe+KFeO+4HO=2Fe(OH)+2KOH,正极为FeO 得3mol电子生成Fe(OH),电极反应式为:FeO + 4HO
2 4 2 3 3 2+3e﹣= Fe(OH) + 5OH﹣。
3