文档内容
第 09 讲 铁及其重要化合物
第一部分:高考真题感悟
1.(2021·河北·高考真题)“灌钢法”是我国古代劳动人民对钢铁冶炼技术的重大贡献,陶弘景在其《本
草经集注》中提到“钢铁是杂炼生鍒作刀镰者”。“灌钢法”主要是将生铁和熟铁(含碳量约0.1%)混合加
热,生铁熔化灌入熟铁,再锻打成钢。下列说法错误的是
A.钢是以铁为主的含碳合金
B.钢的含碳量越高,硬度和脆性越大
C.生铁由于含碳量高,熔点比熟铁高
D.冶炼铁的原料之一赤铁矿的主要成分为Fe O
2 3
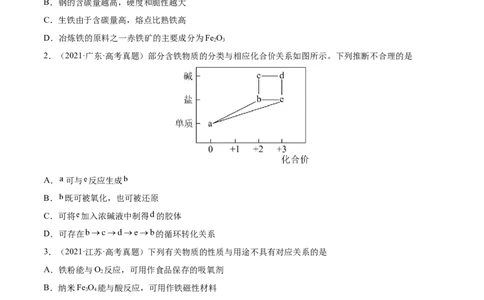
2.(2021·广东·高考真题)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是
A. 可与 反应生成
B. 既可被氧化,也可被还原
C.可将 加入浓碱液中制得 的胶体
D.可存在 的循环转化关系
3.(2021·江苏·高考真题)下列有关物质的性质与用途不具有对应关系的是
A.铁粉能与O 反应,可用作食品保存的吸氧剂
2
B.纳米Fe O 能与酸反应,可用作铁磁性材料
3 4
C.FeCl 具有氧化性,可用于腐蚀印刷电路板上的Cu
3
D.聚合硫酸铁能水解并形成胶体,可用于净水
4.(2022·浙江·高考真题)关于化合物 的性质,下列推测不合理的是
A.与稀盐酸反应生成 、 、
B.隔绝空气加热分解生成FeO、 、C.溶于氢碘酸(HI),再加 萃取,有机层呈紫红色
D.在空气中,与 高温反应能生成
5.(2022·广东·高考真题)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放
入酸化的 溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是
A.加入 溶液产生沉淀 B.加入淀粉碘化钾溶液无蓝色出现
C.加入 溶液无红色出现 D.加入 溶液无蓝色沉淀生成
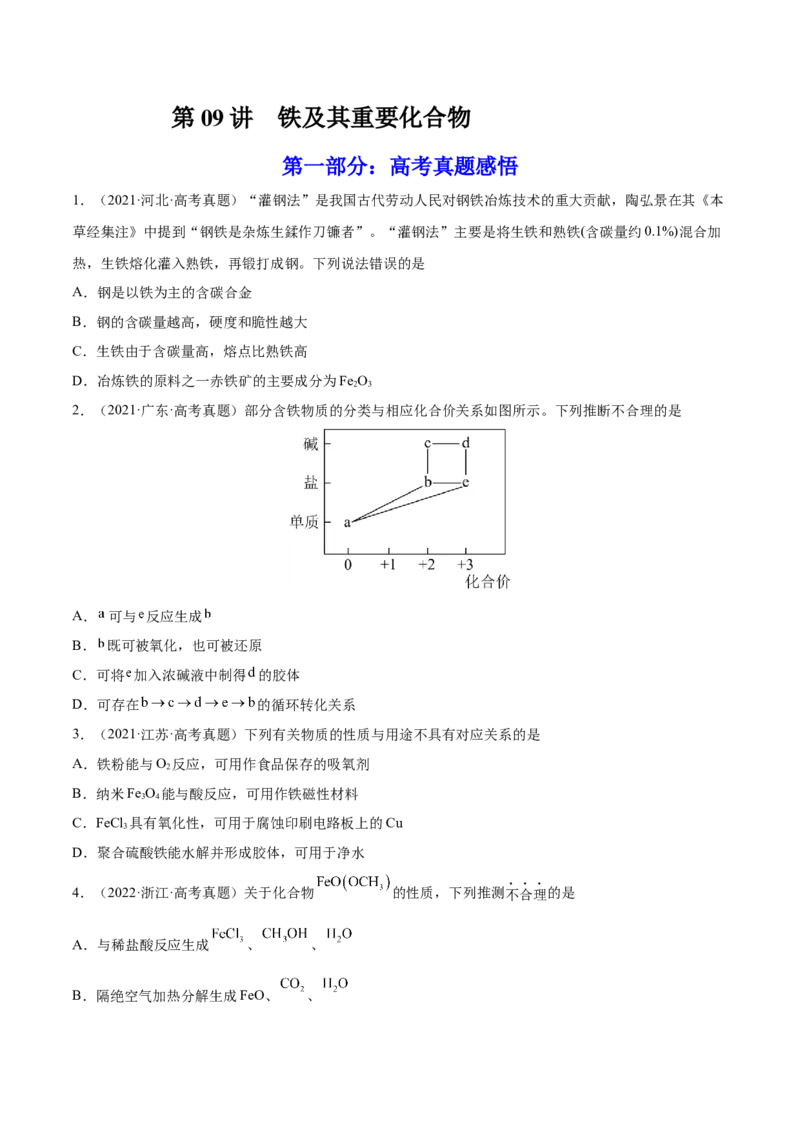
6.(2022·河北·高考真题)以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝
颜料。工艺流程如下:
回答下列问题:
(1)红渣的主要成分为_______(填化学式),滤渣①的主要成分为_______(填化学式)。
(2)黄铁矿研细的目的是_______。
(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(4)工序①的名称为_______,所得母液循环使用。
(5)沉铁工序产生的白色沉淀 中 的化合价为_______,氧化工序发生反应的离子方程式
为_______。
(6)若用还原工序得到的滤液制备 和 ,所加试剂为_______和_______(填化学式,不
引入杂质)。
第二部分:最新模拟精练完卷时间:50分钟
可能用到的相对原子质量:O16 S32 Fe56
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·湖北·襄阳四中模拟预测)下列有关Fe、Co、Ni及其化合物的说法错误的是
A.Fe、 Co、Ni 均位于第四周期第VIII族
B.Fe、 Co、Ni 基态原子未成对电子数分别为4、3、2
C.Fe、 Co、Ni以及它们的合金为黑色金属材料
D.FeO 在空气中受热会迅速变为Fe O
3 4
2.(2022·江苏·扬州中学三模)下列铁及其化合物的性质与用途不具有对应关系的是
A.金属Fe具有导热性,可用于制造炊具
B.纳米Fe O 颗粒呈黑色,可用作磁性材料
3 4
C.Fe(OH) 胶 体具有吸附性,可用作净水剂
3
D.FeCl 溶液具有氧化性,可用于蚀刻铜制品
3
3.(2022·上海静安·二模)指定条件下,以铁为原料,不能一步制得的是
A.Fe FeCl B.Fe Fe O
3 2 3
C.Fe Fe(NO ) D.Fe FeSO
3 3 4
4.(2022·上海普陀·二模)一定量的某磁黄铁矿(主要成分Fe S,S为-2价)与100mL盐酸恰好完全反应(杂
x
质不与盐酸反应),生成0.1mol硫单质、0.4molFeCl 和一定量HS气体,且溶液中无Fe3+。有关说法正确
2 2
的是
A.c(HCl)=4.0mol·L-1 B.x=0.85
C.生成了0.4molHS D.Fe S中,n(Fe2+)∶n(Fe3+)=2∶1
2 x
5.(2022·吉林长春·模拟预测)《天工开物》中“治铁"原典中记载:“凡治铁成器,取已炒熟铁为
之……凡炉中炽铁用炭,煤炭居十七,木炭居十三……即用煤炭也别有铁炭一种,取其火性内攻、焰不虚
腾者,与炊炭同行而有分类也……”。下列说法正确的是
A.熟铁是纯净的铁单质,生铁是铁和碳的混合物
B.治铁过程只涉及化合反应与置换反应,
C.铁炭和炊炭均为碳元素的同素异形体
D.治铁用到的煤炭和木炭均可还原铁的氧化物
6.(2022·江苏省平潮高级中学模拟预测)一种利用废旧镀锌铁皮制备磁性Fe O 纳米粒子的工艺流程如下。
3 4下列有关说法不正确的是
A.“碱洗”主要是为了去除废旧镀锌铁皮中的锌
B.“氧化”后的溶液中金属阳离子主要有Fe3+、Na+
C.“氧化”时发生反应的离子方程式为2Fe2++ClO-+2H+=2Fe3++Cl-+H O
2
D.用激光笔照射“加热沉铁”后所得分散系,产生丁达尔效应
7.(2022·上海上海·模拟预测)硫酸铁溶液中加入少量Fe粉,溶液颜色变浅,要证明该过程发生了氧化
还原反应,加入下列试剂一定可行的是
A.KSCN溶液 B.酸性高锰酸钾溶液
C.NaOH溶液 D.铜粉
8.(2022·上海普陀·二模)向NH Fe(SO )(aq)中逐滴滴加Ba(OH) (aq)至过量的过程中,有关离子反应错
4 4 2 2
误的是
A.2Fe3++3 +3Ba2++6OH-→2Fe(OH) ↓+3BaSO↓
3 4
B.Fe3++5 +4 +4Ba2++8OH-→Fe(OH) ↓+5NH ·H O+4BaSO↓
3 3 2 4
C.3Fe3++ +5 +5Ba2++10OH-→3Fe(OH) ↓+NH ·H O+5BaSO↓
3 3 2 4
D.Fe3++ +2 +2Ba2++4OH-→Fe(OH) ↓+NH ·H O+2BaSO↓
3 3 2 4
9.(2022·上海金山·二模)某溶液含Na+、NH 、SO 、Cl-、Fe2+、Fe3+中的几种,且各离子浓度相同。为
确定其组成,进行实验:①取少量溶液,加入足量HNO 酸化的Ba(NO )(aq),产生白色沉淀,过滤;②向
3 3 2
滤液中加入足量的NaOH(aq),产生红褐色沉淀,微热,产生气体。
关于原溶液的说法正确的是
A.不能确定是否有Fe3+ B.需通过焰色反应确定Na+是否存在
C.Fe2+、Fe3+都存在 D.存在NH 、SO 、Cl-、Fe2+
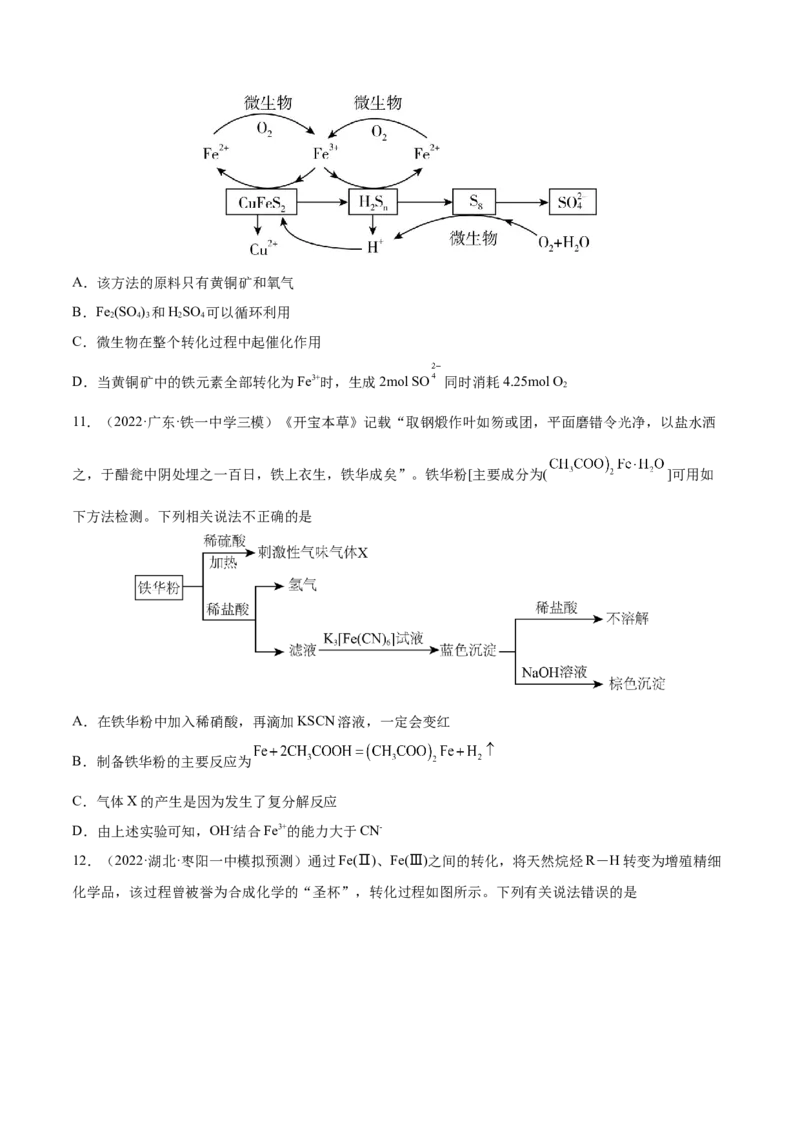
10.(2022·山东省实验中学模拟预测)微生物法浸出黄铜矿(CuFeS,其中Cu为+2价)中铜元素的过程如
2
图。下列说法错误的是A.该方法的原料只有黄铜矿和氧气
B.Fe (SO ) 和HSO 可以循环利用
2 4 3 2 4
C.微生物在整个转化过程中起催化作用
D.当黄铜矿中的铁元素全部转化为Fe3+时,生成2mol SO 同时消耗4.25mol O
2
11.(2022·广东·铁一中学三模)《开宝本草》记载“取钢煅作叶如笏或团,平面磨错令光净,以盐水洒
之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣”。铁华粉[主要成分为( ]可用如
下方法检测。下列相关说法不正确的是
A.在铁华粉中加入稀硝酸,再滴加KSCN溶液,一定会变红
B.制备铁华粉的主要反应为
C.气体X的产生是因为发生了复分解反应
D.由上述实验可知,OH-结合Fe3+的能力大于CN-
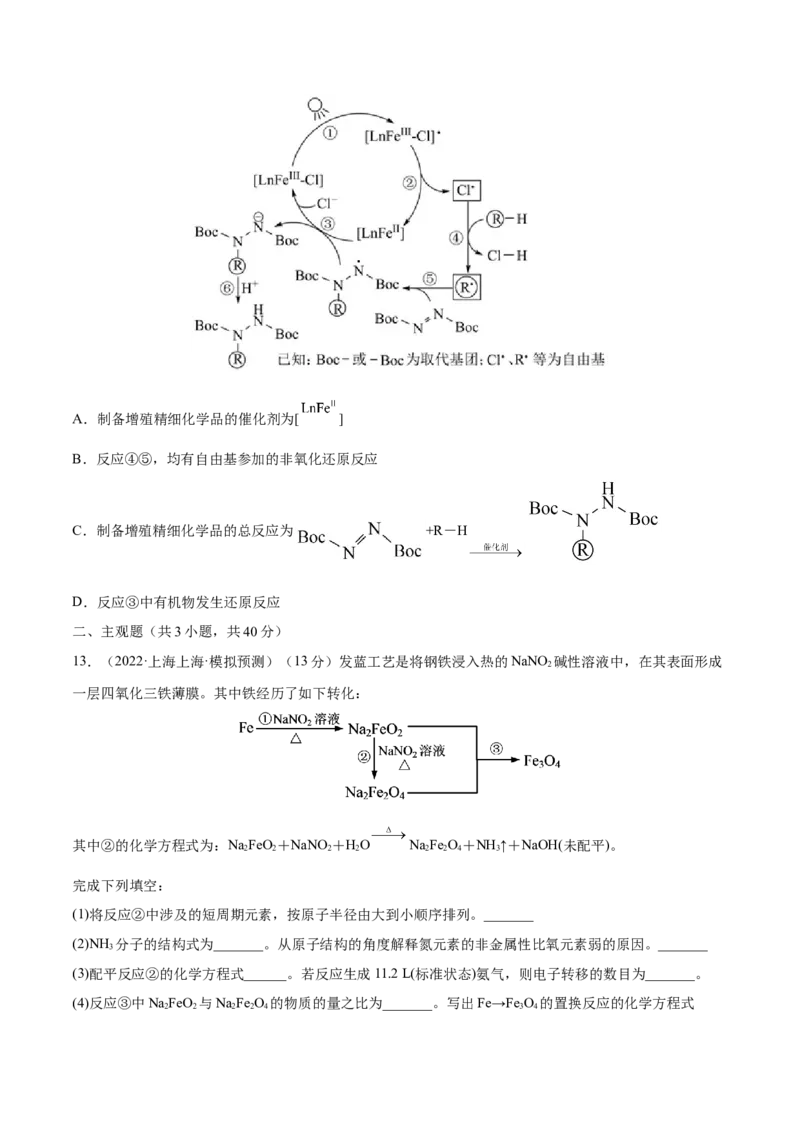
12.(2022·湖北·枣阳一中模拟预测)通过Fe(Ⅱ)、Fe(Ⅲ)之间的转化,将天然烷烃R-H转变为增殖精细
化学品,该过程曾被誉为合成化学的“圣杯”,转化过程如图所示。下列有关说法错误的是A.制备增殖精细化学品的催化剂为[ ]
B.反应④⑤,均有自由基参加的非氧化还原反应
C.制备增殖精细化学品的总反应为 +R-H
D.反应③中有机物发生还原反应
二、主观题(共3小题,共40分)
13.(2022·上海上海·模拟预测)(13分)发蓝工艺是将钢铁浸入热的NaNO 碱性溶液中,在其表面形成
2
一层四氧化三铁薄膜。其中铁经历了如下转化:
其中②的化学方程式为:NaFeO+NaNO +HO NaFe O+NH ↑+NaOH(未配平)。
2 2 2 2 2 2 4 3
完成下列填空:
(1)将反应②中涉及的短周期元素,按原子半径由大到小顺序排列。_______
(2)NH 分子的结构式为_______。从原子结构的角度解释氮元素的非金属性比氧元素弱的原因。_______
3
(3)配平反应②的化学方程式______。若反应生成11.2 L(标准状态)氨气,则电子转移的数目为_______。
(4)反应③中NaFeO 与NaFe O 的物质的量之比为_______。写出Fe→Fe O 的置换反应的化学方程式
2 2 2 2 4 3 4_______
14.(2022·广东广东·一模)(13分)铁元素存在多种价态,且不同价态的铁元素在一定条件下可以相互
转化。
(1)向2 mL 1 mol/L的Fe(NO ) 溶液中加入2 mol/L的HSO 溶液至Fe2+恰好转化为Fe3+为止,写出反应的离
3 2 2 4
子方程式___________。
(2) 是一种新型水处理剂,将 溶液、 溶液与 溶液混合可得到 。
① 中铁元素的化合价为___________,当有 生成时,反应中转移的电子数目为
___________ 。
②发生相应反应的离子方程式为___________。
(3)某同学设计如图装置制备一定量的 ,并使其能在较长时间内存在。
①X不能是硝酸,原因是___________,装置4的作用是___________。
②实验开始时,开关 应___________(填“打开”成“关闭”);这样操作的目的是___________。
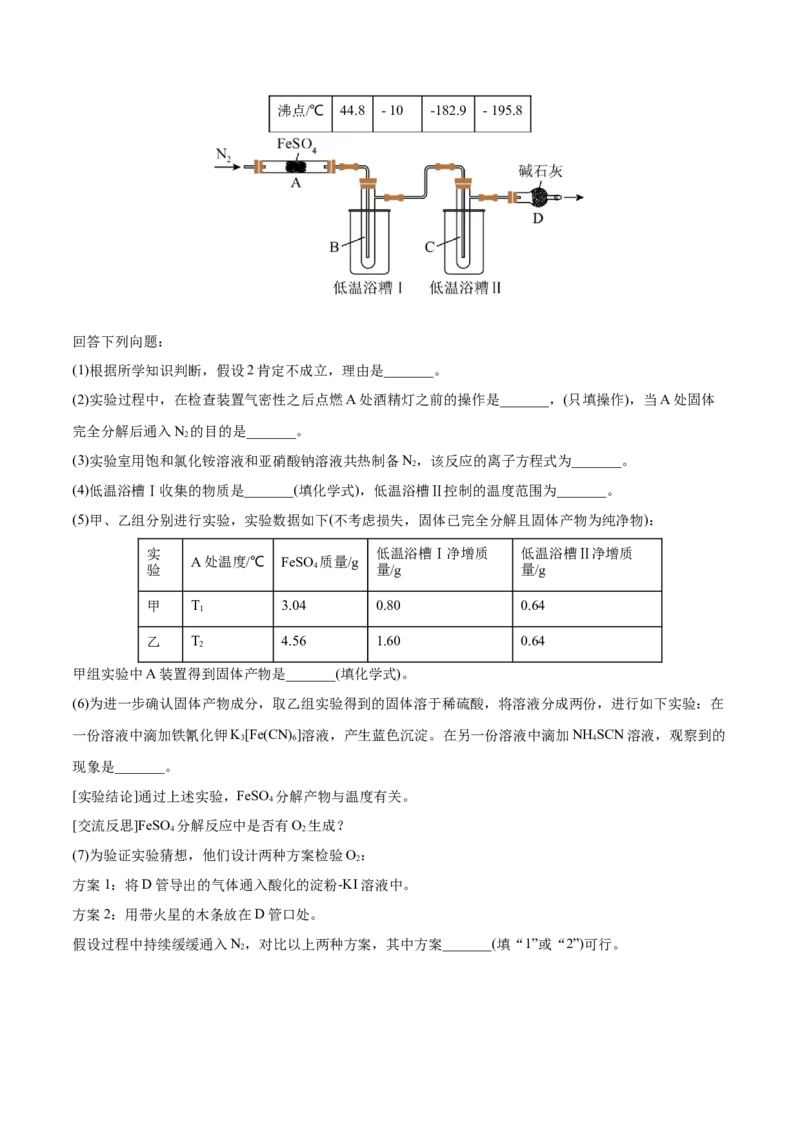
15.(2022·河南·二模)(14分)某学习小组拟研究FeSO 的分解实验探究,请你利用所学知识帮该小组
4
完成以下实验方案。
[实验目的]探究FeSO 分解产物与温度关系。
4
[提出假设]
假设1:Fe O、SO 、SO ;
2 3 3 2
假设2:FeO、SO 、SO ;
3 2
假设3:Fe O、SO 、SO 。
3 4 3 2
[查阅资料]几种物质的物理性质如表所示。
物质 SO SO O N
3 2 2 2
熔点/℃ 16.8 - 72.4 -218.4 -209.9沸点/℃ 44.8 - 10 -182.9 - 195.8
回答下列向题:
(1)根据所学知识判断,假设2肯定不成立,理由是_______。
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是_______,(只填操作),当A处固体
完全分解后通入N 的目的是_______。
2
(3)实验室用饱和氯化铵溶液和亚硝酸钠溶液共热制备N,该反应的离子方程式为_______。
2
(4)低温浴槽Ⅰ收集的物质是_______(填化学式),低温浴槽Ⅱ控制的温度范围为_______。
(5)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
实 低温浴槽Ⅰ净增质 低温浴槽Ⅱ净增质
A处温度/℃ FeSO 质量/g
验 4 量/g 量/g
甲 T 3.04 0.80 0.64
1
乙 T 4.56 1.60 0.64
2
甲组实验中A装置得到固体产物是_______(填化学式)。
(6)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在
一份溶液中滴加铁氰化钾K[Fe(CN) ]溶液,产生蓝色沉淀。在另一份溶液中滴加NH SCN溶液,观察到的
3 6 4
现象是_______。
[实验结论]通过上述实验,FeSO 分解产物与温度有关。
4
[交流反思]FeSO 分解反应中是否有O 生成?
4 2
(7)为验证实验猜想,他们设计两种方案检验O:
2
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N,对比以上两种方案,其中方案_______(填“1”或“2”)可行。
2