文档内容
第三章 金属及其化合物
第09讲 铁及其重要化合物(精讲)
【考情分析】
本讲内容为高考的高频考点,从分值来看,铁所占的比重最大,除铁是重要的金属元素外,还取决于
铁元素与生产生活的紧密联系,Fe、Fe2+、Fe3+之间的转化,以及所承载的氧化还原反应等重要知识点。
考查内容主要集中在“铁三角”,Fe与酸的反应,铁的变价、Fe(OH) 和Fe(OH) 的性质等。考查内容能在
2 3
多种题型中出现,选择、简答、实验、推断、计算都有。
【核心素养分析】
1.宏观辨识与微观探析:认识铁及其化合物的性质及应用,能以“铁三角”转化关系理解变价元素的转化
条件。
2.科学态度与社会责任:利用铁及其化合物的性质,科学认识铁及其化合物的提纯和制备工艺流程,形成
严谨求实的科学态度和崇尚真理的意识。
3.科学探究与创新意识:能提出有价值的氢氧化亚铁及其他铁的化合物的制备方案,并进行实验探究。
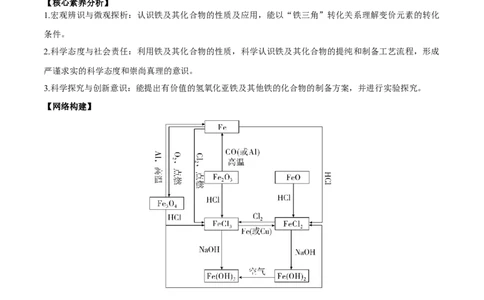
【网络构建】
【知识梳理】
知能点一 铁
1.位置:铁位于元素周期表中第4周期Ⅷ族,是一种应用最广泛的过渡金属元素;铁元素是一种典型的变
价金属元素。
2.结构3.铁的物理性质
银白色固体,熔点较高,具有良好的导热、导电、延展性,能被磁铁吸引。
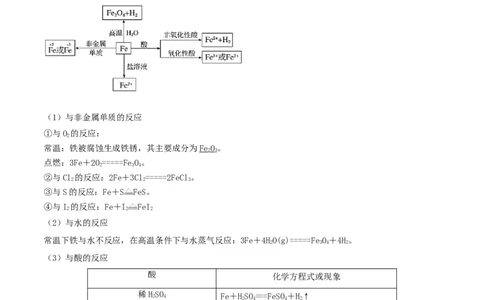
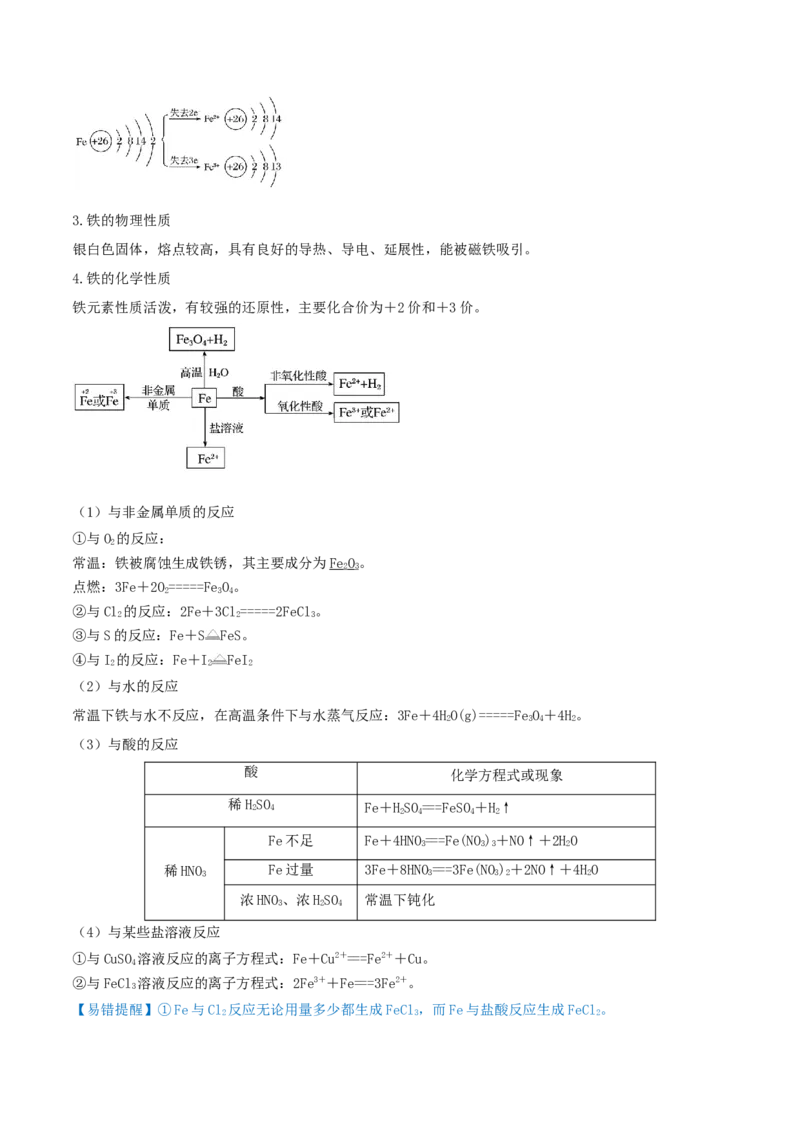
4.铁的化学性质
铁元素性质活泼,有较强的还原性,主要化合价为+2价和+3价。
(1)与非金属单质的反应
①与O 的反应:
2
常温:铁被腐蚀生成铁锈,其主要成分为FeO。
2 3
点燃:3Fe+2O=====FeO。
2 3 4
②与Cl 的反应:2Fe+3Cl=====2FeCl。
2 2 3
③与S的反应:Fe+S FeS。
④与I 的反应:Fe+I FeI
2 2 2
(2)与水的反应
常温下铁与水不反应,在高温条件下与水蒸气反应:3Fe+4HO(g)=====FeO+4H。
2 3 4 2
(3)与酸的反应
酸 化学方程式或现象
稀H 2 SO 4 Fe+H 2 SO 4 ===FeSO 4 +H 2 ↑
Fe不足 Fe+4HNO===Fe(NO)+NO↑+2HO
3 3 3 2
稀HNO Fe过量 3Fe+8HNO===3Fe(NO)+2NO↑+4HO
3 3 3 2 2
浓HNO、浓HSO 常温下钝化
3 2 4
(4)与某些盐溶液反应
①与CuSO 溶液反应的离子方程式:Fe+Cu2+===Fe2++Cu。
4
②与FeCl 溶液反应的离子方程式:2Fe3++Fe===3Fe2+。
3
【易错提醒】①Fe与Cl 反应无论用量多少都生成FeCl,而Fe与盐酸反应生成FeCl。
2 3 2②铁在潮湿的空气中生成的铁锈的主要成分是FeO,而铁在纯氧中燃烧的产物是FeO。
2 3 3 4
③铁与一般氧化剂(如S、HCl、FeCl 、CuSO 、I 等)反应时被氧化为Fe2+,铁与强氧化剂(如Cl 、Br 、
3 4 2 2 2
HNO、浓HSO 等)反应时被氧化为Fe3+。
3 2 4
④在电化学中铁作负极时电极反应式为Fe-2e-===Fe2+。
5.铁的冶炼
(1)原料:铁矿石、焦炭、空气、石灰石。
(2)设备:高炉。
(3)主要反应:
①还原剂的生成:C+O=====CO,CO+C=====2CO;
2 2 2
②铁的生成:FeO+3CO=====2Fe+3CO。
2 3 2
智能点二 铁的重要化合物
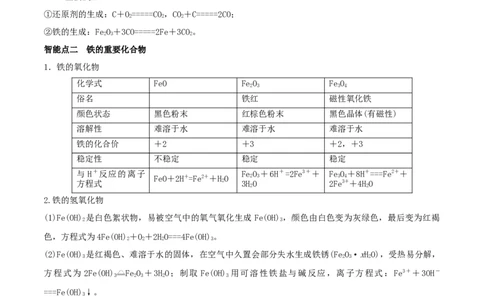
1.铁的氧化物
化学式 FeO FeO FeO
2 3 3 4
俗名 铁红 磁性氧化铁
颜色状态 黑色粉末 红棕色粉末 黑色晶体(有磁性)
溶解性 难溶于水 难溶于水 难溶于水
铁的化合价 +2 +3 +2,+3
稳定性 不稳定 稳定 稳定
与 H+反应的离子 FeO +6H+=2Fe3++ FeO +8H+===Fe2++
FeO+2H+=Fe2++HO 2 3 3 4
方程式 2 3HO 2Fe3++4HO
2 2
2.铁的氢氧化物
(1)Fe(OH) 是白色絮状物,易被空气中的氧气氧化生成 Fe(OH) ,颜色由白色变为灰绿色,最后变为红褐
2 3
色,方程式为4Fe(OH)+O+2HO===4Fe(OH)。
2 2 2 3
(2)Fe(OH) 是红褐色、难溶于水的固体,在空气中久置会部分失水生成铁锈(FeO·xHO),受热易分解,
3 2 3 2
方程式为 2Fe(OH) FeO +3HO;制取 Fe(OH) 用可溶性铁盐与碱反应,离子方程式:Fe3++3OH-
3 2 3 2 3
===Fe(OH)↓。
3
【易错提醒】①Fe(OH) 与硝酸反应不是发生中和反应生成盐和水,而是发生氧化还原反应3Fe(OH) +
2 2
10HNO=3Fe(NO)+NO↑+8HO。
3 3 3 2
②Fe(OH) 与氢碘酸(HI)反应不是发生中和反应生成盐和水,而是发生氧化还原反应2Fe(OH) +6HI=2FeI
3 3 2
+I+6HO。
2 2
(2)制法
①可溶性亚铁盐与强碱或氨水反应:Fe2++2OH-===Fe(OH)↓或Fe2++2NH·HO===Fe(OH)↓+2NH+。
2 3 2 2 4
注意:空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH),防止Fe(OH) 氧化的方法:
2 3 2A.将配制溶液的蒸馏水煮沸,驱除溶液中的氧气。
B.将盛有NaOH溶液的胶头滴管尖端插入盛有亚铁盐溶液的试管底部,并慢慢挤出NaOH溶液。
C.在亚铁盐溶液上面充入保护气,如H、N、稀有气体等。
2 2
D.在亚铁盐溶液上面加保护层,如苯、植物油等。
②可溶性铁盐与强碱或氨水反应:Fe3++3OH-===Fe(OH)↓或Fe3++3NH·HO===Fe(OH)↓+3NH+。
3 3 2 3 4
3.亚铁盐
(1)Fe2+的氧化性和还原性
含有Fe2+的溶液呈浅绿色,Fe2+处于铁的中间价态,既有氧化性,又有还原性,其中以还原性为主,如:
遇Br、Cl、HO、NO(H+)等均表现为还原性。
2 2 2 2
Fe2+的酸性溶液与HO 反应的离子方程式:2Fe2++HO+2H+===2Fe3++2HO。
2 2 2 2 2
(2)可水解
Fe(OH) 是弱碱,含Fe2+的盐(如硫酸亚铁)溶液呈酸性。配制硫酸亚铁溶液时常加少量硫酸抑制Fe2+的水
2
解,加少量铁屑防止Fe2+被氧化。
4.铁盐的性质及应用
(1)氧化性:含有Fe3+的溶液呈棕黄色,Fe3+处于铁的高价态,遇Fe、Cu、HI、HS等均表现为氧化性。
2
①Fe3+与S2-、I-、HS-、SO等具有较强还原性的离子不能大量共存。
②Fe3+可腐蚀印刷电路板上的铜箔,反应的离子方程式为2Fe3++Cu===Cu2++2Fe2+。
(2)易水解:Fe(OH) 是很弱的碱,且溶度积很小,因而Fe3+极易水解,只能存在于酸性较强的溶液中。
3
①利用Fe3+易水解的性质,实验室可用FeCl 滴入沸水中制取氢氧化铁胶体,反应的化学方程式:FeCl +
3 3
3HO Fe(OH)(胶体)+3HCl。
2 3
②利用Fe3+易水解的性质,工业上常用调节pH方法除去溶液中的铁离子。
③利用Fe3+易水解的性质,实验室配制氯化铁溶液,通常将氯化铁固体先溶于较浓的盐酸中,然后再稀释
至所需浓度。
④Fe3+与HCO、[Al(OH)]-、CO、ClO-等水解呈碱性的离子不能大量共存。
4
知能点三 Fe2+和Fe3+的检验
1.亚铁盐
(1)Fe2+的氧化性和还原性
①含有Fe2+的溶液呈浅绿色,Fe2+处于铁的中间价态,既有氧化性,又有还原性,其中以还原性为主,如
遇Br、Cl、HO、NO(H+)、MnO(H+)等均表现为还原性。
2 2 2 2
②Fe2+的酸性溶液与HO 反应的离子方程式:2Fe2++2H++HO===2Fe3++2HO
2 2 2 2 2
③向FeSO 溶液中滴加酸性KMnO 溶液,溶液褪色。反应的离子方程式:MnO+5Fe2++8H+===5Fe3++Mn2++
4 4
4HO。
2(2)可水解
Fe2+的盐(如硫酸亚铁)溶液因水解呈酸性。
2.铁盐
(1)氧化性:含有Fe3+的溶液呈黄色,Fe3+处于铁的高价态,遇Fe、Cu、HI、HS等均表现为氧化性。
2
①Fe3+与Cu反应的离子方程式:2Fe3++Cu===Cu2++2Fe2+。
②Fe3+与I-反应的离子方程式:2Fe3++2I-===2Fe2++I。
2
(2)特性:含有Fe3+的盐溶液遇到KSCN时变成血红色。
(3)易水解:Fe3+极易水解,只能存在于酸性较强的溶液中。
3.Fe2+、Fe3+的检验方法
(1)Fe2+的检验
方法1 ―――――――→无现象―――――――→溶液变红色,证明含有Fe2+
――――――――→产生白色絮状沉淀,迅速变成灰绿色,最终变为红褐色,证明含
方法2
有Fe2+
方法3 ―――――――――→生成蓝色沉淀,证明含有Fe2+
(2)Fe3+的检验
方法1 ――――――――→溶液变红色,证明含有Fe3+
方法2 ―――――――→产生红褐色沉淀,证明含有Fe3+
方法3 ―――――――――→生成蓝色沉淀,证明含有Fe3+
(3)混合溶液中Fe3+、Fe2+的检验
①Fe3+的检验
a.――→溶液变血红色,说明含有Fe3+
b.――→试纸变蓝色,说明含有Fe3+
②Fe2+的检验
a.――→KMnO 溶液褪色,说明含有Fe2+
4
b.――→溴水褪色,说明含有Fe2+
c.――→生成蓝色沉淀,说明含有Fe2+
【易错提醒】检验Fe2+和Fe3+时的注意事项
(1)检验Fe2+时不能先加氯水后加KSCN溶液,也不能将加KSCN后的混合溶液加入足量的新制氯水中(新制
氯水能氧化SCN-)。
(2)Fe3+、Fe2+、Cl-同时存在时不能用酸性KMnO 溶液检验Fe2+(Cl-能还原酸性KMnO,有干扰)。
4 4
知能点四 “铁三角”的转化关系及其应用
(1)“铁三角”的转化用离子方程式表现转化
①2Fe3++HS===2Fe2++S↓+2H+
2
②2Fe3++SO+2HO===2Fe2++4H++SO
2 2
③3Fe2++4H++NO===3Fe3++2HO+NO↑
2
④5Fe2++MnO+8H+===5Fe3++Mn2++4HO
2
⑤2Fe2++HO+2H+===2Fe3++2HO
2 2 2
(2)判断离子共存
Fe2+与NO(H+)、ClO-、MnO(H+)发生氧化还原反应,不能大量共存;
Fe3+与S2-、I-、SO发生氧化还原反应,不能大量共存;
Fe2+、Fe3+与HCO、CO等水解相互促进生成沉淀,不能大量共存。
(3)除杂
溶液 杂质 除杂方法
FeCl FeCl 加过量铁粉后过滤
2 3
FeCl FeCl 加氯水或HO
3 2 2 2
FeCl CuCl 加过量铁粉后过滤
2 2
(4)盐溶液的配制与保存
(5)物质的制备
【典例剖析】
高频考点1 考查铁及其化合物的性质与应用
例1.(2021·上海浦东新区·高三二模)在铁粉与水蒸气反应后的残留固体X中,加入足量的稀硫酸,
充分反应后得到溶液Y。下列说法正确的是
A.若X中含有铁,则反应时一定有气泡B.若向Y中滴入KSCN溶液显红色,则X中无铁
C.Y一定能使高锰酸钾溶液褪色
D.Y中滴入NaOH溶液,一定有沉淀产生
【解析】铁和水蒸气反应生成FeO 和氢气,残留固体为FeO 或FeO 和Fe的混合物。加入足量的稀硫酸,
3 4 3 4 3 4
FeO 和硫酸反应:FeO+4HSO=FeSO+Fe(SO)+4HO,若有铁剩余,由于氧化性:Fe3+>H+,所以还会依次
3 4 3 4 2 4 4 2 4 3 2
发生反应:Fe+Fe(SO)=3FeSO,Fe+HSO=FeSO+H↑。
2 4 3 4 2 4 4 2
A.若X中含有铁,但铁可能全部和Fe(SO) 反应,则没有气泡,故A错误;B.若向Y中滴入KSCN溶液显
2 4 3
红色,说明Y中含Fe3+,可能X中无铁,也可能X中铁不足以将Fe(SO) 全部转化为FeSO,故B错误;
2 4 3 4
C.不论X是FeO,还是FeO 和Fe的混合物,和硫酸反应后都有Fe2+,所以一定能使高锰酸钾溶液褪色,
3 4 3 4
故C正确;D.若硫酸过量,则向Y中滴入NaOH溶液,硫酸消耗了NaOH,则没有沉淀产生,故D错误;故
选C。
【答案】C
【名师点睛】本题考查氧化还原反应以及铁的单质化合物的性质,题目难度不大,本题关键是把握物质的
氧化性、还原性强弱判断反应的先后顺序。
【变式训练】(2021·上海青浦区·高三二模)春秋初年,我国已掌握了冶铁技术。下列有关铁的化学反应
的叙述正确的是
A.室温下,过量Fe与浓硫酸反应生成FeSO
4
B.加热时,过量Fe与氯气反应生成FeCl
2
C.高温下,铁与水蒸气反应有FeO 生成
3 4
D.高温下,铁粉与氧化铝粉末反应生成单质铝
【解析】A.室温下,Fe在浓硫酸中钝化,无法持续反应,A错误;B.氯气氧化性较强,无论Fe是否过量
与氯气加热反应都只生成FeCl,B错误;C.高温条件下,Fe与水蒸气反应得到FeO 和氢气,C正确;
3 3 4
D.Fe的活动性不如Al,不能从氧化铝中置换出Al单质,D错误;综上所述答案为C。
【答案】C
高频考点2 考查Fe2+、Fe3+ 的性质及其检验
例2.(2021·上海静安区·高三一模)欲证明某稀溶液中含有Fe2+而无Fe3+,必要的实验操作及最佳顺序
为
①滴加少量氯水②滴加足量碘水③滴加少量硫氰化钾溶液
A.①→③ B.③→② C.③→① D.①→②→③
【解析】Fe3+遇硫氰化钾溶液会变红色,欲证明某稀溶液中含有Fe2+而无Fe3+,可先滴加少量硫氰化钾溶液,同时,Fe2+易被氧化为Fe3+,氧化剂可以为:氯水,而碘水不能氧化Fe2+,故最佳顺序为③→①,答案选
C。
【答案】C
【易错警示】检验Fe2+和Fe3+时的注意事项
(1)检验Fe2+时不能先加氯水后加KSCN溶液;也不能将加KSCN后的混合溶液加入足量的新制氯水中(新制
氯水可能氧化SCN-)。
(2)Fe3+、Fe2+、Cl-同时存在时不能用酸性KMnO 溶液检验Fe2+(Cl-能还原酸性KMnO,有干扰)。
4 4
【变式训练】(2021·上海奉贤区·高三二模)要证明某久置的 溶液中是否还含有 ,以下最
适合的试剂是
A.KSCN溶液 B. 溶液 C.酸性 溶液 D. 溶液
【解析】A.三价铁离子遇到溶液或是KSCN溶液显红色,常用溶液或是KSCN溶液来检验三价铁离子,无法
检验Fe2+,故A错误;B.加入氯化钡,都生成白色沉淀,不能证明含有亚铁离子,故B错误;C.加入酸
性溶液,可氧化亚铁离子,能证明含有亚铁离子,故C正确;D.加入KI,Fe3+与I-反应,Fe2+与I-不反应,
不能证明含有亚铁离子,故D错误;故选C。
【答案】C
高频考点3 考查“铁三角”的转化及应用
例3.(2020·河北正定中学模拟)硫酸亚铁铵晶体[(NH )Fe(SO )·6H O]在空气中比一般亚铁盐稳定,
4 2 4 2 2
是定量分析化学中常用的还原剂,其实验室制备流程如图所示:
下列说法不正确的是( )
A.“除油污”过程中使用热的NaCO 溶液效果更好
2 3
B.制备硫酸亚铁时铁屑与硫酸反应完全时的现象是不再有气泡产生
C.“趁热过滤”后的滤液略显黄色的原因是4Fe2++O+4H+===4Fe3++2HO
2 2
D.理论上加入(NH )SO 固体的质量为6.0g
4 2 4
【解析】NaCO 溶液中CO水解使溶液呈碱性,油污在碱性环境中能够水解,升高温度,CO水解平衡正
2 3
向移动,溶液碱性增强,故用热的NaCO 溶液除油污效果更好,A项正确;为防止Fe2+被氧化,加入的铁
2 3
屑需过量,铁屑与硫酸反应完全就是硫酸反应完全,反应完全时不再有气泡产生,B项正确;“趁热过
滤”后的滤液略显黄色是因为Fe2+在空气中被氧气氧化为Fe3+,反应的离子方程式为4Fe2++O +4H+
2===4Fe3++2HO,C项正确;由工艺流程图可知,反应的铁的质量为 5.0g-2.2g=2.8g,物质的量为=
2
0.05mol,理论上可制备0.05mol硫酸亚铁铵晶体,则需要加入0.05mol(NH ) SO ,所以加入(NH )
4 2 4 4
SO 固体的质量为0.05mol×132g/mol=6.6g,D项错误。
2 4
【答案】D
【题后归纳】价类二维图在铁及其化合物转化中的应用
(1)横向变化体现了同价态不同类别(氧化物、碱、盐)之间的转化;
(2)纵向变化体现不同价态同类别物质之间的转化,主要体现物质的氧化性或还原性。
(3)斜向变化体现不同价态、不同类别之间物质的转化,主要体现物质的氧化物和还原性。
【变式训练】 (2020·青铜峡市高级中学月考)下列有关铁及其化合物的说法中不正确的是( )
A.为了防止氯化亚铁溶液久置变质,常在其溶液中加入少许铁钉
B.将饱和FeCl 溶液滴入沸水中,能形成胶体
3
C.新制的氢氧化亚铁沉淀露置在空气中最终会变为红褐色
D.除去FeCl 溶液中的FeCl 杂质可以向溶液中加铁粉,然后过滤
3 2
【解析】亚铁离子在空气中易被氧化为铁离子,加铁钉可以防止氯化亚铁溶液的变质,故 A正确;制备氢
氧化铁胶体的方法是将饱和FeCl 溶液滴入沸水中,产生红褐色即可,故B正确;新制的氢氧化亚铁沉淀
3
露置在空气中迅速变成灰绿色,最终会变为红褐色的氢氧化铁,故 C正确;除去FeCl 溶液中的FeCl 杂质
3 2
可以向溶液中滴加氯水,将氯化亚铁氧化为氯化铁,故D错误。
【答案】D
高频考点4 考查氢氧化亚铁的制备
例4.(2020·河北唐山市区县联考)下列各图示中能较长时间看到Fe(OH) 白色沉淀的是( )
2A.①②③④ B.①②③⑤
C.①③④⑤ D.②③④⑤
【解析】①铁与稀硫酸反应产生H ,排出了装置中的空气,烧杯中的水,隔绝空气中的氧气进入试管中,
2
然后滴加NaOH溶液,生成的Fe(OH) 能长时间存在,故①符合题意;②首先打开止水夹 a,铁粉与稀硫酸
2
反应生成H ,排出装置中的空气,以及NaOH溶液中的氧气,让装置处于H 氛围中,关闭止水夹,利用压
2 2
强,将FeSO 压入NaOH溶液中,生成氢氧化亚铁,Fe(OH) 能长时间观察,故②符合题意;③该装置为电解
4 2
装置,铁作阳极,电极反应式为Fe-2e-===Fe2+,C为阴极,电极反应式为O +4e-+2HO===4OH-汽油隔
2 2
绝空气中氧气的进入,能长时间观察到氢氧化亚铁,故③符合题意;④该装置,没有隔绝空气的进入,生
成氢氧化亚铁迅速转化成氢氧化铁,不能长时间观察到氢氧化亚铁,故④不符合题意;⑤苯能隔绝空气的
进入,能够长时间观察到氢氧化亚铁白色沉淀,故⑤符合题意;综上所述,选项B正确。
【答案】B
【反思归纳】防止Fe(OH) 氧化的方法
2
(1)将配制溶液的蒸馏水煮沸,驱除溶液中的氧气。
(2)将盛有NaOH溶液的胶头滴管尖端插入盛有亚铁盐溶液的试管底部,并慢慢挤出NaOH溶液。
(3)在亚铁盐溶液上面充入保护气,如H、N、稀有气体等。
2 2
(4)在亚铁盐溶液上面加保护层,如苯、植物油等。
【变式训练】(2020·山东淄博一中模拟)如图所示,此装置可用来制取和观察Fe(OH) 在空气中被氧
2
化的颜色变化。实验时必须使用铁屑和6mol·L-1的硫酸,其他试剂任选。填写下列空白:(1)B中盛有一定量的NaOH溶液,A中烧瓶内应预先加入的药品是 。A中反应的离子方程式是
_________________________________________________________________________________。
(2)实验开始时先将止水夹a (填“打开”或“关闭”)。
(3)简述生成Fe(OH) 的操作过程:___________________________________________________。
2
(4)实验完毕,打开 b 处止水夹,放入一部分空气,此时 B 中发生反应的化学方程式为
__________________。
【解析】Fe+2H+===Fe2++H↑,产生的H 将Fe2+压入B中,发生反应:Fe2++2OH-===Fe(OH) ↓;Fe
2 2 2
(OH) 在空气中很容易被氧化为红褐色的Fe(OH) ,即发生反应:4Fe(OH) +O +2HO===4Fe(OH)
2 3 2 2 2
。
3
【答案】(1)铁屑 Fe+2H+===Fe2++H↑
2
(2)打开
(3)待A装置反应一段时间后关闭止水夹a,产生的H 将FeSO 溶液压入B中进行反应
2 4
(4)4Fe(OH)+O+2HO===4Fe(OH)
2 2 2 3
高频考点5 考查有关铁及其化合物的计算
例5.(2020·郑州质检)有一块铁的“氧化物”样品,用140 mL 5.0 mol·L-1盐酸恰好将之完全溶解,所
得溶液还能吸收0.025 mol Cl,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
2
A.FeO B.FeO
2 3 3 4
C.FeO D.FeO
4 5 5 7
【解析】n(O)=n(HO)=n(HCl)=××5 mol=0.35 mol,n(Fe)=n(FeCl)=n(Cl-)=[n(HCl)+2n(Cl)]
2 3 2
=(×5+0.05) mol=0.25 mol,n(Fe)∶n(O)=0.25∶0.35=5∶7,即氧化物为FeO。
5 7
【答案】D
【方法归纳】确定铁的氧化物组成的基本方法
设铁的氧化物中铁元素与氧元素的质量比为m∶n,
则氧化物中n(Fe)∶n(O)=∶=a∶b,
若a∶b=1∶1,则铁的氧化物为FeO;
若a∶b=2∶3,则铁的氧化物为FeO;
2 3
若a∶b=3∶4,则铁的氧化物是FeO 或FeO与FeO 按物质的量之比为1∶1的混合物或FeO、FeO 、FeO
3 4 2 3 2 3 3 4的混合物(其中FeO、FeO 物质的量之比为1∶1,FeO 为任意值)。
2 3 3 4
【变式训练】(2020·河北唐山市区县联考)铁的常见化合价有+2价和+3价。据研究,铁在浓HNO 中发
3
生钝化时,可生成一种化学式为FeO 的化合物,它可以看作由FeO和FeO 组成的复杂氧化物。该化合物
8 11 2 3
可以表示为( )
A.FeO·3FeO B.FeO·2FeO
2 3 2 3
C.2FeO·3FeO D.2FeO·FeO
2 3 2 3
【解析】一般拆写成氧化物时,低价在前,高价在后,同时符合原子守恒; FeO·3FeO 中铁原子和氧原
2 3
子个数比为7∶10,不符合8∶11,故A不符合题意; FeO·2FeO 中铁原子和氧原子个数比为5∶7,不符
2 3
合8∶11,故B不符合题意; 2FeO·3FeO 中铁原子和氧原子个数比为8∶11,符合8∶11,故C符合题意;
2 3
2FeO·FeO 中铁原子和氧原子个数比为4∶5,不符合8∶11,故D不符合题意。
2 3
【答案】C
高频考点6、考查铁及其化合物性质的实验探究
例6.(2021·江苏常州市·高三二模)利用如下实验研究 与 的反应。
步骤1:向烧杯中加入10mL 0.1 的KI溶液,再滴加2mL 0.1 的 溶液,振荡,
把溶液分为四等份于编号为①②③④的四支试管中。
步骤2:向试管①中加入淀粉溶液,观察到溶液变蓝。
步骤3:向试管②中滴加15% KSCN溶液5~6滴,观察到溶液变红。
步骤4:向试管③、试管④中分别加入1mL 2.0 的 溶液和1mL的蒸馏水,振荡,观察到试
管③中溶液颜色比试管④中溶液颜色浅。
下列说法不正确的是
A.试管①中的现象说明此条件下 的氧化性大于
B.试管②中的现象说明 与 的反应为可逆反应
C.试管②中红色物质的组成为 ,此微粒中心离子的配位数为
D.步骤4的现象不能说明此条件下 能将 氧化成
【解析】A.向试管①中加入淀粉溶液,观察到溶液变蓝,则有碘单质生成,即此条件下 的氧化性大于 ,故A不选;B.由10mL 0.1 的KI溶液,再滴加2mL 0.1 的 溶液可知,
KI溶液过量;所以向试管②中滴加15% KSCN溶液5~6滴,观察到溶液变红,则溶液中含有铁离子,则说
明该反应为可逆反应,故B不选;C. 中心离子的配位数为n+(6-n)=6,故C不选;
D.向试管③、试管④中分别加入1mL 2.0 的 溶液和1mL的蒸馏水,振荡,观察到试管③
中溶液颜色比试管④中溶液颜色浅,则③中亚铁离子浓度小于④中亚铁离子浓度,说明亚铁离子与碘单质
发生反应,则能说明 能将 氧化成 ,故选D;答案选D。
【答案】D
【名师点睛】性质探究性实验方案的设计:主要是从物质的结构特点或从所属类型的典型代表物去推测物
质可能具有的一系列性质,而后据此设计出合理的实验方案,去探索它所可能具有的性质。设计的基本流
程为:根据物质的组成、结构和类型→提出性质猜想→设计实验逐个验证→记录现象和数据→归纳分析→
合理推断得出结论。
【变式训练】(2021·四川成都市·高三三模)将铁棒插入95%的浓硫酸中(如图所示),探究铁与浓硫酸
的反应。观察到立即产生大量的细腻气泡聚集在液体表面,犹如白色泡沫,由快变慢直至停止,酸液中出
现白色不溶物,静置后分层。下列说法错误的是
A.产生的气体可能是SO 和少量的H
2 2
B.取上层清液滴加少量饱和FeSO 溶液,有白色固体X析出,推测固体X可能是FeSO
4 4
C.反应过程中FeSO 的生成也可能使反应由快变慢
4
D.取反应后铁棒直接放入盛有KSCN溶液的烧杯中,可检验反应时是否有Fe3+生成
【解析】A.Fe和浓硫酸发生氧化还原反应:2Fe+6HSO(浓)=Fe(SO)+3SO↑+6HO,铁与稀硫酸会发生置
2 4 2 4 3 2 2
换反应:Fe+HSO=FeSO+H↑,所用浓硫酸的质量分数为95%,两个反应都可能发生,所以产生的气体可能
2 4 4 2
为SO 和少量的H,故A正确;B.上层清液滴加少量饱和FeSO 溶液,有白色固体X析出,说明此时溶液
2 2 4
中原有溶质已经过饱和,则固体X可能是FeSO,故B正确;C.铁和浓硫酸生成硫酸铁,硫酸铁和铁单质
4
反应生成FeSO:Fe+Fe(SO)=3FeSO,反应生成的FeSO 浓度过大,已经过饱和,会阻碍反应继续进行,
4 2 4 3 4 4可能使反应由快变慢,故C正确;D.反应后的铁棒上沾有浓硫酸,直接放入KSCN溶液的烧杯中,会发生
铁和稀硫酸的置换反应,同时铁和硫酸铁会发生反应:Fe+Fe(SO)=3FeSO,所以用此方法不能检验反应
2 4 3 4
时是否有Fe3+生成,故D错误;故选D。
【答案】D