文档内容
第十二讲 铜及其重要化合物 无机化工流程
【基础巩固】
1.某研究小组通过实验探究Cu及其重要化合物的性质,下列操作正确且能达到目的的是( )
A.将铜丝插入浓硫酸中加热,反应完后把水加入反应器中,观察硫酸铜溶液的颜色
B.常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl 的生成
2
C.将CuCl 溶液在蒸发皿中加热蒸干,得到无水CuCl 固体
2 2
D.将表面有铜绿的铜器放入稀盐酸中浸泡,除去铜绿
2.(2020·全国卷Ⅲ,7)宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自
孔雀石颜料[主要成分为Cu(OH) ·CuCO],青色来自蓝铜矿颜料[主要成分为Cu(OH) ·2CuCO]。下列说法
2 3 2 3
错误的是( )
A.保存《千里江山图》需控制温度和湿度 B.孔雀石、蓝铜矿颜料不易被空气氧化
C.孔雀石、蓝铜矿颜料耐酸耐碱 D.Cu(OH) ·CuCO 中铜的质量分数高于Cu(OH) ·2CuCO
2 3 2 3
3.我国古代“药金”的冶炼方法是将炉甘石(ZnCO)和赤铜矿(Cu O)与木炭按一定的比例混合后加热至
3 2
800 ℃,即可炼出闪烁似金子般光泽的“药金”。下列叙述正确的是( )
A.“药金”实质上是铜锌合金 B.冶炼炉中炉甘石直接被木炭还原为锌
C.用王水可区别黄金和“药金” D.用火焰灼烧不能区别黄金和“药金”
4.人类最早冶金的历史年代曲线图如图所示(-1000表示公元前1000年)。下列说法正确的是( )
A.金属越活泼,冶炼的年代一定越晚
B.冶炼金属的历史:电解氯化物比电解氧化物早
C.自然界中铜元素以游离态形式存在,故铜的冶炼年代最早
D.金属氧化物(如Al O、Cu O)也属于金属材料
2 3 2
5.(2022·湖南,7)铝电解厂烟气净化的一种简单流程如下:
下列说法错误的是( )
A.不宜用陶瓷作吸收塔内衬材料 B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有NaAlF 和CO D.滤液可回收进入吸收塔循环利用
3 6 26.(2022·陕西榆林模拟)水合肼(N H·H O)的性质类似氨水。利用水合肼处理铜氨{[Cu(NH )]2+}
2 4 2 3 4
废液回收铜粉的实验流程如图:
下列说法错误的是( )
A.上述三步反应过程均为氧化还原反应
B.反应1的目的是制备NaClO
C.合成水合肼的反应中每消耗1 mol CO(NH ) 转移电子数为N
2 2 A
D.反应3完成后要用到过滤操作
7.(2023·北京·高三专题练习)氯化亚铜(CuCl)是白色粉末,微溶于水,广泛应用于化工和印染等行业。
某研究性学习小组模拟热分解CuCl •2H O制备CuCl的过程,并进行相关物质转化的探究。
2 2
已知:酸性条件下Cu+不稳定
下列说法不正确的是
A.X气体是HCl,可抑制CuCl •2H O加热时水解
2 2
B.途径1中产生的Cl 可以回收利用,也可以通入饱和NaOH溶液中除去
2
C.途径2中200℃时反应的化学方程式为Cu (OH) Cl 2CuO+2HCl↑
2 2 2
D.CuCl与稀硫酸反应的离子方程式为2Cu++4H++SO =2Cu2++SO↑+2H O
2 2
8.(2023.全国甲卷) 是一种压电材料。以 为原料,采用下列路线可制备粉状 。
回答下列问题:
(1)“焙烧”步骤中碳粉的主要作用是_______。
(2)“焙烧”后固体产物有 、易溶于水的 和微溶于水的 。“浸取”时主要反应的离子方
程式为_______。(3)“酸化”步骤应选用的酸是_______(填标号)。
a.稀硫酸 b.浓硫酸 c.盐酸 d.磷酸
(4)如果焙烧后的产物直接用酸浸取,是否可行?_______,其原因是_______。
(5)“沉淀”步骤中生成 的化学方程式为_______。
(6)“热分解”生成粉状钛酸钡,产生的 _______。
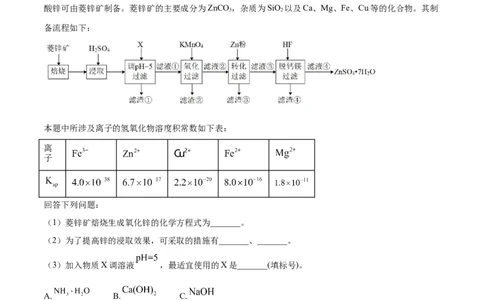
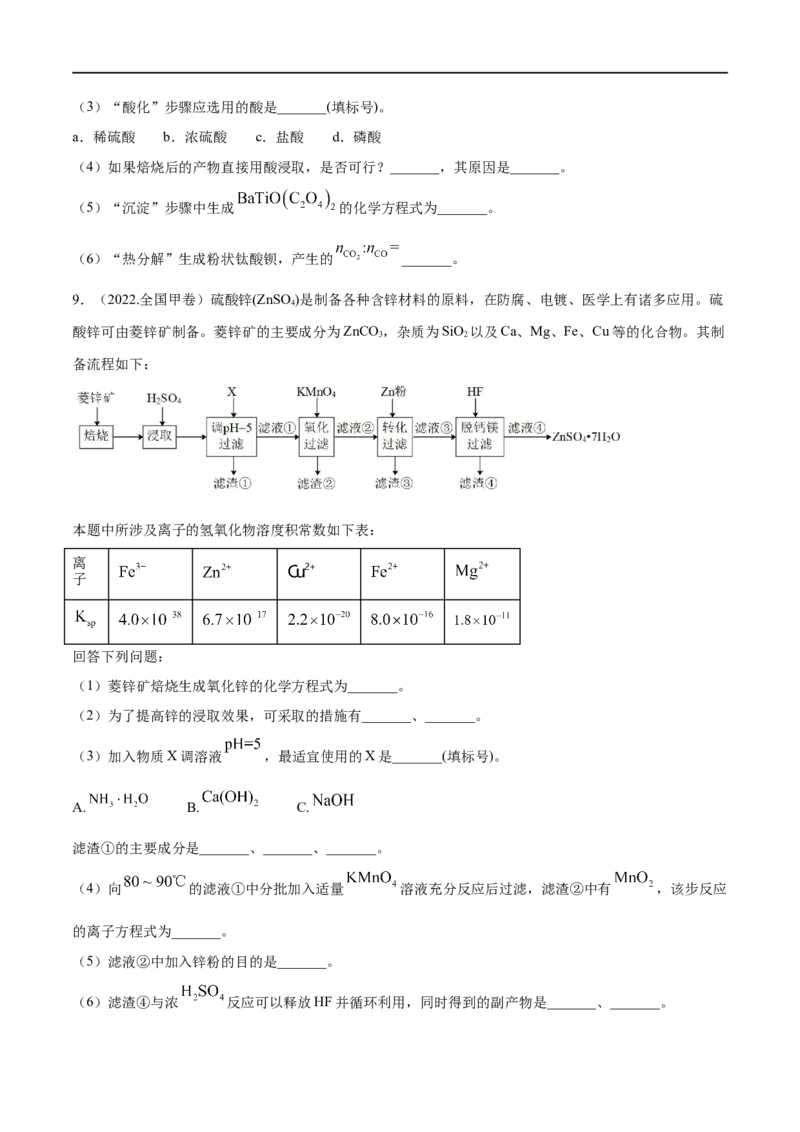
9.(2022.全国甲卷)硫酸锌(ZnSO)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫
4
酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等的化合物。其制
3 2
备流程如下:
本题中所涉及离子的氢氧化物溶度积常数如下表:
离
子
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
(3)加入物质X调溶液 ,最适宜使用的X是_______(填标号)。
A. B. C.
滤渣①的主要成分是_______、_______、_______。
(4)向 的滤液①中分批加入适量 溶液充分反应后过滤,滤渣②中有 ,该步反应
的离子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
(6)滤渣④与浓 反应可以释放HF并循环利用,同时得到的副产物是_______、_______。【拔高练习】
1.氯化亚铜(CuCl)是一种微溶于水、难溶于乙醇、易被氧化的白色粉末,以黄铜矿(主要成分为CuFeS)为
2
原料制取CuCl的流程如图所示:
已知:在水溶液中存在平衡:CuCl(s)+2Cl-(aq)[CuCl ]2-(aq)。下列说法错误的是( )
3
A.“浸取”后所得浸取液可用来腐蚀铜制电路板
B.加入浓盐酸的目的是为了实现CuCl的净化
C.[CuCl ]2-中加水可使平衡CuCl(s)+2Cl-(aq)[CuCl ]2-(aq)逆向移动
3 3
D.采用乙醇洗涤和真空干燥有利于提高CuCl的产率和纯度
2.(2022·四川广元高三模拟)含铬废水会严重污染环境,一种烟气协同处理含铬废水(含CrO、Cr O、泥沙
2
等)的流程如图:
下列说法不正确的是( )
A.“沉降”的主要目的是除去泥沙等不溶物
B.溶液A通常选用硫酸“调pH”,目的是将CrO转化为Cr O
2
C.“还原”过程涉及的氧化还原反应,氧化剂与还原剂的物质的量之比为2∶3
D.母液经处理可获得 SO
2 4
3.(2023·银川高三模拟)工业上以碳酸锰矿(主要成分为MnCO ,另含FeO、Fe O 、CaO等杂质)为主要原
3 2 3
料生产锰酸锂(LiMn O),工艺流程如下:
2 4
下列说法错误的是( )
A.可采用搅拌的方法提高“酸浸”时碳酸锰矿的浸出速率
B.加入CaO的目的是调节pH,使Fe3+转化为Fe(OH) 除去
3
C.“合成MnO ”的化学方程式为MnSO +KSO+2HO===MnO↓+KSO +2HSO
2 4 2 2 8 2 2 2 4 2 4
D.“气体1”中含两种气体,一种是CO,另一种可能是CO
2
4.(2022·陕西延安高三模拟)黏土钒矿(主要成分为钒的+3、+4、+5价的化合物以及SiO、Al O 等)中钒
2 2 3
的化合物溶于酸后多以VO+、VO2+、VO形式存在,采用如图所示工艺流程可由黏土钒矿制备VO。已知:
2 5
VO 在碱性条件下以VO形式存在。下列说法不正确的是( )
2 5A.“酸浸氧化”中欲使3 mol VO+被氧化成VO,至少需要1 mol KClO
3
B.滤液1中主要的阴离子有AlO、VO、Cl-、OH-、SO
C.“煅烧”时需要的仪器主要有蒸发皿、玻璃棒、三脚架、酒精灯
D.“煅烧”时,NH VO 受热分解:2NH VO =====VO+2NH ↑+HO
4 3 4 3 2 5 3 2
5.钼酸钠是一种白色结晶性粉末,广泛应用于颜料和化工等领域。工业上用钼精矿(主要成分是 ,含
少量的 )制备钼酸钠晶体( )的简化流程如图所示。下列说法错误的是
已知:浸取液溶质主要为 和 。
A.焙烧时发生反应 B.气体X为 ,废渣的主要成分为
C.从滤液中获得 的操作为蒸发结晶 D.利用纯碱吸收 ,可获得副产品亚硫酸
钠
6.(2023春·湖南岳阳·高三岳阳一中校考阶段练习)氨广泛应用于化工、化肥、制药等领域,一种新型合
成方法如图所示。下列说法正确的是
A.反应①属于自然固氮
B.反应③可利用电解 溶液的方法实现
C.该转化过程的总反应为
D.反应①、②、③、④均属于氧化还原反应
7.(2023秋·黑龙江齐齐哈尔·高三校联考期末)氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业;
CuCl难溶于水和乙醇,潮湿时易水解氧化。工业以硫化铜精矿为原料,设计符合绿色化学理念的制备
CuCl的流程如图:下列说法错误的是
A.步骤①焙烧产生的有毒气体用NaOH溶液吸收后可用于③的循环利用
B.步骤②中可以用硝酸代替硫酸,不影响后续处理
C.步骤③离子方程式:
D.步骤④用乙醇洗涤的目的是使CuCl加速干燥,防止发生水解氧化
8.(2023秋·江西吉安·高三江西省宜丰中学统考期末)化工专家侯德榜发明的侯氏制碱法为我国纯碱工业
和国民经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟侯氏制碱法制备 ,进一步处理
得到产品 和 。实验流程如图:
下列说法正确的是
A.气体N、M分别为 和 B.该流程中只有“食盐水”可以循环使用
C.操作1为过滤,为了加快过滤速率常用玻璃棒搅拌
D.向“母液”中加入NaCl粉末并通入 可得到副产品 ,通入 的目的是增大 的浓度,
有利于析出 并提高纯度
9.(2023·天津·一模)合成氨及其衍生工业是化工生产的重要门类,请结合图示判断下列说法不正确的是
A.合成氨采用400~500℃是为了提高原料转化率和反应速率
B.湿润的淀粉KI试纸不可以鉴别气体2和溴蒸气C.生成固体1的化学方程式为NaCl+NH +CO +H O=NaHCO ↓+NHCl
3 2 2 3 4
D.1L气体1、2的混合气与1 L NH 在一定条件下转化为对环境无害的物质,混合气中二者的体积比为
3
1∶1
10.(2023.全国乙卷) LiMn O 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO ,含有
2 4 3
少量Si、Fe、Ni、Al等元素)制备LiMn O 的流程如下:
2 4
已知:K [Fe(OH) ]=2.8×10-39,K [Al(OH) ]=1.3×10-33,K [Ni(OH) ]=5.5×10-16。
sp 3 sp 3 sp 2
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为_______。为提高溶矿速率,可采取的措施_______(举1例)。
(2)加入少量MnO 的作用是_______。不宜使用HO 替代MnO ,原因是_______。
2 2 2 2
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=_______mol·L-1;用石灰乳调节至pH≈7,除去的
金属离子是_______。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有_______。
(5)在电解槽中,发生电解反应的离子方程式为_______。随着电解反应进行,为保持电解液成分稳定,
应不断_______。电解废液可在反应器中循环利用。
(6)缎烧窑中,生成LiMn O 反应的化学方程式是_______。
2 4
11.(2023.课标I卷)铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、
铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
已知:最高价铬酸根在酸性介质中以Cr O 存在,在碱性介质中以CrO 存在。
2
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________(填化学
式)。
(2)水浸渣中主要有SiO 和___________。
2(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是___________。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO 和MgNH PO 的形式沉淀,该步需要控制溶液的pH≈9
3 4 4
以达到最好的除杂效果,若pH<9时,会导致___________;pH>9时,会导致___________。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到VO 沉淀,VO 在pH<1时,溶解为VO 或
2 5 2 5
VO3+在碱性条件下,溶解为VO 或VO ,上述性质说明VO 具有___________(填标号)。
2 5
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na SO)溶液,反应的离子方程式为___________。
2 2 5