文档内容
第十七讲 氮及其化合物
【基础巩固】
1.自然界的氮循环如图所示,下列说法正确的是( )
A.①中N 与O 反应生成NO 是自然固氮
2 2 2
B.②中合成氨属于人工固氮
C.③中的氮元素被氧化
D.氮循环过程中没有氧元素参加
【答案】 B
【解析】 ①中N 与O 反应生成NO是自然固氮,A错误;②中N 与H 在高温、高压、催化剂条件下反
2 2 2 2
应产生NH ,属于人工固氮,B正确;③中细菌还原硝酸根中正五价的氮,生成无污染的 0价的N ,所以
3 2
③中氮元素化合价降低,得到电子被还原,C错误;如N 在放电条件下与O 直接化合生成无色且不溶于
2 2
水的NO气体,氧元素参与了反应,二氧化氮易与水反应生成硝酸(HNO)和NO,也有氧元素参加反应,D
3
错误。
2.(2023·天津和平·耀华中学校考一模)固氮是将游离态的氮转变为氮的化合物,一种新型人工固氮的原理
如图所示。下列叙述正确的是
A.转化过程中所涉及的元素均呈现了两种价态
B.反应①②③均为氧化还原反应
C.Li是催化剂,只有 是中间产物
D.整个过程的总反应可表示为
【答案】 D
【解析】 A.根据转化关系可知:在转化过程中 H始终呈+1价,A错误;B.反应②为LiN + 3H2O
3
=NH3↑ + 3LiOH,该反应过程中元素化合价不变,因此反应属于非氧化还原反应,B错误;C.Li是催化
剂,LiN和LiOH均是中间产物,C错误;D.根据分析,整个过程的总反应为氮气和水生成氨气和氧气,
3
资料整理【淘宝店铺:向阳百分百】可表示为 ,D正确;故选D。
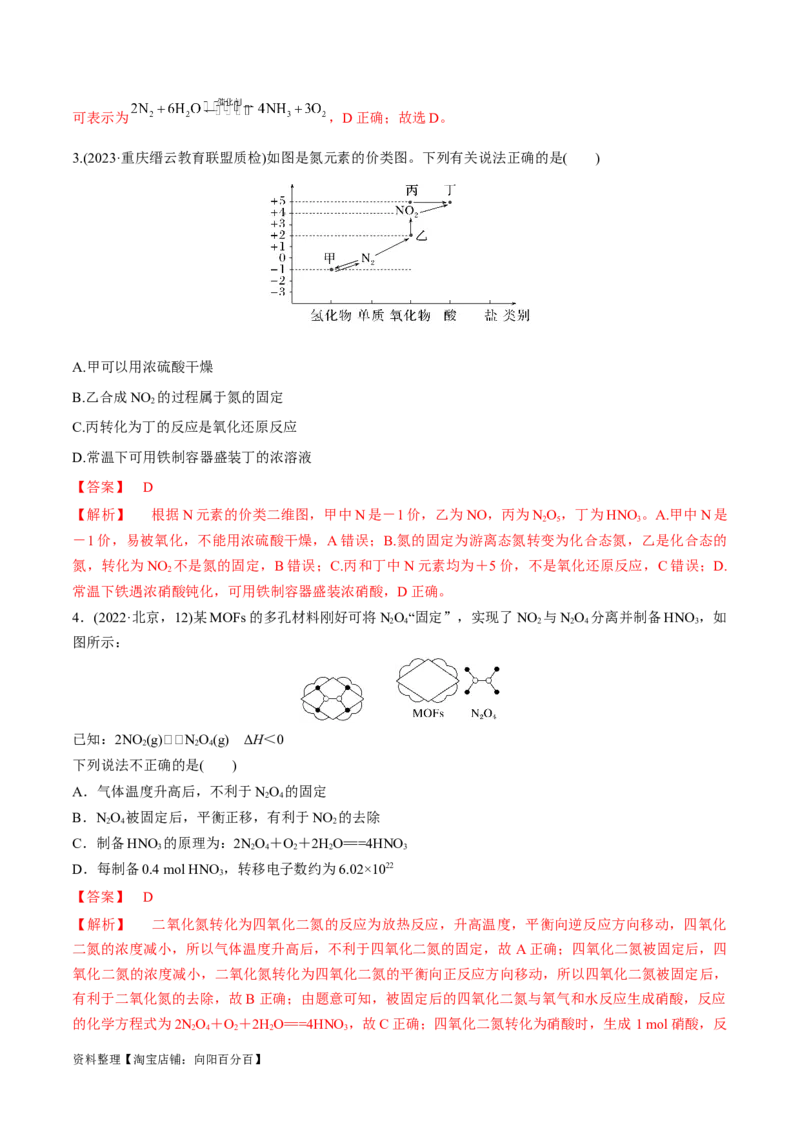
3.(2023·重庆缙云教育联盟质检)如图是氮元素的价类图。下列有关说法正确的是( )
A.甲可以用浓硫酸干燥
B.乙合成NO 的过程属于氮的固定
2
C.丙转化为丁的反应是氧化还原反应
D.常温下可用铁制容器盛装丁的浓溶液
【答案】 D
【解析】 根据N元素的价类二维图,甲中N是-1价,乙为NO,丙为NO ,丁为HNO 。A.甲中N是
2 5 3
-1价,易被氧化,不能用浓硫酸干燥,A错误;B.氮的固定为游离态氮转变为化合态氮,乙是化合态的
氮,转化为NO 不是氮的固定,B错误;C.丙和丁中N元素均为+5价,不是氧化还原反应,C错误;D.
2
常温下铁遇浓硝酸钝化,可用铁制容器盛装浓硝酸,D正确。
4.(2022·北京,12)某MOFs的多孔材料刚好可将NO“固定”,实现了NO 与NO 分离并制备HNO ,如
2 4 2 2 4 3
图所示:
已知:2NO (g)N O(g) ΔH<0
2 2 4
下列说法不正确的是( )
A.气体温度升高后,不利于NO 的固定
2 4
B.NO 被固定后,平衡正移,有利于NO 的去除
2 4 2
C.制备HNO 的原理为:2NO+O+2HO===4HNO
3 2 4 2 2 3
D.每制备0.4 mol HNO ,转移电子数约为6.02×1022
3
【答案】 D
【解析】 二氧化氮转化为四氧化二氮的反应为放热反应,升高温度,平衡向逆反应方向移动,四氧化
二氮的浓度减小,所以气体温度升高后,不利于四氧化二氮的固定,故 A正确;四氧化二氮被固定后,四
氧化二氮的浓度减小,二氧化氮转化为四氧化二氮的平衡向正反应方向移动,所以四氧化二氮被固定后,
有利于二氧化氮的去除,故B正确;由题意可知,被固定后的四氧化二氮与氧气和水反应生成硝酸,反应
的化学方程式为2NO+O+2HO===4HNO ,故C正确;四氧化二氮转化为硝酸时,生成1 mol硝酸,反
2 4 2 2 3
资料整理【淘宝店铺:向阳百分百】应转移1 mol电子,则每制备0.4 mol硝酸,转移电子数约为0.4 mol×6.02×1023 mol-1=2.408×1023,故D错
误。
5.(2022·成都适应性考试)下列有关制取气体的设计方案正确的是( )
所选药品
选项 制取气体 收集装置
① ②
A NH 浓氨水 氧化钙 ④
3
B SO 浓硫酸 亚硫酸钠 ④
2
C CO 醋酸溶液 石灰石 ③
2
D Cl 浓盐酸 二氧化锰 ③
2
【答案】 B
【解析】 A.氨气极易溶于水,密度比空气小,因此一般采用向下排空气法收集氨气,故A错误;B.亚
硫酸钠与浓硫酸反应生成SO ,可用氯化钙干燥,其密度比空气大,用向上排空气法收集,故 B正确;
2
C.CO 是酸性气体,③中碱石灰会吸收二氧化碳,且其密度比空气大,向上排空气法收集,故 C错误;D.
2
二氧化锰和浓盐酸反应生成氯气需要加热,所以该装置不能得到氯气,故D错误。
6.硝酸被称为“国防工业之母”,是因为它是制取炸药的重要原料。下列实验事实与硝酸性质对应不准
确的一组是( )
A.硝酸能与FeO反应——酸性和氧化性
B.不能用稀硝酸与锌反应制氢气——强氧化性
C.要用棕色试剂瓶盛装浓硝酸——不稳定性
D.能使滴有酚酞的氢氧化钠溶液红色褪去——强氧化性
【答案】 D
【解析】 D项中“滴有酚酞的氢氧化钠溶液红色褪去”,其褪色的原因可能是硝酸的强氧化性把酚酞氧
化而褪色,但也有可能是硝酸与氢氧化钠发生中和反应,究竟是哪个原因,还需要实验验证,D项不准确。
7.已知2NO +2OH-===NO+NO+HO,下列装置或操作不能达到相应实验目的的是( )
2 2
A B C D
资料整理【淘宝店铺:向阳百分百】使NO 充分转化为
2
生成NO 收集NO 吸收NO 尾气
2 2 2
HNO
3
【答案】 B
【解析】 浓硝酸和铜反应生成硝酸铜、水和NO ,A正确;NO 的密度比空气大,应用向上排空气法收
2 2
集,即导气管应长进短出,B错误;根据题目所给信息可知NO 可以和NaOH溶液反应得到可溶性盐,所
2
以可以用NaOH溶液处理尾气,C正确;试管中发生反应:4NO +O +2HO===4HNO ,可以使NO 充分
2 2 2 3 2
转化为HNO,D正确。
3
8.(2023·山东东营·东营市第一中学校考二模,双选)下列关于氮及其化合物性质探究,实验结论正确的
是
选
操作和现象 结论
项
A 将灼热木炭伸入浓硝酸中,木炭燃烧,产生大量红棕色气体 木炭和硝酸反应生成了 和
先将注射器充满 气体,然后将活塞往里推,注射器内气 证明加压平衡向生成 气体的方
B
体颜色加深 向移动
反应结束后溶液中的溶质是
向含有等物质的量 和 的混酸稀溶液加入过量铜
C
粉,生成气体,溶液变蓝色 和
将 粉加入强碱性的 溶液,微热,产生气体使湿润红
D 在强碱性溶液中也能显氧化性
色石蕊试纸变蓝
A.A B.B C.C D.D
【答案】CD
【解析】A.将灼热的木炭伸入浓硝酸中,木炭与浓硝酸反应生成二氧化氮、二氧化碳、水,A错误;B.
先将注射器充满 NO2气体,然后将活塞往里推,NO2的浓度增大,颜色加深,与平衡无关,B错误;C.
含有等物质的量 H2SO4 和 HNO3 的混酸中H+与NO -的物质的量之比为3∶1,加入过量铜粉,发生离子
3
反应: ,硝酸根过量,则溶质为 CuSO4 和 Cu(NO3)2 ,C正确;
D.将Al粉加入强碱性的 NaNO3 溶液,微热,产生气体使湿润红色石蕊试纸变蓝,该气体为NH3,硝酸
根离子中的N元素降价,表现氧化性,D正确;故选CD。
资料整理【淘宝店铺:向阳百分百】9.工业上常采用生物硝化法将NH转化为NO来处理氨氮废水,工作流程如图,下列说法错误的是( )
A.生物硝化法处理废水,会导致水体pH逐渐下降:NH+2O===NO+2H++HO
2 2
B.长期过量使用NH Cl等铵态化肥,易导致土壤酸化,水体富营养化
4
C.检验NH所需的试剂是浓NaOH溶液、湿润的蓝色石蕊试纸
D.微生物保持活性的pH范围为7~9,可以加入石灰石来调节水体的pH
【答案】 C
【解析】 根据流程图可知A项正确;NH Cl水解呈酸性,长期过量使用会导致土壤酸化,也会导致水
4
体富营养化,B项正确;检验NH应使用红色石蕊试纸,C项错误;由选项A可知,生物硝化法处理废水
会使水体呈酸性,可以加入石灰石与H+反应来调节水体的pH,D项正确。
10.某兴趣小组设计用铁粉将NO还原为N(同时生成FeO)。下列说法不正确的是( )
2
已知:①浓硝酸可氧化NO;②NaOH溶液能吸收NO ,不吸收NO。
2
A.装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d
B.装置E中发生反应的化学方程式为2NO+2Fe=====2FeO+N
2
C.装置D的作用是吸收挥发出来的硝酸和产生的NO
2
D.装置B的作用是干燥,防止水蒸气进入装置E中干扰反应
【答案】 D
【解析】 根据实验原理“NO被灼热的铁粉还原为N ,同时生成FeO”,所以首先利用铜与稀硝酸反应
2
生成NO,由于硝酸具有挥发性,所以制得的NO中会混有硝酸蒸气和产生的NO ,故先通过装置D除去
2
挥发出的HNO 和产生的NO ,再通过装置F干燥,得到纯净干燥的NO,然后进入装置E中与铁粉反应,
3 2
最后处理多余的NO,由于NaOH溶液不与NO反应,而浓硝酸可氧化NO生成NO ,所以先通过装置B氧
2
化NO,再通过装置C吸收,故上述装置的连接顺序为a→f→e→j→i→h→g(或g→h)→b→c→d,A正确。
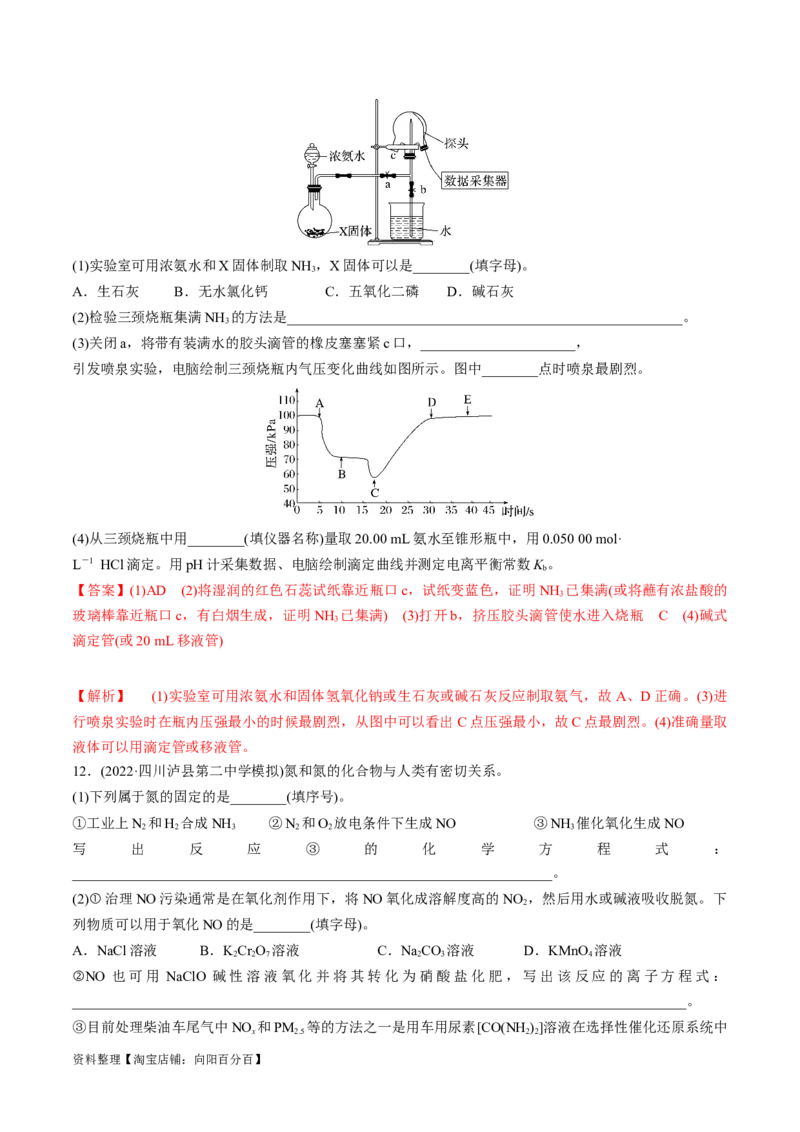
11.现代传感信息技术在化学实验中有广泛的应用。某小组用传感技术测定喷泉实验中的压强变化来认识
喷泉实验的原理(如图所示),并测定电离平衡常数K 。
b
资料整理【淘宝店铺:向阳百分百】(1)实验室可用浓氨水和X固体制取NH ,X固体可以是________(填字母)。
3
A.生石灰 B.无水氯化钙 C.五氧化二磷 D.碱石灰
(2)检验三颈烧瓶集满NH 的方法是________________________________________________________。
3
(3)关闭a,将带有装满水的胶头滴管的橡皮塞塞紧c口,______________________,
引发喷泉实验,电脑绘制三颈烧瓶内气压变化曲线如图所示。图中________点时喷泉最剧烈。
(4)从三颈烧瓶中用________(填仪器名称)量取20.00 mL氨水至锥形瓶中,用0.050 00 mol·
L-1 HCl滴定。用pH计采集数据、电脑绘制滴定曲线并测定电离平衡常数K 。
b
【答案】(1)AD (2)将湿润的红色石蕊试纸靠近瓶口c,试纸变蓝色,证明NH 已集满(或将蘸有浓盐酸的
3
玻璃棒靠近瓶口c,有白烟生成,证明NH 已集满) (3)打开b,挤压胶头滴管使水进入烧瓶 C (4)碱式
3
滴定管(或20 mL移液管)
【解析】 (1)实验室可用浓氨水和固体氢氧化钠或生石灰或碱石灰反应制取氨气,故 A、D正确。(3)进
行喷泉实验时在瓶内压强最小的时候最剧烈,从图中可以看出C点压强最小,故C点最剧烈。(4)准确量取
液体可以用滴定管或移液管。
12.(2022·四川泸县第二中学模拟)氮和氮的化合物与人类有密切关系。
(1)下列属于氮的固定的是________(填序号)。
①工业上N 和H 合成NH ②N 和O 放电条件下生成NO ③NH 催化氧化生成NO
2 2 3 2 2 3
写 出 反 应 ③ 的 化 学 方 程 式 :
____________________________________________________________________。
(2)①治理NO污染通常是在氧化剂作用下,将NO氧化成溶解度高的NO ,然后用水或碱液吸收脱氮。下
2
列物质可以用于氧化NO的是________(填字母)。
A.NaCl溶液 B.KCr O 溶液 C.NaCO 溶液 D.KMnO 溶液
2 2 7 2 3 4
②NO 也可用 NaClO 碱性溶液氧化并将其转化为硝酸盐化肥,写出该反应的离子方程式:
_______________________________________________________________________________________。
③目前处理柴油车尾气中NO 和PM 等的方法之一是用车用尿素[CO(NH)]溶液在选择性催化还原系统中
x 2.5 2 2
资料整理【淘宝店铺:向阳百分百】将 NO 无 害 化 处 理 , 写 出 该 系 统 无 害 化 处 理 NO 的 化 学 方 程 式 :
x
_______________________________________。
(3)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应,用 Rh做催化剂时该
反应的过程示意图如下:
过程Ⅰ为________(填“吸热”或“放热”)过程。该反应中氧化产物为________,当生成
1 mol N 时,转移电子________mol。
2
【答案】 (1)①② 4NH +5O=====4NO+6HO
3 2 2
(2)①BD ②2NO+3ClO- +2OH-===2NO+3Cl-+HO ③2CO(NH) +6NO===5N +2CO +4HO (3)
2 2 2 2 2 2
吸热 CO 4
2
【解析】 (1)固氮是指将游离态的氮元素转化为化合态的氮元素,N 和H 合成NH ,N 和O 放电条件下
2 2 3 2 2
生成NO,符合固氮的定义,故选①②;反应③NH 催化氧化生成NO和水,反应的化学方程式为4NH +
3 3
5O=====4NO+6HO。(2)①氧化NO需要氧化剂,NaCl溶液、NaCO 溶液均不与NO反应,KCr O 、
2 2 2 3 2 2 7
KMnO 溶液具有强氧化性,可以氧化NO,故选BD。(3)过程Ⅰ断裂化学键需要吸热,该反应的化学方程
4
式为2CO+2NO=====N+2CO,C元素化合价升高,氧化产物为CO,氮元素从+2价降低至0价,当生
2 2 2
成1 mol N 时,转移电子4 mol。
2
【拔高练习】
1.清代《本草纲目拾遗》中关于“鼻冲水(氨水)”的记载明确指出:“鼻冲水,……贮以玻璃瓶,紧塞其
口,勿使泄气,则药力不减……唯以此水瓶口对鼻吸其气,即遍身麻颤出汗而愈,虚弱者忌之。宜外用,
勿服。”下列有关“鼻冲水”的推断不正确的是( )
A.鼻冲水是弱电解质
B.鼻冲水滴入酚酞溶液中,溶液变红色
C.鼻冲水中含有分子和离子的种类为6种
D.存在平衡:NH +HONH·H ONH+OH-
3 2 3 2
【答案】 A
【解析】 鼻冲水为氨水,氨水本身为混合物,所以鼻冲水不是弱电解质,故A错误;氨水中含有的分子
为NH 、HO、NH ·H O,离子有NH、 OH-、H+,共六种,故C正确。
3 2 3 2
2.(2023·河北·高三专题练习)氮是生命的基础,氮及其化合物在生产生活中具有广泛应用。工业上用氨
的催化氧化生产硝酸,其热化学方程式为4NH (g)+5O(g) 4NO(g)+ 6HO(g) △H=-904kJ•mol-1。生产硝
3 2 2
酸的尾气中主要含有NO、NO 等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO )、
2 3 2
Ca(NO ) 等化工产品。下列氮及其化合物的性质与用途具有对应关系的是
2 2
A.N 不溶于水,可用作保护气
2
资料整理【淘宝店铺:向阳百分百】B.NH 极易溶于水,可用作制冷剂
3
C.NO 具有强氧化性,可用作火箭燃料推进剂
2
D.HNO 具有易挥发性,可用来制备硝酸纤维
3
【答案】 C
【解析】 A.氮气含有氮氮三键,其化学性质稳定,一般不与物质发生反应,可用作保护气,与氮气难
溶于水无关,故A错误;B.液氨汽化吸收大量的热,具有制冷作用,可以用作制冷剂,与其溶解性无关
故B错误;C.NO2具有强氧化性,可作氧化剂,可用作火箭燃料推进剂,故 C正确;D.硝酸具有酸性,
可发生酯化反应,用来制备硝酸纤维,与挥发性无关,故D错误;故答案为C。
3.(2023·河北·高三专题练习)氮是生命的基础,氮及其化合物在生产生活中具有广泛应用。工业上用氨
的催化氧化生产硝酸,其热化学方程式为4NH (g)+5O(g) 4NO(g)+6H O(g) △H=-904kJ·mol-1。生产硝
3 2 2
酸的尾气中主要含有NO、NO 等大气污染物,可用石灰浆等碱性溶液吸收处理,并得到Ca(NO )、
2 3 2
Ca(NO ) 等化工产品。实验室采用下列装置制取氨气,正确的是
2 2
A.装置甲生成NH B.装置乙干燥NH
3 3
C.装置丙收集NH 并验满 D.装置丁吸收多余NH
3 3
【答案】D
【解析】A.加热氯化铵分解后生成氨气和HCl,气体在试管口冷凝生成氯化铵固体,应加热氯化铵和熟
石灰制取氨气,故A错误;B.NH3是碱性气体,可与硫酸反应,不能用来干燥,故 B错误;C.氨气的
密度比空气小,应向下排空气法收集氨气,导管应插入试管底部,故C错误;D.氨气极易溶于水,为防
倒吸,可将漏斗倒扣来吸收多余NH3,故D正确;故选:D。
4.(2023春·河北石家庄·高三校联考期中)氮的化合物对人类生存和社会发展意义重大,下列说法错误的
是
A.基态氮原子核外有5种空间运动状态不同的电子
B.同周期元素中第一电离能比N大的有两种
资料整理【淘宝店铺:向阳百分百】C.含氨基( )的有机物分子间易形成氢键
D.将含氮气体转化为固体化合物的过程被称之为固氮
【答案】D
【解析】A.基态氮原子核外有5种空间运动状态不同的电子,分别是1s、2s、2p,其中2p轨道有三种运
动状态不同的电子,A正确;B.同周期元素中第一电离能比N大的有两种,分别为F和Ne,B正确;
C.含氨基(-NH )的有机物分子间易形成氢键,C正确;D.将氮气转化为化合物的过程被称之为固氮,而
2
不是固体化合物,D错误;故选D。
5.(2023·河南TOP二十名校摸底)用如图所示装置进行实验(①②③是浸有相应试剂的棉花),下列分析错误
的是( )
A.铜丝与浓硝酸反应,具支试管中充满红棕色气体
B.①处浸有紫色石蕊试液的棉花变红
C.②处棉花颜色变深体现了NO 的氧化性
2
D.NaOH吸收尾气是氧化还原反应
【答案】C
【解析】 A.铜丝与浓硝酸反应生成红棕色气体NO ,A正确;B.NO 溶于水生成硝酸,可使紫色石蕊试
2 2
液变红,B正确;C.NO 溶于水生成的硝酸具有氧化性,可将Fe2+氧化为Fe3+,②处棉花颜色由浅绿色变
2
为黄色,体现了硝酸的氧化性,C错误;D.NaOH吸收NO 和NO尾气生成亚硝酸钠,有化合价的变化,
2
是氧化还原反应,D正确。
6.(2023·沈阳二中段测)为了防止NO、NO 、NO 对大气的污染,常用氢氧化钠溶液进行吸收处理,现有由
2 2 4
a mol NO、b mol NO 、c mol N O 组成的混合气体,能被1.0 mol·L-1的氢氧化钠溶液完全吸收,则消耗
2 2 4
氢氧化钠溶液的体积最小为( )
A.(a+b+c) L B.(a+b+2c) L C.2(a+b+c) L D.3(a+b+c) L
【答案】 B
【解析】 根据方程式知,氮氧化物被NaOH吸收生成钠盐,无论生成硝酸钠还是亚硝酸钠,N、Na原子
个数之比都是1∶1,根据N、Na原子关系式得V(NaOH)==(a+b+2c) L;答案选B。
7.(2022·宝鸡模拟)为探究氨及铵盐性质,将NH Cl晶体装入如图所示T形三通管两端,进行微型实验。
4
下列说法错误的是( )
资料整理【淘宝店铺:向阳百分百】A.轻轻挤压任一乳胶头,若蒸馏水中有气泡冒出,则装置气密性良好
B.同时点燃两个酒精灯后,两端湿润的pH试纸均变蓝
C.实验过程中竖直支管上方会出现白烟
D.停止加热后可以交替挤压两边乳胶头,使气体更充分吸收,减少污染
【答案】 B
【解析】 整套装置是密闭体系,若装置气密性良好,轻轻挤压任一乳胶头,则蒸馏水中有气泡冒出,故
A正确;pH试纸遇酸变红,遇碱变蓝,氯化铵受热分解生成氨气和HCl,左边氯化钙会吸收氨气,右边
NaOH会吸收HCl,因此同时点燃两个酒精灯后,左端pH试纸变红,右端pH试纸变蓝,故B错误;竖直
支管上方同时有氨气和HCl,两者相遇变为氯化铵,因此实验过程中竖直支管上方会出现白烟,故C正确;
停止加热后,不断交替挤压两边乳胶头,增大压强,将残余的气体全部赶入到蒸馏水中被吸收,减少污染,
故D正确。
8.(2023·咸阳检测)某学习小组设计实验制备Ca(NO ) ,实验装置如图所示(夹持装置已略去)。已知:2NO
2 2
+CaO===Ca(NO);2NO +CaO===Ca(NO)。下列说法不正确的是( )
2 2 2 2 2 3 2
A.通入N 是为了排尽装置中的空气
2
B.装置B、D中的试剂可分别为水和浓硫酸
C.将铜片换成木炭也可以制备纯净的亚硝酸钙
D.借助装置A及氢氧化钠溶液和稀硫酸可以分离CO 和CO
2
【答案】C
【解析】 装置内的空气会将NO氧化为NO ,影响产物的产量,所以通入N 是为了排尽装置中的空气,
2 2
故A正确;由于硝酸具有挥发性,所以在A中生成的NO气体中会含有少量HNO 蒸气,可用装置B中的
3
水除去,为防止CaO 与水反应,用装置D中的浓硫酸对NO气体进行干燥,故B正确;将铜片换成木炭,
2
由于木炭与稀硝酸不能反应,所以得不到要制备的产物,故C错误;装置A中盛氢氧化钠溶液,通过进气
管通入CO 和CO的混合气体,CO 被NaOH吸收后生成NaCO ,在出气管口即可收集到CO,然后将分
2 2 2 3
液漏斗中的稀硫酸滴入A中,与生成的NaCO 反应再释放出CO,达到分离的目的,故D正确。
2 3 2
9.(2022·武汉市汉阳一中高三模拟)用如图所示装置进行实验,探究硝酸与铁反应的产物。
资料整理【淘宝店铺:向阳百分百】主要实验操作 实验现象
①A 中有红棕色气体产生,一段时间
打开弹簧夹,通入一段时间CO 后,滴入浓
2
后,气体颜色逐渐变浅;反应停止后,
硝酸后无明显现象,加热三颈烧瓶,反应开
A 中无固体剩余;
始后停止加热
②B 中溶液变棕色
取少量A 中溶液,加几滴氯水,再滴入硫氰
③溶液变为红色
化钾溶液
④B中棕色溶液变浅,有无色气体逸
取少量 B 中溶液,加热
出,且在空气中变为红棕色
已知:FeSO +NO[Fe(NO)]SO (棕色) ΔH<0 。
4 4
下列说法正确的是( )
A.滴入浓硝酸加热前没有明显现象的原因是温度低,反应速率太慢
B.实验现象③说明反应后A 中溶液含有 Fe2+
C.实验现象④说明 A 中有 NO 生成
D.可用浓NaOH溶液和湿润的红色石蕊试纸检验硝酸的还原产物中是否有 NH
【答案】 D
【解析】 常温时,铁遇浓硝酸形成致密氧化膜,阻止反应进一步发生,故 A错误;取少量A中溶液,加
几滴氯水,再滴入KSCN溶液,溶液变为红色,只能说明这时溶液中有Fe3+,无法说明原溶液中是Fe2+还
是Fe3+,故B错误;取少量B中溶液加热,B中棕色溶液变浅,有无色气体逸出,且在空气中变为红棕色,
只能说明[Fe(NO)]SO 分解生成NO,但由于铜和浓硝酸反应生成红棕色气体二氧化氮,二氧化氮和水反应
4
生成一氧化氮,一氧化氮能使硫酸亚铁溶液变成棕色,所以不能证明铁和浓硝酸反应过程中有 NO生成,
故C错误。
10.足量铜溶于一定量浓硝酸,产生NO 、NO 、NO的混合气体,这些气体若与1.12 L O (标准状况)混合
2 2 4 2
后通入水中,气体被水完全吸收。若向原所得溶液中加入5 mol·L-1 HSO 溶液100 mL,则继续溶解的Cu
2 4
的质量为( )
A.6.4 g B.9.6 g C.19.2 g D.24 g
【答案】 C
【解析】 设原来溶解的Cu的物质的量为x,Cu失去的电子被N元素得到生成氮的氧化物,这些氮的氧
化物再与O 、HO反应生成HNO ,可看成Cu失电子,O 得电子,则根据得失电子守恒可知,2x=×4,
2 2 3 2
解得x=0.1 mol,所以原所得溶液中NO的物质的量为0.2 mol;
资料整理【淘宝店铺:向阳百分百】3Cu+8H++2NO===3Cu2++2NO↑+4HO
2
1 mol 0.2 mol
H+过量,所以继续溶解的Cu的质量为×3×64 g·mol-1=19.2 g。
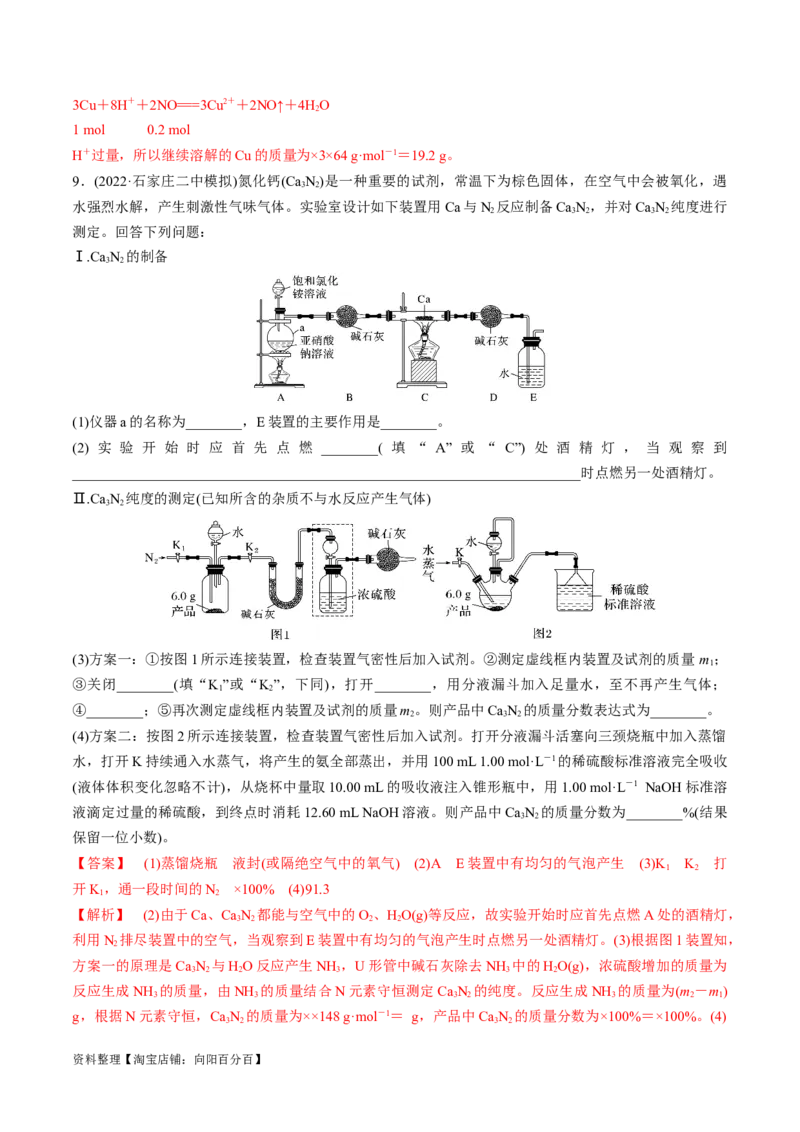
9.(2022·石家庄二中模拟)氮化钙(Ca N)是一种重要的试剂,常温下为棕色固体,在空气中会被氧化,遇
3 2
水强烈水解,产生刺激性气味气体。实验室设计如下装置用Ca与N 反应制备Ca N ,并对Ca N 纯度进行
2 3 2 3 2
测定。回答下列问题:
Ⅰ.Ca N 的制备
3 2
(1)仪器a的名称为________,E装置的主要作用是________。
(2) 实 验 开 始 时 应 首 先 点 燃 ________( 填 “ A” 或 “ C”) 处 酒 精 灯 , 当 观 察 到
________________________________________________________________________时点燃另一处酒精灯。
Ⅱ.Ca N 纯度的测定(已知所含的杂质不与水反应产生气体)
3 2
(3)方案一:①按图1所示连接装置,检查装置气密性后加入试剂。②测定虚线框内装置及试剂的质量 m;
1
③关闭________(填“K”或“K”,下同),打开________,用分液漏斗加入足量水,至不再产生气体;
1 2
④________;⑤再次测定虚线框内装置及试剂的质量m。则产品中Ca N 的质量分数表达式为________。
2 3 2
(4)方案二:按图2所示连接装置,检查装置气密性后加入试剂。打开分液漏斗活塞向三颈烧瓶中加入蒸馏
水,打开K持续通入水蒸气,将产生的氨全部蒸出,并用100 mL 1.00 mol·L-1的稀硫酸标准溶液完全吸收
(液体体积变化忽略不计),从烧杯中量取10.00 mL的吸收液注入锥形瓶中,用1.00 mol·L-1 NaOH标准溶
液滴定过量的稀硫酸,到终点时消耗12.60 mL NaOH溶液。则产品中Ca N 的质量分数为________%(结果
3 2
保留一位小数)。
【答案】 (1)蒸馏烧瓶 液封(或隔绝空气中的氧气) (2)A E装置中有均匀的气泡产生 (3)K K 打
1 2
开K,通一段时间的N ×100% (4)91.3
1 2
【解析】 (2)由于Ca、Ca N 都能与空气中的O 、HO(g)等反应,故实验开始时应首先点燃A处的酒精灯,
3 2 2 2
利用N 排尽装置中的空气,当观察到E装置中有均匀的气泡产生时点燃另一处酒精灯。(3)根据图1装置知,
2
方案一的原理是Ca N 与HO反应产生NH ,U形管中碱石灰除去NH 中的HO(g),浓硫酸增加的质量为
3 2 2 3 3 2
反应生成NH 的质量,由NH 的质量结合N元素守恒测定Ca N 的纯度。反应生成NH 的质量为(m -m)
3 3 3 2 3 2 1
g,根据N元素守恒,Ca N 的质量为××148 g·mol-1= g,产品中Ca N 的质量分数为×100%=×100%。(4)
3 2 3 2
资料整理【淘宝店铺:向阳百分百】方案二的原理是Ca N 与HO反应产生NH ,打开K持续通入水蒸气,将产生的氨全部蒸出,NH 完全被
3 2 2 3 3
稀硫酸标准溶液吸收,然后用NaOH标准溶液滴定过量的稀硫酸,则10.00 mL溶液中过量硫酸的物质的量
n (H SO )=
过量 2 4
n(NaOH)=×1.00 mol·L-1×0.012 60 L=0.006 3 mol,与NH 反应的硫酸的物质的量为
3
1.00 mol·L-1×0.1 L-0.006 3 mol×=0.037 mol,根据反应2NH +HSO ===(NH)SO 以及N元素守恒可知,
3 2 4 4 2 4
Ca N 的物质的量为0.037 mol,产品中Ca N 的质量分数为×100%≈91.3%。
3 2 3 2
11.某处工厂排出的烟道气中含氮氧化物(主要为NO、NO )、粉尘和少量水蒸气。课外兴趣活动小组对该
2
工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图所示:
(1)装置A中放置无碱玻璃棉,其目的是除去______________________________________。
为保证检测的准确性,装置C中盛放的化学试剂可以是________(填字母,下同)。
a.碱石灰 b.浓硫酸 c.五水合硫酸铜(CuSO ·5H O)
4 2
(2)装置D中主要发生:2NaOH+2NO ===NaNO +NaNO +HO;2NaOH+NO+NO ===2NaNO +HO
2 2 3 2 2 2 2
①若反应后尾气无残留,则参加反应的NO 、NO物质的量的比值________。
2
a.≥1 b.≤1 c.任意值
②可使用适量酸性 HO 溶液,将溶液中的 NO 全部氧化为 NO,发生反应的离子方程式是
2 2
_______________________________________________________________________________________。
(3)溶液中NO直接排放在水体中也会造成污染,现用活泼金属将溶液中的 NO转化为N ,实现氮元素的脱
2
除,具体步骤如下:
步骤一 取适量(2)中HO 处理后的溶液,调节pH至中性,蒸发浓缩,得到c(NO)为
2 2
0.100 mol·L-1的溶液甲。
步骤二 取三份50 mL溶液甲,分别用金属铝、金属铁和铝铁合金在45 ℃、惰性气体氛围中对溶液甲进
行氮脱除。
步骤三 重复实验2~3次,溶液中NO的残留情况与反应时间的关系如图所示。
①金属铝和金属铁在 0~3 h 内,NO 的脱除效率均很低,几乎没被脱除,其可能的原因是
___________________________________________________________________________________________。
②0 ~ 3 h 内 铝 铁 合 金 的 氮 脱 除 效 率 比 金 属 铝 、 金 属 铁 大 得 多 , 其 可 能 的 原 因 是
__________________________________________________________________________________________。
资料整理【淘宝店铺:向阳百分百】(4)气囊用来储存处理后的气体,其中可能含少量NO气体,可用酸性NaClO溶液来处理。HClO氧化NO
生成NO和Cl-,发生反应的离子方程式是_______________________________________________________。
【答案】 (1)粉尘 b (2)①a ②HO +NO===NO+HO (3)①金属铁和金属铝表面都有一层氧化膜
2 2 2
②铝铁合金在溶液中形成原电池,加快化学反应速率 (4)3HClO+2NO+HO===2NO+3Cl-+5H+
2
【解析】 (1)烟道气中含有粉尘,装置A中放置无碱玻璃棉,可以除去粉尘;装置C用于除去少量的水蒸
气,应该选择浓硫酸,NO 会与碱石灰反应,而五水合硫酸铜不能起到干燥的作用。(2)①根据化学方程式
2
可知,NO 可以单独被NaOH吸收,而NO需与NO 按照1∶1混合才能被NaOH吸收,现无尾气残留,说明
2 2
NO无残留,因此NO 至少和NO一样多,则参加反应的NO 、NO物质的量的比值≥1,a符合题意。(3)①
2 2
根据题意,活泼金属能够将溶液中的NO转化为N,但是金属铝和金属铁在0~3 h内,NO的脱除效率很
2
低,几乎没有脱除,可认为金属与NO可能没有反应,可能是金属表面有氧化膜,阻碍了NO的脱除反应。
②铝铁合金中,铁和铝的活动性不同,可以构成原电池,加快化学反应速率。(4)HClO中Cl元素的化合价
从+1降低到-1,NO中N元素的化合价从+2升高到+5,根据化合价升降守恒、元素守恒和电荷守恒,
离子方程式为3HClO+2NO+HO===2NO+3Cl-+5H+。
2
资料整理【淘宝店铺:向阳百分百】