文档内容
第 18 讲 原电池 化学电源
目录
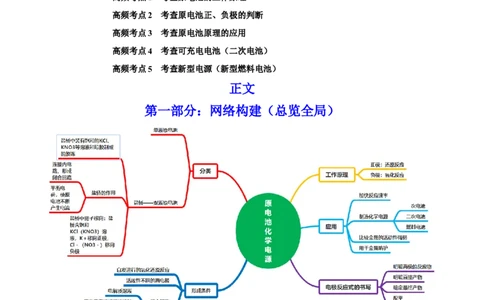
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查原电池的工作原理
高频考点2 考查原电池正、负极的判断
高频考点3 考查原电池原理的应用
高频考点4 考查可充电电池(二次电池)
高频考点5 考查新型电源(新型燃料电池)
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 原电池的工作原理及应用
1.概念和反应本质
原电池是把化学能转化为电能的装置,其反应本质是自发进行的氧化还原反应。
2.构成条件
(1)一看反应:看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与电解质溶液反应)。(2)二看两电极:一般是活泼性不同的两电极。
(3)三看是否形成闭合回路,形成闭合回路需三个条件:
①电解质溶液;
②两电极直接或间接接触;
③两电极插入电解质溶液中。
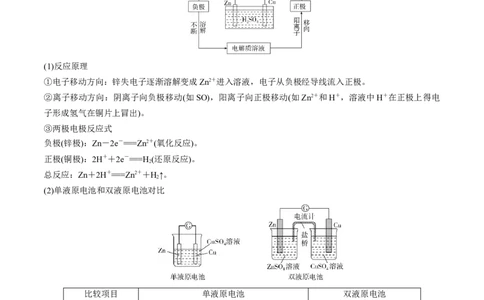
3.工作原理
以锌铜原电池为例
(1)反应原理
①电子移动方向:锌失电子逐渐溶解变成Zn2+进入溶液,电子从负极经导线流入正极。
②离子移动方向:阴离子向负极移动(如SO),阳离子向正极移动(如Zn2+和H+,溶液中H+在正极上得电
子形成氢气在铜片上冒出)。
③两极电极反应式
负极(锌极):Zn-2e-===Zn2+(氧化反应)。
正极(铜极):2H++2e-===H (还原反应)。
2
总反应:Zn+2H+===Zn2++H↑。
2
(2)单液原电池和双液原电池对比
比较项目 单液原电池 双液原电池
相同点 正负极,电极反应,总反应式,电极现象
不同 能量变化 化学能转化为电能和热能 化学能只转化为电能
点 反应区域 两极反应在相同区域 两极反应在不同区域
(3)双液原电池中盐桥的组成和作用
①盐桥中装有饱和的KCl、KNO 等溶液和琼胶制成的胶冻。
3
②盐桥中离子移向:盐桥含饱和KCl(KNO)溶液,K+移向正极,Cl-(NO -)移向负极
3 3
③盐桥的作用:a.连接内电路,形成闭合回路;b.平衡电荷,使原电池不断产生电流。
4.原电池原理的应用(1)比较金属的活动性强弱:原电池中,负极一般是活动性较强的金属,正极一般是活动性较弱的金属(或
非金属)。
(2)加快化学反应速率:一个自发进行的氧化还原反应,形成原电池时会使反应速率增大。如在 Zn与稀硫
酸反应时加入少量CuSO 溶液构成原电池,反应速率增大。
4
(3)用于金属的防护:使被保护的金属制品作原电池正极而得到保护。如要保护一个铁质的输水管道或钢铁
桥梁等,可用导线将其与一块锌块相连,使锌作原电池的负极。
(4)设计制作化学电源
①拆分反应:将氧化还原反应分成两个半反应。
②选择电极材料:将还原剂(一般为比较活泼的金属)作负极,活泼性比负极弱的金属或非金属导体作正
极。如果还原剂不是金属而是其它还原性物质,可选择惰性电极——石墨棒、铂片作负极。
③构成闭合回路:电解质溶液一般要能够与负极发生反应,或者电解质溶液中溶解的其他物质能与负极发
生反应(如溶解于溶液中的空气)。如果两个半反应分别在两个容器进行(中间连接盐桥),则两个容器中
的电解质溶液应含有与电极材料相同的金属的阳离子。
④画装置图:结合要求及反应特点,画出原电池装置图,标出电极材料名称、正负极、电解质溶液等。
知识点二 常见化学电源及工作原理
1.化学电源的优点和优劣判断标准
(1)相对其他能源,电池的优点是能量转换效率较高,供能稳定可靠,形状、大小可根据需要设计,使用方
便等。
(2)判断电池优劣的标准是电池单位质量或单位体积所能输出的比能量或比功率及可储存时间的长短。
2.日常生活中的几种电池
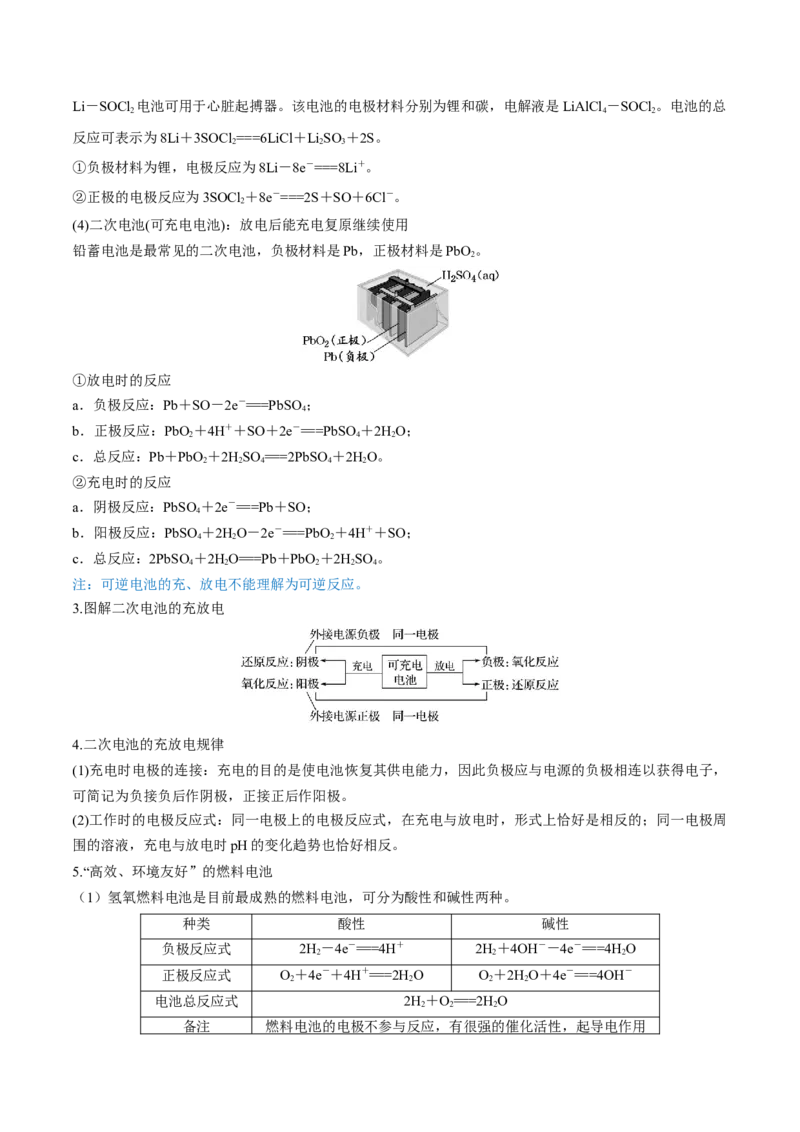
(1)碱性锌锰干电池——一次电池
正极反应:2MnO +2HO+2e-===2MnOOH+2OH-;
2 2
负极反应:Zn+2OH--2e-===Zn(OH) ;
2
总反应:Zn+2MnO +2HO===2MnOOH+Zn(OH) 。
2 2 2
(2)银锌电池——一次电池
负极反应:Zn+2OH--2e-===Zn(OH) ;
2
正极反应:Ag O+HO+2e-===2Ag+2OH-;
2 2
总反应:Zn+Ag O+HO===Zn(OH) +2Ag。
2 2 2
(3)锂电池——一次电池Li-SOCl 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl -SOCl 。电池的总
2 4 2
反应可表示为8Li+3SOCl ===6LiCl+LiSO +2S。
2 2 3
①负极材料为锂,电极反应为8Li-8e-===8Li+。
②正极的电极反应为3SOCl +8e-===2S+SO+6Cl-。
2
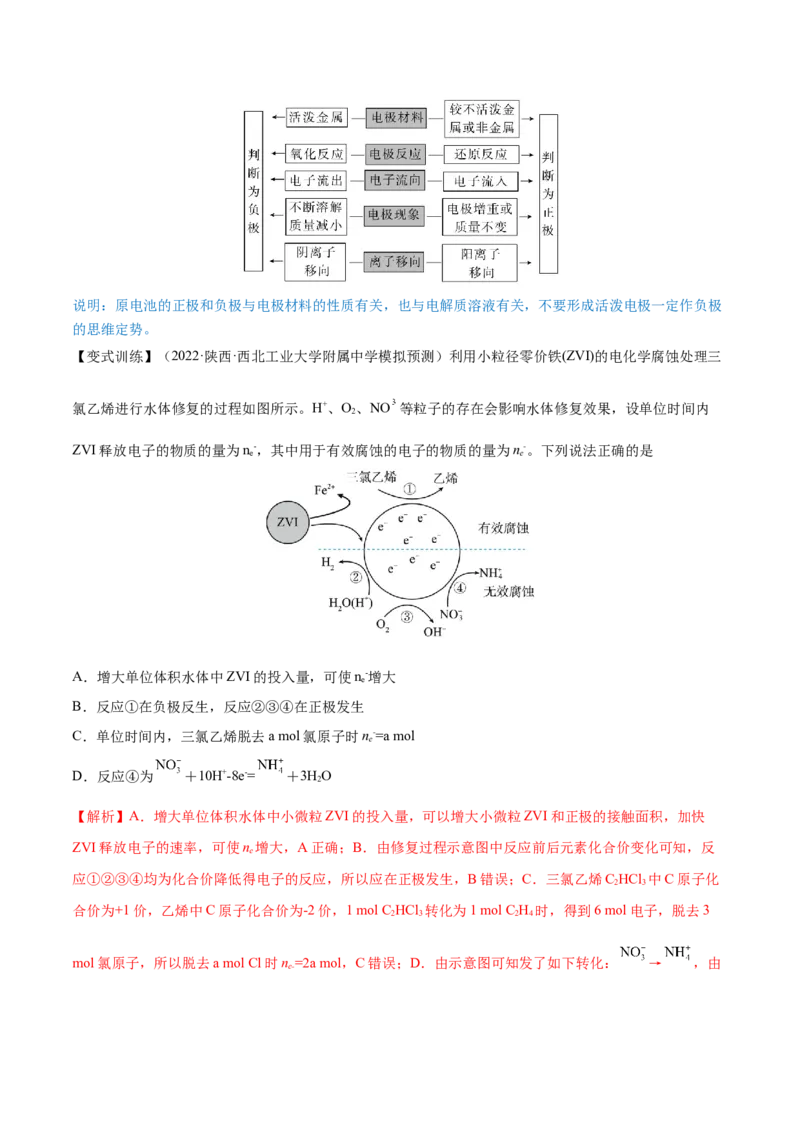
(4)二次电池(可充电电池):放电后能充电复原继续使用
铅蓄电池是最常见的二次电池,负极材料是Pb,正极材料是PbO 。
2
①放电时的反应
a.负极反应:Pb+SO-2e-===PbSO;
4
b.正极反应:PbO +4H++SO+2e-===PbSO+2HO;
2 4 2
c.总反应:Pb+PbO +2HSO ===2PbSO+2HO。
2 2 4 4 2
②充电时的反应
a.阴极反应:PbSO +2e-===Pb+SO;
4
b.阳极反应:PbSO +2HO-2e-===PbO+4H++SO;
4 2 2
c.总反应:2PbSO +2HO===Pb+PbO +2HSO 。
4 2 2 2 4
注:可逆电池的充、放电不能理解为可逆反应。
3.图解二次电池的充放电
4.二次电池的充放电规律
(1)充电时电极的连接:充电的目的是使电池恢复其供电能力,因此负极应与电源的负极相连以获得电子,
可简记为负接负后作阴极,正接正后作阳极。
(2)工作时的电极反应式:同一电极上的电极反应式,在充电与放电时,形式上恰好是相反的;同一电极周
围的溶液,充电与放电时pH的变化趋势也恰好相反。
5.“高效、环境友好”的燃料电池
(1)氢氧燃料电池是目前最成熟的燃料电池,可分为酸性和碱性两种。
种类 酸性 碱性
负极反应式 2H-4e-===4H+ 2H+4OH--4e-===4H O
2 2 2
正极反应式 O+4e-+4H+===2H O O+2HO+4e-===4OH-
2 2 2 2
电池总反应式 2H+O===2H O
2 2 2
备注 燃料电池的电极不参与反应,有很强的催化活性,起导电作用(2)甲烷燃料电池
①酸性介质(如HSO )或传导质子(H+)固体介质
2 4
总反应式:CH+2O===CO +2HO。
4 2 2 2
负极反应式:CH-8e-+2HO===CO +8H+。
4 2 2
正极反应式:2O+8e-+8H+===4H O。
2 2
②碱性介质(如KOH)
总反应式:CH+2O+2OH-===CO+3HO。
4 2 2
负极反应式:CH-8e-+10OH-===CO+7HO。
4 2
正极反应式:2O+8e-+4HO===8OH-。
2 2
③熔融盐介质(如KCO)
2 3
总反应式:CH+2O===CO +2HO。
4 2 2 2
负极反应式:CH-8e-+4CO2-===5CO +2HO。
4 3 2 2
正极反应式:2O+8e-+4CO===4CO 2-。
2 2 3
④用能传导氧离子(O2-)的固体作介质
总反应式:CH+2O===CO +2HO。
4 2 2 2
负极反应式:CH-8e-+4O2-===CO +2HO。
4 2 2
正极反应式:2O+8e-===4O2-。
2
(3)解答燃料电池题目的思维模型
(4)解答燃料电池题目的几个关键点
①要注意介质是什么?是电解质溶液还是熔融盐或氧化物。
②通入负极的物质为燃料,通入正极的物质为氧气。
③通过介质中离子的移动方向,可判断电池的正负极,同时考虑该离子参与靠近一极的电极反应。
6.化学电源中电极反应式书写的一般方法
(1)明确两极的反应物;
(2)明确直接产物:根据负极氧化、正极还原,明确两极的直接产物;
(3)确定最终产物:根据介质环境和共存原则,找出参与的介质粒子,确定最终产物;
(4)配平:根据电荷守恒、原子守恒配平电极反应式。
注意:①H+在碱性环境中不存在;②O2-在水溶液中不存在,在酸性环境中结合H+,生成HO,在中性
2或碱性环境结合HO,生成OH-;③若已知总反应式时,可先写出较易书写的一极的电极反应式,然后在
2
电子守恒的基础上,总反应式减去较易写出的一极的电极反应式,即得到较难写出的另一极的电极反应式。
第三部分:典型例题剖析
高频考点1 考查原电池的工作原理
例1. (2022·河南洛阳·模拟预测)某种新型热激活电池的结构与工作原理如图所示。下列说法正确的是
A.电池冷却时,电子由电极b经过导线流向电极a
B.电池加热时,电极a的电势比电极b的低,且发生氧化反应
C.为了保证电池持久工作,理论上应不断地向电解质中补充Fe2+
D.应加入适量稀HSO 使电解质溶液呈较强的酸性
2 4
【解析】由图可知,加热时,PANI失去了电子,发生氧化反应,应作负极;电池冷却时,电池再生,
PANI得到了电子,发生还原反应,应作正极。电子的流动方向是由负极流向正极,电势正极高于负极,在
装置中Fe3+可以和Fe2+相互转化,Fe3+在水溶液中易发生水解,需加酸抑制其水解。A.电池冷却时,电极
b上的 得到电子重新生成 ,A错误;B.电池加热时,根据b极的电极反应式判断电极a是正
极,电极a的电势比电极b的高﹐B错误;C.电池工作时,铁离子在电极a上转变成亚铁离子,冷却时亚
铁离子转变成铁离子,理论上不需要补充亚铁离子,C错误;D.Fe3+易发生水解,适量硫酸的加入可以增
强溶液酸性,抑制Fe3+的水解,D正确;故选D。
【答案】D
【名师归纳】原电池的工作原理简图
注意:①若有盐桥,盐桥中的阴离子移向负极区,阳离子移向正极区。
②若有交换膜,离子可选择性通过交换膜,如阳离子交换膜,阳离子可通过交换膜移向正极。
【变式训练】(2022·广东·模拟预测)新型NaBH /H O 燃料电池总反应方程式为
4 2 2
NaBH +4H O=NaBO +6H O。下列有关说法中正确的是
4 2 2 2 2
A.电池正极区发生氧化反应B.电池工作时,将电能转化为化学能
C.电池工作时,HO 得电子
2 2
D.电池在工作过程中,Na+从正极区向负极区迁移
【解析】新型NaBH /H O 燃料电池总反应方程式为NaBH +4H O=NaBO +6H O,由总反应式,可确定负
4 2 2 4 2 2 2 2
极反应物为NaBH ,正极反应物为HO。A.电池正极区HO 得电子,发生还原反应,A不正确;B.电
4 2 2 2 2
池工作时,通过发生氧化还原反应,将化学能转化为电能,B不正确;C.从总反应式可知,电池工作时,
HO 中的O元素从-1价降低到-2价,则HO 得电子,C正确;D.电池工作过程中,阳离子向正极移动,
2 2 2 2
则Na+从负极区向正极区迁移,D不正确;故选C。
【答案】C
高频考点2 考查原电池正、负极的判断
例2.(2022·安徽·模拟预测)中科院开发的一种新型电池的反应原理如图所示,其中电解质LiCIO 溶于混
4
合有机溶剂中,Li +通过电解质可自由移动,b极参与反应的物质是二氯亚砜(SOCl ),且有刺激性气味气
2
体产生。下列说法正确的是
A.a极为正极,电极反应式为LiClO +e-=Li + ClO
4
B.可用水代替有机溶剂
C.正极产生的有刺激性气味气体为Cl
2
D.用该电池电解饱和食盐水(用惰性电极),若消耗1mol锂,则理论上阴阳两极共产生气体22. 4 L(标准状
况)
【解析】A.负极为Li失电子,生成锂离子,a应为负极,A项错误;B.Li容易与水反应,故不能用水代
替有机溶剂,B项错误;C.正极电极反应式为2SOCl +4e- =S+SO ↑+4Cl-,刺激性气味是二氧化硫,C项
2 2
错误;D.消耗1mol锂,说明转移1mol电子,阴极产生氢气0.5mol,阳极产生氯气0.5mol,故产生气体
共22.4L(标准状况),D项正确;故答案选D。
【答案】D
【题后归纳】判断原电池正、负极的5种方法说明:原电池的正极和负极与电极材料的性质有关,也与电解质溶液有关,不要形成活泼电极一定作负极
的思维定势。
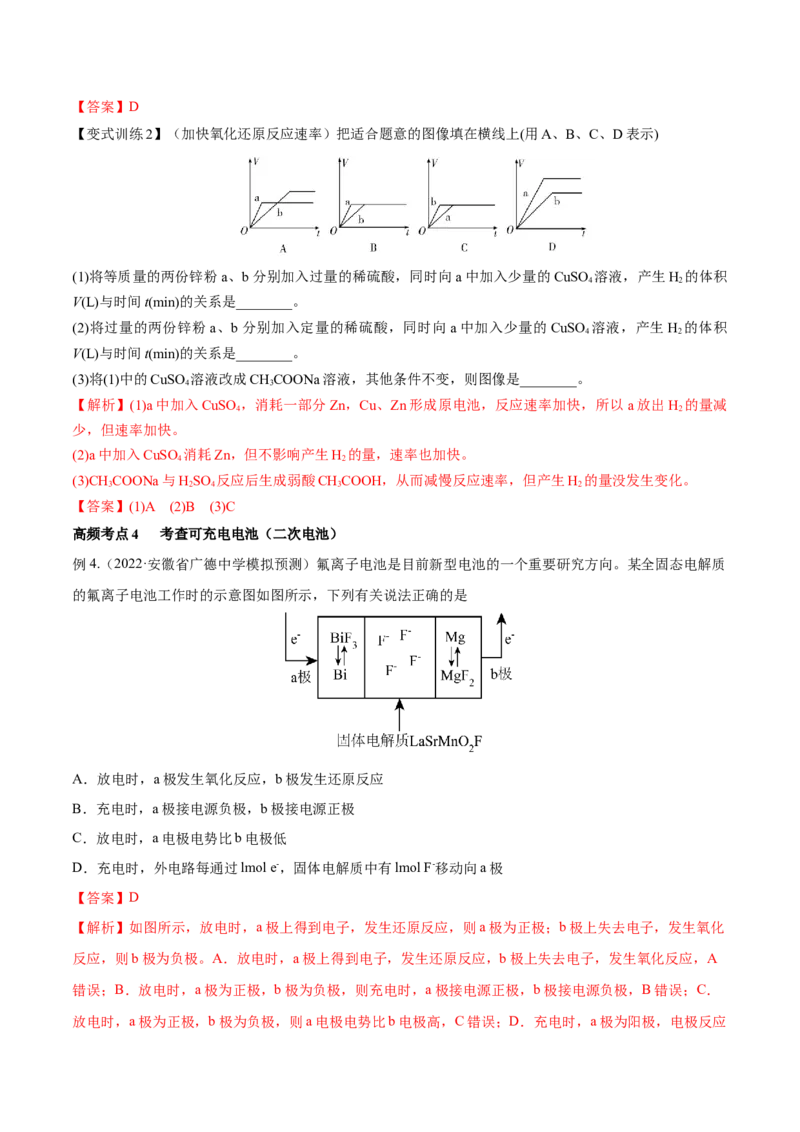
【变式训练】(2022·陕西·西北工业大学附属中学模拟预测)利用小粒径零价铁(ZVI)的电化学腐蚀处理三
氯乙烯进行水体修复的过程如图所示。H+、O、NO 等粒子的存在会影响水体修复效果,设单位时间内
2
ZVI释放电子的物质的量为n-,其中用于有效腐蚀的电子的物质的量为n-。下列说法正确的是
e e
A.增大单位体积水体中ZVI的投入量,可使n-增大
e
B.反应①在负极反生,反应②③④在正极发生
C.单位时间内,三氯乙烯脱去a mol氯原子时n-=a mol
e
D.反应④为 +10H+-8e-= +3HO
2
【解析】A.增大单位体积水体中小微粒ZVI的投入量,可以增大小微粒ZVI和正极的接触面积,加快
ZVI释放电子的速率,可使n 增大,A正确;B.由修复过程示意图中反应前后元素化合价变化可知,反
e
应①②③④均为化合价降低得电子的反应,所以应在正极发生,B错误;C.三氯乙烯C HCl 中C原子化
2 3
合价为+1价,乙烯中C原子化合价为-2价,1 mol C HCl 转化为1 mol C H 时,得到6 mol电子,脱去3
2 3 2 4
mol氯原子,所以脱去a mol Cl时n =2a mol,C错误;D.由示意图可知发了如下转化: → ,由
e-于生成物中有 ,所以只能用H+和HO来配平该反应, 得到电子,发生还原反应,所以④的电极
2
反应式为: +10H++8e-= +3H O,D错误;故合理选项是A。
2
【答案】A
高频考点3 考查原电池原理的应用
例3.(2021·全国·高三专题练习)A、B、C、D都是金属,把C浸入A的硫酸盐溶液中,C的表面有A
析出;A与D组成原电池时,A质量减少;B与D构成原电池时,电子是从D经导线流向B。A、B、C、
D四种金属的活动性顺序为
A.A>B>C>D B.A>C>D>B C.C>A>D>B D.C>D>B>A
【解析】C能置换出A,故活泼性C>A;A质量减少,A为负极,活泼性A>D;电子D经导线流向B,电
子是从负极流向正极,活泼性D>B,金属活泼型综合为C>A>D>B。故选C。
【答案】C
【题后归纳】利用原电池原理比较A、B两种金属活泼性的方法:将A、B两种金属用导线连接后,插入
到稀硫酸中,一段时间后,若观察到A溶解,而B上有气体放出,则说明A作负极,B作正极,即可以断
定金属活泼性A>B。
【变式训练1】(2021·全国·高三专题练习)现有A、B、C、D四种金属片:①把A、B用导线连接后同时
浸入稀硫酸中,B表面逐渐溶解;②把C、D用导线连接后同时浸入稀硫酸中,C发生氧化反应;③把A、
C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C
根据上述情况,下列说法中正确的是
A.在①中,金属片B发生还原反应
B.在②中,金属片C作正极
C.上述四种金属的活动性由强到弱的顺序是:A>B>C>D
D.如果把B、D用导线连接后同时漫入稀硫酸中,则金属片D上有气泡产生
【解析】在①中,B表面逐渐溶解,则B作负极,A作正极;在②中,C发生氧化反应,则C作负极,D
作正极;在③中,电子流动方向为A→导线→C,则A作负极,C作正极。
A.①把A、B用导线连接后同时浸入稀硫酸中,B表面变黑并逐渐溶解;则活动性B>A,B发生氧化反应,
A错误;B.在②中,由于金属片C发生氧化反应,所以C作负极,B错误;C.②把C、D用导线连接后
同时浸入稀硫酸中,C发生氧化反应;则活动性C>D;③把A、C用导线连接后同时浸入稀硫酸中,电子
流动方向为A→导线→C,则活动性A>C,所以四种金属活动性由强到弱的顺序是:B>A> C>D,C错误;
D.如果把B、D用导线连接后同时浸入稀硫酸中,由于活动性B> D,则金属片D作正极,在D上氢离子
得到电子产生氢气,所以有气泡产生,D正确;答案选D。【答案】D
【变式训练2】(加快氧化还原反应速率)把适合题意的图像填在横线上(用A、B、C、D表示)
(1)将等质量的两份锌粉a、b分别加入过量的稀硫酸,同时向a中加入少量的CuSO 溶液,产生H 的体积
4 2
V(L)与时间t(min)的关系是________。
(2)将过量的两份锌粉a、b分别加入定量的稀硫酸,同时向 a中加入少量的CuSO 溶液,产生H 的体积
4 2
V(L)与时间t(min)的关系是________。
(3)将(1)中的CuSO 溶液改成CHCOONa溶液,其他条件不变,则图像是________。
4 3
【解析】(1)a中加入CuSO ,消耗一部分Zn,Cu、Zn形成原电池,反应速率加快,所以a放出H 的量减
4 2
少,但速率加快。
(2)a中加入CuSO 消耗Zn,但不影响产生H 的量,速率也加快。
4 2
(3)CH COONa与HSO 反应后生成弱酸CHCOOH,从而减慢反应速率,但产生H 的量没发生变化。
3 2 4 3 2
【答案】(1)A (2)B (3)C
高频考点4 考查可充电电池(二次电池)
例4.(2022·安徽省广德中学模拟预测)氟离子电池是目前新型电池的一个重要研究方向。某全固态电解质
的氟离子电池工作时的示意图如图所示,下列有关说法正确的是
A.放电时,a极发生氧化反应,b极发生还原反应
B.充电时,a极接电源负极,b极接电源正极
C.放电时,a电极电势比b电极低
D.充电时,外电路每通过lmol e-,固体电解质中有lmol F-移动向a极
【答案】D
【解析】如图所示,放电时,a极上得到电子,发生还原反应,则a极为正极;b极上失去电子,发生氧化
反应,则b极为负极。A.放电时,a极上得到电子,发生还原反应,b极上失去电子,发生氧化反应,A
错误;B.放电时,a极为正极,b极为负极,则充电时,a极接电源正极,b极接电源负极,B错误;C.
放电时,a极为正极,b极为负极,则a电极电势比b电极高,C错误;D.充电时,a极为阳极,电极反应为Bi+3F--3e-=BF ,则外电路每通过1mol e-,固体电解质中有1mol F-移动向a极,D正确;故选D。
3
【题后归纳】可充电电池的思维模型
因此,充电时电极的连接可简记为“负接负后作阴极,正接正后作阳极”。
【变式训练】(2022·天津·耀华中学一模)高电压水系锌—有机混合液流电池的装置如图所示。下列说法
错误的是
A.充电时,中性电解质NaCl的浓度增大
B.放电时,负极反应式为Zn-2e-+4OH-=Zn(OH)
C.充电时,1molFQH 转化为FQ转移2mol电子
2
D.放电时,正极区溶液的pH增大
【答案】A
【解析】高电压水系锌-有机混合液流电池工作原理为:放电时为原电池,金属Zn发生失电子的氧化反应
生成Zn2+,为负极,则FQ所在电极为正极,正极反应式为2FQ+2e-+2H+═FQH,负极反应式为Zn-2e-
2
+4OH-=Zn(OH) ;充电时电解池,原电池的正负极连接电源的正负极,阴阳极的电极反应与原电池的负正
极的反应式相反,电解质中阳离子移向阴极、阴离子移向阳极。A. 充电时装置为电解池,电解质中阳离
子移向阴极、阴离子移向阳极,NaCl溶液中的钠离子和氯离子分别发生定向移动,即电解质NaCl的浓度
减小,故A错误;B. 放电时为原电池,金属Zn为负极,负极反应式为Zn-2e-+4OH-=Zn(OH) ,故B正
确;C. 充电时电解池,阳极反应为FQH -2e-=2FQ+2e-+2H+,则1molFQH 转化为FQ时转移2mol电子,
2 2
故C正确;D.放电时为原电池,正极反应式为2FQ+2e-+2H+═FQH,即正极区溶液的pH增大,故D正确;
2
故选:A。高频考点5 考查新型电源(新型燃料电池)
例5.(2022·河南·模拟预测)水系锌离子电池由于具有对环境友好、成本低等优点,被认为是电池工业的
未来,其放电时的工作原理如图所示。电池进行放电时,MnO /Ti电极上生成的是ZnMn O。下列有关说
2 2 4
法错误的是
A.放电时,H+向MnO /Ti电极移动
2
B.放电时,电池总反应方程式为Zn+2MnO =ZnMn O
2 2 4
C.充电时,当外电路转移1mole-时,理论上Zn电极减重32.5g
D.充电时,MnO /Ti电极上发生反应:ZnMn O-2e-=Zn2++2MnO
2 2 4 2
【解析】放电时,Zn电极作负极,失去电子,发生氧化反应,电极反应式为Zn-2e-=Zn2+;MnO /Ti电极作
2
正极,得到电子,发生还原反应,电极反应式为Zn2++2MnO+2e-=ZnMn O;电池总反应方程式为
2 2 4
Zn+2MnO =ZnMn O。A.放电时,阳离子向正极移动,MnO /Ti电极作正极,则H+向MnO /Ti电极移动,
2 2 4 2 2
A正确;B.放电时,电池总反应方程式为Zn+2MnO =ZnMn O,B正确;C.充电时,Zn电极作阴极,
2 2 4
电极反应为Zn2++2e-=Zn,当外电路转移1mol e-时,理论上Zn电极增重32.5g,C错误;D.充电时,
MnO /Ti电极作阳极,电极反应为ZnMn O-2e-=Zn2++2MnO,D正确;故选C。
2 2 4 2
【答案】C
【名师归纳】间接电化学反应原理分析
(1)定义:间接电化学反应是以具有“电子传递”功能的物质为媒质(催化剂),对反应基质进行间接氧化或
还原,从而得到目的产物。
(2)原理:媒质也称为“电对”或“介对”,其首先在电极表面失去(或得到)电子,形成氧化态(或还原态)
在电解溶液中进一步氧化(或还原)反应基质,最终生成目的产物。
其原理如下图所示:
【变式训练】(2022·辽宁·鞍山一中模拟预测)图是碳呼吸电池(仅转化空气中的CO)工作原理示意图,已
2
知Al (C O) 难溶于水,有关说法错误的是
2 2 4 3A.该装置可将化学能转变为电能
B.正极的电极反应为2CO+2e- =
2
C.每生成1 mol Al (C O),有6 mol电子流过负载
2 2 4 3
D.随着反应进行,草酸盐浓度大幅减小
【解析】A.该装置属于原电池,可将化学能转化为电能,故A正确;B.原电池的正极得到电子发生还
原反应,即CO 得到电子被还原为 ,则其电极方程式为2CO+2e- = ,故B正确;C.每生成1
2 2
mol Al (C O),需消耗2molAl,2molAl失去6mol电子,所以每生成1 mol Al (C O),有6 mol电子流过
2 2 4 3 2 2 4 3
负载,故C正确;D.该原电池的总反应为 ,生成的 难溶于水,所以
随着反应的进行,草酸盐的浓度保持不变,故D错误;答案选D。
【答案】D