文档内容
1.目前市场上有一种专门为婴幼儿设计的电解质饮料,适合在婴幼儿感冒、发烧时快速补
充体内流失的电解质成分。下列物质可用作该饮料中的电解质的是( )
A.Fe B.葡萄糖 C.MgSO D.CO
4 2
2.下列说法正确的是( )
A.CO 的水溶液能导电,所以CO 是电解质
2 2
B.BaSO 难溶于水,其水溶液的导电能力极弱,所以BaSO 的电离方程式为BaSOBa2+
4 4 4
+SO
C.液溴不导电,所以溴是非电解质
D.强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强
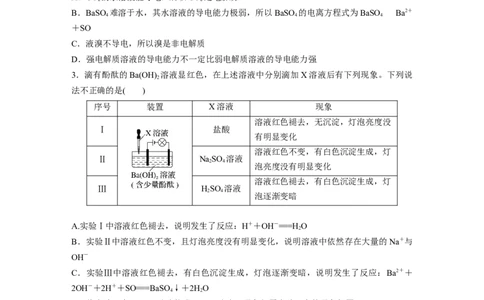
3.滴有酚酞的Ba(OH) 溶液显红色,在上述溶液中分别滴加X溶液后有下列现象。下列说
2
法不正确的是( )
序号 装置 X溶液 现象
溶液红色褪去,无沉淀,灯泡亮度没
Ⅰ 盐酸
有明显变化
溶液红色不变,有白色沉淀生成,灯
Ⅱ NaSO 溶液
2 4
泡亮度没有明显变化
溶液红色褪去,有白色沉淀生成,灯
Ⅲ HSO 溶液
2 4
泡逐渐变暗
A.实验Ⅰ中溶液红色褪去,说明发生了反应:H++OH-===HO
2
B.实验Ⅱ中溶液红色不变,且灯泡亮度没有明显变化,说明溶液中依然存在大量的Na+与
OH-
C.实验Ⅲ中溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗,说明发生了反应:Ba2++
2OH-+2H++SO===BaSO↓+2HO
4 2
D.将实验Ⅱ中NaSO 溶液换成CuSO 溶液,现象与原实验Ⅱ中的现象相同
2 4 4
4.(2021·广东,15)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应
的反应方程式书写正确的是( )
A.NaO 放入水中:NaO+HO===2NaOH+O↑
2 2 2 2 2 2
B.HO(g)通过灼热铁粉:3HO+2Fe===Fe O + 3H
2 2 2 3 2
C.铜丝插入热的浓硫酸中:Cu+HSO ===CuSO + H↑
2 4 4 2
D.SO 通入酸性KMnO 溶液中:5SO +2HO+2MnO===5SO+4H++2Mn2+
2 4 2 2
5.(2021·全国乙卷,9)下列过程中的化学反应,相应的离子方程式正确的是( )A.用碳酸钠溶液处理水垢中的硫酸钙:CO+CaSO===CaCO + SO
4 3
B.过量铁粉加入稀硝酸中:Fe +4H++NO===Fe3++NO↑+2HO
2
C.硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-===AlO+2HO
2
D.氯化铜溶液中通入硫化氢:Cu2++ S2-===CuS↓
6.(2021·浙江6月选考,13)不能正确表示下列变化的离子方程式的是( )
A.碳酸镁与稀盐酸反应:CO+2H+===CO↑+HO
2 2
B.亚硫酸氢钠的水解:HSO+HOHSO +OH-
2 2 3
C.锌溶于氢氧化钠溶液:Zn+2OH-+2HO===[Zn(OH) ]2-+H↑
2 4 2
D.亚硝酸钠与氯化铵溶液受热反应:NO+NH=====N↑+2HO
2 2
7.(2021·湖南1月适应性考试,10)下列离子方程式书写正确的是( )
A.饱和NaCO 溶液中通入过量CO:CO+CO+HO===2HCO
2 3 2 2 2
B.NaClO溶液中通入少量SO :SO +HO+ClO-===SO+Cl-+2H+
2 2 2
C.FeI 溶液中通入少量Cl:Cl+2Fe2+===2Fe3++2Cl-
2 2 2
D.Ca(HCO ) 溶液中滴入少量Ca(OH) 溶液:
3 2 2
Ca2++OH-+HCO===CaCO ↓+HO
3 2
8.(2022·武汉高三5月联考)下列有关反应的离子方程式书写错误的是( )
A.Fe与稀硝酸反应:当n(Fe)∶n(HNO)=1∶2时,3Fe+2NO+8H+===3Fe2++2NO↑+
3
4HO
2
B.向碳酸氢钙溶液中加入足量石灰水:Ca2++HCO+OH-===CaCO ↓+HO
3 2
C.NaO 与HO反应:2NaO+2HO===4Na++4OH-+18O↑
2 2 2 2 2
D.NaSO 溶液中通入足量氯气:SO+4Cl+5HO===2SO+8Cl-+10H+
2 2 3 2 2 2
9.(2023·郑州联考) 下列过程中的化学反应,相应的离子方程式正确的是( )
A.向石灰石中加入盐酸:CaCO +2H+===Ca2++CO↑+HO
3 2 2
B.利用氢氧化钠溶液吸收废气NO :2NO +2OH-===2NO+HO
2 2 2
C.向硫酸镁溶液中滴加氢氧化钡溶液:Mg2++2OH-===Mg(OH) ↓
2
D.将ICl滴入NaOH溶液中:ICl+2OH-===I-+ClO-+HO
2
10.(2022·宁夏银川一中模拟)下列离子方程式与实验对应不正确的是( )
选项 实验 离子方程式
向橙色KCr O 溶液中加入NaOH溶
2 2 7
A Cr O+2OH-2CrO+HO
2 2
液,溶液变黄色
向AgCl悬浊液中加入NaS溶液,有
2
B 2AgCl+S2-===Ag S+2Cl-
2
黑色难溶物生成
向NH HCO 溶液中加入过量Ba(OH) NH+HCO+Ba2++2OH-
4 3 2
C
稀溶液,有白色沉淀产生 ===BaCO ↓+NH ·H O+HO
3 3 2 2
D 向KMnO 溶液(墨绿色)中加入适量醋 3MnO+4H+===2MnO+MnO ↓
2 4 2酸,溶液变为紫色且有黑色沉淀生成 +2HO
2
11. 向50 g质量分数为10.6%的NaCO 溶液中,逐滴加入CaCl 稀溶液。测得溶液中离子的
2 3 2
数量变化如图。请据此分析以下问题:
(1)请指出以下曲线表示的离子符号:A______;C________;D________。
(2)反应的化学方程式为__________________________________________。
(3)当A、C曲线相交时,生成的沉淀质量为____g。
12.无机化合物按照组成和性质可进行如下分类。其中②、③、⑥均由Na、K、H、N、
O、S中的三种元素组成。
强酸 强碱 可溶性盐 ★
①HCl ③ ⑤NaCO ⑦CO
2 3 2
② ④Ba(OH) ⑥ ⑧SO
2 3
(1)表中★可以代表的物质类别为__________________________________。
(2)③ 水 溶 液 呈 碱 性 , 写 出 电 离 方 程 式 :
_____________________________________________(写一种即可)。
(3)②与④在水溶液中发生反应的离子方程式:____________________________________(无
沉淀生成)。
(4)④与少量的⑦在水溶液中发生反应的离子方程式:______________________________。
(5)④与⑥在水溶液中发生反应的离子方程式:____________________________________。
13.请按要求书写下列离子方程式:
(1)向 Ba(HCO ) 溶液中滴入 NaHSO 溶液,至沉淀完全,写出反应的离子方程式:
3 2 4
________________________________________________________________________。
在上述溶液中继续滴入NaHSO 溶液,此时离子方程式为_____________________________。
4
(2)0.2 mol·L-1的NH Al(SO ) 溶液与0.3 mol·L-1的Ba(OH) 溶液等体积混合:
4 4 2 2
________________________________________________________________________。
(3)AlCl 溶 液 与 烧 碱 溶 液 反 应 , 当 n(OH - )∶n(Al3 + ) = 7∶2 时 :
3
_________________________。
(4)CuCl 溶 液 与 NaHS 溶 液 反 应 , 当 n(CuCl )∶n(NaHS) = 1∶2 时 :
2 2
_______________________。
(5) 标 准 状 况 下 , 2.24 L CO 通 入 250 mL 0.5 mol·L - 1 的 NaOH 溶 液 中 :
2
________________________________________________________________________。
(6)100 mL 0.1 mol·L - 1 的 NaCO 溶 液 中 加 入 0.01 mol CH COOH :
2 3 3_______________________。
(7)4 mol·L-1的NaAlO 溶液和7 mol·L-1的盐酸等体积均匀混合:_______________________。
2