文档内容
训练(二十四) 原子结构 化学键
1.(2021·全国百校联盟联考)二氧化碳是导致地球温室效应的主要气体,可采用碱性溶
液吸收工业生产中的CO,反应为:CO+2NaOH===Na CO+HO,下列相关微粒的化学用
2 2 2 3 2
语正确的是( )
A.中子数为10的氧原子:O
B.CO 的结构式:O—C—O
2
C.NaOH电子式:
D.H+的结构示意图:
A [CO 的结构式为O=C=O,B项错误;NaOH的电子式为 ,C项错误;
2
H+的核外电子数为0,D项错误。]
2.(2020.1·浙江选考)有共价键的离子化合物是( )
A.NaO B.HSO
2 2 2 4
C.CHCl D.SiCl
2 2
A [H SO 、CHCl、SiCl都是含共价键的共价化合物;由NaO 由Na+和O离子构成,
2 4 2 2 2 2
是含有共价键和离子键的离子化合物。]
3.(2021·北京房山区检测)含氯消毒液(主要成分为NaClO)与含氯洁厕灵(主要成分为
HCl)混用可能会引起中毒,其原因是NaClO+2HCl===Cl↑+NaCl+HO,下列说法中正确
2 2
的是( )
A.NaCl的电子式为
B.NaClO中只含有离子键
C.当释放2.24 L Cl 时,一定有6.02×1022个氯气分子扩散到室内
2
D.使用消毒液时滴加食醋可增强消毒作用,其原因用离子方程式表示为 ClO-+
CHCOOH===HClO+CHCOO-
3 3
D [NaCl是离子化合物,写电子式时阴离子要用括号括起来,即NaCl的电子式为
,A项错误;NaClO中含有离子键和极性共价键,B项错误;没有说明是在标
准状况下,故2.24 L Cl 的物质的量不一定是0.1 mol,C项错误;使用消毒液时滴加食醋,依
2
据强酸制弱酸原理,醋酸可以与 ClO-反应生成 HClO,离子方程式为 ClO-+
CHCOOH===HClO+CHCOO-,D项正确。]
3 3
4.(2021·北京石景山区检测)在NH 和NH Cl存在的条件下,以活性炭为催化剂,用
3 4
HO 氧化CoCl 溶液来制备化工产品[Co(NH )]Cl ,下列表述正确的是( )
2 2 2 3 6 3
A.中子数为32,质子数为27的钴原子:CoB.HO 的电子式:
2 2
C.NH 和NH Cl的化学键类型相同
3 4
D.[Co(NH )]Cl 中Co的化合价是+3价
3 6 3
D [ 中子数为32,质子数为27的钴原子的质量数为32+27=59,A项错误;HO 为共
2 2
价化合物,其电子式为 ,B项错误;NH 中存在共价键,NH Cl中存在离子键和共
3 4
价键,C项错误;[Co(NH )]Cl 中NH 整体为0价,Cl为-1价,所以Co的化合价是+3价,D
3 6 3 3
项正确。]
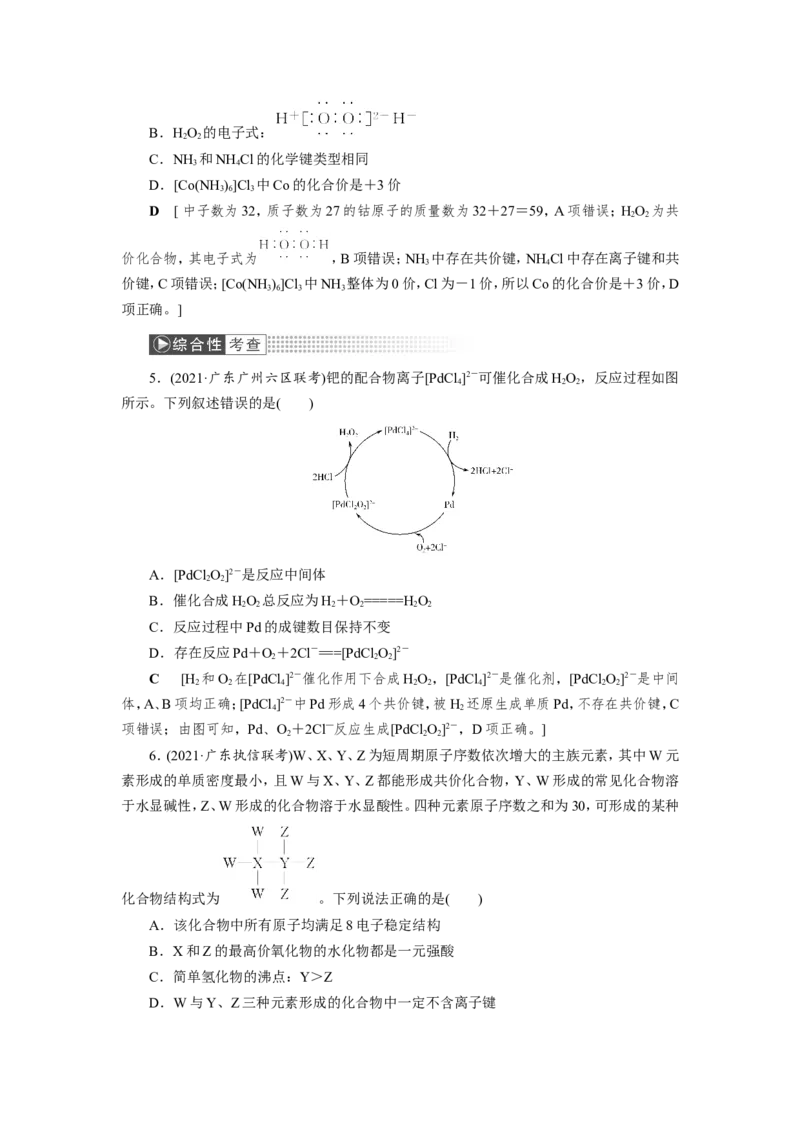
5.(2021·广东广州六区联考)钯的配合物离子[PdCl ]2-可催化合成HO,反应过程如图
4 2 2
所示。下列叙述错误的是( )
A.[PdCl O]2-是反应中间体
2 2
B.催化合成HO 总反应为H+O=====HO
2 2 2 2 2 2
C.反应过程中Pd的成键数目保持不变
D.存在反应Pd+O+2Cl-===[PdCl O]2-
2 2 2
C [H 和O 在[PdCl ]2-催化作用下合成HO,[PdCl ]2-是催化剂,[PdCl O]2-是中间
2 2 4 2 2 4 2 2
体,A、B项均正确;[PdCl ]2-中Pd形成4个共价键,被H 还原生成单质Pd,不存在共价键,C
4 2
项错误;由图可知,Pd、O+2Cl—反应生成[PdCl O]2-,D项正确。]
2 2 2
6.(2021·广东执信联考)W、X、Y、Z为短周期原子序数依次增大的主族元素,其中W元
素形成的单质密度最小,且W与X、Y、Z都能形成共价化合物,Y、W形成的常见化合物溶
于水显碱性,Z、W形成的化合物溶于水显酸性。四种元素原子序数之和为30,可形成的某种
化合物结构式为 。下列说法正确的是( )
A.该化合物中所有原子均满足8电子稳定结构
B.X和Z的最高价氧化物的水化物都是一元强酸
C.简单氢化物的沸点:Y>Z
D.W与Y、Z三种元素形成的化合物中一定不含离子键C [由题给信息推知,W、X、Y、Z分别为H、B、N、Cl,形成化合物为BH·NCl ,其中H
3 3
原子不满足最外层8电子稳定结构,A项错误;HBO 是一元弱酸,B项错误;NH 形成分子
3 3 3
间氢键,HCl只存在范德华力,故沸点:NH >HCl,C项正确;H、N、Cl三种元素可形成离子
3
化合物NH Cl,含有离子键和共价键,D项错误。]
4
7.(2020·河北唐山摸底)短周期元素X、Y、Z、W、M的原子序数依次增大且不含稀有气
体元素,X元素原子核内只含1个质子且与W同主族,Y的最外层电子数是次外层电子数2
倍,Z、M同主族且能形成两种常见的化合物。则下列说法中不正确的是( )
A.Y单质的氧化性小于Z单质
B.元素简单离子的半径大小为M>Z>W>X
C.YX 与XM均能使溴水褪色,且褪色原理相同
2 4 2
D.X、Z、W形成的化合物中既含离子键又含共价键
C [X原子核内只有1个质子,则X是H元素;Y原子最外层电子数是次外层电子数2
倍,则Y是C元素;Z、M同主族且能形成两种常见的化合物,应是SO 和SO ,则Z是O,M
2 3
是S;X与W同主族,且W的原子序数介于Z和M之间,则W是Na。元素的非金属性:C<
O,则单质的氧化性:碳单质<O,A项正确;简单离子半径:S2->O2->Na+>H+,即M>Z
2
>W>X,B项正确;YX、XM分别为C H、HS,前者与溴水发生加成反应,后者与溴水发
2 4 2 2 4 2
生氧化还原反应,褪色原理不同,C项错误;H、O、Na可形成离子化合物NaOH,既含有离子
键又含有共价键,D项正确。]
8.(2021·河北衡水中学调研)A、B、C、D、E是原子序数依次增大的五种短周期元素且B、
C相邻,A元素可以与B、C、E元素分别形成甲、乙、丙三种物质,且甲、乙均为10电子化合
物,丙为18电子化合物。D元素的最外层电子数与核外电子层数相等。已知:甲+E―→丙+
2
B ,甲+丙―→丁,下列说法中正确的是( )
2
A.离子半径:D>C>B
B.A与C两种元素共同形成的10电子粒子有3种
C.D元素在周期表中的位置是第二周期第ⅡA族
D.丁物质均由非金属元素构成,只含共价键
B [A、B、C、D、E是原子序数依次增大的五种短周期元素,A元素可以与B、C、E元素
分别形成甲、乙、丙三种物质,且甲、乙均为10电子化合物,丙为18电子化合物,则A为氢元
素,10电子化合物可能为CH、NH 、HO、HF等;已知甲+E―→丙+B ,甲+丙―→丁,则
4 3 2 2 2
E的单质为双原子分子,故E为Cl元素,则B为N元素,因B、C相邻,则C为O元素,故甲
为NH 、乙为HO、丙为HCl、丁为NH Cl;D元素的最外层电子数与核外电子层数相等,原子
3 2 4
序数大于氧元素,处于第三周期,最外层电子数为3,故D为Al元素。N3-、O2-、Al3+电子层
结构相同,核电荷数越大离子半径越小,故离子半径:N3->O2->Al3+,A项错误;H和O两种
元素共同形成的10电子粒子有HO、HO+、OH- 3种,B项正确;Al元素在元素周期表中的
2 3
位置是第三周期第ⅢA族,C项错误;丁为NH Cl,含有离子键、共价键,D项错误。]
49.(2021·广东湛江联考)X、Y、Z、W是四种原子序数依次增大的短周期元素,W的最外
层电子数为X最外层电子数的一半,X、Y、Z的原子半径依次减小,X、Y、Z组成的一种化合
物(ZXY) 的结构式为Y≡X—Z—Z—X≡Y。下列说法正确的是( )
2
A.简单氢化物的稳定性:X>Y
B.Y的氧化物对应的水化物都是强酸
C.化合物WY 中只含有离子键
3 2
D.X和Z组成的化合物中不可能所有原子都达到8电子稳定结构
C [X、Y、Z的原子序数依次增大,但原子半径依次减小,则X、Y、Z处于同周期;化合
物(ZXY) 中,X、Y、Z形成共价键个数分别为4、3、2,则X、Y、Z分别处于第ⅣA、ⅤA、ⅥA
2
族;又知“W的最外层电子数为X最外层电子数的一半”,则W处于第ⅡA族,且原子序数
最大,则W是Mg,从而推知X、Y、Z分别为C、N、O元素。非金属性:C