文档内容
[复习目标] 1.了解速率常数、平衡常数的关系。2.掌握化学平衡常数的计算。
1.化学平衡常数
(1)意义:化学平衡常数K表示反应进行的程度,K越大,反应进行的程度越大。K>105时,
可以认为该反应已经进行完全。K的大小只与温度有关。
(2)化学平衡常数表达式:对于可逆化学反应mA(g)+nB(g)pC(g)+qD(g)在一定温度下达
到化学平衡时,K=。另可用压强平衡常数表示:K =[p(C)为平衡时气体C的分压]。
p
(3)依据化学方程式计算平衡常数
①同一可逆反应中,K ·K =1。
正 逆
②同一方程式中的化学计量数等倍扩大或缩小n倍,则新平衡常数K′与原平衡常数K间的
关系是K′=Kn或K′=。
③几个可逆反应方程式相加,得总方程式,则总反应的平衡常数等于各分步反应平衡常数之
积。
2.转化率、产率及分压的计算
反应物的转化率=×100%
产物的产率=×100%
分压=总压×物质的量分数
3.常用的气体定律
同温同体积:p(前)∶p(后)=n(前)∶n(后)
同温同压强:===
4.速率常数与化学平衡常数关系的应用
温度为T ,在三个容积均为1 L的恒容密闭容器中仅发生反应CH(g)+HO(g)CO(g)+
1 4 2
3H
2
(g) ΔH=+206.3 kJ·mol-1,该反应中,正反应速率为v正 =k
正
c(CH
4
)·c(H
2
O),逆反应
速率为v逆 =k
逆
c(CO)·c3(H
2
),k
正
、k
逆
为速率常数,受温度影响。
已知T 时,k =k ,则该温度下,平衡常数K =____;当温度改变为T 时,若k =1.5k ,
1 正 逆 1 2 正 逆
则T______(填“>”“=”或“<”)T。
2 1
1.[2022·全国乙卷,28(3)(4)]油气开采、石油化工、煤化工等行业废气普遍含有硫化氢,需
要回收处理并加以利用。回答下列问题:(3)在1 470 K、100 kPa反应条件下,将n(H S)∶n(Ar)=1∶4的混合气进行HS热分解反应。
2 2
平衡时混合气中 HS 与 H 的分压相等,HS 平衡转化率为__________,平衡常数 K =
2 2 2 p
__________ kPa。
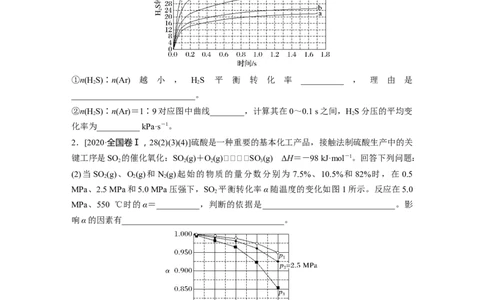
(4)在1 373 K、100 kPa反应条件下,对于n(H S)∶n(Ar)分别为4∶1、1∶1、1∶4、1∶9、
2
1∶19的HS-Ar混合气,热分解反应过程中HS转化率随时间的变化如图所示。
2 2
①n(H S)∶n(Ar) 越 小 , HS 平 衡 转 化 率 __________ , 理 由 是
2 2
_____________________________。
②n(H S)∶n(Ar)=1∶9对应图中曲线________,计算其在0~0.1 s之间,HS分压的平均变
2 2
化率为__________ kPa·s-1。
2.[2020·全国卷Ⅰ,28(2)(3)(4)]硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关
键工序是SO 的催化氧化:SO (g)+O(g)SO (g) ΔH=-98 kJ·mol-1。回答下列问题:
2 2 2 3
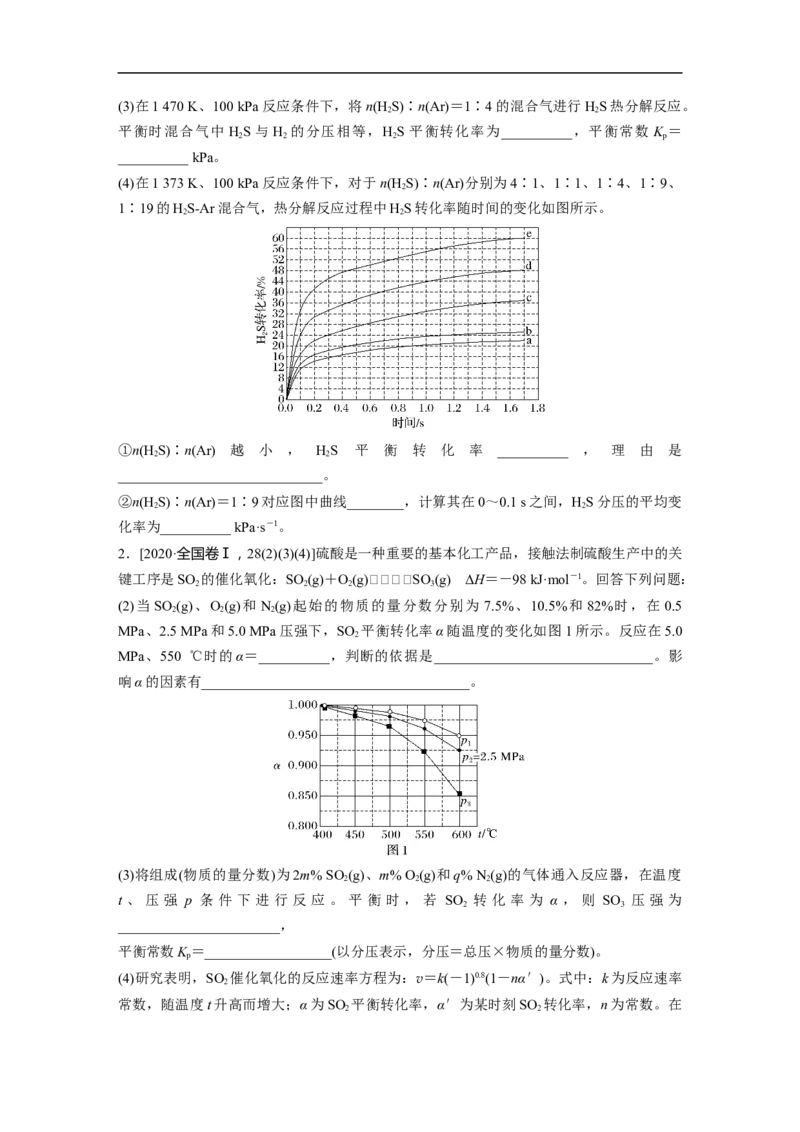
(2)当 SO (g)、O(g)和 N(g)起始的物质的量分数分别为 7.5%、10.5%和 82%时,在 0.5
2 2 2
MPa、2.5 MPa和5.0 MPa压强下,SO 平衡转化率α随温度的变化如图1所示。反应在5.0
2
MPa、550 ℃时的α=__________,判断的依据是_______________________________。影
响α的因素有______________________________________。
(3)将组成(物质的量分数)为2m% SO(g)、m% O (g)和q% N (g)的气体通入反应器,在温度
2 2 2
t 、 压 强 p 条 件 下 进 行 反 应 。 平 衡 时 , 若 SO 转 化 率 为 α , 则 SO 压 强 为
2 3
_______________________,
平衡常数K =__________________(以分压表示,分压=总压×物质的量分数)。
p
(4)研究表明,SO 催化氧化的反应速率方程为:v=k(-1)0.8(1-nα′)。式中:k为反应速率
2
常数,随温度t升高而增大;α为SO 平衡转化率,α′为某时刻SO 转化率,n为常数。在
2 2α′=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线,如图2所示。
曲线上v最大值所对应温度称为该α′下反应的最适宜温度t 。tt 后,
m m m
v逐渐下降。原因是___________________________________________________________。
3.[2020·全国卷Ⅱ,28(1)]乙烷在一定条件可发生如下反应:C H(g)===C H(g)+H(g)
2 6 2 4 2
ΔH,相关物质的燃烧热数据如下表所示:
1
物质 C H(g) C H(g) H(g)
2 6 2 4 2
燃烧热ΔH/( kJ·mol-1) -1 560 -1 411 -286
①ΔH=________ kJ·mol-1。
1
②提高该反应平衡转化率的方法有________________、________________。
③容器中通入等物质的量的乙烷和氢气,在等压下(p)发生上述反应,乙烷的平衡转化率为
α。反应的平衡常数K =______________(用平衡分压代替平衡浓度计算,分压=总压×物
p
质的量分数)。
4.(2020·全国卷Ⅲ,28)二氧化碳催化加氢合成乙烯是综合利用CO 的热点研究领域。回答
2
下列问题:
(1)CO 催化加氢生成乙烯和水的反应中,产物的物质的量之比 n(C H)∶n(H O)=
2 2 4 2
__________。当反应达到平衡时,若增大压强,则 n(C H)____________(填“变大”“变
2 4
小”或“不变”)。
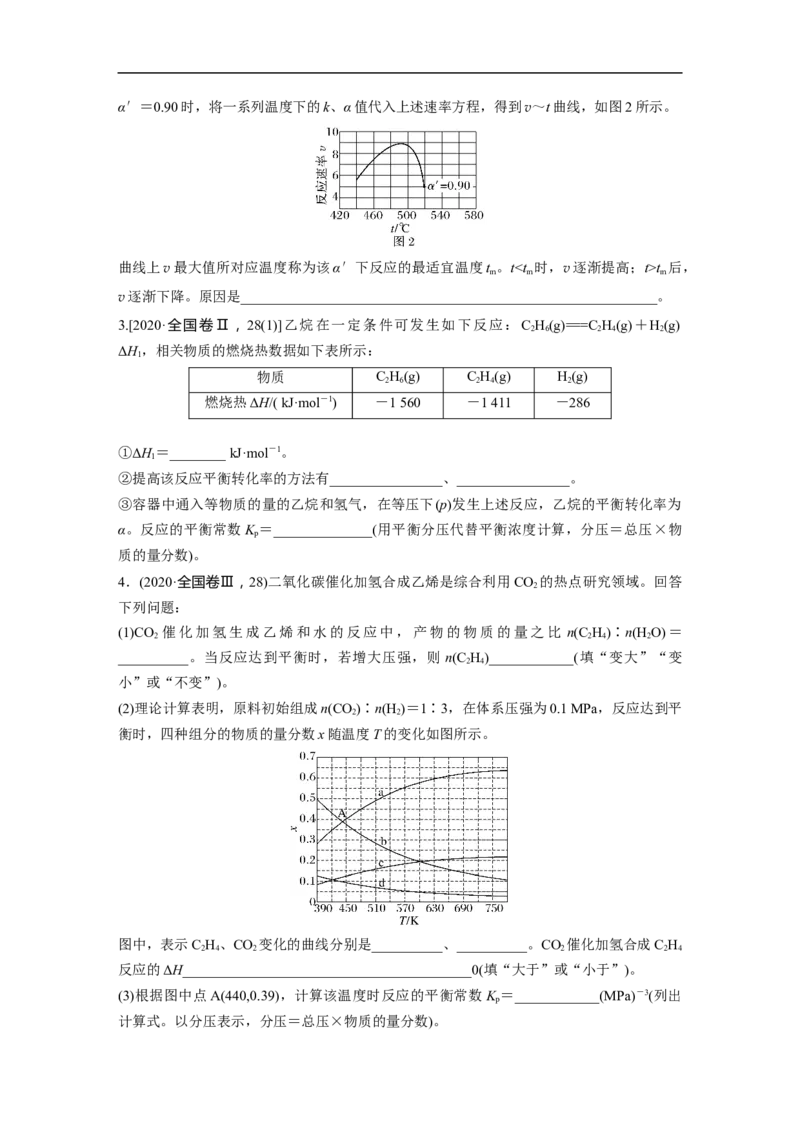
(2)理论计算表明,原料初始组成n(CO)∶n(H )=1∶3,在体系压强为0.1 MPa,反应达到平
2 2
衡时,四种组分的物质的量分数x随温度T的变化如图所示。
图中,表示C H、CO 变化的曲线分别是__________、__________。CO 催化加氢合成C H
2 4 2 2 2 4
反应的ΔH_________________________________________0(填“大于”或“小于”)。
(3)根据图中点A(440,0.39),计算该温度时反应的平衡常数K =____________(MPa)-3(列出
p
计算式。以分压表示,分压=总压×物质的量分数)。(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成 C H 、C H 、C H 等低碳烃。一
3 6 3 8 4 8
定温度和压强条件下,为了提高反应速率和乙烯选择性,应当___________________。
5.[2019·全国卷Ⅰ,28(1)(2)(4)]水煤气变换[CO(g)+HO(g)===CO(g)+H(g) ΔH<0]是重
2 2 2
要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。
回答下列问题:
(1)Shibata曾做过下列实验:①使纯H 缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化
2
钴部分被还原为金属钴Co(s),平衡后气体中H 的物质的量分数为0.025 0。
2
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.019 2。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO______H (填“大于”或“小于”)。
2
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和HO(g)混合,采用适当的催化剂进行
2
反应,则平衡时体系中H 的物质的量分数为__________(填标号)。
2
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
(4)Shoichi研究了467 ℃、489 ℃时水煤气变换中CO和H 分压随时间变化关系(如图所示),
2
催化剂为氧化铁,实验初始时体系中的 和p 相等、 和 相等。
CO
计算曲线a的反应在30~90 min内的平均速率(a)=________ kPa·min-1。467 ℃时 和
p 随时间变化关系的曲线分别是________、________。489 ℃时 和p 随时间变化关系
CO CO
的曲线分别是______、______。
6.[2019·全国卷Ⅱ,27(2)(3)改编]环戊二烯( )是重要的有机化工原料,广泛用于农药、
橡胶、塑料等生产。回答下列问题:
(2)某温度,等物质的量的碘和环戊烯( )在刚性容器内发生反应[ (g)+I(g)===
2
(g)+2HI(g) ΔH=+89.3 kJ·mol-1],起始总压为105 Pa,平衡时总压增加了20%,环戊烯
的转化率为________,该反应的平衡常数K =________Pa。达到平衡后,欲增加环戊烯的
p
平衡转化率,可采取的措施有________(填标号)。
A.通入惰性气体
B.提高温度C.增加环戊烯浓度
D.增加碘浓度
(3)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下,溶液中环戊二烯
浓度与反应时间的关系如图所示,下列说法正确的是______(填标号)。
A.T>T
1 2
B.a点的反应速率小于c点的反应速率
C.a点的正反应速率大于b点的逆反应速率
D.b点时二聚体的浓度为0.45 mol·L-1
考向一 连续反应、竞争反应平衡常数的计算
1.加热NO 依次发生的分解反应为①NO(g)NO(g)+O(g),②NO(g)NO(g)+
2 5 2 5 2 3 2 2 3 2
O(g)。在容积为2 L的密闭容器中充入8 mol N O ,加热到t ℃,达到平衡状态后O 为9
2 2 5 2
mol,NO 为3.4 mol。则t ℃时反应①的平衡常数为( )
2 3
A.10.7 B.8.5
C.9.6 D.10.2
考向二 分压常数的计算
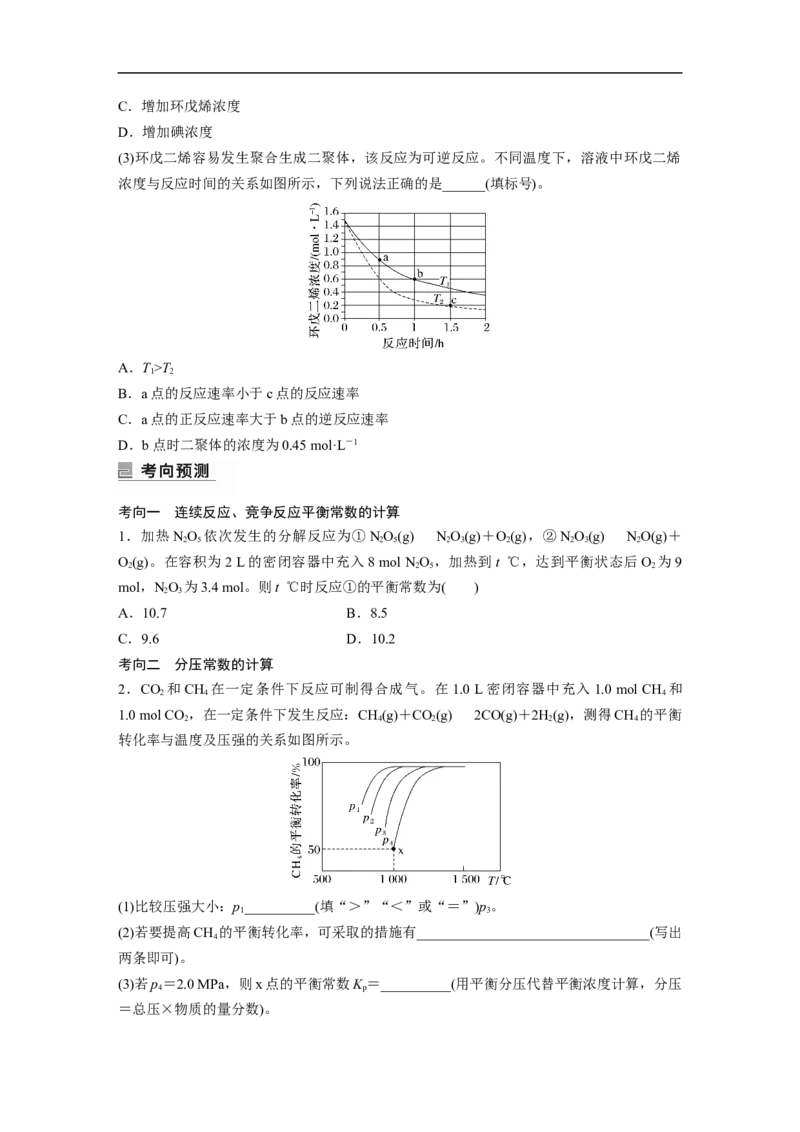
2.CO 和CH 在一定条件下反应可制得合成气。在 1.0 L密闭容器中充入1.0 mol CH 和
2 4 4
1.0 mol CO ,在一定条件下发生反应:CH(g)+CO(g)2CO(g)+2H(g),测得CH 的平衡
2 4 2 2 4
转化率与温度及压强的关系如图所示。
(1)比较压强大小:p__________(填“>”“<”或“=”)p。
1 3
(2)若要提高CH 的平衡转化率,可采取的措施有_________________________________(写出
4
两条即可)。
(3)若p=2.0 MPa,则x点的平衡常数K =__________(用平衡分压代替平衡浓度计算,分压
4 p
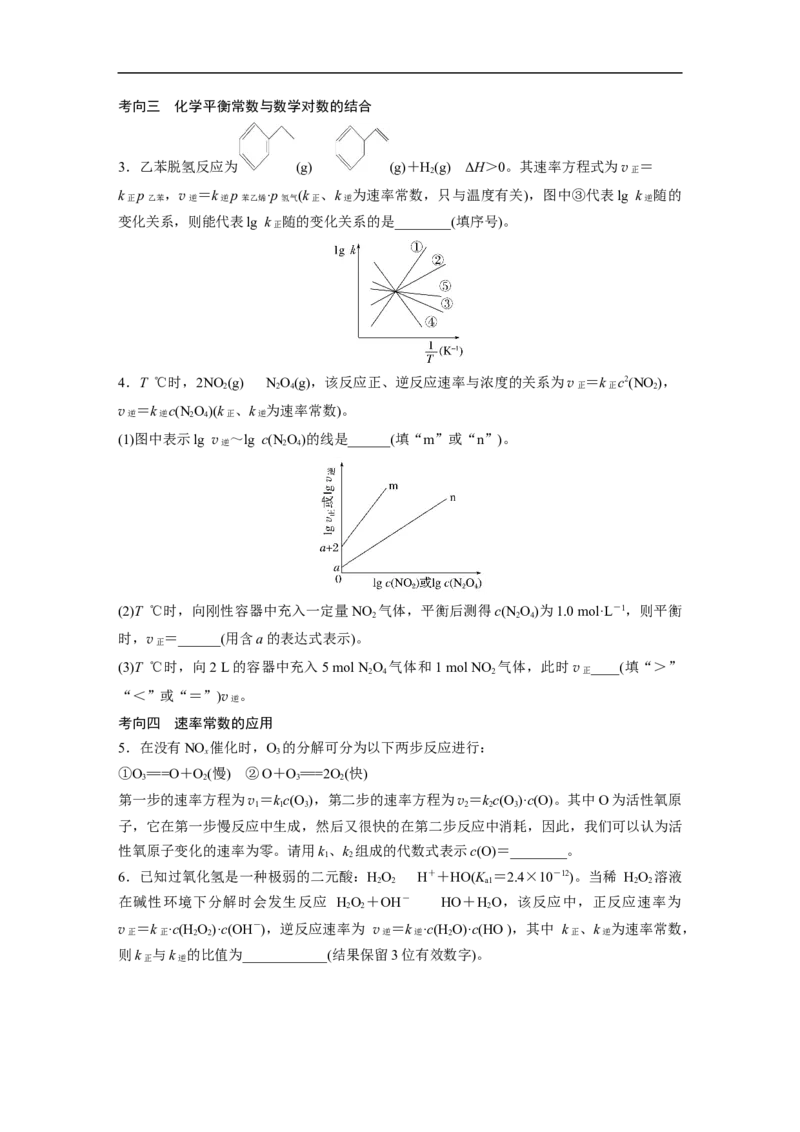
=总压×物质的量分数)。考向三 化学平衡常数与数学对数的结合
3.乙苯脱氢反应为 (g) (g)+H
2
(g) ΔH>0。其速率方程式为v正 =
k
正
p
乙苯
,v逆 =k
逆
p
苯乙烯
·p
氢气
(k
正
、k
逆
为速率常数,只与温度有关),图中③代表lg k
逆
随的
变化关系,则能代表lg k 随的变化关系的是________(填序号)。
正
4.T ℃时,2NO
2
(g)N
2
O
4
(g),该反应正、逆反应速率与浓度的关系为v正 =k
正
c2(NO
2
),
v逆 =k 逆 c(N 2 O 4 )(k 正 、k 逆 为速率常数)。
(1)图中表示lg v逆 ~lg c(N
2
O
4
)的线是______(填“m”或“n”)。
(2)T ℃时,向刚性容器中充入一定量NO 气体,平衡后测得c(N O)为1.0 mol·L-1,则平衡
2 2 4
时,v正 =______(用含a的表达式表示)。
(3)T ℃时,向2 L的容器中充入5 mol N
2
O
4
气体和1 mol NO
2
气体,此时v正 ____(填“>”
“<”或“=”)v逆 。
考向四 速率常数的应用
5.在没有NO 催化时,O 的分解可分为以下两步反应进行:
x 3
①O===O+O(慢) ②O+O===2O(快)
3 2 3 2
第一步的速率方程为v=kc(O ),第二步的速率方程为v=kc(O )·c(O)。其中O为活性氧原
1 1 3 2 2 3
子,它在第一步慢反应中生成,然后又很快的在第二步反应中消耗,因此,我们可以认为活
性氧原子变化的速率为零。请用k、k 组成的代数式表示c(O)=________。
1 2
6.已知过氧化氢是一种极弱的二元酸:HOH++HO(K =2.4×10-12)。当稀 HO 溶液
2 2 a1 2 2
在碱性环境下分解时会发生反应 HO +OH-HO+HO,该反应中,正反应速率为
2 2 2
v正 =k 正 ·c(H 2 O 2 )·c(OH-),逆反应速率为 v逆 =k 逆 ·c(H 2 O)·c(HO ),其中 k 正 、k 逆 为速率常数,
则k 与k 的比值为____________(结果保留3位有效数字)。
正 逆