文档内容
第 21 讲 化学反应的热效应
(模拟精练+真题演练)
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12×5分)
1.(2023·浙江·校联考三模)标准状态下,气态反应物、生成物及活化分子[A(B)表示“A+B→产物”的
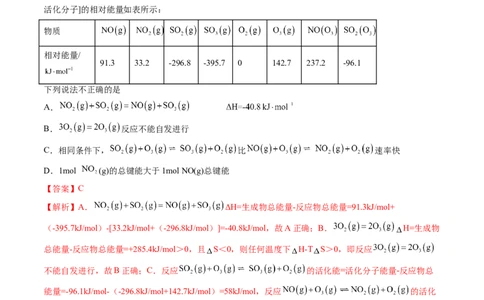
活化分子]的相对能量如表所示:
物质
相对能量/
91.3 33.2 -296.8 -395.7 0 142.7 237.2 -96.1
下列说法不正确的是
A.
B. 反应不能自发进行
C.相同条件下, 比 速率快
D.1mol (g)的总键能大于1mol NO(g)总键能
【答案】C
【解析】A. ΔH=生成物总能量-反应物总能量=91.3kJ/mol+
(-395.7kJ/mol)-[33.2kJ/mol+(-296.8kJ/mol)]=-40.8kJ/mol,故A正确;B. H=生成物
总能量-反应物总能量=+285.4kJ/mol>0,且 S<0,则任何温度下 H-T S>0,即反应
不能自发进行,故B正确;C.反应 的活化能=活化分子能量-反应物总
能量=-96.1kJ/mol-(-296.8kJ/mol+142.7kJ/mol)=58kJ/mol,反应 的活化
能为237.2kJ/mol-(91.3kJ/mol+142.7kJ/mol)=3.2kJ/mol<58kJ/mol,反应的活化能越高,反应速率越慢,
则相同条件下, 比 速率慢,故C错误;
D.反应 ΔH=生成物总能量-反应物总能量=2×33.2kJ/mol-2×91.3kJ/mol-0kJ/
mol=-116.2kJ/mol,为放热反应,焓变△H=反应物总键能-生成物总键能,则该反应反应物总键能<生成物
总键能,即1molNO(g)和0.5molO 总键能<1molNO (g)的总键能,所以1molNO (g)的总键能大于
2 2 2
1molNO(g)总键能,故D正确;故选:C。
2.(2023·辽宁·模拟预测)工业上利用 和 制备 ,相关化学键的键能如下表所示:键
键能
745 436 462.8 413.4 351
已知:①温度为 时, ;②实验测得:
, 为速率常数。
下列说法不正确的是
A.反应 的
B. 时,密闭容器充入浓度均为 的 ,反应至平衡,则 体积分数为
C. 时,
D.若温度为 时, ,则
【答案】D
【分析】T℃时,反应达到平衡时,正逆反应速率相等,则 ,反应的
1
平衡常数K= = ,设平衡时生成甲酸的浓度为amol/L,由题意可建立如下三段式:
由平衡常数可得:a(1-a)(1-a)=2,解得a=0.5,反应的平衡常数K= =2。
【解析】A.由反应热与反应物的键能之和和生成物的键能之和的差值相等可知,反应△H=(745kJ/
mol×2+436kJ/mol)-(745kJ/mol+426kJ/mol+413.4 kJ/mol+351 kJ/mol) <0,故A正确;B.由分析可知,甲酸
的体积分数为 ,故B正确;C.由分析可知,反应的平衡常数K= =2,则k =0.5k ,故C正
逆 正
确;D.该反应为放热反应,升高温度,平衡向逆反应方向移动,化学平衡常数减小,由温度为T℃时,k
2
=2.1k 可知,反应的平衡常数K'= =2.1>K,则反应温度T℃<T℃,故D错误;故选:D。
正 逆 2 1
3.(2023·河北唐山·统考三模)我国首创光伏发电——固态储氢技术,解决了“绿电”与“绿氢”灵活转
换的难题。下列说法不正确的是
A.该技术直接将光能转换成化学能储存起来
B.规模化使用氢能有助于实现“碳达峰”
C.“绿电”电解水制氢成本比煤炭等化石燃料制氢成本低
D.固态储氢技术使新能源汽车电池加氢更加便捷【答案】A
【解析】A.光伏发电将光能转化为电能,利用光伏发电产生的电能电解水将电能转化为化学能,而不是
将光能直接转化为化学能储存起来,A错误;B.规模化使用氢能,可以有效减少化石能源的使用,有助
于实现“碳达峰”,B正确;C.用“绿电”电解水制氢的能源利用率高,故用“绿电”电解水制氢的成
本比煤炭等化石燃料制氢成本低,C正确;D.气体难于存在且气体大,故固态储氢技术使新能源汽车电
池加氢更加便捷,D正确;故答案为:A。
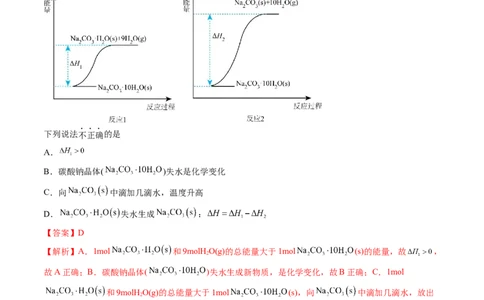
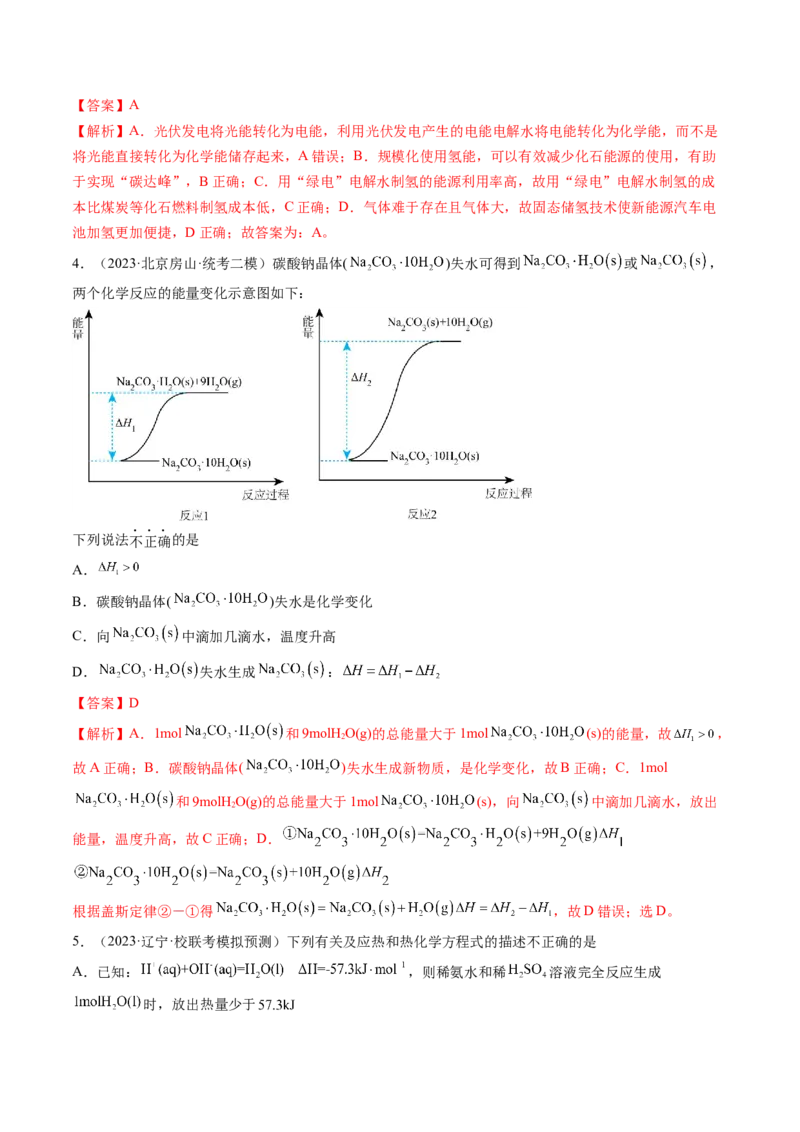
4.(2023·北京房山·统考二模)碳酸钠晶体( )失水可得到 或 ,
两个化学反应的能量变化示意图如下:
下列说法不正确的是
A.
B.碳酸钠晶体( )失水是化学变化
C.向 中滴加几滴水,温度升高
D. 失水生成 :
【答案】D
【解析】A.1mol 和9molH O(g)的总能量大于1mol (s)的能量,故 ,
2
故A正确;B.碳酸钠晶体( )失水生成新物质,是化学变化,故B正确;C.1mol
和9molH O(g)的总能量大于1mol (s),向 中滴加几滴水,放出
2
能量,温度升高,故C正确;D.
根据盖斯定律②-①得 ,故D错误;选D。
5.(2023·辽宁·校联考模拟预测)下列有关及应热和热化学方程式的描述不正确的是
A.已知: ,则稀氨水和稀 溶液完全反应生成
时,放出热量少于B.热化学方程式各物质前的化学计量数既可以是整数也可以是分数,既表示分子数也表示物质的量
C. ,20℃和25℃时, 的燃烧热不同
D.键能数值为平均值,用键能求出的反应热是估算值
【答案】B
【解析】A.已知: ,由于氨水是弱碱,属于弱电解质,其在
水溶液中边反应边电离,电离是一个吸热过程,则稀氨水和稀 溶液完全反应生成 时,放
出热量少于 ,A正确;B.热化学方程式各物质前的化学计量数用于表示其物质的量,而不是其分
子数,故热化学方程式各物质前的化学计量数既可以是整数也可以是分数,B错误;C.燃烧热与外界的
压强和温度有关,相同质量的物质在不同温度下具有的总能量不同,故101kpa,20℃和25℃时,CH 的燃
4
烧热不同,C正确;D.化学反应的微观本质为旧化学键的断裂和新化学键的形成过程,可以用反应物的
总键能减去生成物的总键能来估算反应热,即键能数值为平均值,用键能求出的反应热是估算值,D正确;
故答案为:B。
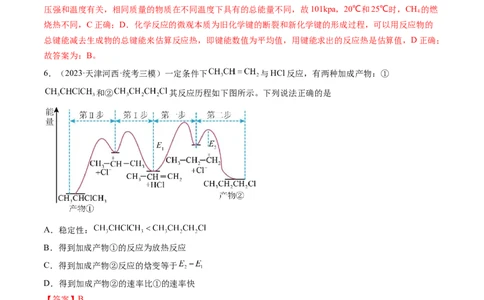
6.(2023·天津河西·统考三模)一定条件下 与HCl反应,有两种加成产物:①
和② 其反应历程如下图所示。下列说法正确的是
A.稳定性:
B.得到加成产物①的反应为放热反应
C.得到加成产物②反应的焓变等于
D.得到加成产物②的速率比①的速率快
【答案】B
【解析】A.能量越高越不稳定,能量:CHCHClCH <CHCHCHCl,则稳定性:CHCHClCH >
3 3 3 2 2 3 3
CHCHCHCl,故A错误;B.得到加成产物①时,反应物总能量大于生成物总能量,则该反应为放热反
3 2 2
应,故B正确;C.焓变=生成物总能量-反应物总能量,根据图中数据无法计算加成产物②反应的焓变,
故C错误;D.活化能越小,反应速率越快,活化能:加成产物②大于加成产物①,所以得到加成产物①
的速率比②的速率快,故D错误;故选:B。
7.(2023·重庆九龙坡·重庆市育才中学校考模拟预测)乙烯在酸催化下水合制乙醇的反应机理、能量与反
应进程的关系如图所示。下列说法正确的是A.由图可知,总反应为放热反应,所以不需加热就能进行
B.第①步反应只断裂非极性键
C.增大催化剂酸的浓度,可以加快总反应速率
D.中间体i比中间体ii更稳定
【答案】C
【解析】A.由图可知,反应物的总能量大于生成物的总能量,该反应为放热反应,反应热与反应条件无
关,故A错误;B.由图可知,第①步反应中有O-H键和C-C键发生断裂,即断裂非极性键,又断裂极性
键,故B错误;C.总反应速率由慢反应决定,第①步的活化能最大,反应速率最慢,因此增大催化剂酸
的浓度,可以加快总反应速率,故C正确;D.第①步反应的中间体比第②步反应的中间体能量高,能量
越高越不稳定,则中间体i不如中间体ii稳定,故D错误;故选:C。
8.(2023·浙江·校联考三模)甲酸常用于橡胶、医药等工业。在一定条件下可分解生成CO和 ,在无、
有催化剂条件下的能量与反应历程的关系如图所示,下列说法不正确的是
A.可以通过 和 计算HCOOH的总键能
B.
C.途径Ⅱ中 参与反应,通过改变反应途径加快反应速率
D.途径Ⅰ未使用催化剂,但途径Ⅱ与途径Ⅰ甲酸平衡转化率相同
【答案】A
【解析】A.由图可知,可以通过E 和E 计算甲酸转化为一氧化碳和水的正反应活化能,但不能计算甲酸
1 2
的总键能,故A错误;B.催化剂能改变反应途径,但不能改变反应的焓变,则甲酸转化为一氧化碳和水
的焓变△H= ,故B正确;C.由图可知,途径Ⅱ中氢离子先做反应物,后做生成物,是改变反应途径的催化剂,能加快反应速率,故C正确;D.催化剂能改变反应途径,但不能改变平衡的移动方
向,则途径Ⅱ与途径Ⅰ甲酸平衡转化率相同,故D正确;故选A。
9.(2023·天津南开·南开中学校考模拟预测)下列有关实验操作的叙述错误的是
A.滴定管上标有使用温度和“0”刻度,使用前用水洗净,直接加入待装液
B.配制溶液时,容量瓶底部有少量蒸塯水对实验无影响
C.测中和反应的反应热时,温度计测完盐酸温度后,应冲洗干净并擦干,再测氢氧化钠溶液的温度
D.萃取后的分液操作中,下层液体从分液漏斗下端放出,上层液体从上口倒出
【答案】A
【解析】A.滴定管使用应先水洗再润洗,否则会对标准液稀释,产生误差,故A 错误;B.配制溶液时,
开始在烧杯中溶解或稀释,后还需在容量瓶中加水,所以容量瓶中有少许水无影响,故B正确;C.测定
中和热,温度计会沾有盐酸,不洗会和碱反应,再次测量会引起误差,故C 正确;D.为防止液体污染,
分液时,分液漏斗中下层液体下口放出,上层液体上口倒出,故D正确;故选A。
10.(2023·浙江·校联考模拟预测)标准状态下, (g)与HCl(g)反应生成 (g)和
(g)的反应历程与相对能量的示意图如下。下列说法正确的是
A.
B.其他条件不变,往反应体系中加入适量 (g)可有效提高反应速率
C.其他条件不变,适当升高温度可提高加成产物中 的比例
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:
【答案】C
【分析】过渡态物质的总能量与反应物总能量的差值为活化能,即图中峰值越大则活化能越大,峰值越小
则活化能越小,活化能越小反应越快,活化能越大反应越慢,决定总反应速率的是慢反应;
【解析】A. 、 对应两者的反应物、生成物均不同,故反应的焓变不同,故 ,A
错误;B.由图可知,历程Ⅰ、历程Ⅱ的决速步均为第一步,故其他条件不变,往反应体系中加入适量
(g)不会有效提高反应速率,B错误;C.由图可知,反应历程Ⅱ的最大活化能更大,受温度的影响程度更
大,故其他条件不变,适当升高温度可提高加成产物中 的比例,C正确;D.由图可知,历程Ⅰ中速率最快的一步反应的热化学方程式为:
;历程Ⅱ中速率最快的一步反应的热化学方程式为:
,D错误;故选C。
11.(2023·江苏南京·南京师大附中校考模拟预测)在298K、101kPa下,由稳定的单质发生反应生成
1mol化合物的反应热叫该化合物的标准摩尔生成热△Hmθ。氧族元素氢化物a、b、c、d的生成热数据如
f
图。下列判断正确的是
A.沸点:HO>HS>HSe>H Te
2 2 2 2
B.HS(g)+ O(g)=S(s)+HO(1) H=-265 kJ/mol
2 2 2
C.HSe(g)=Se(g)+H(g) H=+8△1 kJ/mol
2 2
D.反应Te(s)+H(g) HTe(g)达平衡后升温,平衡常数将减小
2 2 △
【答案】B
【解析】A. 分子间形成氢键,其沸点最高,其余氢化物随相对分子质量增加而增大,故沸点:
,A错误;B.由题中信息可得热化学方程式:
, ,由盖斯定律可知
反应 可由:II-I得到,则 ,
反应热化学方程式为: ,B正确;C. 的摩尔生
成焓为:∆H= ,则反应 的 ,C错误;D.
该反应为吸热反应,生成高温平衡正向移动,平衡常数增大,D错误;故选B。
12.(2023·江苏连云港·连云港高中校考模拟预测) 的燃烧热为 。下列化学反应表示正
确的是
A.在空气中煅烧 的反应:B.在弱碱性条件下,FeS与 反应:
C.FeS与 反应的离子方程式:
D. 的燃烧:
【答案】B
【解析】A.空气中煅烧 时,铁被氧气氧化生成Fe O,正确的方程式为:
2 3
,故A错误。B.FeS具有还原性, 具有氧化性,铁被氧化为+3价,
铬被还原为+3价,弱碱性条件下分别生成对应的氢氧化物,离子方程式为
,故B正确。C.FeS是难溶物,不能拆,正确的离子
方程式为: ,故C错误。D.HS的燃烧热表示1molH S完全燃烧生成液态水时释放
2 2
出的热量,选项中生成的水为气态水, >- ,故D错误。故选B。
二、主观题(共3小题,共40分)
13.(14分)(2022·四川泸州·四川省泸县第二中学校联考一模)氮和氮的化合物与人类有密切关系。
(1)下列属于氮的固定的是 (填序号)。
①工业上N 和H 合成NH
2 2 3
②N 和O 放电条件下生成NO
2 2
③NH 催化氧化生成NO
3
写出反应③的化学方程式 。
(2)①治理NO污染通常是在氧化剂作用下,将NO氧化成溶解度高的NO ,然后用水或碱液吸收脱氮。下
2
列物质可以用于氧化NO的是 (填序号)。
ANaCl溶液 B.KCr O 溶液 C. NaCO 溶液 D.KMnO 溶液
2 2 7 2 3 4
②NO也可用NaClO碱性溶液氧化并将其转化为硝酸盐化肥,写出该反应的离子方程式: 。
③目前处理柴油车尾气中NO 和PM 等的方法之一,是用车用尿素[CO(NH)]溶液在选择性催化还原系统
x 2.5 2 2
中将NO 无害化处理,写出该系统无害化处理NO的化学方程式: 。
x
(3)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应,用Rh做催化剂时该
反应的过程示意图如下:
①过程I为 过程(填“吸热”或“放热”)。该反应中氧化产物为 ,当生成1molN 时,转移电子
2
mol。
②已知过程I的焓变(lmolCO参加)为akJ/mol,过程II的焓变为bkJ/mol,则该反应的热化学方程式为 。
【答案】(除标注外,每空2分)(1)①② 4NH +5O 4NO+6H O(1分)
3 2 2(2)BD 2NO+3ClO- +2OH- = 2 +3Cl-+H O 2CO(NH )+6NO=5N+2CO +4H O
2 2 2 2 2 2
(3)吸热(1分) CO(1分) 4(1分) 2NO(g)+2CO(g)=2CO (g)+N(g) ΔH=+2(a+b)kJ/mol
2 2 2
【解析】(1)固氮是指将游离态的氮元素转化为化合态的氮元素,N 和H 合成NH ,N 和O 放电条件下
2 2 3 2 2
生成NO,符合固氮的定义,故选:①②;反应③NH 催化氧化生成NO和水,反应的化学方程式
3
;
(2)①氧化NO需要氧化剂,NaCl溶液、NaCO 溶液均不与NO反应,KCr O、KMnO 溶液具有强氧化
2 3 2 2 7 4
性,可以氧化NO,故选:BD;②NO也可用NaClO碱性溶液氧化并将其转化为硝酸盐化肥,该反应的离
子方程式:2NO+3ClO- +2OH- = 2 +3Cl-+H O;③尿素[CO(NH)]溶液与NO反应生成氮气和二氧化碳,
2 2 2
化学方程式:2CO(NH)+6NO=5N+2CO +4H O;
2 2 2 2 2
(3)①过程I断裂化学键需要吸热,该反应方程式为2C0+2NO=N+2CO ,C元素化合价升高,氧化产物
2 2
为CO,氮元素从+2降低至0价,有2个N原子降价,当生成1molN 时,转移电子4mol;②反应的热效
2 2
应为过程I和过程II的热效应之和,则反应的热化学方程式为2NO(g)+2CO(g)=2CO (g)+N(g) ΔH=+2(a+b)
2 2
kJ/mol。
14.(12分)(2022·河北衡水·河北衡水中学校考模拟预测)根据所学知识,回答下列问题。
(1)向 的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的
热效应(对应反应中各物质的化学计量数均为1)分别为 、 、 ,则三者由大到小的顺序为 。
(2)已知:①
②
③
碳与水制氢气总反应的热化学方程式是 。
(3)已知CO与 合成甲醇反应过程中的能量变化如图所示:
下表为断裂1mol化学键所需的能量数据:
化学键 H—H H—O C—O
断裂1mol化学键所需的能量/kJ 436 1084 465 343则甲醇中C—H键的键能为 。
(4)一定条件下,在水溶液中 、 的相对能量(kJ)大小如图所示:
①D是 (填离子符号)。
②反应B→A+C的热化学方程式为 (用离子符号表示)。
(5)汽车发动机工作时会引发 和 反应,其能量变化示意图如下:
写出该反应的热化学方程式: 。
【答案】(每空2分)(1)
(2)
(3)413
(4)
(5)
【解析】(1)反应中放出热量越多, 越小,与1L NaOH溶液反应时,与稀硝酸相比,浓硫酸
稀释时放出大量热,醋酸电离时吸收热量,故 。
(2)根据盖斯定律,①+②+③得碳与水制氢气的总反应 ,则
,故热化学方程式为
。
(3)由题图可知,CO与 合成 的反应热 ,设
甲醇中 键的键能为 ,则
,解得 。
(4)①由题图可知,D点对应氯元素的化合价为 价,则D为 ;
②由题图可知,A为 、B为 、C为 ,则 转化为 和 的方程式为, ,即热化学方程式为
, 。
(5)由题图可知,该反应的 ,故其热化学方程
式为 。
15.(14分)(2022·河北廊坊·霸州市第一中学校考模拟预测)低碳经济已成为人们一种新的生活理念,
二氧化碳的捕捉和利用是能源领域的一个重要研究方向。回答下列问题:
(1)用 催化加氢可以制取乙烯: ,该反应体系的能量随反应过
程变化关系如图所示,则该反应的 (用含a、b的式子表示)。相关化学键的键能如下表,实验测得
上述反应的 ,则表中反应过程的 。
化学键 C=O H-H C=C C-H H-O
键能( ) x 436 764 414 464
(2)工业上用 和 反应合成二甲醚。
已知:
则 。
(3)用 表示阿伏加德罗常数的值,在 (g)完全燃烧生成 和液态水的反应中,每有5 个电子转
移时,放出650kJ的热量。 的热值为 。
(4)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由 制取C的太阳能工艺如
图。①工艺过程中的能量转化形式为 。
②已知“重整系统”发生的反应中 ,则 (y<8)的化学式为 ,“热分解系统”中每转移
2mol电子,需消耗 mol。
【答案】(每空2分)(1) 803
(2)
(3)50KJ·g-1
(4)太阳能转化为化学能 1
【解析】(1)根据反应热等于正反应活化能-逆反应的活化能分析,该反应热为 。根据反应
热=反应物的键能总和-生成物的键能总和计算,有 ,解x=803
。
(2)根据盖斯定律分析,① ,②
,有①×2-②得
-53.7×2-23.4=-130.8 。
(3) 表示阿伏加德罗常数的值,在 (g)完全燃烧生成 和液态水的反应中,每有5 个电子转
移时,说明有0.5mol乙炔反应,放出650kJ的热量,则1mol乙炔完全燃烧放出的热量为1300kJ,则
的热值为 。
(4)①工艺过程中的能量转化形式为太阳能变化学能。
②已知“重整系统”发生的反应中 ,根据反应中的质量守恒分析,则x:y=6:8,则 (y<8)的
化学式为 ,反应方程式为 ,反应中转移4个电子,故“热分解系统”中每转
移2mol电子,需消耗 1mol。
1.(2023·浙江·统考高考真题)一定条件下, 苯基丙炔( )可与 发生催化加成,反应如下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正确的
是
A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
【答案】C
【解析】A.反应I、Ⅲ为放热反应,相同物质的量的反应物,反应I放出的热量小于反应Ⅱ放出的热量,
反应放出的热量越多,其焓变越小,因此反应焓变:反应I>反应Ⅱ,故A正确;B.短时间里反应I得到
的产物比反应Ⅱ得到的产物多,说明反应I的速率比反应Ⅱ的速率快,速率越快,其活化能越小,则反应
活化能:反应I<反应Ⅱ,故B正确;C.增加 浓度,平衡正向移动,但平衡时产物Ⅱ和产物I的比例
可能降低,故C错误;D.根据图中信息,选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ,
故D正确。综上所述,答案为C。
2.(2023·湖北·统考高考真题)2023年5月10日,天舟六号货运飞船成功发射,标志着我国航天事业进
入到高质量发展新阶段。下列不能作为火箭推进剂的是
A.液氮-液氢 B.液氧-液氢 C.液态 -肼 D.液氧-煤油
【答案】A
【解析】A.虽然氮气在一定的条件下可以与氢气反应,而且是放热反应,但是,由于 键能很大,
该反应的速率很慢,氢气不能在氮气中燃烧,在短时间内不能产生大量的热量和大量的气体,因此,液氮-
液氢不能作为火箭推进剂,A符合题意;B.氢气可以在氧气中燃烧,反应速率很快且放出大量的热、生
成大量气体,因此,液氧-液氢能作为火箭推进剂,B不符合题意;C.肼和 在一定的条件下可以发生
剧烈反应,该反应放出大量的热,且生成大量气体,因此,液态 -肼能作为火箭推进剂,C不符合题意;
D.煤油可以在氧气中燃烧,反应速率很快且放出大量的热、生成大量气体,因此,液氧-煤油能作为火箭
推进剂,D不符合题意;综上所述,本题选A。
3.(2023·辽宁·统考高考真题)科技是第一生产力,我国科学家在诸多领域取得新突破,下列说法错误的
是
A.利用CO 合成了脂肪酸:实现了无机小分子向有机高分子的转变
2
B.发现了月壤中的“嫦娥石[(Ca Y)Fe(PO)]”:其成分属于无机盐
8 4 7C.研制了高效率钙钛矿太阳能电池,其能量转化形式:太阳能→电能
D.革新了海水原位电解制氢工艺:其关键材料多孔聚四氟乙烯耐腐蚀
【答案】A
【解析】A.常见的脂肪酸有:硬脂酸(C H COOH)、油酸(C H COOH),二者相对分子质量虽大,但没
17 35 17 33
有达到高分子化合物的范畴,不属于有机高分子,A错误;B.嫦娥石因其含有Y、Ca、Fe等元素,属于
无机化合物,又因含有磷酸根,是无机盐,B正确;C.电池是一种可以将其他能量转化为电能的装置,
钙钛矿太阳能电池可以将太阳能转化为电能,C正确;D.海水中含有大量的无机盐成分,可以将大多数
物质腐蚀,而聚四氟乙烯塑料被称为塑料王,耐酸、耐碱,不会被含水腐蚀,D正确;故答案选A。
4.(2023·全国·统考高考真题(节选))硫酸亚铁在工农业生产中有许多用途,如可用作农药防治小麦黑
穗病,制造磁性氧化铁、铁催化剂等。回答下列问题:
(2)已知下列热化学方程式:
则 的 。
【答案】(2)(a+c-2b)
【解析】(2)①
②
③
根据盖斯定律可知,①+③-② 2可得 ,则
(a+c-2b) 。
5.(2023·全国·统考高考真题(节选))甲烷选择性氧化制备甲醇是一种原子利用率高的方法。回答下列
问题:
(1)已知下列反应的热化学方程式:
①
②
反应③ 的 。
(3) 分别与 反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以 示
例)。(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则 与 反应的能量变
化应为图中曲线 (填“c”或“d”)。
【答案】(1)
(3) (ⅱ)c
【解析】(1)根据盖斯定律可知,反应③= (反应②-①),所以对应
;故答案为: ;(3)(ⅱ)直接参与化
学键变化的元素被替换为更重的同位素时,反应速率会变慢,则此时正反应活化能会增大,根据图示可知,
与 反应的能量变化应为图中曲线c;
6.(2023·北京·统考高考真题(节选))尿素 合成的发展体现了化学科学与技术的不断进步。
(2)二十世纪初,工业上以 和 为原料在一定温度和压强下合成尿素。反应分两步:
ⅰ. 和 生成 ;ⅱ. 分解生成尿素。
结合反应过程中能量变化示意图,下列说法正确的是 (填序号)。
a.活化能:反应ⅰ<反应ⅱ
b.ⅰ为放热反应,ⅱ为吸热反应
c.
【答案】(2)ab【解析】(2)a.反应ⅰ的活化能是 ,反应ⅱ活化能是 , ,a项正确;b.从图中反应物和生成
物能量的相对大小可看出反应ⅰ放热,反应ⅱ吸热,b项正确;c.总反应的: ,c项错误;
故选ab。
7.(2023·山东·统考高考真题(节选))一定条件下,水气变换反应 的中间产物是
。为探究该反应过程,研究 水溶液在密封石英管中的分子反应:
Ⅰ.
Ⅱ.
研究发现,在反应Ⅰ、Ⅱ中, 仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建
立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
(1)一定条件下,反应Ⅰ、Ⅱ的焓变分别为 、 ,则该条件下水气变换反应的焓变 (用含
的代数式表示)。
【答案】(1) -
【解析】(1)根据盖斯定律,反应II-反应I=水气变换反应,故水气变换反应的焓变 = - ;