文档内容
第 23 讲 盐类水解
1.生活中处处有化学,下列有关说法正确的是( )
A.天然弱碱性水呈碱性的原因是其中含有较多的Mg2+、Ca2+等离子
B.焊接时用NHCl溶液除锈与盐类水解无关
4
C.生活中用电解食盐水的方法制取消毒液,运用了盐类的水解原理
D.在滴有酚酞的NaCO 溶液中慢慢滴入BaCl 溶液,溶液的红色逐渐褪去
2 3 2
2.室温下0.1 mol·L-1的NHCN溶液的pH等于9.32,据此,在室温下,下列说法错误的是( )
4
A.上述溶液能使甲基橙试剂变黄色
B.室温下,NH·HO是比HCN更弱的电解质
3 2
C.上述溶液中CN-的水解程度大于NH的水解程度
D.室温下,0.1 mol·L-1NaCN溶液中,CN-的水解程度小于上述溶液中CN-的水解程度
3.下列指定溶液中一定能大量共存的离子组是 ( )
A.pH=1的溶液中:NH、Na+、Fe3+、SO
B.含有大量AlO的溶液中:Na+、K+、HCO、NO
C.中性溶液中:K+、Al3+、Cl-、SO
D.NaS溶液中:SO、K+、Cu2+、Cl-
2
4.对滴有酚酞试液的下列溶液,操作后颜色变深的是( )
A.明矾溶液加热
B.CHCOONa溶液加热
3
C.氨水中加入少量NHCl固体
4
D.小苏打溶液中加入少量NaCl固体
5.一定条件下,CHCOONa溶液存在水解平衡:CHCOO-+HO CHCOOH+OH-,下列说法正确的
3 3 2 3
是( )
A.加入少量NaOH固体,c(CHCOO-)增大
3
B.加入少量FeCl 固体,c(CHCOO-)增大
3 3
C.稀释溶液,溶液的pH增大
D.加入适量醋酸得到的酸性混合溶液中:c(Na+)>c(CHCOO-)>c(H+)>c(OH-)
3
6.现有4种混合溶液分别由等体积0.1 mol·L-1的两种溶液混合而成:①NHCl与CHCOONa;②NHCl
4 3 4与HCl;③NHCl 与NaCl;④NHCl与NH·HO(混合溶液呈碱性)。下列各项排序正确的是( )
4 4 3 2
A.pH:②<①<③<④
B.溶液中c(H+):①<③<②<④
C.溶液中c(NH):①<③<②<④
D.溶液中c(NH·HO):①<③<④<②
3 2
7.下列有关问题与盐的水解有关的是( )
①NH Cl与ZnCl 溶液可作焊接金属时的除锈剂
4 2
②NaHCO 与Al (SO ) 两种溶液可作泡沫灭火剂
3 2 4 3
③草木灰与铵态氮肥不能混合施用
④实验室中盛放NaCO 溶液的试剂瓶不能用磨口玻璃塞
2 3
⑤加热蒸干CuCl 溶液得到Cu(OH) 固体
2 2
⑥要除去FeCl 溶液中混有的Fe2+,可先通入氧化剂Cl,再调节溶液的pH
3 2
A.①②③⑥ B.②③④⑥
C.①④⑤⑥ D.①②③④⑤
8.化学在日常生活和生产中有着重要的应用。下列说法不正确的是( )
A.某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为溶液中的SO水解
B.明矾水解形成的Al(OH) 胶体能吸附水中悬浮物,可用于水的净化
3
C.将饱和FeCl 溶液滴入沸水中可制备Fe(OH) 胶体,利用的是盐类水解原理
3 3
D.配制FeCl 溶液时加入少量的盐酸,抑制Fe3+水解
3
9.下列应用与碳酸钠或碳酸氢钠能发生水解的事实无关的是( )
A.实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞
B.泡沫灭火器用碳酸氢钠溶液和硫酸铝溶液,使用时只需将其混合就可产生大量二氧化碳的泡沫
C.厨房中常用碳酸钠溶液洗涤餐具上的油污
D.可用碳酸钠与醋酸制取少量二氧化碳
10.草酸(HCO,二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用。
2 2 4
(1)NaCO 溶液显碱性,请用离子方程式解释原因____________________________。
2 2 4
(2)KMnO 能与硫酸酸化的NaCO 溶液反应生成Mn2+和CO,该反应的离子方程式为
4 2 2 4 2
____________________________________________。
(3)常温下,pH=3的HCO 溶液的物质的量浓度为c,水电离出的c(H+)为c;pH=4的HCO 溶液的物
2 2 4 1 3 2 2 4
质的量浓度为c,水电离出的c(H+)为c。则c______10c(填“>”“<”或“=”,下同);c______10c。
2 4 1 2 3 4
(4)常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL某未知浓度的HCO 溶液,滴定曲线如图,c点所
2 2 4
示溶液中:2c(CO)+2c(HCO)+2c(HCO)=c(Na+)
2 2 2 2 4①该草酸溶液的物质的量浓度为____________________________ _____(列出计算式,并得出计算结果)。
②a点所示溶液中各离子的浓度由大到小的顺序为_________________________。
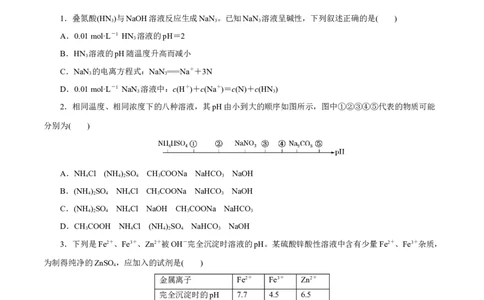
1.叠氮酸(HN)与NaOH溶液反应生成NaN。已知NaN 溶液呈碱性,下列叙述正确的是( )
3 3 3
A.0.01 mol·L-1 HN 溶液的pH=2
3
B.HN 溶液的pH随温度升高而减小
3
C.NaN 的电离方程式:NaN===Na++3N
3 3
D.0.01 mol·L-1 NaN 溶液中:c(H+)+c(Na+)=c(N)+c(HN)
3 3
2.相同温度、相同浓度下的八种溶液,其pH由小到大的顺序如图所示,图中①②③④⑤代表的物质可能
分别为( )
A.NHCl (NH)SO CHCOONa NaHCO NaOH
4 4 2 4 3 3
B.(NH)SO NHCl CHCOONa NaHCO NaOH
4 2 4 4 3 3
C.(NH)SO NHCl NaOH CHCOONa NaHCO
4 2 4 4 3 3
D.CHCOOH NHCl (NH)SO NaHCO NaOH
3 4 4 2 4 3
3.下列是Fe2+、Fe3+、Zn2+被OH-完全沉淀时溶液的pH。某硫酸锌酸性溶液中含有少量Fe2+、Fe3+杂质,
为制得纯净的ZnSO,应加入的试剂是( )
4
金属离子 Fe2+ Fe3+ Zn2+
完全沉淀时的pH 7.7 4.5 6.5
A.HO、ZnO B.氨水
2 2
C.KMnO、ZnCO D.NaOH溶液
4 3
4.下列有关问题与盐的水解有关的是( )
①NHCl与ZnCl 溶液可作焊接金属中的除锈剂
4 2
②草木灰与铵态氮肥不能混合施用
③实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
④加热蒸干CuCl 溶液得到Cu(OH) 固体
2 2A.仅①②③ B.仅②③④
C.仅①④ D.①②③④
5.在一定条件下,NaS溶液中存在水解平衡:S2-+HO HS-+OH-。下列说法正确的是( )
2 2
A.稀释溶液,水解平衡常数增大
B.加入CuSO 固体,HS-浓度减小
4
C.升高温度,减小
D.加入NaOH固体,溶液pH减小
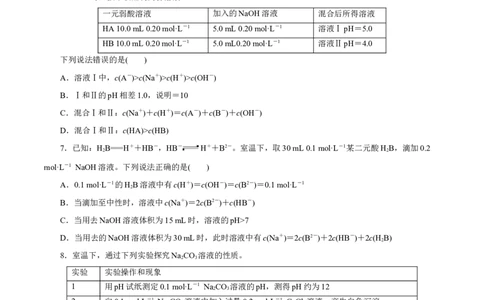
6.25 ℃时,按下表配制两份溶液。
一元弱酸溶液 加入的NaOH溶液 混合后所得溶液
HA 10.0 mL 0.20 mol·L-1 5.0 mL 0.20 mol·L-1 溶液ⅠpH=5.0
HB 10.0 mL 0.20 mol·L-1 5.0 mL0.20 mol·L-1 溶液ⅡpH=4.0
下列说法错误的是( )
A.溶液Ⅰ中,c(A-)>c(Na+)>c(H+)>c(OH-)
B.Ⅰ和Ⅱ的pH相差1.0,说明=10
C.混合Ⅰ和Ⅱ:c(Na+)+c(H+)=c(A-)+c(B-)+c(OH-)
D.混合Ⅰ和Ⅱ:c(HA)>c(HB)
7.已知:HB===H++HB-,HB- H++B2-。室温下,取30 mL 0.1 mol·L-1某二元酸HB,滴加0.2
2 2
mol·L-1 NaOH溶液。下列说法正确的是( )
A.0.1 mol·L-1的HB溶液中有c(H+)=c(OH-)=c(B2-)=0.1 mol·L-1
2
B.当滴加至中性时,溶液中c(Na+)=2c(B2-)+c(HB-)
C.当用去NaOH溶液体积为15 mL时,溶液的pH>7
D.当用去的NaOH溶液体积为30 mL时,此时溶液中有c(Na+)=2c(B2-)+2c(HB-)+2c(HB)
2
8.室温下,通过下列实验探究NaCO 溶液的性质。
2 3
实验 实验操作和现象
1 用pH试纸测定0.1 mol·L-1 NaCO 溶液的pH,测得pH约为12
2 3
2 向0.1 mol·L-1 NaCO 溶液中加入过量0.2 mol·L-1 CaCl 溶液,产生白色沉淀
2 3 2
3 向0.1 mol·L-1 NaCO 溶液中通入过量CO,测得溶液pH约为8
2 3 2
4 向0.1 mol·L-1 NaCO 溶液中滴加几滴0.05 mol·L-1 HCl,观察不到实验现象
2 3
下列有关说法正确的是( )
A.0.1 mol·L-1 NaCO 溶液中存在c(OH-)=c(H+)+2c(HCO)+c(HCO)
2 3 2 3
B.实验2反应静置后的上层清液中有c(Ca2+)·c(CO)c(Cl
3 3
-)>c(CHCOOH)>c(H+)
3
10.X、Y、Z、W分别是HNO、NHNO、NaOH、NaNO 四种强电解质中的一种。下表是常温下浓度均
3 4 3 2
为0.01 mol·L-1的X、Y、Z、W溶液的pH。
0.01 mol·L-1的溶液 X Y Z W
pH 12 2 8.5 4.5
(1)X、W的化学式分别为_____________、___________。
(2)W在溶液中的电离方程式为____________________________________。
(3)25 ℃时,Z溶液的pH>7的原因是_____________________________________(用离子方程式表示)。
(4)将X、Y、Z各1 mol同时溶于水中制得混合溶液,则混合溶液中各离子的浓度由大到小的顺序为
__________________________________________________________。
(5)Z溶液与W溶液混合加热,可产生一种无色无味的单质气体,该反应的化学方程式为
_________________________________________________________________。
1.(2021·浙江卷)25 ℃时,下列说法正确的是( )
A.NaHA溶液呈酸性,可以推测HA为强酸
2
B.可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C.0.010 mol·L-1、0.10 mol·L-1的醋酸溶液的电离度分别为α、α,则α<α
1 2 1 2
D.100 mL pH=10.00的NaCO 溶液中水电离出H+的物质的量为1.0×10-5 mol
2 3
2.(2020·浙江卷)常温下,用0.1 mol·L-1氨水滴定10 mL浓度均为0.1 mol·L-1的HCl和CHCOOH的混合
3
液,下列说法不正确的是( )
A.在氨水滴定前,HCl和CHCOOH的混合液中c(Cl-)>c(CHCOO-)
3 3
B.当滴入氨水10 mL时,c(NH)+c(NH·HO)=c(CHCOO-)+c(CHCOOH)
3 2 3 3C.当滴入氨水20 mL时,c(CHCOOH)+c(H+)=c(NH·HO)+c(OH-)
3 3 2
D.当溶液呈中性时,氨水滴入量大于20 mL,c(NH)<c(Cl-)
3.(2020·江苏卷)室温下,将两种浓度均为0.10 mol·L-1的溶液等体积混合,若溶液混合引起的体积变化可
忽略,下列各混合溶液中微粒物质的量浓度关系正确的是( )
A.NaHCONaCO 混合溶液(pH=10.30):c(Na+)>c(CO)>c(HCO)>c(OH-)
3 2 3
B.氨水NHCl混合溶液(pH=9.25):c(NH)+c(H+)=c(NH·HO)+c(OH-)
4 3 2
C.CHCOOHCHCOONa混合溶液(pH=4.76):c(Na+)>c(CHCOOH)>c(CHCOO-)>c(H+)
3 3 3 3
D.HCONaHCO 混合溶液(pH=1.68,HCO 为二元弱酸):c(H+)+c(HCO)=c(Na+)+c(CO)+c(OH-)
2 2 4 2 4 2 2 4 2 2 4 2
4.(2018·北京卷)测定0.1 mol·L-1 Na SO 溶液先升温再降温过程中的pH,数据如下。
2 3
时刻 ① ② ③ ④
温度/℃ 25 30 40 25
pH 9.66 9.52 9.37 9.25
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl 溶液做对比实验,④产生白色沉淀多。
2
下列说法不正确的是
A. Na SO 溶液中存在水解平衡:SO2− +H O HSO− +OH−
2 3 3 2 3
B.
④的pH与①不同,是由于SO2−
浓度减小造成的
3
C. ①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D. ①与④的K 值相等
w