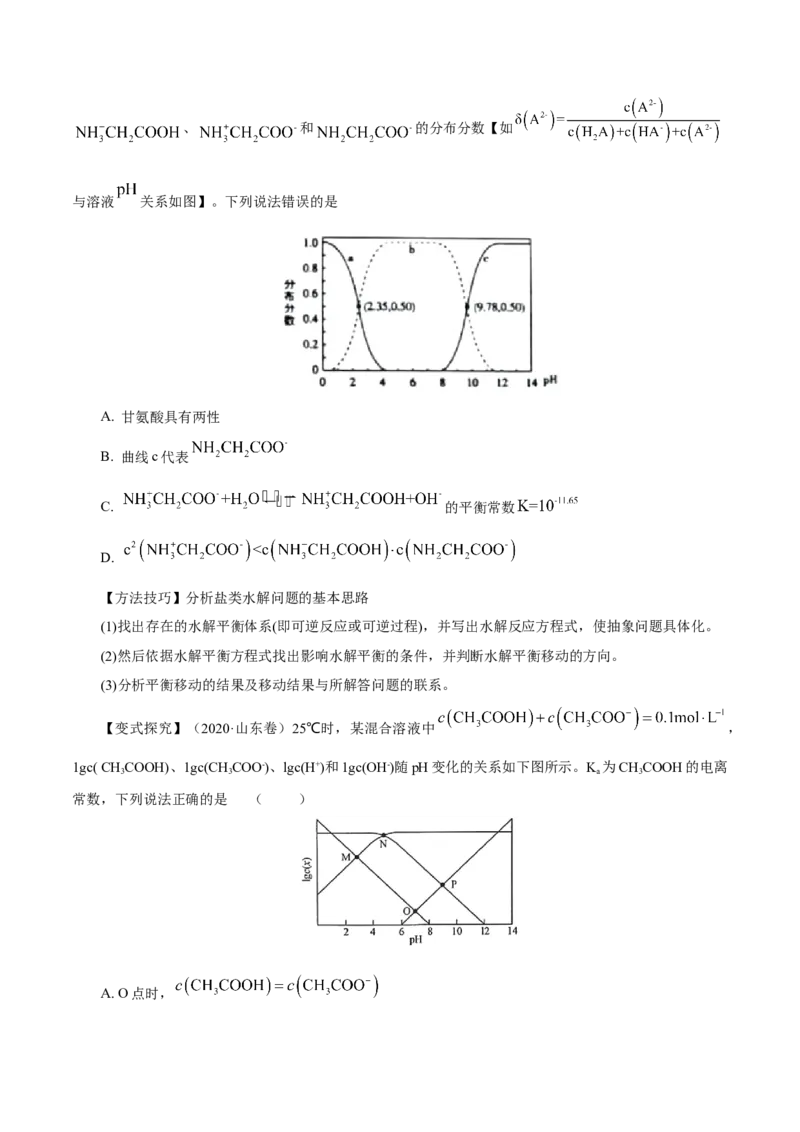
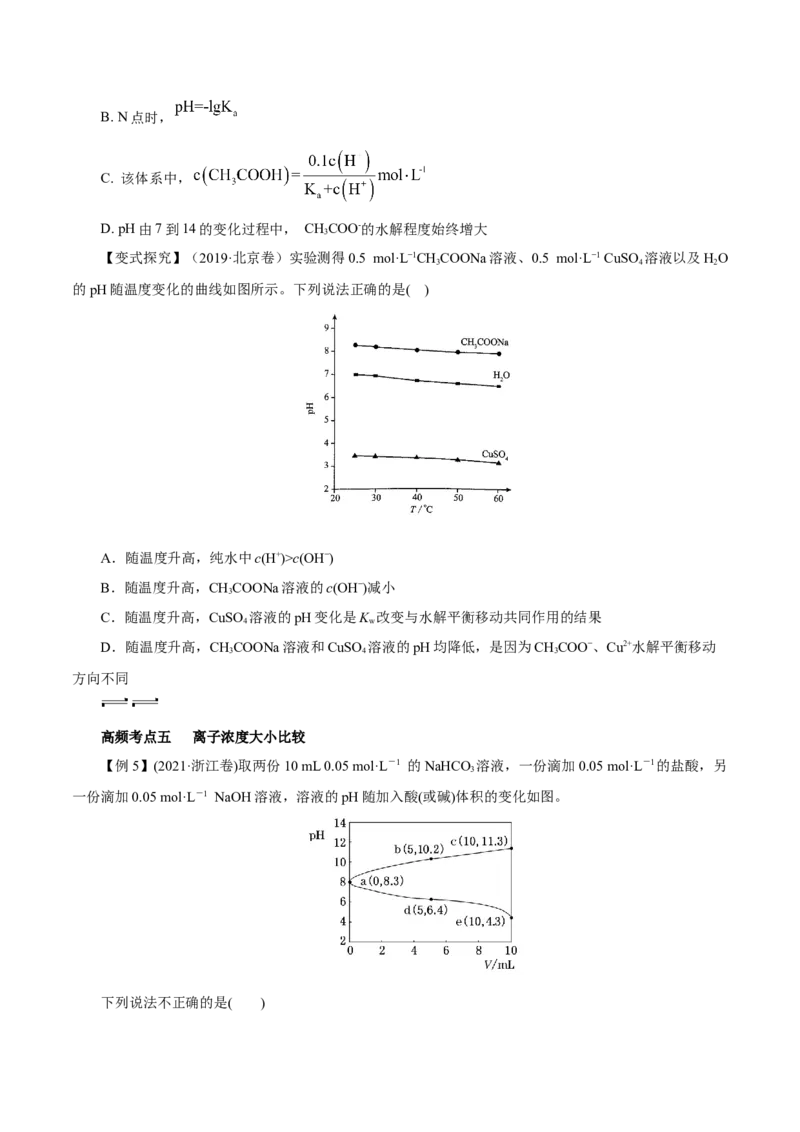
文档内容
第 23 讲 盐类水解
1.了解盐类水解的原理。
2.了解影响盐类水解程度的主要因素。
3.了解盐类水解的应用。
4.能利用水解常数(K )进行相关计算。
h
【核心素养分析】
1.变化观念与平衡思想:认识盐类水解有一定限度,是可以调控的。能多角度、动态地分析盐类水解
平衡,并运用平衡移动原理解决实际问题。
2.科学研究与创新意识:能发现和提出有关盐类水解的判断问题;能从问题和假设出发,确定探究目
的,设计探究方案,进行实验探究。
3.证据推理与模型认知:知道可以通过分析、推理等方法认识盐类水解的本质特征,建立模型。能运
用模型解释盐类水解平衡的移动,揭示现象的本质和规律。
知识点一 盐类水解及其规律
1.定义
在溶液中盐电离出来的离子跟水电离产生的H+或OH-结合生成弱电解质的反应。
2.实质
盐电离―→―→
破坏了水的电离平衡―→水的电离程度增大―→溶液呈碱性、酸性或中性
3.特点
→水解反应是可逆反应
|
→水解反应是酸碱中和反应的逆反应
|
→水解反应程度很微弱
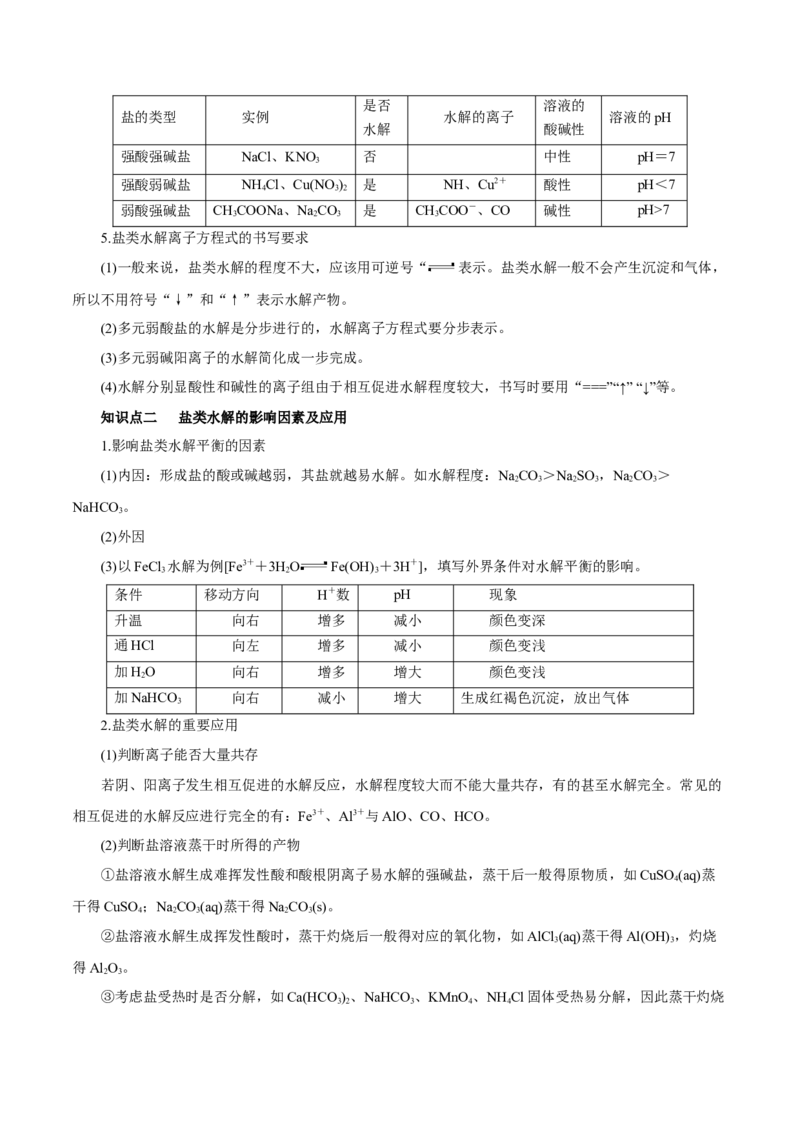
4.规律
有弱才水解,越弱越水解;谁强显谁性,同强显中性。是否 溶液的
盐的类型 实例 水解的离子 溶液的pH
水解 酸碱性
强酸强碱盐 NaCl、KNO 否 中性 pH=7
3
强酸弱碱盐 NH Cl、Cu(NO ) 是 NH、Cu2+ 酸性 pH<7
4 3 2
弱酸强碱盐 CHCOONa、NaCO 是 CHCOO-、CO 碱性 pH>7
3 2 3 3
5.盐类水解离子方程式的书写要求
(1)一般来说,盐类水解的程度不大,应该用可逆号“ 表示。盐类水解一般不会产生沉淀和气体,
所以不用符号“↓”和“↑”表示水解产物。
(2)多元弱酸盐的水解是分步进行的,水解离子方程式要分步表示。
(3)多元弱碱阳离子的水解简化成一步完成。
(4)水解分别显酸性和碱性的离子组由于相互促进水解程度较大,书写时要用“===”“↑” “↓”等。
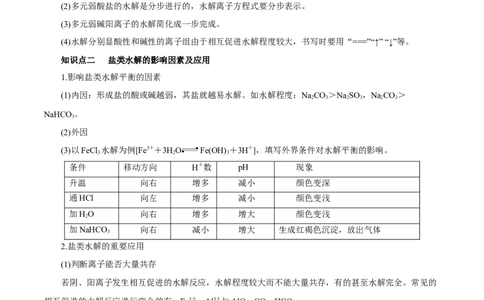
知识点二 盐类水解的影响因素及应用
1.影响盐类水解平衡的因素
(1)内因:形成盐的酸或碱越弱,其盐就越易水解。如水解程度:NaCO>NaSO ,NaCO>
2 3 2 3 2 3
NaHCO 。
3
(2)外因
(3)以FeCl 水解为例[Fe3++3HO Fe(OH) +3H+],填写外界条件对水解平衡的影响。
3 2 3
条件 移动方向 H+数 pH 现象
升温 向右 增多 减小 颜色变深
通HCl 向左 增多 减小 颜色变浅
加HO 向右 增多 增大 颜色变浅
2
加NaHCO 向右 减小 增大 生成红褐色沉淀,放出气体
3
2.盐类水解的重要应用
(1)判断离子能否大量共存
若阴、阳离子发生相互促进的水解反应,水解程度较大而不能大量共存,有的甚至水解完全。常见的
相互促进的水解反应进行完全的有:Fe3+、Al3+与AlO、CO、HCO。
(2)判断盐溶液蒸干时所得的产物
①盐溶液水解生成难挥发性酸和酸根阴离子易水解的强碱盐,蒸干后一般得原物质,如CuSO (aq)蒸
4
干得CuSO ;NaCO(aq)蒸干得NaCO(s)。
4 2 3 2 3
②盐溶液水解生成挥发性酸时,蒸干灼烧后一般得对应的氧化物,如AlCl (aq)蒸干得Al(OH) ,灼烧
3 3
得Al O。
2 3
③考虑盐受热时是否分解,如Ca(HCO )、NaHCO 、KMnO 、NH Cl固体受热易分解,因此蒸干灼烧
3 2 3 4 4后分别为Ca(HCO )―→CaCO (CaO);NaHCO ―→NaCO;KMnO ―→KMnO 和MnO ;NH Cl―→NH
3 2 3 3 2 3 4 2 4 2 4 3
和HCl。
④还原性盐在蒸干时会被O 氧化。
2
如NaSO (aq)蒸干得NaSO (s)。
2 3 2 4
⑤弱酸的铵盐蒸干后无固体。如:NH HCO 、(NH )CO。
4 3 4 2 3
(3)保存、配制某些盐溶液
如配制FeCl 溶液时,为防止出现Fe(OH) 沉淀,常加几滴盐酸来抑制FeCl 的水解;在实验室盛放
3 3 3
NaCO、CHCOONa、NaS等溶液的试剂瓶不能用玻璃塞,应用橡胶塞。
2 3 3 2
(4)利用盐类的水解反应制取胶体、净水
如实验室制备Fe(OH) 胶体的原理为FeCl +3HO Fe(OH) (胶体)+3HCl。
3 3 2 ==== 3
明矾净水的原理:Al3+水解生成氢氧化铝胶体,胶体具有很大的表面积,吸附水中悬浮物而聚沉。
(5)解释热的纯碱溶液去污能力强
碳酸钠溶液中存在水解平衡CO+HO HCO+OH-,升高温度,水解平衡右移,c(OH-)增大。
2
(6)解释泡沫灭火器的反应原理
成分NaHCO 、Al (SO ) 发生反应Al3++3HCO===Al(OH) ↓+3CO↑。
3 2 4 3 3 2
高频考点一 盐类水解的实质及规律
【例1】(2022·浙江卷)水溶液呈酸性的盐是
A.NH Cl B.BaCl C.HSO D.Ca(OH)
4 2 2 4 2
【方法技巧】盐类水解的规律及拓展应用
(1)强酸的酸式盐只电离,不水解,溶液呈酸性。
如NaHSO 溶液中:NaHSO===Na++H++SO。
4 4
(2)弱酸的酸式盐溶液的酸碱性,取决于酸式酸根离子的电离程度和水解程度的相对大小。
①若电离程度小于水解程度,则溶液呈碱性。
如NaHCO 溶液中:HCO H++CO(次要),HCO+HO HCO+OH-(主要)。
3 2 2 3
同类离子还有HS-、HPO。
②若电离程度大于水解程度,则溶液呈酸性。
如NaHSO 溶液中:HSO H++SO(主要),HSO+HO HSO +OH-(次要)。
3 2 2 3
同类离子还有HPO。
2
(3)相同条件下的水解程度①正盐>相应酸式盐。
如相同条件下水解程度:CO>HCO。
②水解相互促进的盐>单独水解的盐>水解相互抑制的盐。
如相同条件下NH的水解程度:(NH )CO>(NH)SO >(NH)Fe(SO )。
4 2 3 4 2 4 4 2 4 2
(4)弱酸弱碱盐中的阴、阳离子都水解,其溶液的酸碱性取决于弱酸阴离子和弱碱阳离子水解程度的相
对大小。
当K =K (K为电离常数)时,溶液呈中性,如CHCOONH;当K >K 时,溶液呈酸性,如
酸 碱 3 4 酸 碱
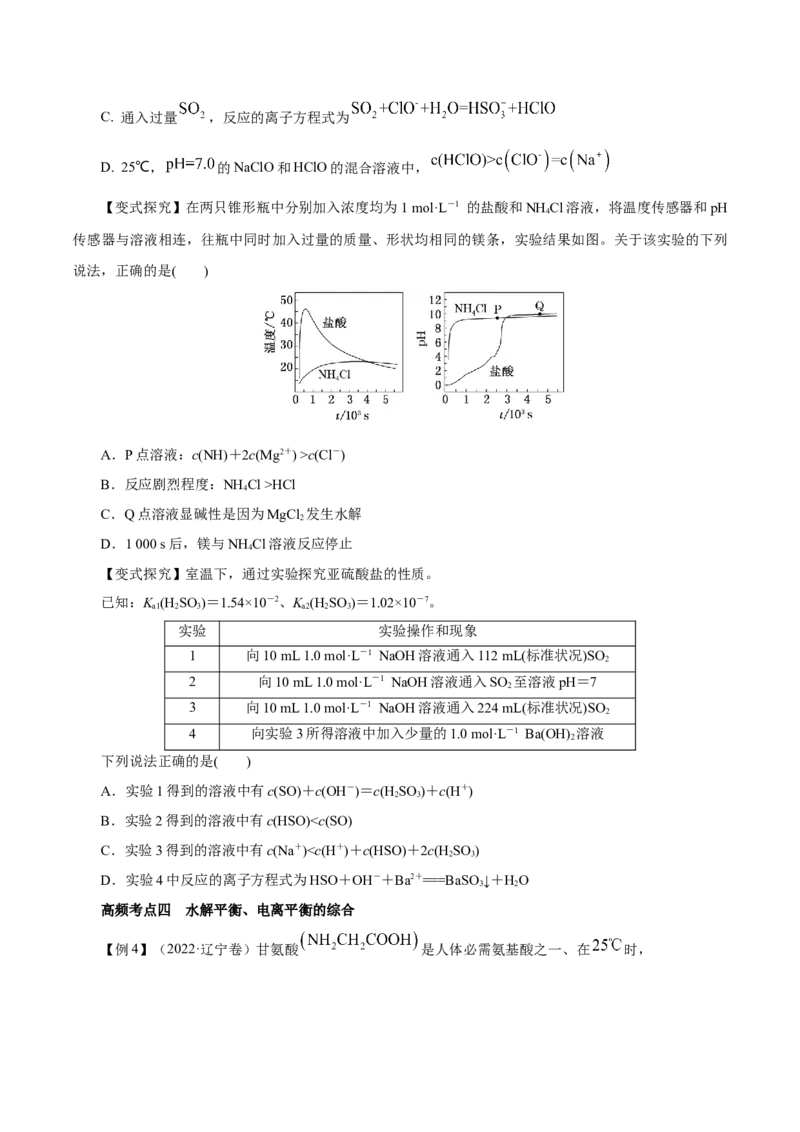
HCOONH ;当K c(Cl-)
B.反应剧烈程度:NH Cl >HCl
4
C.Q点溶液显碱性是因为MgCl 发生水解
2
D.1 000 s后,镁与NH Cl溶液反应停止
4
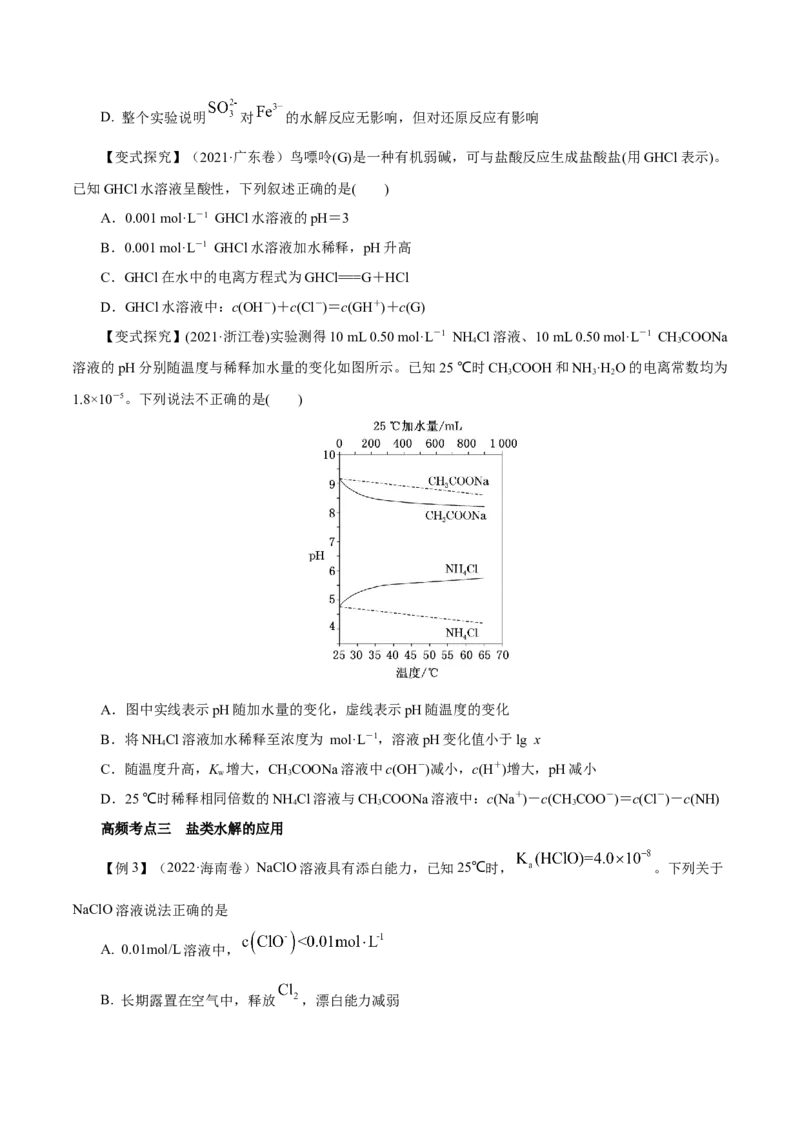
【变式探究】室温下,通过实验探究亚硫酸盐的性质。
已知:K (H SO )=1.54×10-2、K (H SO )=1.02×10-7。
a1 2 3 a2 2 3
实验 实验操作和现象
1 向10 mL 1.0 mol·L-1 NaOH溶液通入112 mL(标准状况)SO
2
2 向10 mL 1.0 mol·L-1 NaOH溶液通入SO 至溶液pH=7
2
3 向10 mL 1.0 mol·L-1 NaOH溶液通入224 mL(标准状况)SO
2
4 向实验3所得溶液中加入少量的1.0 mol·L-1 Ba(OH) 溶液
2
下列说法正确的是( )
A.实验1得到的溶液中有c(SO)+c(OH-)=c(H SO )+c(H+)
2 3
B.实验2得到的溶液中有c(HSO)c(OH−)
B.随温度升高,CHCOONa溶液的c(OH−)减小
3
C.随温度升高,CuSO 溶液的pH变化是K 改变与水解平衡移动共同作用的结果
4 w
D.随温度升高,CHCOONa溶液和CuSO 溶液的pH均降低,是因为CHCOO−、Cu2+水解平衡移动
3 4 3
方向不同
高频考点五 离子浓度大小比较
【例5】(2021·浙江卷)取两份10 mL 0.05 mol·L-1 的NaHCO 溶液,一份滴加0.05 mol·L-1的盐酸,另
3
一份滴加0.05 mol·L-1 NaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图。
下列说法不正确的是( )A.由a点可知:NaHCO 溶液中HCO的水解程度大于电离程度
3
B.a→b→c过程中:c(HCO)+2c(CO)+c(OH-)逐渐减小
C.a→d→e过程中:c(Na+)y
【方法技巧】
1.比较粒子浓度关系时紧扣两个微弱
(1)弱电解质(弱酸、弱碱、水)的电离是微弱的,且水的电离能力远远小于弱酸和弱碱的电离能力。如
稀醋酸溶液中:CHCOOH CHCOO-+H+、HO OH-+H+,粒子浓度由大到小的顺序为
3 3 2
c(CHCOOH)>c(H+)>c(CHCOO-)>c(OH-)。
3 3
(2)弱酸根阴离子或弱碱阳离子的水解是微弱的,但水的电离程度远远小于盐的水解程度。如稀
CHCOONa溶液中:CHCOONa===CH COO-+Na+、CHCOO-+HO CHCOOH+OH-、HO H
3 3 3 3 2 3 2
++OH-,粒子浓度由大到小的顺序为c(Na+)>c(CHCOO-)>c(OH-)>c(CHCOOH)>c(H+)。
3 3
2.酸式盐与多元弱酸的强碱正盐溶液的酸碱性的比较
(1)酸式盐溶液的酸碱性主要取决于酸式盐中酸式酸根离子的电离能力和水解能力的相对强弱。如
NaHCO 溶液中HCO的水解能力大于其电离能力,故溶液显碱性。
3
(2)多元弱酸的强碱正盐溶液中,多元弱酸根离子的水解以第一步为主。如NaS溶液中:c(Na+)>c(S2
2
-)>c(OH-)>c(HS-)>c(H+)。
3.规避等量关系中的两个易失分点
(1)电荷守恒式不只是各离子浓度的简单相加。如2c(CO)的系数“2”代表一个CO带两个负电荷,不可
漏掉。
(2)物料守恒式中,离子浓度系数不能漏写或颠倒。如NaS溶液中的物料守恒式c(Na+)=2[c(S2-)+
2
c(HS-)+c(H S)]中,“2”表示c(Na+)是溶液中各种硫元素存在形式的硫原子总浓度的2倍。
2
【变式探究】(2020·天津卷)常温下,下列有关电解质溶液的说法错误的是( )
A. 相同浓度的 HCOONa和NaF两溶液,前者的pH较大,则
B. 相同浓度的CHCOOH和CHCOONa两溶液等体积混合后pH约为4.7,则溶液中
3 3
C. FeS溶于稀硫酸,而CuS不溶于稀硫酸,则
D. 在 溶液中,【变式探究】(2020·天津卷)常温下,下列有关电解质溶液的说法错误的是( )
A.相同浓度的HCOONa和NaF两溶液,前者的pH较大,则K(HCOOH)>K(HF)
a a
B.相同浓度的CHCOOH和CHCOONa两溶液等体积混合后pH约为4.7,则溶液中c(CHCOO-)>
3 3 3
c(Na+)>c(H+)>c(OH-)
C.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则K (FeS)>K (CuS)
sp sp
D.在1 mol·L-1 Na S溶液中,c(S2-)+c(HS-)+c(H S)=1 mol·L-1
2 2