文档内容
第二十四、二十五讲 化学反应速率与化学平衡
【基础巩固】
1.对于化学反应:3W(g)+2X(g)===4Y(g)+3Z(g),下列反应速率关系正确的是( )
A.v(W)=3v(Z) B.2v(X)=3v(Z) C.2v(X)=v(Y) D.3v(W)=2v(X)
2.(2023·福州质检)某温度下,在体积一定的密闭容器中进行如下反应:2X(g)+Y(g)Z(g)+W(s)
ΔH>0, 下列叙述正确的是( )
A.加入少量W,逆反应速率增大
B.升高温度,正反应和逆反应速率都增大
C.在容器中加入氦气,压强增大,反应速率增大
D.将容器的体积压缩,可增大活化分子的百分数,有效碰撞次数增大
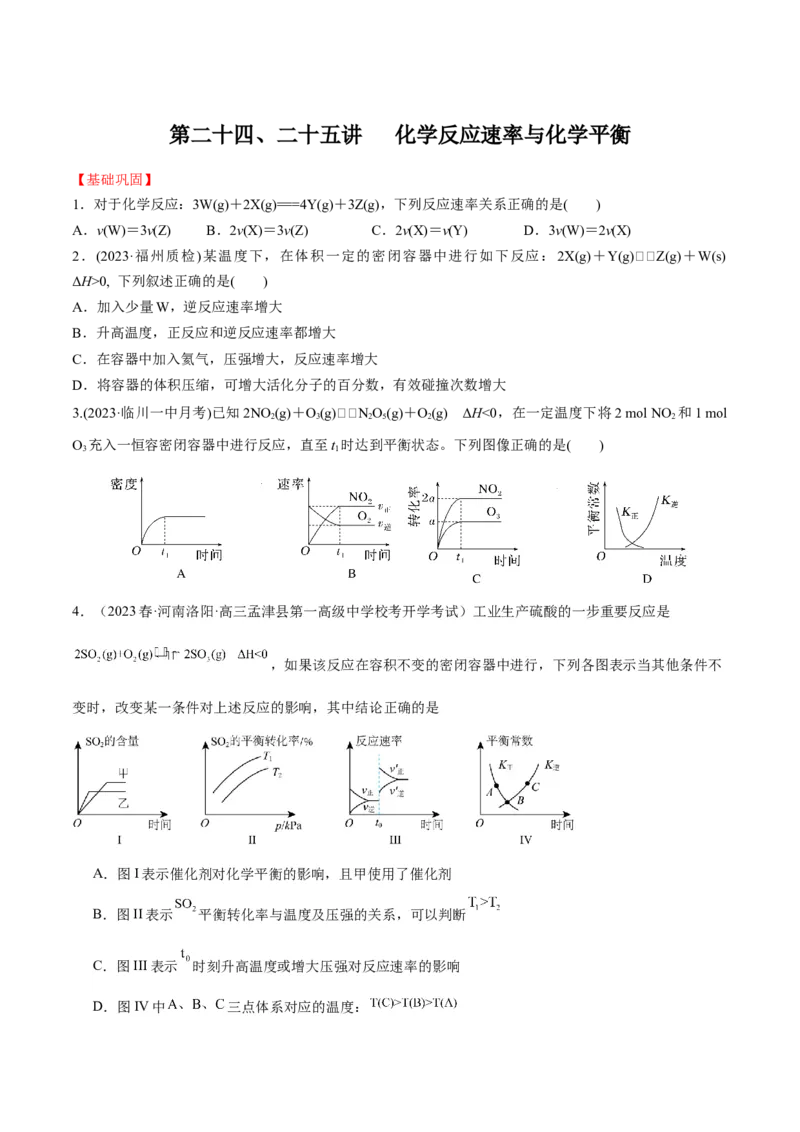
3.(2023·临川一中月考)已知2NO (g)+O(g)N O(g)+O(g) ΔH<0,在一定温度下将2 mol NO 和1 mol
2 3 2 5 2 2
O 充入一恒容密闭容器中进行反应,直至t 时达到平衡状态。下列图像正确的是( )
3 1
4.(2023春·河南洛阳·高三孟津县第一高级中学校考开学考试)工业生产硫酸的一步重要反应是
,如果该反应在容积不变的密闭容器中进行,下列各图表示当其他条件不
变时,改变某一条件对上述反应的影响,其中结论正确的是
A.图I表示催化剂对化学平衡的影响,且甲使用了催化剂
B.图II表示 平衡转化率与温度及压强的关系,可以判断
C.图III表示 时刻升高温度或增大压强对反应速率的影响
D.图IV中 三点体系对应的温度:5.(2023春·河南洛阳·高三新安县第一高级中学校考开学考试)科研人员进行了 加氢制 和
转化为 催化反应的研究,反应历程分别如甲、乙两图所示。
下列说法不正确的是
A. 经过Ni活性中心裂解产生活化态H·的过程中
B.使用 作催化剂可以降低反应的焓变,从而提高化学反应速率
C.生成 的总反应原子利用率为100%
D. 过程中,有C—H键发生断裂,①→②放出热量并形成了C—C键
6.下列说法正确的是( )
①活化分子间的碰撞一定能发生化学反应 ②普通分子有时也能发生有效碰撞 ③升高温度会加快反应速
率,原因是增加了活化分子的有效碰撞次数 ④增大反应物浓度会加快反应速率的原因是单位体积内有效
碰撞的次数增多 ⑤使用催化剂能提高反应速率,原因是提高了分子的能量,使有效碰撞频率增大 ⑥化
学反应实质是活化分子有合适取向时的有效碰撞
A.①②⑤ B.③④⑥ C.③④⑤⑥ D.②③④
7.已知:2KMnO +5HC O +3HSO ===2MnSO +KSO +10CO↑+8HO。某化学小组欲探究HC O 溶
4 2 2 4 2 4 4 2 4 2 2 2 2 4
液和酸性KMnO 溶液反应过程中浓度、温度对化学反应速率的影响,进行了如下实验(忽略溶液体积变化):
4
0.01 mol·L-1酸性KMnO 0.1 mol·L-1 HC O 反应时间/
4 2 2 4
编号 水的体积/mL 反应温度/℃
溶液体积/mL 溶液体积/mL min
Ⅰ 2 2 0 20 2.1
Ⅱ V 2 1 20 5.5
1
Ⅲ V 2 0 50 0.5
2
下列说法不正确的是( )
A.V=1,V=2
1 2
B.设计实验Ⅰ、Ⅲ的目的是探究温度对反应速率的影响
C.实验计时是从溶液混合开始,溶液呈紫红色时结束D.实验Ⅲ中用酸性KMnO 溶液的浓度变化表示的反应速率v(KMnO)=0.01 mol·L-1·min-1
4 4
8.(2023·西安模拟)反应NH
4
HS(s)⇌NH
3
(g)+H
2
S(g)在某温度下达到平衡,下列各种情况不会使平衡发生移
动的是( )
A.温度、容积不变时,通入SO 气体 B.移走一部分NH HS固体
2 4
C.容器体积不变,充入HCl气体 D.保持压强不变,充入氮气
9.(2023·江西上饶·万年中学校考一模)下列叙述正确的是
A.Na与无水乙醇反应时,增大无水乙醇的用量可明显增大化学反应速率
B.原电池中发生的反应达到平衡时,该电池仍有电流产生
C.催化剂能改变化学反应速率,是因为它能改变反应历程和反应的活化能
D.Na与 的反应是熵减的放热反应,该反应能自发进行
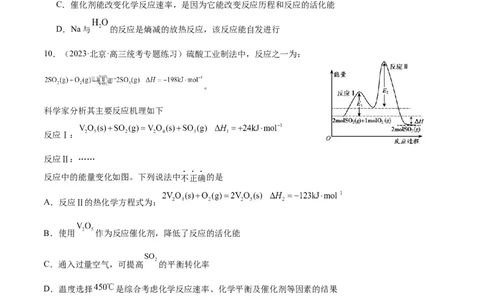
10.(2023·北京·高三统考专题练习)硫酸工业制法中,反应之一为:
。
科学家分析其主要反应机理如下
反应Ⅰ:
反应Ⅱ:……
反应中的能量变化如图。下列说法中不正确的是
A.反应Ⅱ的热化学方程式为:
B.使用 作为反应催化剂,降低了反应的活化能
C.通入过量空气,可提高 的平衡转化率
D.温度选择 是综合考虑化学反应速率、化学平衡及催化剂等因素的结果
11.(2023·北京石景山·统考模拟预测)利用下列实验药品,不能达到实验目的的是
实验目的 实验药品
比较水和四氯化碳分子的极
A 、 、橡胶棒、毛皮
性
B 验证乙醇的消去产物乙烯 乙醇、酸性高锰酸钾溶液、浓硫酸
C 探究温度对化学平衡的影响 溶液、冷水、热水D 证明牺牲阳极法保护铁 Fe、Zn、酸化的食盐水、 溶液
A.A B.B C.C D.D
12.(2023·海南·高三统考专题练习)下列关于“化学反应速率和化学平衡”的说法正确的是
A.在恒温恒容条件下,当N
2
O
4
(g)⇌2NO
2
(g)达到平衡后,再充入一定量的Ar后,活化分子百分数减小,
反应速率减慢
B.已知2Mg(s)+CO
2
(g)⇌C(s)+2MgO(s) ΔH<0,则该反应能在高温下自发进行
C.某温度下,在恒容密闭容器中加入一定量X,发生反应2X(g)⇌Y(g)+Z(g),一段时间后达到平衡,再加
入一定量X,达新平衡后X的物质的量分数增大
D.对于反应2NH
3
(g)⇌N
2
(g)+3H
2
(g)达平衡后,缩小容器体积,N
2
的浓度增大
13.(2023·陕西·统考三模)工业上在催化剂的作用下CO可以合成甲醇,用计算机模拟单个CO分子合成
甲醇的反应历程如图。下列说法正确的是。
A.反应过程中有极性键的断裂和生成
B.反应的决速步骤为III→IV
C.使用催化剂降低了反应的
D.反应的热化学方程式为
14.(2023·宝鸡模拟)研究CO 的综合利用对促进“低碳经
2
济”的发展有重要意义。CO 与H 合成二甲醚(CHOCH )是一种CO 转化的方法,其过程中主要发生下列
2 2 3 3 2
反应:
反应Ⅰ CO
2
(g)+3H
2
(g)⇌CH
3
OH(g)+H
2
O(g) ΔH
1
=-49.0 kJ·mol-1
反应Ⅱ 2CH
3
OH(g)⇌CH
3
OCH
3
(g)+H
2
O(g) ΔH
2
=-24.5 kJ·mol-1
反应Ⅲ CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O(g) ΔH
3
=+41.2 kJ·mol-1
(1)写出CO 与H 一步合成二甲醚(反应Ⅳ)的热化学方程式:_______________________________________。
2 2
(2)有利于提高反应Ⅳ平衡转化率的条件是______(填字母)。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(3)在恒压、CO 和H 起始物质的量之比为1∶3的条件下,CO 平衡转化率和平衡时二甲醚的选择性随温度
2 2 2
的变化如图所示。CHOCH 的选择性=×100%。
3 3①温度低于300 ℃,CO 平衡转化率随温度升高而下降的原因是_____________________。
2
②关于合成二甲醚工艺的理解,下列说法正确的是________(填字母)。
A.反应Ⅳ在A点和B点时的化学平衡常数:K(A)小于K(B)
B.当温度、压强一定时,在原料气(CO 和H 的比例不变)中添加少量惰性气体,有利于提高平衡转化率
2 2
C.其他条件不变,在恒容条件下的二甲醚平衡选择性比恒压条件下的平衡选择性低
D.提高催化剂的活性和选择性,减少CO等副产物是工艺的关键
15.(2022·重庆模拟)尿素[CO(NH)]是首个由无机物人工合成的有机物。
2 2
(1)已知:①2NH (g)+CO(g)===NHCONH (s) ΔH=-159.5 kJ·mol-1
3 2 2 2 4
②NH CONH (s)===CO(NH )(s)+HO(g) ΔH=+116.5 kJ·mol-1
2 2 4 2 2 2
则氨气与二氧化碳气体合成固态尿素和气态水的热化学方程式为___________________________________。
(2)一定条件下,向容积恒定为2 L的密闭容器中加入0.10 mol CO 和0.40 mol NH ,发生反应:2NH (g)+
2 3 3
CO
2
(g)⇌CO(NH
2
)
2
(l)+H
2
O(g),60 min开始达到平衡。反应中CO
2
的物质的量随时间变化如下表所示:
时间/min 0 20 60 80
n(CO)/mol 0.10 0.06 0.04 0.04
2
①60 min内,上述反应的平均反应速率v(CO)=________。
2
②NH 的平衡转化率为__________。
3
(3)一定条件下,恒容容器中,若原料气中的 NH 和CO 的物质的量之比=x,发生反应:2NH (g)+
3 2 3
CO
2
(g)⇌CO(NH
2
)
2
(l)+H
2
O(g),x与CO
2
的平衡转化率(α)的关系如图所示:
①α随着x增大而增大的原因是_______________________________________________。
②A点平衡时容器内总压强为p kPa,则上述反应的平衡常数K =________(用平衡分压代替平衡浓度计算,
0 p
分压=总压×物质的量分数)。
16.(2023·哈尔滨质监)游离态氮称为惰性氮,游离态氮转化为化合态氮称为氮的活化,在氮的循环系统中,
氮的过量“活化”会导致氮向大气和水体过量迁移,氮的循环平衡被打破,导致全球环境问题。
已知:SO 、CO、NH 等都可以催化还原氮氧化物生成惰性氮。
2 3
在25 ℃,101 kPa时,存在如下反应:
a.N
2
(g)+3H
2
(g)⇌2NH
3
(g) ΔH
1
=-92.4 kJ·mol-1
b.2H (g)+O(g)===2H O(l) ΔH=-571.6 kJ·mol-1
2 2 2 2
c.N (g)+O(g)===2NO(g) ΔH=+180.0 kJ·mol-1
2 2 3
(1) 结 合 以 上 热 化 学 方 程 式 , 写 出 NO 与 NH 反 应 生 成 惰 性 氮 的 热 化 学 方 程 式
3
____________________________。(2)工业合成氨是氮的活化的重要途径之一,在一定条件下,将N 和H 通入到体积为1 L的恒容容器中,
2 2
下列说法能说明该可逆反应达到平衡状态的是________(填字母)。
A.容器中气体密度不变 B.3v(H ) =2v(NH ) C.容器中压强不变 D.N、H、NH 分子数之比为1∶3∶2
2 正 3 逆 2 2 3
(3)在合成氨工业中,为提高化学反应速率并提高原料平衡转化率可采取的措施为________(填字母)。
A.升高温度 B.将氨液化体系中分离 C.加入催化剂 D.增大压强
(4)在有氧条件下,新型催化剂 M 能催化 CO 与 NO 反应生成 N ,该反应的方程式为 4CO(g)+
2 2
2NO
2
(g)⇌N
2
(g)+4CO
2
(g) ΔH<0。
①现向某密闭容器中充入等物质的量浓度的NO 和CO气体,维持恒温恒容,在催化剂作用下发生反应。
2
相关数据如下:
0 min 5 min 10 min 15 min 20 min
c(NO )/(mol·L-1) 2.0 1.7 1.56 1.5 1.5
2
c(N )/(mol·L-1) 0 0.15 0.22 0.25 0.25
2
在0~5 min内,以CO 的浓度变化表示的反应速率为________ mol·L-1·min-1,在10 min时,CO的转化率
2
为________。此温度下,该反应的化学平衡常数K=________(保留两位有效数字)。
②该反应的正、逆反应的平衡常数(K)与温度(T)的关系如图所示,其中表示正反应的平衡常数(K )的是
正
________( 填 “ A” 或 “ B”) , 原 因 是
_________________________________________________________________。
【拔高练习】
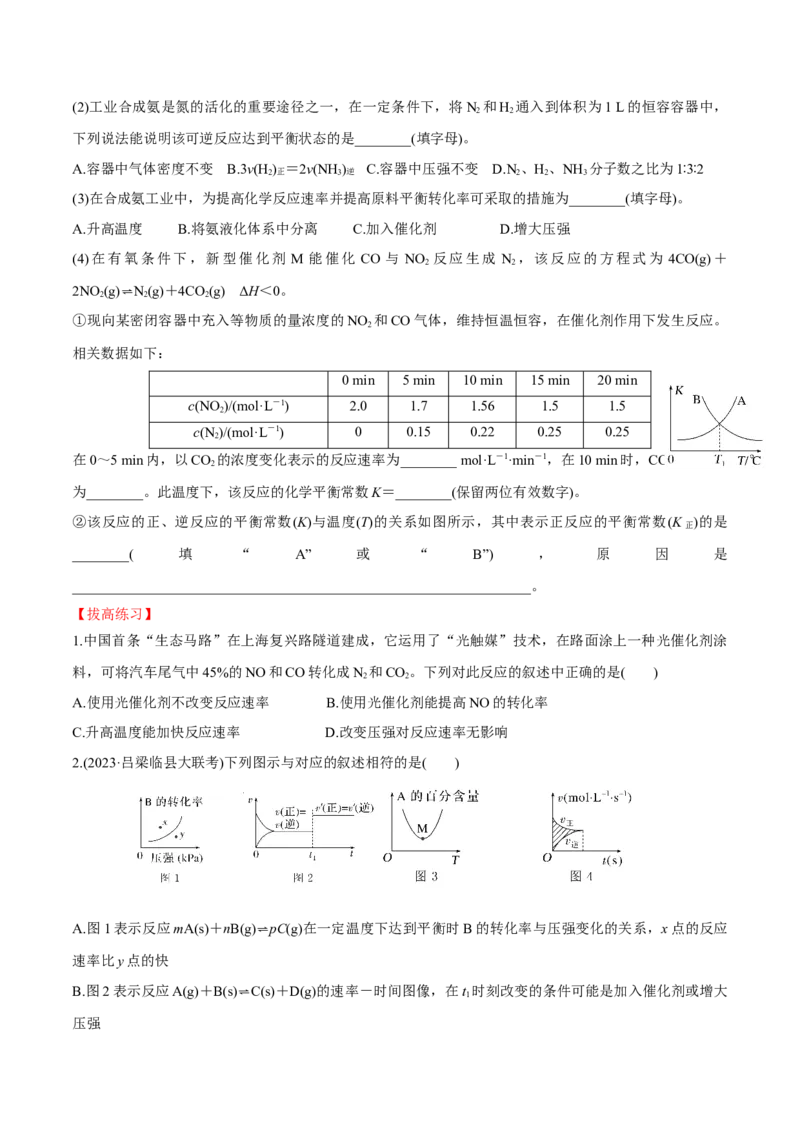
1.中国首条“生态马路”在上海复兴路隧道建成,它运用了“光触媒”技术,在路面涂上一种光催化剂涂
料,可将汽车尾气中45%的NO和CO转化成N 和CO。下列对此反应的叙述中正确的是( )
2 2
A.使用光催化剂不改变反应速率 B.使用光催化剂能提高NO的转化率
C.升高温度能加快反应速率 D.改变压强对反应速率无影响
2.(2023·吕梁临县大联考)下列图示与对应的叙述相符的是( )
A.图1表示反应mA(s)+nB(g)⇌pC(g)在一定温度下达到平衡时B的转化率与压强变化的关系,x点的反应
速率比y点的快
B.图2表示反应A(g)+B(s)⇌C(s)+D(g)的速率-时间图像,在t
1
时刻改变的条件可能是加入催化剂或增大
压强C.图3表示反应mA(g)+nB(g)⇌pC(g)+qD(g)中A的百分含量与温度(T)的变化情况,则该反应的ΔH>0
D.图4所示图中的阴影部分面积的含义是(v -v )
正 逆
3.(2023·江苏如东中学检测)合成气是一种重要的化工原料气,主要组分为CO和H 。用甲烷、二氧化碳自
2
热重整可制备合成气,反应原理如下:
反应Ⅰ:CH
4
(g)+2O
2
(g)⇌CO
2
(g)+2H
2
O(g) ΔH
1
=-820.6 kJ·mol-1
反应Ⅱ:CH
4
(g)+CO
2
(g)⇌2CO(g)+2H
2
(g) ΔH
2
=+247.1 kJ·mol-1
反应Ⅲ:CH
4
(g)+H
2
O(g)⇌CO(g)+3H
2
(g) ΔH
3
=+205.9 kJ·mol-1
反应Ⅳ:CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O(g) ΔH
4
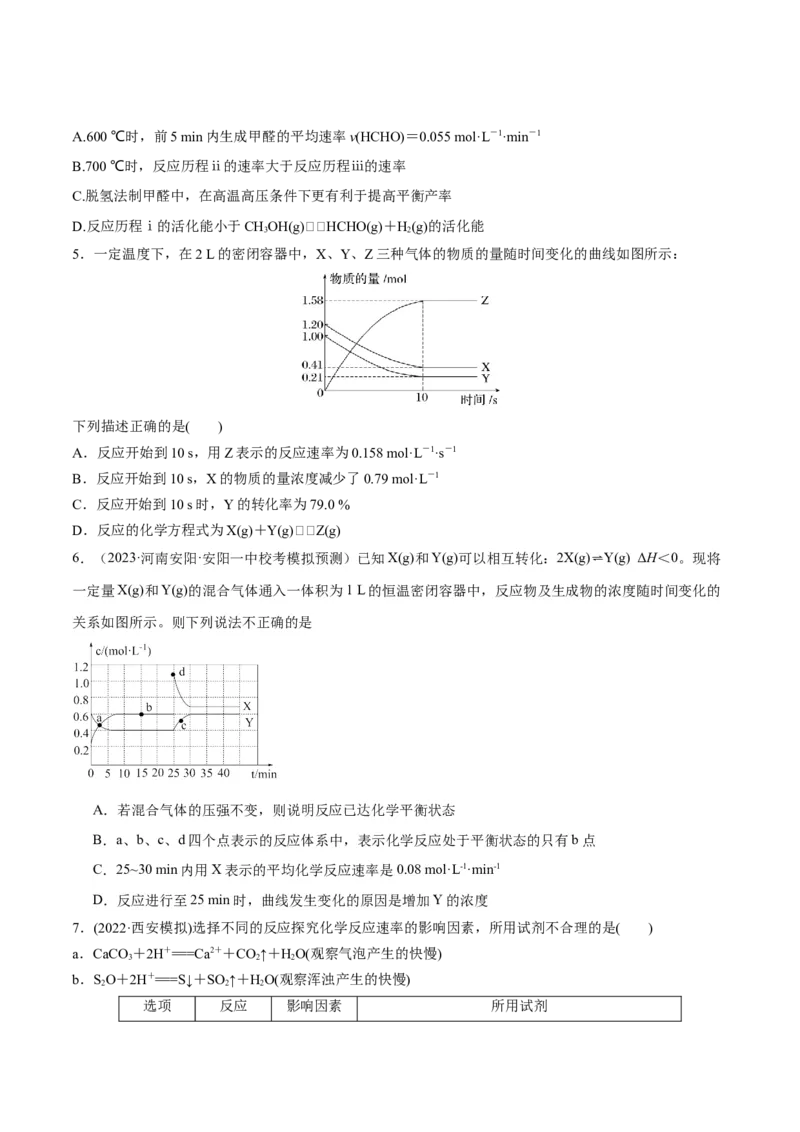
不同温度下,向体积为V L的含少量O 的恒压容器按照n(CO)∶n(CH)=1投料,实验测得不同压强下平衡
2 2 4
时随温度的变化关系如图所示。下列说法正确的是( )
A.ΔH=-41.2 kJ·mol-1
4
B.某温度下,反应Ⅱ的平衡常数随压强增大而减小
C.由图可知,p>p>p
1 2 3
D.压强为p 时,T>T 后,升高温度对反应Ⅳ的促进作用更大
2 m
4.(2023·江苏包场中学检测)甲醛在木材加工、医药等方面有重要用途。甲醇利用脱氢法可制备甲醛,主要
反应为:CHOH(g)HCHO(g)+H(g) ΔH=+85.2 kJ·mol-1。NaCO 是甲醇脱氢制甲醛的催化剂,有研
3 2 2 3
究指出,催化反应的部分机理如下:
历程ⅰ:CHOH→·H+·CHOH
3 2
历程ⅱ:·CHOH→·H+HCHO
2
历程ⅲ:·CHOH→3·H+CO
2
历程ⅳ:·H+·H→H
2
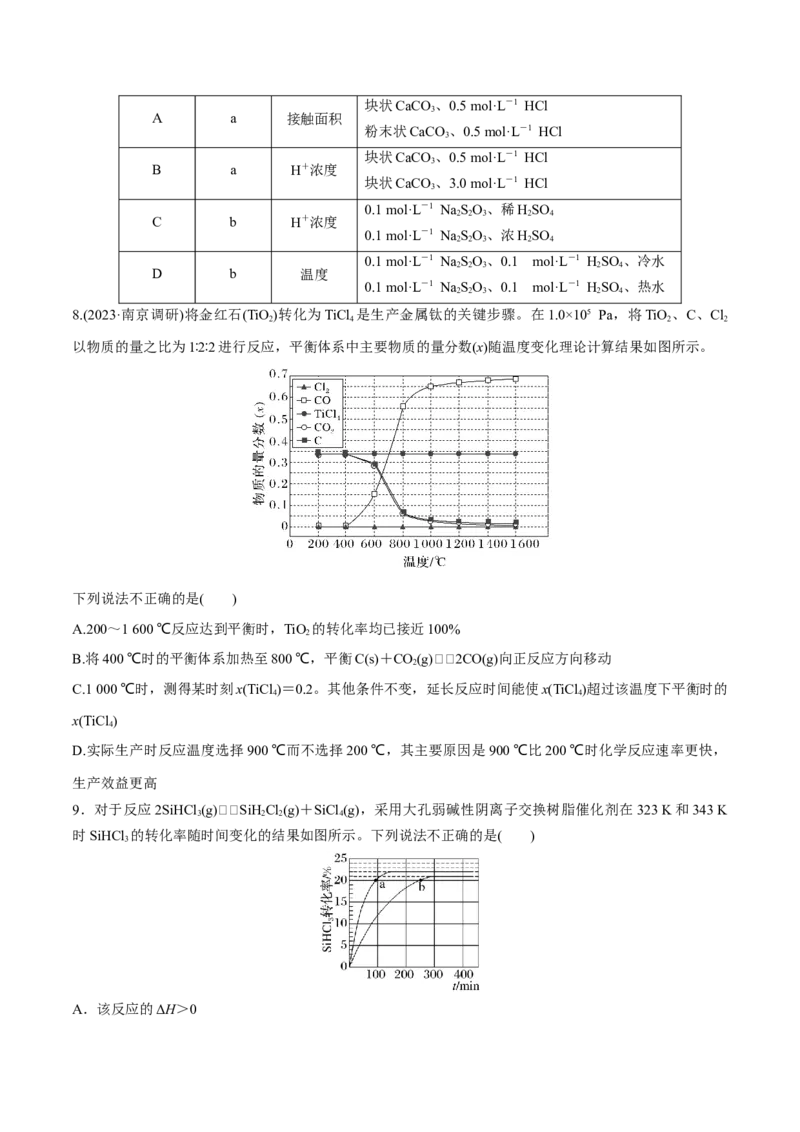
如图所示为在体积2 L的恒容容器中,投入1 mol CH OH,在碳酸钠催化剂作用下,经过5 min反应,测得
3
甲醇转化率与甲醛的选择性与温度的关系(甲醛的选择性:转化的CHOH中生成HCHO的百分比),下列有
3
关说法正确的是( )A.600 ℃时,前5 min内生成甲醛的平均速率v(HCHO)=0.055 mol·L-1·min-1
B.700 ℃时,反应历程ⅱ的速率大于反应历程ⅲ的速率
C.脱氢法制甲醛中,在高温高压条件下更有利于提高平衡产率
D.反应历程ⅰ的活化能小于CHOH(g)HCHO(g)+H(g)的活化能
3 2
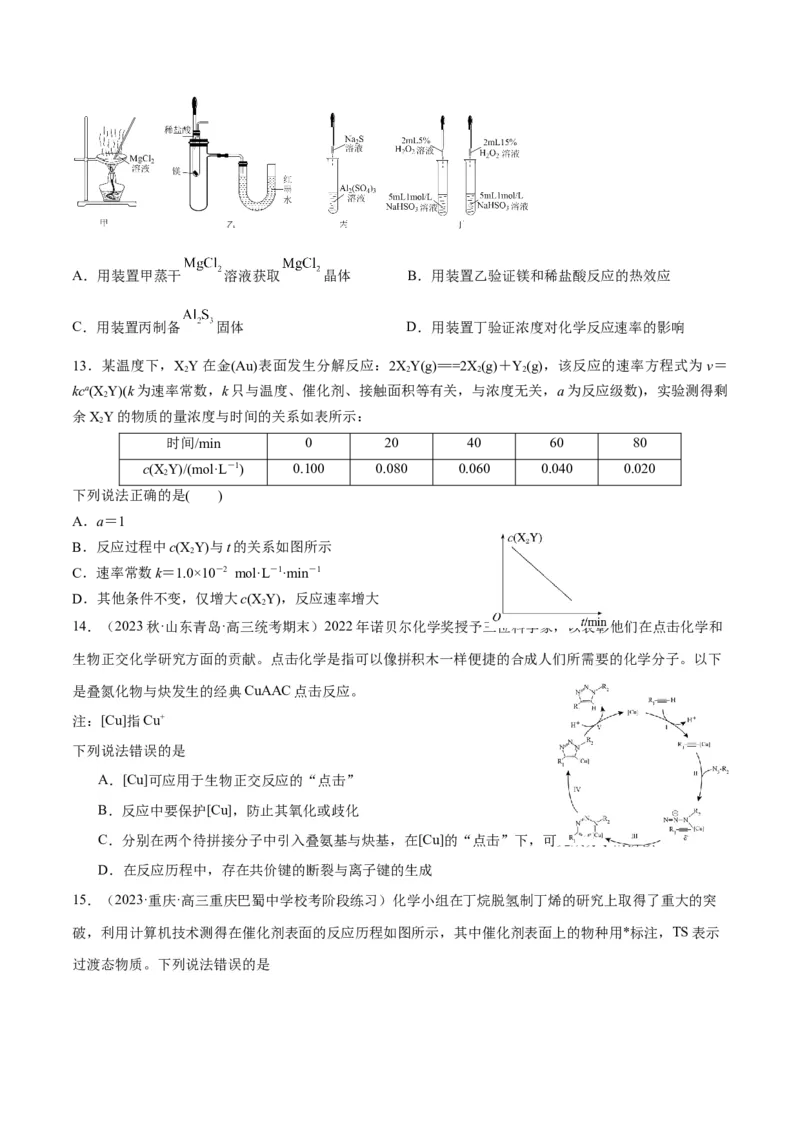
5.一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
下列描述正确的是( )
A.反应开始到10 s,用Z表示的反应速率为0.158 mol·L-1·s-1
B.反应开始到10 s,X的物质的量浓度减少了0.79 mol·L-1
C.反应开始到10 s时,Y的转化率为79.0 %
D.反应的化学方程式为X(g)+Y(g)Z(g)
6.(2023·河南安阳·安阳一中校考模拟预测)已知X(g)和Y(g)可以相互转化:2X(g)⇌Y(g) ΔH<0。现将
一定量X(g)和Y(g)的混合气体通入一体积为1 L的恒温密闭容器中,反应物及生成物的浓度随时间变化的
关系如图所示。则下列说法不正确的是
A.若混合气体的压强不变,则说明反应已达化学平衡状态
B.a、b、c、d四个点表示的反应体系中,表示化学反应处于平衡状态的只有b点
C.25~30 min内用X表示的平均化学反应速率是0.08 mol·L-1·min-1
D.反应进行至25 min时,曲线发生变化的原因是增加Y的浓度
7.(2022·西安模拟)选择不同的反应探究化学反应速率的影响因素,所用试剂不合理的是( )
a.CaCO +2H+===Ca2++CO↑+HO(观察气泡产生的快慢)
3 2 2
b.SO+2H+===S↓+SO ↑+HO(观察浑浊产生的快慢)
2 2 2
选项 反应 影响因素 所用试剂块状CaCO 、0.5 mol·L-1 HCl
3
A a 接触面积
粉末状CaCO 、0.5 mol·L-1 HCl
3
块状CaCO 、0.5 mol·L-1 HCl
3
B a H+浓度
块状CaCO 、3.0 mol·L-1 HCl
3
0.1 mol·L-1 Na SO、稀HSO
2 2 3 2 4
C b H+浓度
0.1 mol·L-1 Na SO、浓HSO
2 2 3 2 4
0.1 mol·L-1 Na SO、0.1 mol·L-1 HSO 、冷水
2 2 3 2 4
D b 温度
0.1 mol·L-1 Na SO、0.1 mol·L-1 HSO 、热水
2 2 3 2 4
8.(2023·南京调研)将金红石(TiO)转化为TiCl 是生产金属钛的关键步骤。在1.0×105 Pa,将TiO 、C、Cl
2 4 2 2
以物质的量之比为1∶2∶2进行反应,平衡体系中主要物质的量分数(x)随温度变化理论计算结果如图所示。
下列说法不正确的是( )
A.200~1 600 ℃反应达到平衡时,TiO 的转化率均已接近100%
2
B.将400 ℃时的平衡体系加热至800 ℃,平衡C(s)+CO(g)2CO(g)向正反应方向移动
2
C.1 000 ℃时,测得某时刻x(TiCl )=0.2。其他条件不变,延长反应时间能使x(TiCl )超过该温度下平衡时的
4 4
x(TiCl )
4
D.实际生产时反应温度选择900 ℃而不选择200 ℃,其主要原因是900 ℃比200 ℃时化学反应速率更快,
生产效益更高
9.对于反应2SiHCl (g)SiH Cl(g)+SiCl (g),采用大孔弱碱性阴离子交换树脂催化剂在 323 K和343 K
3 2 2 4
时SiHCl 的转化率随时间变化的结果如图所示。下列说法不正确的是( )
3
A.该反应的ΔH>0B.a、b处反应速率大小关系:v 大于v
a b
C.在343 K下,要提高SiHCl 的转化率,可以及时移去产物或增加反应物浓度
3
D.343 K时,SiHCl 的平衡转化率为22%,可以求得该温度下的平衡常数约为0.02
3
10.(2023·陕西宝鸡·统考一模)下列方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
探究温度对化 将2mL0.5mol/L的CuCl 溶液加 若溶液由黄绿色变为蓝绿色,说明降低温度,
A 2
学平衡的影响 热后置于冷水中,观察现象 [Cu(H O) ]2++4Cl-⇌[CuCl ]2-+4H O向逆方向移动
2 4 4 2
取脱氧剂包装内固体粉末于试
检验食品脱氧
管中,加足量稀盐酸溶解,充 若溶液未变红色,说明脱氧剂中还原铁粉没有变
B 剂中还原铁粉
分反应后滴加KSCN溶液,振 质
是否已变质
荡,观察溶液颜色变化
比较CHCOO-
3 用pH试纸分别测定同浓度 若测得CHCOONa溶液pH大,说明CHCOO-水
C 和ClO-水解程 3 3
CHCOONa和NaClO溶液的pH 解程度大于ClO-
度大小 3
将电石与饱和食盐水反应产生
探究电石与水 若酸性高锰酸钾溶液褪色,说明电石与水反应生
D 的气体通入酸性高锰酸钾溶
的反应 成了乙炔
液,观察现象
A.A B.B C.C D.D
11(2023·北京东城·统考一模)某温度下,H(g)+I (g) 2HI(g)的平衡常数K=4。该温度下,在甲、乙、丙、
2 2
丁4个相同的恒容密闭容器中进行该反应,起始浓度如表所示。
甲 乙 丙 丁
c(H )/(mol•L-1) 0.01 0.02 0.01 0.02
2
c(I)/(mol•L-1) 0.01 0.01 0.01 0.01
2
c(HI)/(mol•L-1) 0 0 0.02 0.02
下列判断不正确的是
A.化学反应速率:乙>甲 B.平衡时,甲中I 的转化率为50%
2
C.平衡时,丙中c(I)=0.01mol•L-1 D.平衡时,乙和丁中 相等
2
12.(2023秋·天津河西·高三天津市新华中学校考期末)下列实验装置能达到实验目的的是A.用装置甲蒸干 溶液获取 晶体 B.用装置乙验证镁和稀盐酸反应的热效应
C.用装置丙制备 固体 D.用装置丁验证浓度对化学反应速率的影响
13.某温度下,XY在金(Au)表面发生分解反应:2XY(g)===2X (g)+Y(g),该反应的速率方程式为v=
2 2 2 2
kca(X Y)(k为速率常数,k只与温度、催化剂、接触面积等有关,与浓度无关,a为反应级数),实验测得剩
2
余XY的物质的量浓度与时间的关系如表所示:
2
时间/min 0 20 40 60 80
c(X Y)/(mol·L-1) 0.100 0.080 0.060 0.040 0.020
2
下列说法正确的是( )
A.a=1
B.反应过程中c(X Y)与t的关系如图所示
2
C.速率常数k=1.0×10-2 mol·L-1·min-1
D.其他条件不变,仅增大c(X Y),反应速率增大
2
14.(2023秋·山东青岛·高三统考期末)2022年诺贝尔化学奖授予三位科学家,以表彰他们在点击化学和
生物正交化学研究方面的贡献。点击化学是指可以像拼积木一样便捷的合成人们所需要的化学分子。以下
是叠氮化物与炔发生的经典CuAAC点击反应。
注:[Cu]指Cu+
下列说法错误的是
A.[Cu]可应用于生物正交反应的“点击”
B.反应中要保护[Cu],防止其氧化或歧化
C.分别在两个待拼接分子中引入叠氨基与炔基,在[Cu]的“点击”下,可完成分子的拼接
D.在反应历程中,存在共价键的断裂与离子键的生成
15.(2023·重庆·高三重庆巴蜀中学校考阶段练习)化学小组在丁烷脱氢制丁烯的研究上取得了重大的突
破,利用计算机技术测得在催化剂表面的反应历程如图所示,其中催化剂表面上的物种用*标注,TS表示
过渡态物质。下列说法错误的是A.该历程中决速步骤为
B.该反应在任意温度下均可自发进行
C.催化剂起到降低反应活化能,加快反应速率的作用
D.该历程中伴随着极性键断裂与非极性键的形成
16.(2023秋·陕西西安·高三西安市铁一中学校考期末)一定温度下,将0.16 mol X和0.16 mol Y加入10
L的恒容密闭容器中,发生反应X(s)+2Y(g) 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的
数据如表:
t/min 2 4 7 9
n(Y)/mol 0.12 0.11 0.10 0.10
下列说法正确的是( )
A.温度升高,此反应的化学平衡常数K>0.36
B.当容器内气体的密度不变时,反应达到化学平衡状态
C.反应前2 min的平均反应速率v(Z)=4.0×10-3 mol·L-1·min-1
D.其他条件不变,再充入0.6 mol Z,平衡时Z的体积分数增大
17.(2023·陕西宝鸡·统考二模,双选)2022年诺贝尔化学奖授予在“点击化学和生物正交化学”领域做出
贡献的三位科学家。点击化学经典反应之一是:一价铜[Cu]催化的叠氮化物-端炔烃环加成反应,反应机理
示意如下。下列说法正确的是
A.一价铜[Cu]能有效降低总反应的焓变,加快反应速率
B.反应③过程中,涉及极性键和非极性键的断裂和形成
C.总反应为
D.反应过程中共生成4种中间产物
18.(2023春·河南洛阳·高三孟津县第一高级中学校考阶段练习,双选)Ni可活化 放出 ,其反应
历程如图所示:
下列关于活化历程的说法错误的是
A.决速步骤:中间体1→中间体2
B.中间体2比中间体1稳定
C.Ni—H键的形成有利于氢原子的迁移
D.总反应为吸热反应
19.(2023·全国·高三专题练习)硫和氮是生物必须的营养元素,含硫和氮的化合物在自然界中广泛存在。
(1)火山喷发产生HS在大气中发生如下反应:
2
①2HS(g)+O(g)=2S(g)+2H O(l) △H=akJ•mol-1
2 2 2
②S(g)+O (g)=SO(g) △H=bkJ•mol-1
2 2
写出HS(g)燃烧的热化学方程式 。
2
(2)工业上可用NaClO碱性溶液吸收SO 。为了提高吸收效率,常用Ni O 作为催化剂。反应过程中产生的
2 2 3
四价镍和原子氧具有极强的氧化能力,可加快对SO 的吸收。该催化过程的示意图如图所示。Ca(ClO) 也
2 2
可用于脱硫,且脱硫效果比NaClO更好,原因是 。(3)氮的氧化物脱除可以利用电化学原理处理,利用如图所示装置可同时吸收SO 和NO。
2
已知:HSO 是一种弱酸。
2 2 4
①阴极的电极反应式为 。
②若无能量损失,相同条件下,SO 和NO的体积比为 时,两种气体都能被完全处理。
2
(4)已知2NO(g)+O (g) 2NO (g)的反应历程分两步。
2 2
第一步:2NO(g)+ NO(g)(快反应)
2 2
第二步:NO(g)+O(g) 2NO (g)(慢反应)
2 2 2 2
用O 表示的速率方程为v(O )=k c2(NO)•c(O );用NO 表示的速率方程为v(NO )=k c2(NO)•c(O ),k 与k 分
2 2 1 2 2 2 2 2 1 2
别表示速率常数,则 = 。(填数值)
(5)太阳能光电催化—化学耦合分解HS的装置如图所示。
2
①该太阳能光电催化—化学耦合分解HS的过程可描述为 。
2
②从能源利用和资源综合利用角度分析该方法优点是 。
20.(2023·成都模拟)亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO和Cl 反应得到,化学方程式为
2
2NO(g)+Cl
2
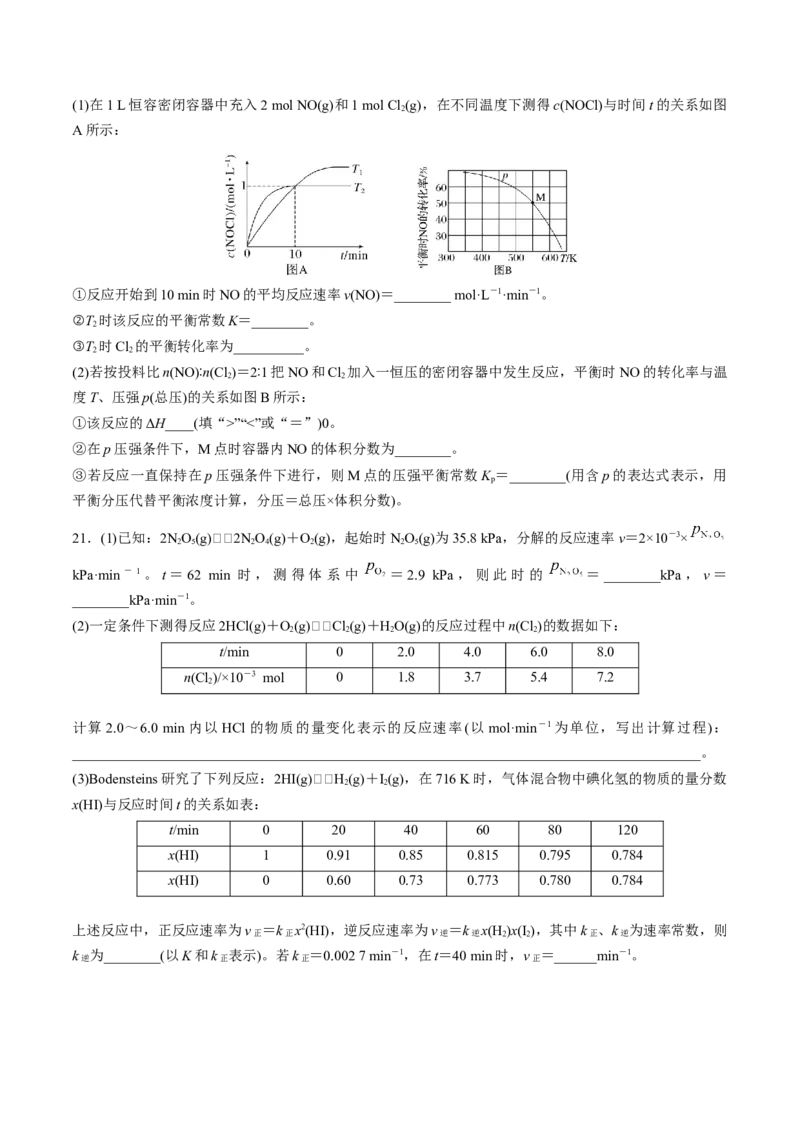
(g)⇌2NOCl(g)。(1)在1 L恒容密闭容器中充入2 mol NO(g)和1 mol Cl (g),在不同温度下测得c(NOCl)与时间t的关系如图
2
A所示:
①反应开始到10 min时NO的平均反应速率v(NO)=________ mol·L-1·min-1。
②T 时该反应的平衡常数K=________。
2
③T 时Cl 的平衡转化率为__________。
2 2
(2)若按投料比n(NO)∶n(Cl )=2∶1把NO和Cl 加入一恒压的密闭容器中发生反应,平衡时NO的转化率与温
2 2
度T、压强p(总压)的关系如图B所示:
①该反应的ΔH____(填“>”“<”或“=”)0。
②在p压强条件下,M点时容器内NO的体积分数为________。
③若反应一直保持在p压强条件下进行,则M点的压强平衡常数K =________(用含p的表达式表示,用
p
平衡分压代替平衡浓度计算,分压=总压×体积分数)。
21.(1)已知:2NO(g)2N O(g)+O(g),起始时NO(g)为35.8 kPa,分解的反应速率v=2×10-3×
2 5 2 4 2 2 5
kPa·min-1。t=62 min 时,测得体系中 =2.9 kPa,则此时的 =________kPa,v=
________kPa·min-1。
(2)一定条件下测得反应2HCl(g)+O(g)Cl(g)+HO(g)的反应过程中n(Cl )的数据如下:
2 2 2 2
t/min 0 2.0 4.0 6.0 8.0
n(Cl )/×10-3 mol 0 1.8 3.7 5.4 7.2
2
计算2.0~6.0 min 内以 HCl 的物质的量变化表示的反应速率(以mol·min-1为单位,写出计算过程):
_________________________________________________________________________________________。
(3)Bodensteins研究了下列反应:2HI(g)H(g)+I(g),在716 K时,气体混合物中碘化氢的物质的量分数
2 2
x(HI)与反应时间t的关系如表:
t/min 0 20 40 60 80 120
x(HI) 1 0.91 0.85 0.815 0.795 0.784
x(HI) 0 0.60 0.73 0.773 0.780 0.784
上述反应中,正反应速率为v =k x2(HI),逆反应速率为v =k x(H )x(I),其中k 、k 为速率常数,则
正 正 逆 逆 2 2 正 逆
k 为________(以K和k 表示)。若k =0.002 7 min-1,在t=40 min时,v =______min-1。
逆 正 正 正