文档内容
训练(三十五) 化学平衡及其移动
1.(2021·河南部分重点校联考)在恒温恒容的密闭容器中发生反应 4NH (g)+5O(g)
3 2
4NO(g)+6HO(g) ΔH<0,下列能说明该反应达到平衡状态的是( )
2
①反应速率5v(NH
3
)=4v(O
2
) ②体系的压强不再发生变化 ③混合气体的密度不再发
生变化 ④气体的平均摩尔质量不再发生变化 ⑤单位时间内生成5 mol O ,同时断裂12
2
mol O—H键 ⑥NO的浓度不变
A.②④⑥ B.①②④⑥
C.②⑤⑥ D.①②③④⑤
A [无论反应是否达到平衡,用不同物质表示的反应速率之比等于其化学计量数之比,
v(NH
3
)∶ v(O
2
)=4∶5,则有5v(NH
3
)=4v(O
2
),①错误;该反应的正向是气体总分子数增加的
反应,恒温恒容时,体系的压强不变,则气体总物质的量不变,达到平衡状态,②正确;恒容时,
反应中各物质均为气体,则混合气体的密度始终不变,③错误;气体的总质量一定,平均摩尔
质量不变,则气体总物质的量不变,该反应达到平衡状态,④正确;单位时间内生成5 mol O
2
必然消耗6 mol H O,断裂12 mol H—O键,不能判断是否平衡,⑤错误;NO的浓度不变,则
2
其消耗速率等于生成速率,该反应达到平衡,⑥正确。]
2.(2021·山东日照检测)对可逆反应2A(s)+3B(g)C(g)+2D(g) ΔH<0,在一定条件
下达到平衡。下列有关叙述正确的是( )
①增加A的量,平衡向正反应方向移动 ②升高温度,平衡向逆反应方向移动, v(正)减
小 ③压强增大一倍,平衡不移动, v(正)、 v(逆)不变 ④增大B的浓度, v(正)>v(逆) ⑤加
入催化剂,B的转化率提高
A.①② B.④
C.③ D.④⑤
B [A是固体,其量的变化对平衡无影响,①错误;而增大B的浓度,正反应速率增大,
平衡向正反应方向移动, v(正)>v(逆),④正确;升高温度, v(正)、 v(逆)均增大,但 v(逆)增大的程度大,平衡向逆反应方向移动,②错误;此反应为反应前后气体分子数不变的反应,故增大
压强,平衡不移动,但 v(正)、 v(逆)都增大,③错误;催化剂不能使化学平衡发生移动,B的转
化率不变,⑤错误。]
3.(2021·北京师大附中检测)实验:
①0.005 mol/L FeCl 溶液和0.015 mol/L KSCN溶液各1 mL混合得到红色溶液a,均分
3
溶液a置于b、c两支试管中;
②向b中滴加3滴饱和FeCl 溶液,溶液颜色加深;
3
③再向上述b溶液中滴加3滴1 mol/L NaOH溶液,溶液颜色变浅且出现浑浊;
④向c中逐渐滴加1 mol/L KSCN溶液2 mL,溶液颜色先变深后变浅。
下列分析不正确的是( )
A.实验②中增大Fe3+浓度使平衡Fe3++3SCN-Fe(SCN) 正向移动
3
B.实验③中发生反应:Fe3++3OH-===Fe(OH) ↓
3
C.实验③和④中溶液颜色变浅的原因相同
D.实验②、③、④均可说明浓度改变对平衡移动的影响
C [实验②中增大Fe3+浓度使平衡Fe3++3SCN-Fe(SCN) 正向移动,c[Fe(SCN) ]
3 3
增大,溶液的红色加深,A项正确;实验③中滴加3滴1 mol/L NaOH溶液,发生反应:Fe3++
3OH-===Fe(OH) ↓,使平衡Fe3++3SCN-Fe(SCN) 逆向移动,溶液的颜色变浅,B项正
3 3
确;实验④逐渐滴加1 mol/L KSCN溶液,使平衡正向移动,后继续加溶液相当于稀释,红色
变浅,二者原因不同,C项错误;根据上述分析,实验②、③、④均可说明浓度改变对平衡移动
的影响,D项正确。]
4.(2021·山东日照实验中学检测)一定条件下,反应CO(g)+HO(g)CO(g)+H(g)
2 2 2
ΔH>0,达到平衡状态后,分别改变某个条件,下面四个说法中,条件改变、影响原因及影响结
果均正确的是( )
条件改变 影响原因 影响结果
活化分子所占百分比增大,正逆反应速率
A 适当缩小容器的容积 平衡不移动
均同等程度加快
活化分子所占百分比增大,正逆反应速率
B 适当升高温度 平衡正向移动
加快,逆反应速率减慢
分子能量增大,活化分子所占百分比增
C 加入催化剂 平衡不移动
大,正逆反应速率均同等程度加快
活化分子所占百分比不变,但是单位体积
D 适当扩大容器的容积 内的活化分子数减少,正逆反应速率同等 平衡不移动
程度减慢D [缩小容器的容积,单位体积内活化分子的数目增大,正、逆反应速率同等程度加快,
平衡不移动,但活化分子所占百分比不变,A项错误;适当升高温度,活化分子所占百分比增
大,正、逆反应速率均增大,但正反应速率增大倍数大于逆反应速率,平衡正向移动,B项错
误;加入催化剂,降低了活化能,分子能量不变,活化分子数目及所占百分比均增大,正、逆反
应速率同等程度加快,平衡不移动,C项错误;扩大容器的容积,单位体积内活化分子数目减
少,正、逆反应速率均同等程度地减慢,平衡不移动,D项正确。]
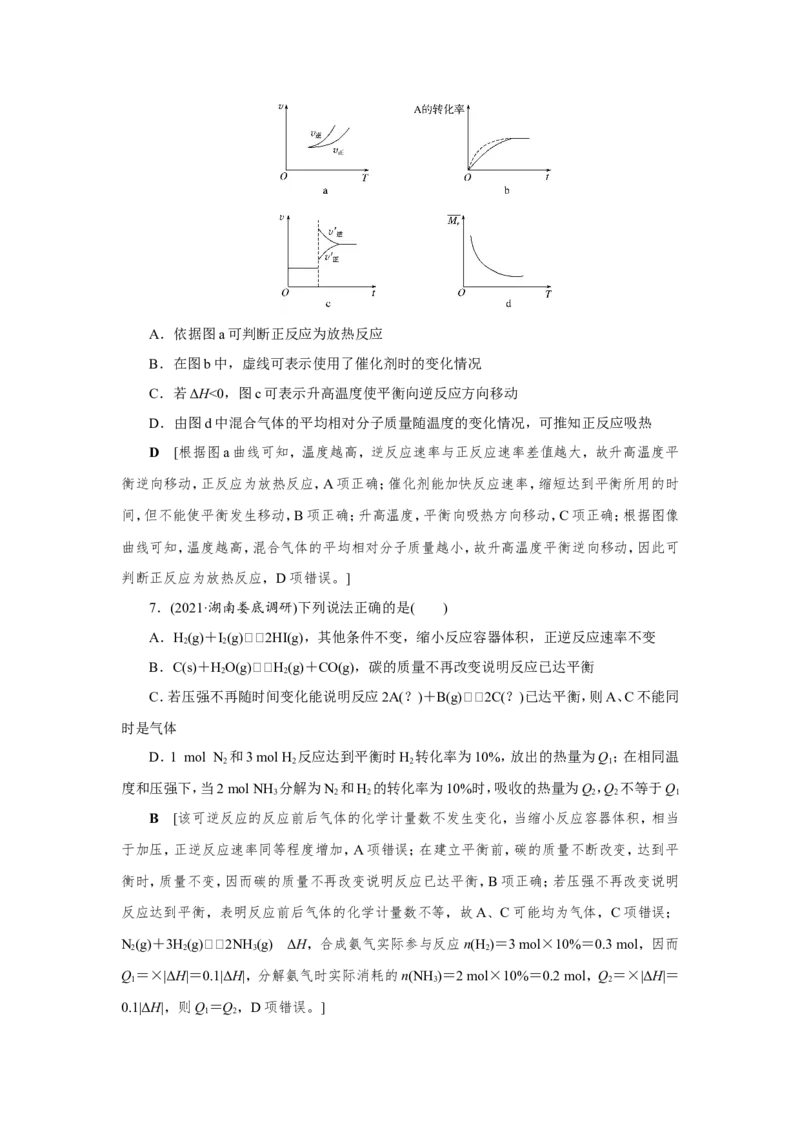
5.下列说法正确的是( )
A. (海南卷)已知反应CO(g)+HO(g)CO(g)+H(g)
2 2 2
ΔH<0。在一定温度和压强下于密闭容器中,反应达到平衡,若减小压强,n(CO)增加;若
2
充入一定量的氮气,n(H )不变
2
B.(天津卷)常压下,羰基化法精炼镍的原理为:Ni(s)+4CO(g)Ni(CO) (g),该反应达
4
到平衡时,
v生成 [Ni(CO) 4 ]=4v生成 (CO)
C.(天津卷)在恒温恒容的密闭容器中,某储氢反应:
MH(s)+yH(g) MH (s) ΔH<0,若容器内气体压强保持不变,达到化学平衡
x 2 x+2y
D.(天津卷)在恒温恒容的密闭容器中,某储氢反应:
MH
x
(s)+yH
2
(g)MH
x+2y
(s) ΔH<0,达到化学平衡,若向容器内通入少量氢气,则 v(放
氢)>v(吸氢)
C [减压平衡不移动,n(CO)不变,恒压充入氮气,体积增大,效果等同于减压,平衡不
2
移动,n(H 2 )不变,A项错误;达到平衡时,4v生成 [Ni(CO) 4 ]= v生成 (CO),B项错误;该反应是气
体压强减小的反应,所以压强不变可以说明达到了平衡状态,C项正确;加入氢气正反应速
率增大, v(放氢)v(逆)。
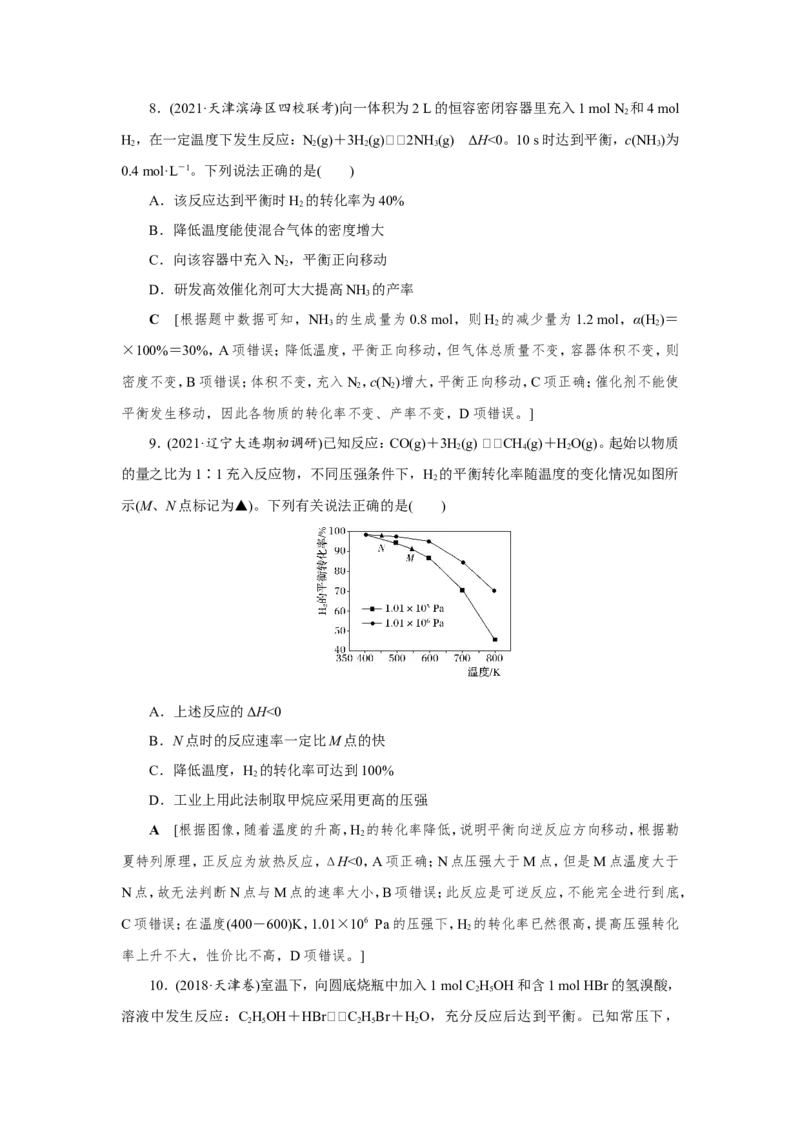
(2)①由图可知,温度升高时CO的产率上升,说明反应②是吸热反应,升高温度平衡正
向移动,CO的产率升高。
②图中250 ℃时CHOH产率最大,随后升高温度,CHOH产率下降,故获取CHOH最
3 3 3
适宜的温度是250 ℃。提高CO 转化为CHOH的平衡转化率,可使用对反应①选择性更高
2 3
的催化剂,促使反应①更有利于发生,A正确;压缩体积,反应①正向移动,CHOH的平衡转
3
化率增大,反应②的平衡不移动,B正确;增大CO 和H 的初始投料比,CO 的转化率降低,C
2 2 2
错误。
答案 (1)①0.375 ②D ③>
(2)①反应②是吸热反应,升高温度平衡正向移动,CO产率升高
②250 ℃ AB
13.(2021·辽宁六校协作体联考)CO 和H 充入一定体积的密闭容器中,反应过程和在两
2 2
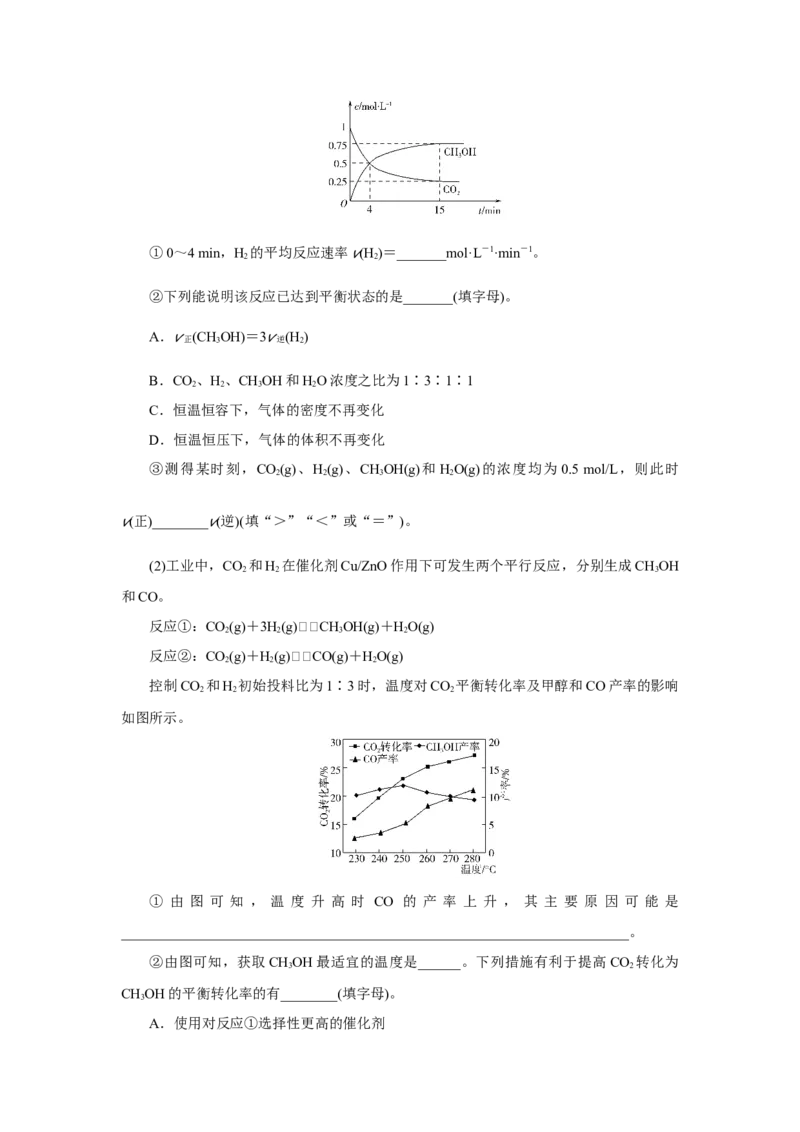
种温度下CHOH的物质的量随时间的变化如图1所示。
3图1
(1)已知图1所示反应每消耗1 mol H ,热量变化是16.3 kJ,则反应的热化学方程式为
2
________________________________________________________________________
________________________________________________________________________。
曲线Ⅰ、Ⅱ对应的平衡常数大小关系为K ________K (填“>”“=”或“<”)。
Ⅰ Ⅱ
(2)一定温度下,若此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是
________(填字母)。
a.容器中压强不变
b.H 的体积分数不变
2
c.c(H )=3c(CHOH)
2 3
d.容器中密度不变
e.2个C===O断裂的同时有3个H—H断裂
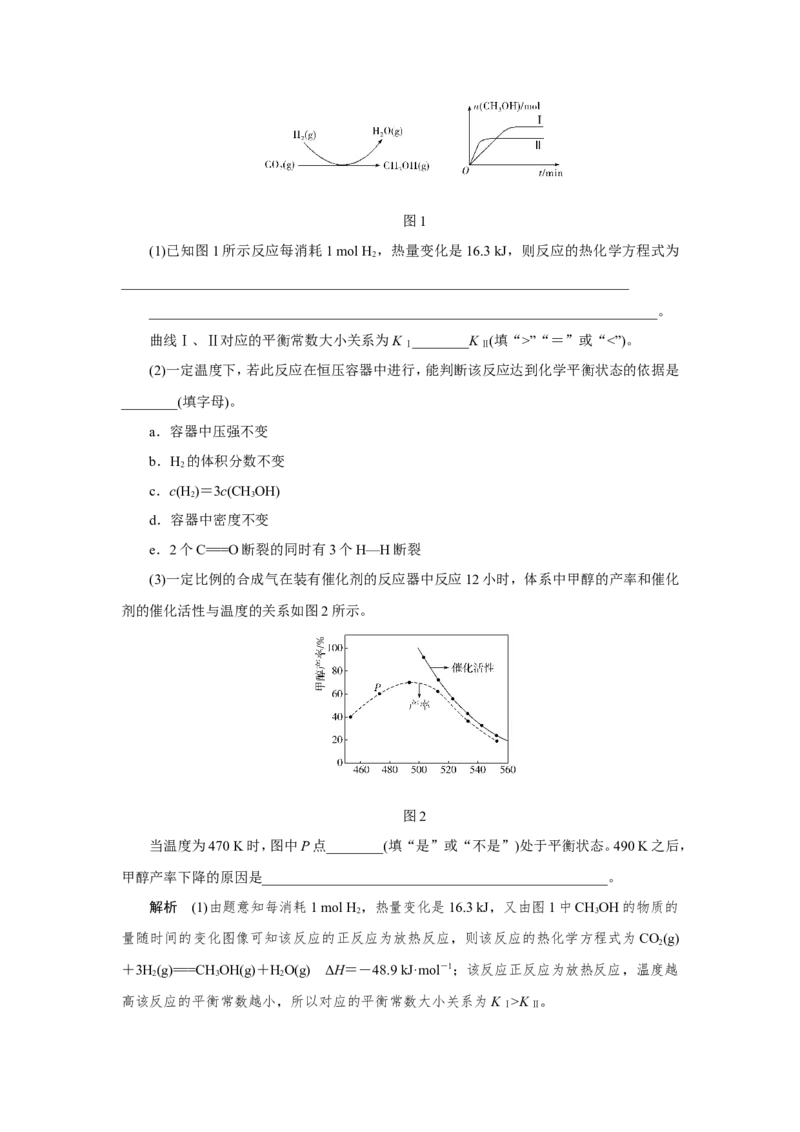
(3)一定比例的合成气在装有催化剂的反应器中反应12小时,体系中甲醇的产率和催化
剂的催化活性与温度的关系如图2所示。
图2
当温度为470 K时,图中P点________(填“是”或“不是”)处于平衡状态。490 K之后,
甲醇产率下降的原因是_________________________________________________。
解析 (1)由题意知每消耗1 mol H ,热量变化是16.3 kJ,又由图1中CHOH的物质的
2 3
量随时间的变化图像可知该反应的正反应为放热反应,则该反应的热化学方程式为CO(g)
2
+3H(g)===CH OH(g)+HO(g) ΔH=-48.9 kJ·mol-1;该反应正反应为放热反应,温度越
2 3 2
高该反应的平衡常数越小,所以对应的平衡常数大小关系为K >K 。
Ⅰ Ⅱ(2)一定温度下发生反应CO(g)+3H(g)===CH OH(g)+HO(g)。因为此反应是在恒压容
2 2 3 2
器中进行,容器中压强始终不变,所以压强不变不能判断反应达到化学平衡状态,a项错误;
因为压强恒定,且化学方程式两边计量数之和是不等的,所以H 的体积分数不变能说明反应
2
达到化学平衡状态,b项正确;c(H )=3c(CHOH)不能说明正、逆反应速率相等,所以不能判
2 3
断化学反应是否达到平衡状态,c项错误;容器中密度ρ=,反应物和生成物都是气体,因为
反应是在恒压容器中进行且反应后气体体积减小,所以密度不变可以说明反应达到化学平
衡状态,d项正确;CO 和H 都是反应物,只要2个C===O断裂的同时就有3个H—H断裂,
2 2
不能说明正反应速率和逆反应速率相等,e项错误。
(3)在490 K之前,甲醇产率随着温度升高而增大的原因是:反应尚未达到平衡,温度越
高化学反应速率越快;490 K之后,甲醇产率下降的原因是:反应达到平衡后升高温度,平衡
逆向移动,且催化剂活性降低。
答案 (1)CO (g)+3H(g)===CH OH(g)+HO(g) ΔH=-48.9 kJ·mol-1 >
2 2 3 2
(2)bd (3)不是 反应为放热反应,升高温度,平衡逆向移动,且催化剂活性降低