文档内容
第 3 讲 硫及其重要化合物
课 程 标 准 知 识 建 构
1.结合真实情境中的应用实例或通过
实验探究了解硫及其重要化合物的主
要性质。
2.知道硫及其主要化合物的制备方
法,认识硫的氧化物对生态环境的影
响。
一、硫及其氧化物
1.硫单质
(1)自然界中硫元素的存在
(2)硫单质的物理性质
俗称硫黄,是一种黄色固体,不溶于水,微溶于酒精,易溶于CS 。
2
(3)从化合价的角度认识硫单质的化学性质
S ――→――→S
2.二氧化硫
(1)物理性质:无色有刺激性气味的气体,有毒,密度比空气的大,易溶于水。
(2)化学性质填写相应化学方程式:
①酸性氧化物的通性
②氧化性
如与H S溶液反应:SO + 2H S == =3S ↓ + 2H O
2 2 2 2
③还原性
④漂白性:可使品红溶液等有机色质褪色,生成不稳定的化合物。
【特别提醒】
(1)SO 只能使紫色的石蕊溶液变红,但不能使之褪色。
2
(2)SO 能使溴水、酸性KMnO 溶液褪色,体现了SO 的还原性,而不是漂白
2 4 2
性。
3.三氧化硫
(1)物理性质:在常温下为液体,在标准状况下为固体。
(2)化学性质:
【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)硫在空气中的燃烧产物是二氧化硫,在纯氧中的燃烧产物是三氧化硫(
)
(2)SO 可广泛应用于食品漂白( )
2
(3)SO 和Cl 等物质的量混合后通入装有湿润的有色布条的集气瓶中,漂白
2 2
效果更好( )
(4)SO 、漂白粉、活性炭、Na O 都能使红墨水褪色,其原理相同( )
2 2 2
(5)汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理( )
答案 (1)× (2)× (3)× (4)× (5)√
二、硫酸 硫酸根离子的检验
1.硫酸的物理性质(1)纯硫酸是一种无色油状液体,沸点高,难挥发。
(2)溶解性:浓硫酸与水以任意比混溶,溶解时可放出大量热。
(3)稀释方法:将浓硫酸沿器壁慢慢注入水中并不断搅拌。
2.硫酸的化学性质
(1)稀硫酸具有酸的通性
硫酸是强电解质,在水溶液中的电离方程式为H SO == =2H + + SO ,具有酸的
2 4
通性。
(2)浓硫酸的特性
3.硫酸的工业制备
三步骤 三反应
黄铁矿煅烧 4FeS + 11O ==== = 2F e O + 8SO
2 2 2 3 2
SO 的催化氧化 2SO + O 2SO
2 2 2 3
SO 吸收 SO + H O == =H SO
3 3 2 2 4
4.SO的检验
(1)检验方法:被检液――→取清液――→产生白色沉淀,证明原溶液中存在
SO,反之则没有SO。
(2)注意事项:检验时溶液中可能存在的CO、SO、Ag+有干扰,整个过程中可
能发生反应的离子方程式: CO + 2H + == =CO ↑ + H O、 SO + 2H + == =SO ↑ +
2 2 2
H O、 Ag + + Cl - == =AgCl ↓ 、 Ba 2 + + SO == =BaSO ↓。
2 4
【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)将少量铜加入浓硫酸中加热,很快能观察到溶液变为蓝色( )
(2)铜片溶于热的浓硫酸,体现了浓硫酸的酸性和强氧化性( )
(3)50 mL 18.4 mol·L-1的浓硫酸与足量的铜反应,可产生 SO 物质的量为
2
0.46 mol( )
(4)一定量浓硫酸中加入足量锌粒加热,产生的气体为SO 和H 的混合气体(
2 2)
(5)浓H SO 使胆矾(CuSO ·5H O)变成白色粉末,体现了浓H SO 的脱水性(
2 4 4 2 2 4
)
(6)某溶液中加入BaCl 溶液,产生白色沉淀,加稀盐酸后,白色沉淀不溶解,
2
也无其他现象,说明该溶液中一定含有SO( )
(7)向Na SO 溶液中加入硝酸酸化的Ba(NO ) 溶液,有白色沉淀出现,说明
2 3 3 2
Na SO 溶液已经变质( )
2 3
答案 (1)× (2)√ (3)× (4)√ (5)× (6)× (7)×
三、硫及其化合物的转化
1.硫及其化合物的价类二维图
2.硫及其化合物的转化
(1)相同价态硫的转化通过酸、碱反应实现
如:
写出②、③、④反应的化学方程式:
②H SO + 2NaOH == =N a SO + 2H O;
2 3 2 3 2
③Na SO + H SO == =Na SO + H O + SO ↑;
2 3 2 4 2 4 2 2
④SO + N a SO + H O == =2NaHSO 。
2 2 3 2 3
(2)不同价态硫的转化通过氧化还原反应实现
如:H SSSO ――→SO
2 2 3
写出③、④、⑤反应的化学方程式:
③2SO + O 2SO ;
2 2 3
④ S + H ==== = H S;
2 2
⑤SO + 2H S == =3S ↓ + 2H O。
2 2 2
【诊断3】 物质的类别和核心元素的化合价是研究物质性质的两个重要角度。
请根据下图所示,回答下列问题:(1)X的化学式为________,Y的化学式为________。
(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程
式为_______________________________________________________________
___________________________________________________________________。
(3)欲制备Na S O ,从氧化还原角度分析,合理的是________(填字母)。
2 2 3
A.Na S+S B.Na SO +S
2 2 3
C.Na SO +Na SO D.SO +Na SO
2 3 2 4 2 2 4
(4)将X与SO 混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质
2
量之比为________。
答案 (1)H S SO
2 2
(2)Cu+2H SO (浓)=====CuSO +SO ↑+2H O
2 4 4 2 2
(3)B (4)2∶1
解析 (2)W的浓溶液是浓硫酸,与铜单质在加热条件下发生反应:Cu+
2H SO (浓)=====CuSO +SO ↑+2H O。(3)Na S O 中S元素的化合价是+2价,
2 4 4 2 2 2 2 3
从氧化还原的角度分析,反应物中S元素的化合价必须分别高于2和低于2,A
中S的化合价都低于2,C、D中S的化合价都高于2,故B符合题意。(4)X为
H S,与SO 混合可生成淡黄色固体:2H S+SO ===3S↓+2H O,H S作还原剂,
2 2 2 2 2 2
二氧化硫作氧化剂,则该反应的氧化剂与还原剂的物质的量之比为1∶2,氧化产
物与还原产物的质量之比为2∶1。
考点一 硫及其化合物的性质与应用
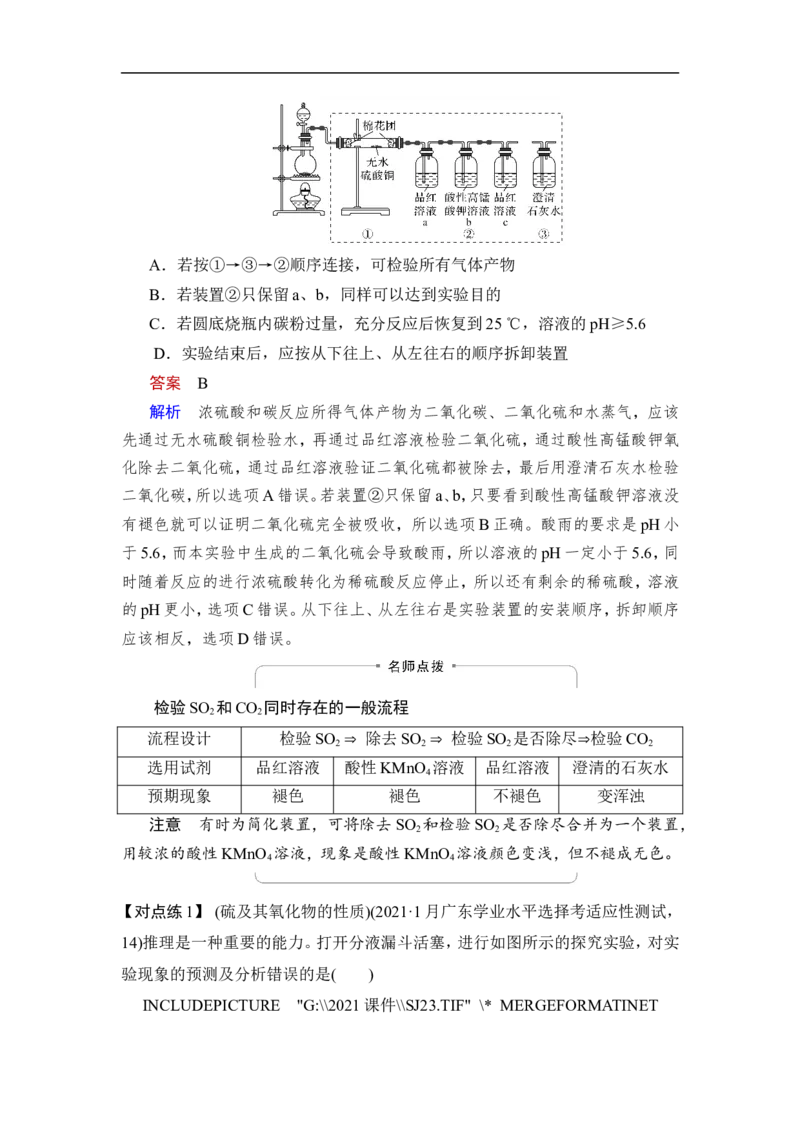
【典例1】 (2020·重庆市模拟)下图所示为某同学设计的检验浓硫酸和碳反应
所得气体产物的实验装置图。下列说法正确的是( )A.若按①→③→②顺序连接,可检验所有气体产物
B.若装置②只保留a、b,同样可以达到实验目的
C.若圆底烧瓶内碳粉过量,充分反应后恢复到25 ℃,溶液的pH≥5.6
D.实验结束后,应按从下往上、从左往右的顺序拆卸装置
答案 B
解析 浓硫酸和碳反应所得气体产物为二氧化碳、二氧化硫和水蒸气,应该
先通过无水硫酸铜检验水,再通过品红溶液检验二氧化硫,通过酸性高锰酸钾氧
化除去二氧化硫,通过品红溶液验证二氧化硫都被除去,最后用澄清石灰水检验
二氧化碳,所以选项A错误。若装置②只保留a、b,只要看到酸性高锰酸钾溶液没
有褪色就可以证明二氧化硫完全被吸收,所以选项B正确。酸雨的要求是pH小
于5.6,而本实验中生成的二氧化硫会导致酸雨,所以溶液的pH一定小于5.6,同
时随着反应的进行浓硫酸转化为稀硫酸反应停止,所以还有剩余的稀硫酸,溶液
的pH更小,选项C错误。从下往上、从左往右是实验装置的安装顺序,拆卸顺序
应该相反,选项D错误。
检验SO 和CO 同时存在的一般流程
2 2
流程设计 检验SO ⇒ 除去SO ⇒ 检验SO 是否除尽⇒检验CO
2 2 2 2
选用试剂 品红溶液 酸性KMnO 溶液 品红溶液 澄清的石灰水
4
预期现象 褪色 褪色 不褪色 变浑浊
注意 有时为简化装置,可将除去SO 和检验SO 是否除尽合并为一个装置,
2 2
用较浓的酸性KMnO 溶液,现象是酸性KMnO 溶液颜色变浅,但不褪成无色。
4 4
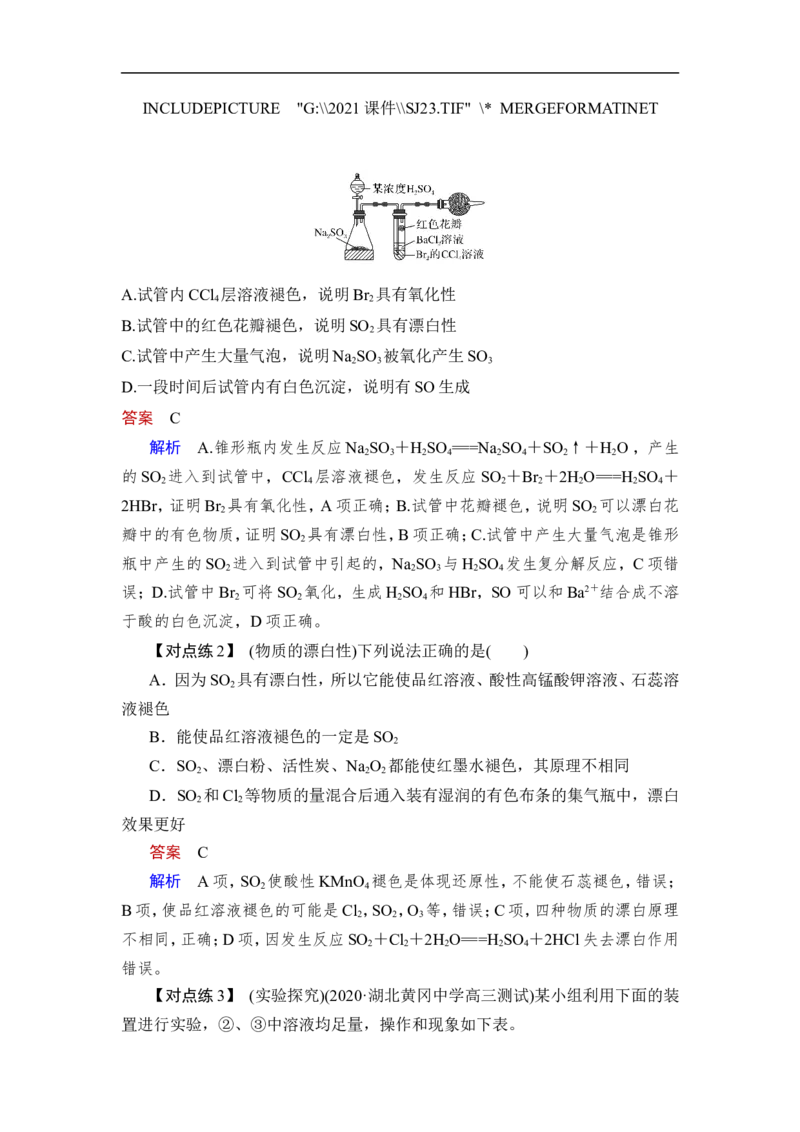
【对点练1】 (硫及其氧化物的性质)(2021·1月广东学业水平选择考适应性测试,
14)推理是一种重要的能力。打开分液漏斗活塞,进行如图所示的探究实验,对实
验现象的预测及分析错误的是( )
INCLUDEPICTURE "G:\\2021课件\\SJ23.TIF" \* MERGEFORMATINETINCLUDEPICTURE "G:\\2021课件\\SJ23.TIF" \* MERGEFORMATINET
A.试管内CCl 层溶液褪色,说明Br 具有氧化性
4 2
B.试管中的红色花瓣褪色,说明SO 具有漂白性
2
C.试管中产生大量气泡,说明Na SO 被氧化产生SO
2 3 3
D.一段时间后试管内有白色沉淀,说明有SO生成
答案 C
解析 A.锥形瓶内发生反应Na SO +H SO ===Na SO +SO ↑+H O ,产生
2 3 2 4 2 4 2 2
的SO 进入到试管中,CCl 层溶液褪色,发生反应SO +Br +2H O===H SO +
2 4 2 2 2 2 4
2HBr,证明Br 具有氧化性,A项正确;B.试管中花瓣褪色,说明SO 可以漂白花
2 2
瓣中的有色物质,证明SO 具有漂白性,B项正确;C.试管中产生大量气泡是锥形
2
瓶中产生的SO 进入到试管中引起的,Na SO 与H SO 发生复分解反应,C项错
2 2 3 2 4
误;D.试管中Br 可将SO 氧化,生成H SO 和HBr,SO 可以和Ba2+结合成不溶
2 2 2 4
于酸的白色沉淀,D项正确。
【对点练2】 (物质的漂白性)下列说法正确的是( )
A.因为SO 具有漂白性,所以它能使品红溶液、酸性高锰酸钾溶液、石蕊溶
2
液褪色
B.能使品红溶液褪色的一定是SO
2
C.SO 、漂白粉、活性炭、Na O 都能使红墨水褪色,其原理不相同
2 2 2
D.SO 和Cl 等物质的量混合后通入装有湿润的有色布条的集气瓶中,漂白
2 2
效果更好
答案 C
解析 A项,SO 使酸性KMnO 褪色是体现还原性,不能使石蕊褪色,错误;
2 4
B项,使品红溶液褪色的可能是Cl ,SO ,O 等,错误;C项,四种物质的漂白原理
2 2 3
不相同,正确;D项,因发生反应SO +Cl +2H O===H SO +2HCl失去漂白作用
2 2 2 2 4
错误。
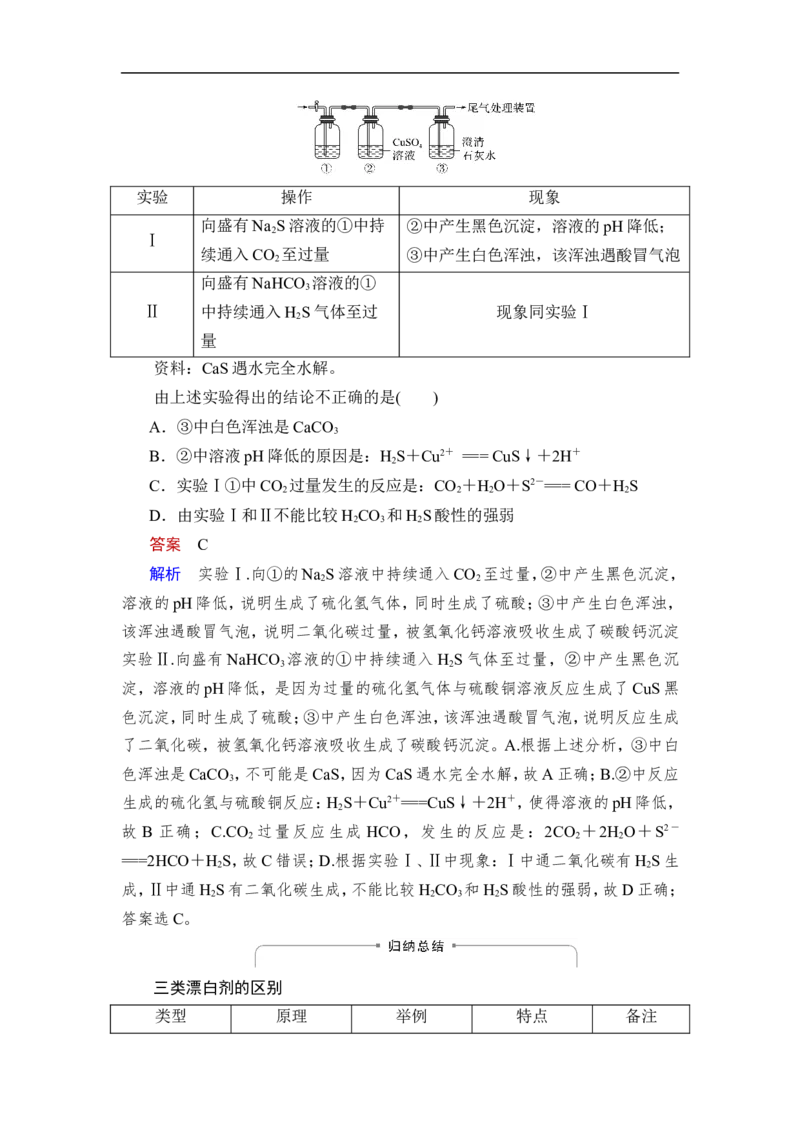
【对点练3】 (实验探究)(2020·湖北黄冈中学高三测试)某小组利用下面的装
置进行实验,②、③中溶液均足量,操作和现象如下表。实验 操作 现象
向盛有Na S溶液的①中持 ②中产生黑色沉淀,溶液的pH降低;
2
Ⅰ
续通入CO 至过量 ③中产生白色浑浊,该浑浊遇酸冒气泡
2
向盛有NaHCO 溶液的①
3
Ⅱ 中持续通入H S气体至过 现象同实验Ⅰ
2
量
资料:CaS遇水完全水解。
由上述实验得出的结论不正确的是( )
A.③中白色浑浊是CaCO
3
B.②中溶液pH降低的原因是:H S+Cu2+ === CuS↓+2H+
2
C.实验Ⅰ①中CO 过量发生的反应是:CO +H O+S2-=== CO+H S
2 2 2 2
D.由实验Ⅰ和Ⅱ不能比较H CO 和H S酸性的强弱
2 3 2
答案 C
解析 实验Ⅰ.向①的Na S溶液中持续通入CO 至过量,②中产生黑色沉淀,
2 2
溶液的pH降低,说明生成了硫化氢气体,同时生成了硫酸;③中产生白色浑浊,
该浑浊遇酸冒气泡,说明二氧化碳过量,被氢氧化钙溶液吸收生成了碳酸钙沉淀
实验Ⅱ.向盛有NaHCO 溶液的①中持续通入H S气体至过量,②中产生黑色沉
3 2
淀,溶液的pH降低,是因为过量的硫化氢气体与硫酸铜溶液反应生成了CuS黑
色沉淀,同时生成了硫酸;③中产生白色浑浊,该浑浊遇酸冒气泡,说明反应生成
了二氧化碳,被氢氧化钙溶液吸收生成了碳酸钙沉淀。A.根据上述分析,③中白
色浑浊是CaCO ,不可能是CaS,因为CaS遇水完全水解,故A正确;B.②中反应
3
生成的硫化氢与硫酸铜反应:H S+Cu2+===CuS↓+2H+,使得溶液的pH降低,
2
故 B 正确;C.CO 过量反应生成 HCO,发生的反应是:2CO +2H O+S2-
2 2 2
===2HCO+H S,故C错误;D.根据实验Ⅰ、Ⅱ中现象:Ⅰ中通二氧化碳有H S生
2 2
成,Ⅱ中通H S有二氧化碳生成,不能比较H CO 和H S酸性的强弱,故D正确;
2 2 3 2
答案选C。
三类漂白剂的区别
类型 原理 举例 特点 备注HClO、NaClO、
将有机色质内
Ca(ClO) 、 无选
2
氧化型 部“生色团” 不可逆、持久
Na O 、 择性
2 2
破坏
H O 、O 等
2 2 3
与有机色质内
部“生色团” 可逆、 有选
加合型 SO
2
“化合”成无 不持久 择性
色物质
将有色物质吸 物理 吸附
吸附型 活性炭
附而褪色 变化 色素
考点二 浓硫酸的性质及应用
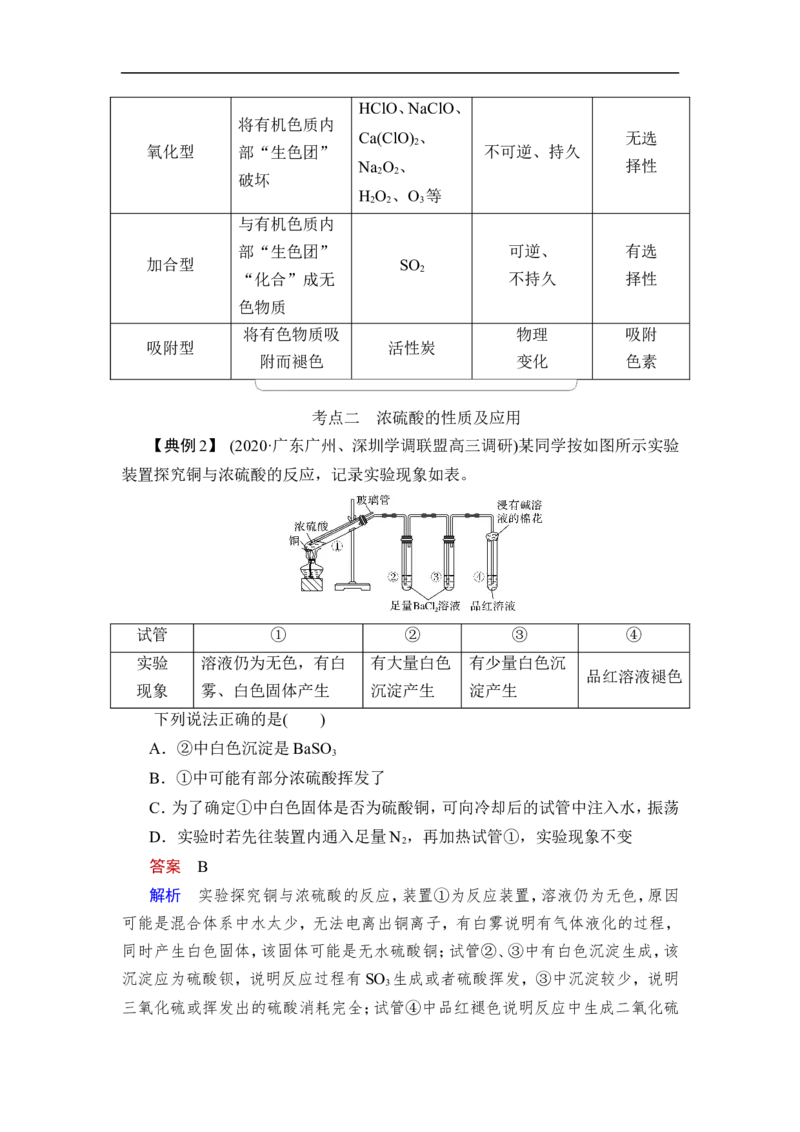
【典例2】 (2020·广东广州、深圳学调联盟高三调研)某同学按如图所示实验
装置探究铜与浓硫酸的反应,记录实验现象如表。
试管 ① ② ③ ④
实验 溶液仍为无色,有白 有大量白色 有少量白色沉
品红溶液褪色
现象 雾、白色固体产生 沉淀产生 淀产生
下列说法正确的是( )
A.②中白色沉淀是BaSO
3
B.①中可能有部分浓硫酸挥发了
C.为了确定①中白色固体是否为硫酸铜,可向冷却后的试管中注入水,振荡
D.实验时若先往装置内通入足量N ,再加热试管①,实验现象不变
2
答案 B
解析 实验探究铜与浓硫酸的反应,装置①为反应装置,溶液仍为无色,原因
可能是混合体系中水太少,无法电离出铜离子,有白雾说明有气体液化的过程,
同时产生白色固体,该固体可能是无水硫酸铜;试管②、③中有白色沉淀生成,该
沉淀应为硫酸钡,说明反应过程有SO 生成或者硫酸挥发,③中沉淀较少,说明
3
三氧化硫或挥发出的硫酸消耗完全;试管④中品红褪色说明反应中生成二氧化硫浸有碱的棉花可以处理尾气。A.二氧化硫不与氯化钡溶液反应,白色沉淀不可能
是BaSO ,故A错误;B.根据分析可知①中可能有部分硫酸挥发了,故B正确;C.
3
冷却后的试管中仍有浓硫酸剩余,浓硫酸稀释放热,不能将水注入试管,防止发
生危险,故C错误;D.反应过程中SO 是氧气将二氧化硫氧化生成,若先往装置
3
内通入足量N ,体系内没有氧气,则无SO 生成,试管②、③中将无沉淀产生,实
2 3
验现象发生变化,故D错误。
【对点练4】 (硫酸的性质)将一定量的锌与100 mL 18.5 mol/L浓硫酸充分反
应后,锌完全溶解,同时生成气体A 33.6 L(标准状况)。将反应后的溶液稀释至1
L,测得溶液的pH=1,则下列叙述错误的是( )
A.气体A为SO 和H 的混合物
2 2
B.反应中共消耗Zn 97.5 g
C.气体A中SO 和H 的体积比为4∶1
2 2
D.反应中共转移3 mol 电子
答案 C
解析 锌与浓硫酸发生反应:Zn+2H SO (浓)=====ZnSO +SO ↑+2H O,
2 4 4 2 2
随着反应的进行,H SO 的浓度变小,发生反应:Zn+H SO ===ZnSO +H ↑,设
2 4 2 4 4 2
反应生成的SO 物质的量为x,H 物质的量为y,则有x+y==1.5 mol,消耗的硫
2 2
酸:2x+y=18.5 mol/L×0.1 L-,解得x=0.3 mol,y=1.2 mol,V(SO )∶V(H )=
2 2
1∶4,参加反应的Zn:x+y=1.5 mol,质量是97.5 g,转移电子为1.5 mol×2=3
mol。
【对点练5】 (硫酸根离子的检验)下列过程中,最终的白色沉淀物不一定是
BaSO 的是( )
4
A.Fe(NO ) 溶液―――――――――――――――――――――→白色沉
3 2
淀
B.Ba(NO ) 溶液――――――――――――――――――→白色沉淀
3 2
C.无色溶液―――――――――――――――→白色沉淀
D.无色溶液―――――→无色溶液――――――→白色沉淀
答案 C
解析 A项,二氧化硫被硝酸氧化为硫酸,加氯化钡一定生成硫酸钡沉淀;B
项,亚硫酸根被硝酸氧化为硫酸根,沉淀也是硫酸钡;C项,所得沉淀可能是氯化
银;D项,先加过量盐酸无沉淀,再加氯化钡产生的白色沉淀一定是硫酸钡。
考点三 含硫化合物的转化关系及应用【典例3】 某化学兴趣小组为探究Na SO 固体在隔绝空气加热条件下的分解
2 3
产物,设计如下实验流程:
已知:气体Y是一种纯净物,在标准状况下密度为1.518 g/L。请回答下列问
题:
(1)气体Y为________(填化学式)。
(2)固体X与稀盐酸反应产生淡黄色沉淀的离子方程式为
_______________________________________________________________。
(3)实验过程中若测得白色沉淀的质量为 6.291 g,则 Na SO 的分解率为
2 3
________。
(4)Na SO 在空气中易被氧化,检验 Na SO 是否氧化变质的实验操作是
2 3 2 3
_____________________________________________________________________
___________________________________________________________________。
答案 (1)H S (2)2S2-+SO+6H+===3S↓+3H O
2 2
(3)90% (4)取少量Na SO 样品于试管中,加入足量盐酸溶解,再加入BaCl
2 3 2
溶液,若产生白色沉淀,则Na SO 已被氧化变质;若不产生白色沉淀,则Na SO
2 3 2 3
未被氧化变质
解析 气体Y是一种纯净物,在标准状况下密度为1.518 g/L,则Y的摩尔质
量为22.4 L/mol×1.518 g/L≈34.0 g/mol,Y应为H S气体,淡黄色沉淀为S,溶液
2
Z中加入BaCl 溶液生成白色沉淀,说明溶液Z中有Na SO ,则Na SO 隔绝空气
2 2 4 2 3
加热分解生成了 Na S 和 Na SO ,反应的化学方程式为 4Na SO =====Na S+
2 2 4 2 3 2
3Na SO 。
2 4
(1)由以上分析可知Y为H S;(2)固体X与稀盐酸反应产生淡黄色沉淀,这是
2
Na S和Na SO 在酸性溶液中发生了归中反应,离子方程式为2S2-+SO+6H+
2 2 3
===3S↓+3H O;(3)实验过程中测得白色沉淀的质量为6.291 g,且该白色沉淀为
2
BaSO ,则n(BaSO )===0.027 mol,说明生成的Na SO 的物质的量为0.027
4 4 2 4
mol,反应的化学方程式为4Na SO =====Na S+3Na SO ,可知分解的Na SO 的
2 3 2 2 4 2 3
物质的量为0.027 mol×=0.036 mol,则Na SO 的分解率为×100%=90%;
2 3
(4)Na SO 在空气中被氧化,生成Na SO ,检验Na SO 是否氧化变质的实质就是
2 3 2 4 2 3
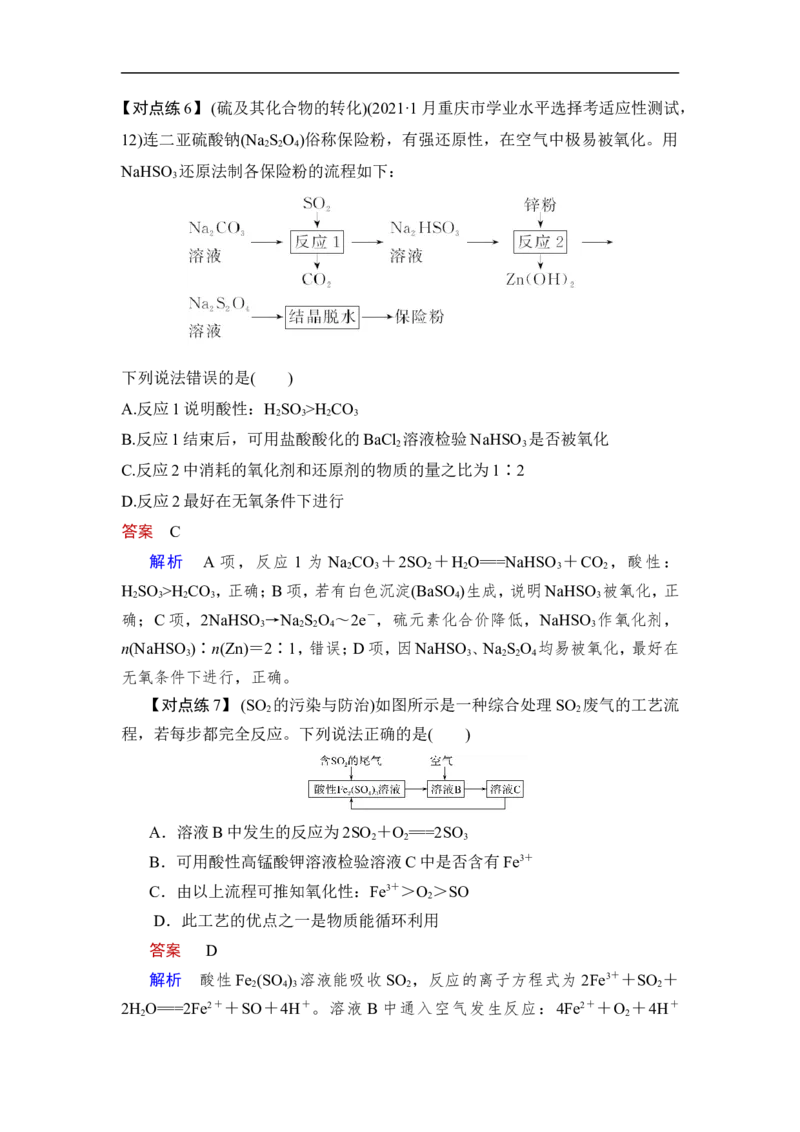
检验是否存在SO。【对点练6】 (硫及其化合物的转化)(2021·1月重庆市学业水平选择考适应性测试,
12)连二亚硫酸钠(Na S O )俗称保险粉,有强还原性,在空气中极易被氧化。用
2 2 4
NaHSO 还原法制各保险粉的流程如下:
3
下列说法错误的是( )
A.反应1说明酸性:H SO >H CO
2 3 2 3
B.反应1结束后,可用盐酸酸化的BaCl 溶液检验NaHSO 是否被氧化
2 3
C.反应2中消耗的氧化剂和还原剂的物质的量之比为1∶2
D.反应2最好在无氧条件下进行
答案 C
解析 A 项,反应 1 为 Na CO +2SO +H O===NaHSO +CO ,酸性:
2 3 2 2 3 2
H SO >H CO ,正确;B项,若有白色沉淀(BaSO )生成,说明NaHSO 被氧化,正
2 3 2 3 4 3
确;C项,2NaHSO →Na S O ~2e-,硫元素化合价降低,NaHSO 作氧化剂,
3 2 2 4 3
n(NaHSO )∶n(Zn)=2∶1,错误;D项,因NaHSO 、Na S O 均易被氧化,最好在
3 3 2 2 4
无氧条件下进行,正确。
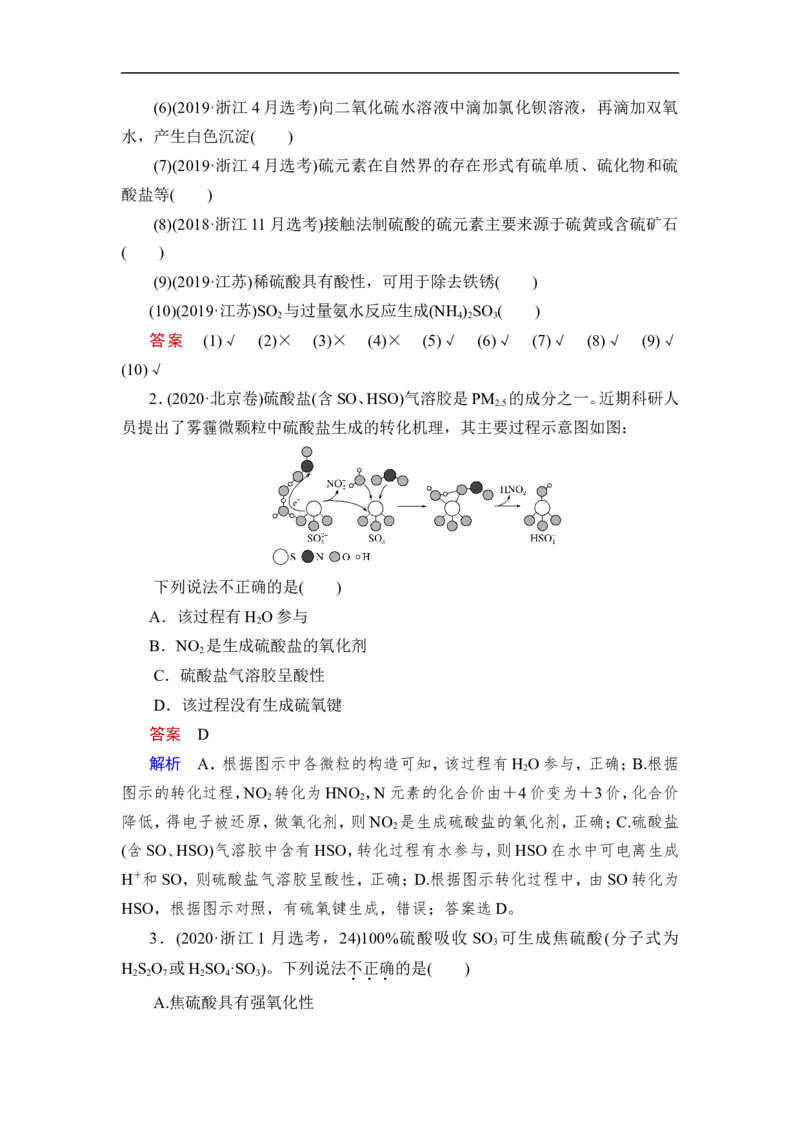
【对点练7】 (SO 的污染与防治)如图所示是一种综合处理SO 废气的工艺流
2 2
程,若每步都完全反应。下列说法正确的是( )
A.溶液B中发生的反应为2SO +O ===2SO
2 2 3
B.可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+
C.由以上流程可推知氧化性:Fe3+>O >SO
2
D.此工艺的优点之一是物质能循环利用
答案 D
解析 酸性Fe (SO ) 溶液能吸收 SO ,反应的离子方程式为 2Fe3++SO +
2 4 3 2 2
2H O===2Fe2++SO+4H+。溶液 B 中通入空气发生反应:4Fe2++O +4H+
2 2===4Fe3++2H O,氧化性:O >Fe3+,A、C两项错误;溶液C中含有Fe (SO ) ,可
2 2 2 4 3
用KSCN溶液检验Fe3+,B项错误;Fe (SO ) 可循环利用,D项正确。
2 4 3
四种常见的SO 尾气处理方法
2
方法一:钙基固硫法
为防治酸雨,工业上常用生石灰和含硫的煤混合后燃烧,燃烧时硫、生石灰、
O 共同反应生成硫酸钙,从而使硫转移到煤渣中,反应原理为 CaO+
2
SO =====CaSO 2CaSO +O =====2CaSO ,总反应方程式为 2CaO+2SO +
2 3, 3 2 4 2
O =====2CaSO 。
2 4
方法二:氨水脱硫法
该脱硫法采用喷雾吸收法,雾化的氨水与烟气中的SO 直接接触吸收SO ,其
2 2
反 应 的 化 学 方 程 式 为 2NH + SO + H O===(NH ) SO 2(NH ) SO +
3 2 2 4 2 3, 4 2 3
O ===2(NH ) SO 。(或生成NH HSO ,然后进一步氧化)
2 4 2 4 4 3
方法三:钠碱脱硫法
钠碱脱硫法是用NaOH/Na CO 吸收烟气中的SO ,得到Na SO 和NaHSO ,
2 3 2 2 3 3
发 生 反 应 的 化 学 方 程 式 为 2NaOH + SO ===Na SO + H O , Na CO +
2 2 3 2 2 3
SO ===Na SO +CO ,Na SO +SO +H O===2NaHSO 。
2 2 3 2 2 3 2 2 3
方法四:双碱脱硫法
先利用烧碱吸收SO ,再利用熟石灰浆液进行再生,再生后的 NaOH碱液可
2
循环使用,化学方程式为
①吸收反应:2NaOH+SO ===Na SO +H O,2Na SO +O ===2Na SO 。
2 2 3 2 2 3 2 2 4
②再生反应:Na SO +Ca(OH) ===CaSO ↓+2NaOH,Na SO +
2 3 2 3 2 4
Ca(OH) ===CaSO ↓+2NaOH。
2 4
1.正误判断,正确的打“√”,错误的打“×”。
(1)(2020·山东卷)用浓H SO 干燥SO ( )
2 4 2
(2)(2020·天津卷)用澄清石灰水检验SO 气体( )
2
(3)(2020·浙江7月选考)FeS 在沸腾炉中与O 反应主要生成SO ( )
2 2 3
(4)(2020·江苏卷)室温下,Fe与浓H SO 反应生成FeSO ( )
2 4 4
(5)(2019·浙江4月选考,11B)在表面皿中加入少量胆矾,再加入3 mL浓硫酸
搅拌,固体由蓝色变白色( )(6)(2019·浙江4月选考)向二氧化硫水溶液中滴加氯化钡溶液,再滴加双氧
水,产生白色沉淀( )
(7)(2019·浙江4月选考)硫元素在自然界的存在形式有硫单质、硫化物和硫
酸盐等( )
(8)(2018·浙江11月选考)接触法制硫酸的硫元素主要来源于硫黄或含硫矿石
( )
(9)(2019·江苏)稀硫酸具有酸性,可用于除去铁锈( )
(10)(2019·江苏)SO 与过量氨水反应生成(NH ) SO ( )
2 4 2 3
答案 (1)√ (2)× (3)× (4)× (5)√ (6)√ (7)√ (8)√ (9)√
(10)√
2.(2020·北京卷)硫酸盐(含SO、HSO)气溶胶是PM 的成分之一。近期科研人
2.5
员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如图:
下列说法不正确的是( )
A.该过程有H O参与
2
B.NO 是生成硫酸盐的氧化剂
2
C.硫酸盐气溶胶呈酸性
D.该过程没有生成硫氧键
答案 D
解析 A.根据图示中各微粒的构造可知,该过程有H O参与,正确;B.根据
2
图示的转化过程,NO 转化为HNO ,N元素的化合价由+4价变为+3价,化合价
2 2
降低,得电子被还原,做氧化剂,则NO 是生成硫酸盐的氧化剂,正确;C.硫酸盐
2
(含SO、HSO)气溶胶中含有HSO,转化过程有水参与,则HSO在水中可电离生成
H+和SO,则硫酸盐气溶胶呈酸性,正确;D.根据图示转化过程中,由SO转化为
HSO,根据图示对照,有硫氧键生成,错误;答案选D。
3.(2020·浙江 1 月选考,24)100%硫酸吸收 SO 可生成焦硫酸(分子式为
3
H S O 或H SO ·SO )。下列说法不正确的是( )
2 2 7 2 4 3
A.焦硫酸具有强氧化性B.Na S O 水溶液呈中性
2 2 7
C.Na S O 可与碱性氧化物反应生成新盐
2 2 7
D.100%硫酸吸收SO 生成焦硫酸的变化是化学变化
3
答案 B
解析 焦硫酸是由等物质的量的 SO 和纯 H SO 化合而成的:H SO +
3 2 4 2 4
SO ===H S O ,焦硫酸分子中硫元素的化合价是+6价,为最高价,具有强氧化性,
3 2 2 7
有强烈的吸湿性,遇水分解生成硫酸,故A项和D项正确;Na S O 溶于水,水溶
2 2 7
液呈酸性,故B项错误;Na S O 可与碱性氧化物反应生成硫酸盐,故C项正确。
2 2 7
答案选B。
4.(2017·北京理综)根据SO 通入不同溶液中实验现象,所得结论不正确的是
2
( )
实验 现象 结论
A 含HCl、BaCl 的FeCl 溶液 产生白色沉淀 SO 有还原性
2 3 2
B H S溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
D Na SiO 溶液 产生胶状沉淀 酸性:H SO >H SiO
2 3 2 3 2 3
答案 C
解析 A.溶液中SO 被FeCl 氧化生成SO,再与BaCl 反应产生白色沉淀,
2 3 2
体现了SO 的还原性;B.SO 与H S溶液发生反应SO +2H S===3S↓+2H O,体
2 2 2 2 2 2
现了SO 的氧化性;C.SO 使酸性KMnO 溶液褪色,体现了SO 的还原性;D.SO
2 2 4 2 2
与Na SiO 溶液反应产生胶状沉淀,根据强酸制弱酸,可得结论,酸性:H SO >
2 3 2 3
H SiO 。
2 3
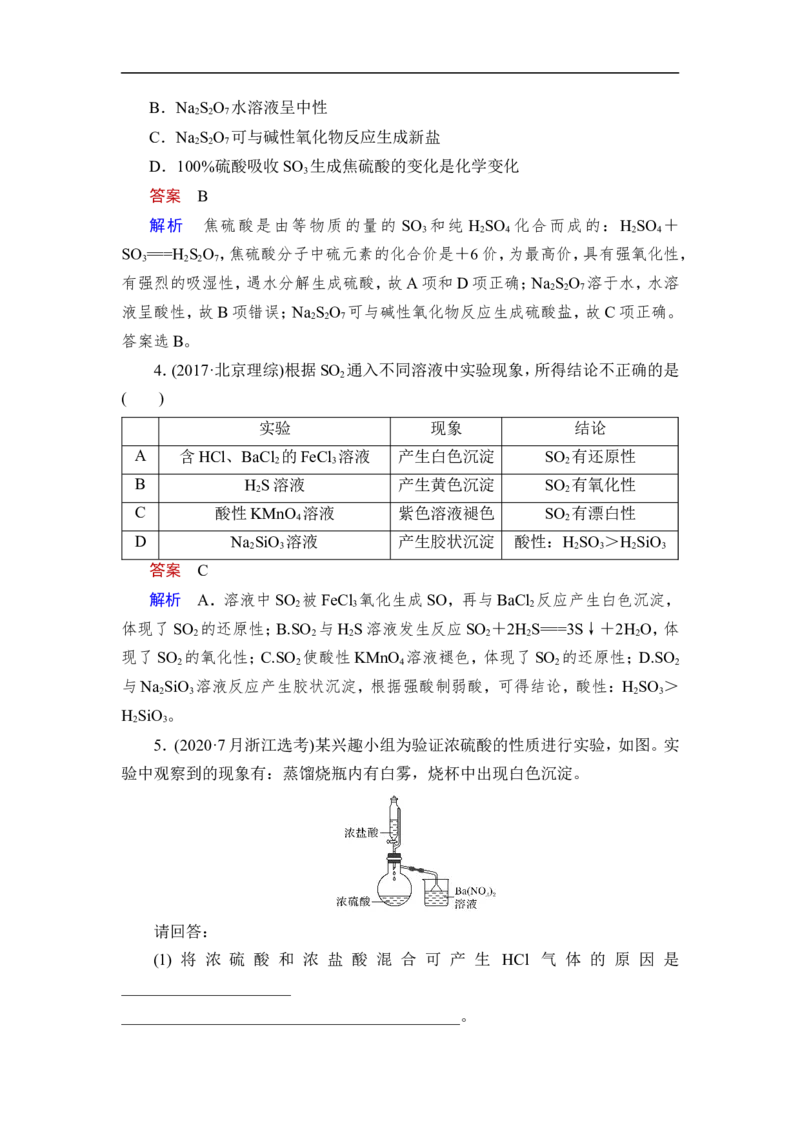
5.(2020·7月浙江选考)某兴趣小组为验证浓硫酸的性质进行实验,如图。实
验中观察到的现象有:蒸馏烧瓶内有白雾,烧杯中出现白色沉淀。
请回答:
(1) 将 浓 硫 酸 和 浓 盐 酸 混 合 可 产 生 HCl 气 体 的 原 因 是
_____________________
__________________________________________。(2)烧杯中出现白色沉淀的原因是___________________________________
___________________________________________________________________。
答案 (1)浓硫酸吸水放热导致HCl挥发
(2)HCl气体会将H SO 带出,与Ba(NO ) 作用生成BaSO
2 4 3 2 4
解析 (1)将浓硫酸和浓盐酸混合,浓硫酸溶解时吸水并放出热量,导致HCl
挥发。(2)烧杯中出现的白色沉淀显然为BaSO 沉淀,说明HCl气体挥发逸出时将
4
H SO 带出,与Ba(NO ) 发生复分解反应生成BaSO 。
2 4 3 2 4
6.(2020·北京卷)探究Na SO 固体的热分解产物。
2 3
资料:①4Na SO =====Na S+3Na SO 。
2 3 2 2 4
②Na S能与S反应生成Na S ,Na S 与酸反应生成S和H S。③BaS易溶于
2 2 x 2 x 2
水。
隔绝空气条件下,加热无水Na SO 固体得到黄色固体A,过程中未检测到气
2 3
体生成。黄色固体A加水得到浊液,放置得无色溶液B。
(1)检验分解产物Na S
2
取少量溶液B,向其中滴加CuSO 溶液,产生黑色沉淀,证实有S2-.反应的离
4
子方程式是_______________________________________________________。
(2)检验分解产物Na SO
2 4
取少量溶液B,滴加BaCl 溶液,产生白色沉淀,加入盐酸,沉淀增多(经检验
2
该沉淀含S),同时产生有臭鸡蛋气味的气体(H S),由于沉淀增多对检验造成干扰,
2
另取少量溶液B,加入足量盐酸,离心沉降(固液分离)后,________(填操作和现
象),可证实分解产物中含有SO。
(3)探究(2)中S的来源
来源1:固体A中有未分解的Na SO ,在酸性条件下与Na S反应生成S。
2 3 2
来源2:溶液B中有Na S ,加酸反应生成S。
2 x
针对来源1进行如下实验:
①实验可证实来源1不成立。实验证据是_____________________________
___________________________________________________________________。
②不能用盐酸代替硫酸的原因是___________________________________
___________________________________________________________________。③写出来源2产生S的反应的离子方程式:____________________________
___________________________________________________________________。
(4)实验证明Na SO 固体热分解有Na S、Na SO 和S产生。运用氧化还原反
2 3 2 2 4
应规律分析产物中S产生的合理性:
_______________________________________________________________。
答案 (1)S2-+Cu2+===CuS↓
(2)滴加BaCl 溶液,产生白色沉淀
2
(3)①向溶液2中加入KMnO 溶液,溶液没有褪色
4
②盐酸中Cl元素为-1价,是Cl元素的最低价,具有还原性,会与KMnO 溶
4
液发生氧化还原反应,使KMnO 溶液应该褪色,干扰实验现象和实验结论
4
③S+2H+===H S↑+(x-1)S↓
2
(4)根据反应4Na SO =====Na S+3Na SO 可知,Na SO 发生歧化反应,其中
2 3 2 2 4 2 3
的S元素化合价即可升高也可降低,能从+4价降为-2价,也应该可以降到0价
生成硫单质。
解答 (1)Na S和CuSO 溶液反应生成硫化铜和硫酸钠,反应的离子方程式
2 4
是S2-+Cu2+===CuS↓;(2)根据题干资料:Na S能与S反应生成Na S ,Na S 与
2 2 x 2 x
酸反应生成S和H S,取少量溶液B,滴加BaCl 溶液,产生白色沉淀,加入盐酸,
2 2
沉淀增多(经检验该沉淀含S),同时产生有臭鸡蛋气味的气体(H S),说明B溶液
2
中含有Na S ,Na S 与酸反应生成S和H S,由于沉淀增多对检验造成干扰,另取
2 x 2 x 2
少量溶液B,加入足量盐酸,离心沉降(固液分离)后,滴加BaCl 溶液,产生白色沉
2
淀,可证实分解产物中含有SO;(3)①实验可证实来源1不成立。根据分析,溶液
2为H SO ,向溶液2中加入少量KMnO 溶液,H SO 具有还原性,酸性条件下
2 3 4 2 3
KMnO 具有强氧化性,二者混合后应发生氧化还原反应,KMnO 溶液应该褪色,
4 4
但得到的仍为紫色,说明溶液B中不含Na SO ;②不能用盐酸代替硫酸的原因是
2 3
盐酸中Cl元素为-1价,是Cl元素的最低价,具有还原性,会与KMnO 溶液发生
4
氧化还原反应,使KMnO 溶液应该褪色,干扰实验现象和实验结论;③来源2认
4
为溶液B中有Na S ,加酸反应生成S,反应的离子方程式:S+2H+===H S↑+(x
2 x 2
-1)S↓;(4)根据已知资料:4Na SO =====Na S+3Na SO ,亚硫酸钠中硫为+4价,
2 3 2 2 4
硫酸钠中硫为+6价,硫化钠中硫为-2价,根据反应可知Na SO 发生歧化反应,
2 3
其中的S元素化合价即可升高也可降低,能从+4价降为-2价,也应该可以降到
0价生成硫单质。一、选择题(每小题只有一个选项符合题意)
1.下列能使品红溶液褪色,且褪色原理基本相同的是( )
①活性炭 ②氯水 ③二氧化硫 ④臭氧 ⑤过氧化钠
⑥双氧水
A.①②④ B.②③⑤
C.②④⑤⑥ D.①②③④⑤⑥
答案 C
2.化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是(
)
A.检验溶液是否含有SO时,在无其他阳离子干扰的条件下,先用盐酸酸化,
所得溶液再加BaCl 溶液
2
B.为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化
C.检验溶液中是否含有Fe3+时,用硝酸酸化
D.定性检验SO,将BaCl 溶液用HNO 酸化
2 3
答案 A
解析 在无其他阳离子干扰的条件下,用盐酸酸化可以排除CO、SO等阴离
子的干扰,加BaCl 溶液若出现白色沉淀说明溶液中含SO,故A正确;高锰酸钾
2
溶液能将盐酸氧化,不能用盐酸将高锰酸钾溶液酸化,故B错误;硝酸有强氧化
性,若溶液中有Fe2+,就会被氧化得到Fe3+,故C错误;HNO 能将SO氧化为
3
SO,造成错误的检验结果.故D错误。
3.有关硫及其化合物的说法合理的是( )
A.可用酒精洗刷做过硫黄性质实验的试管
B.SO 具有很强的还原性,在化学反应中只能作还原剂
2
C.浓硫酸具有强氧化性,常温下与铜反应可制取SO
2
D.1 mol硫与其他物质完全反应,转移的电子数不一定是2 mol
答案 D
解析 硫微溶于酒精,应该用二硫化碳洗刷做过硫黄性质实验的试管,故A
错误;SO 中S元素为+4价,处于中间价态,在化学反应中能作还原剂,也可以
2
作氧化剂,例如SO 与H S反应生成单质S和H O,故B错误;浓硫酸在常温下与
2 2 2
铜不反应,故C错误;1 mol硫与其他物质完全反应,转移的电子数不一定是 2
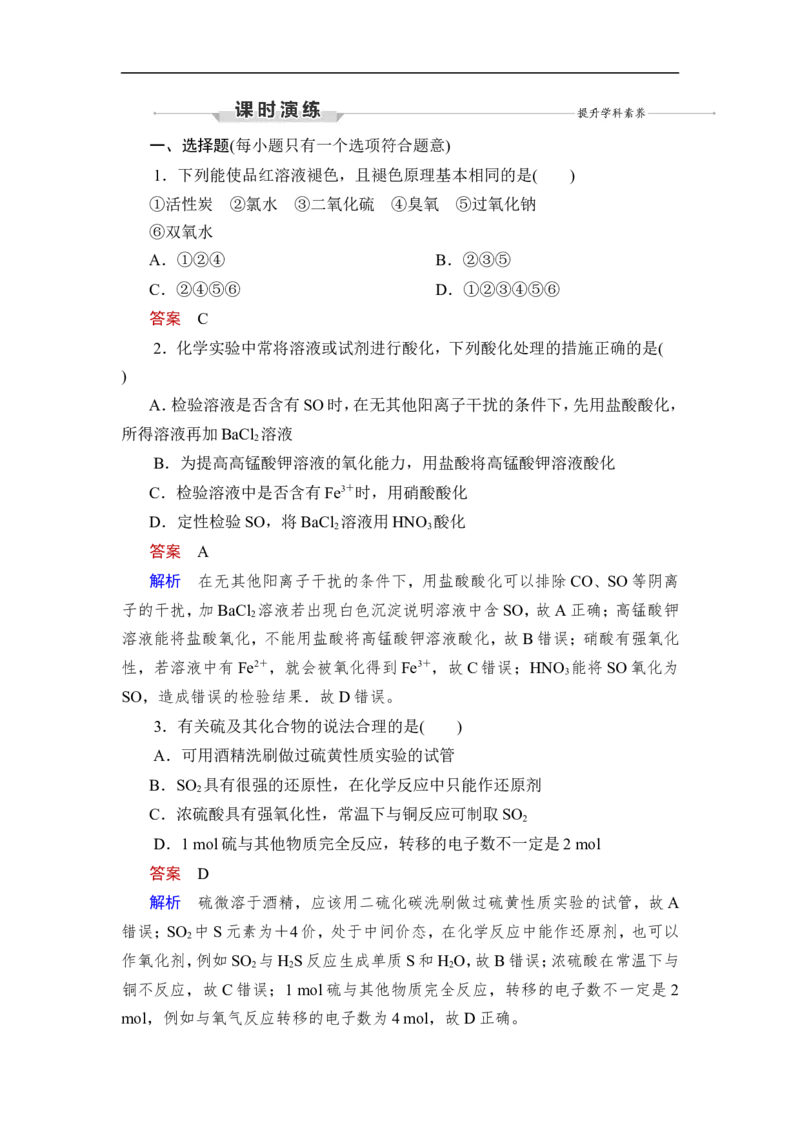
mol,例如与氧气反应转移的电子数为4 mol,故D正确。4.(2020·福建漳州市高三质检)下列四套装置用于实验室制取二氧化硫并回
收胆矾,其中不能达到实验目的的是( )
A.用A装置制取二氧化硫
B.用B装置吸收尾气中的二氧化硫
C.用C装置溶解反应后烧瓶内混合物中的硫酸铜固体
D.用D装置加热硫酸铜溶液制备胆矾
答案 D
解析 浓硫酸和铜在加热条件下可以生成SO ,A项可以达到实验目的;利用
2
NaOH溶液吸收SO 防止污染空气且该装置又可防止倒吸,B项可以达到实验目
2
的;由于反应后还有浓硫酸剩余,所以用水溶解硫酸铜固体时须把烧瓶中的物质
加到水中防止暴沸,相当于浓硫酸的稀释,C项可以达到实验目的;胆矾为含有
结晶水的硫酸铜,从硫酸铜溶液得到胆矾须用蒸发浓缩再冷却结晶,不可直接加
热蒸发,D项不能达到实验目的。
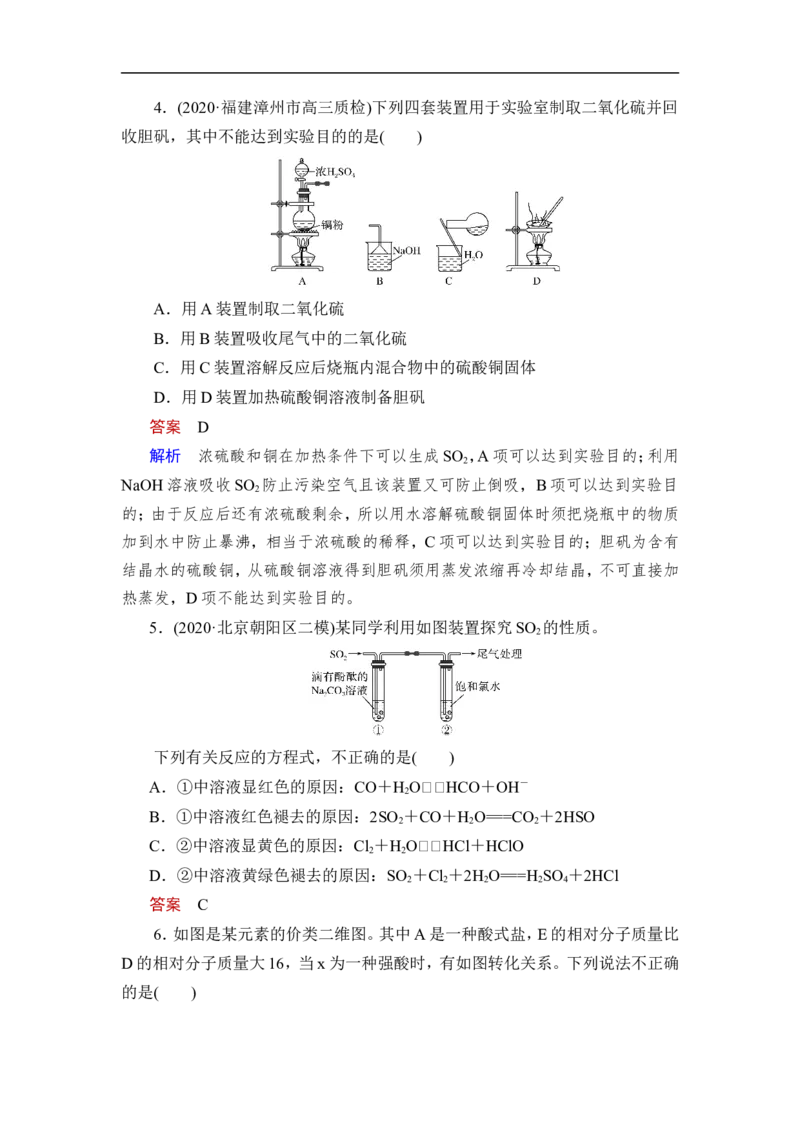
5.(2020·北京朝阳区二模)某同学利用如图装置探究SO 的性质。
2
下列有关反应的方程式,不正确的是( )
A.①中溶液显红色的原因:CO+H OHCO+OH-
2
B.①中溶液红色褪去的原因:2SO +CO+H O===CO +2HSO
2 2 2
C.②中溶液显黄色的原因:Cl +H OHCl+HClO
2 2
D.②中溶液黄绿色褪去的原因:SO +Cl +2H O===H SO +2HCl
2 2 2 2 4
答案 C
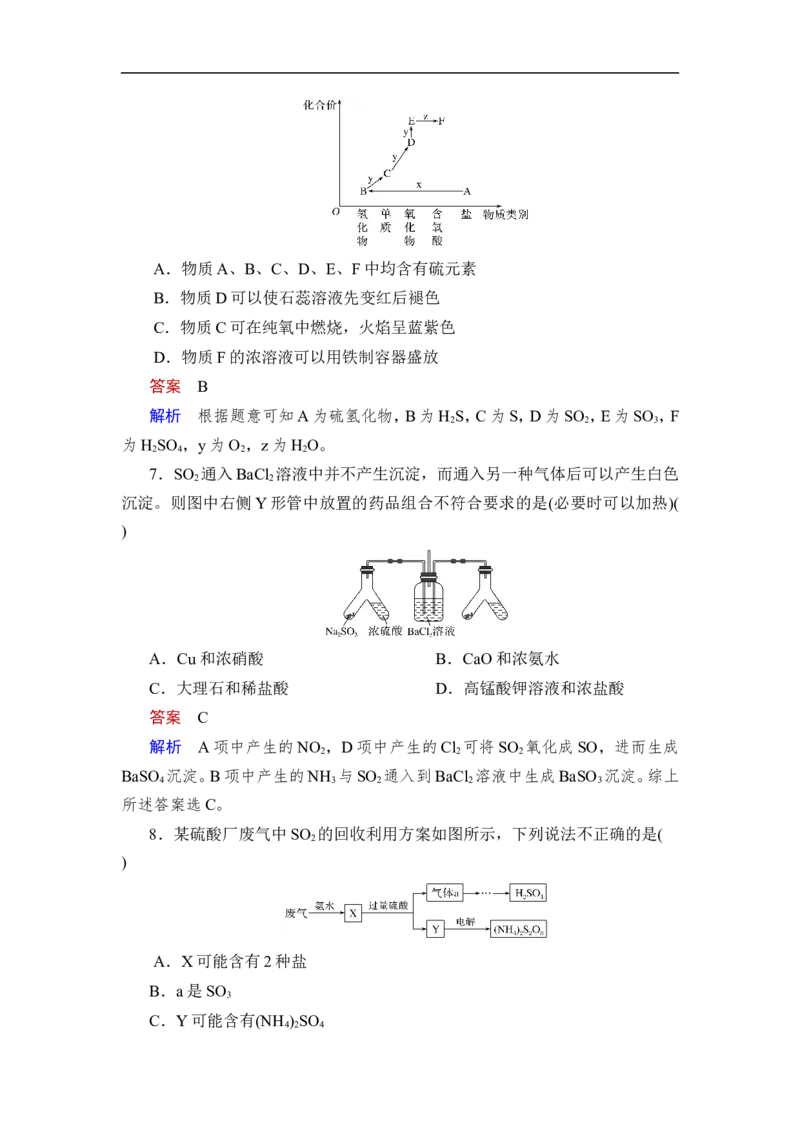
6.如图是某元素的价类二维图。其中A是一种酸式盐,E的相对分子质量比
D的相对分子质量大16,当x为一种强酸时,有如图转化关系。下列说法不正确
的是( )A.物质A、B、C、D、E、F中均含有硫元素
B.物质D可以使石蕊溶液先变红后褪色
C.物质C可在纯氧中燃烧,火焰呈蓝紫色
D.物质F的浓溶液可以用铁制容器盛放
答案 B
解析 根据题意可知A为硫氢化物,B为H S,C为S,D为SO ,E为SO ,F
2 2 3
为H SO ,y为O ,z为H O。
2 4 2 2
7.SO 通入BaCl 溶液中并不产生沉淀,而通入另一种气体后可以产生白色
2 2
沉淀。则图中右侧Y形管中放置的药品组合不符合要求的是(必要时可以加热)(
)
A.Cu和浓硝酸 B.CaO和浓氨水
C.大理石和稀盐酸 D.高锰酸钾溶液和浓盐酸
答案 C
解析 A项中产生的NO ,D项中产生的Cl 可将SO 氧化成SO,进而生成
2 2 2
BaSO 沉淀。B项中产生的NH 与SO 通入到BaCl 溶液中生成BaSO 沉淀。综上
4 3 2 2 3
所述答案选C。
8.某硫酸厂废气中SO 的回收利用方案如图所示,下列说法不正确的是(
2
)
A.X可能含有2种盐
B.a是SO
3
C.Y可能含有(NH ) SO
4 2 4D.(NH ) S O 中S的化合价不可能为+7价
4 2 2 8
答案 B
解析 二氧化硫与氨气反应可能生成亚硫酸铵和亚硫酸氢铵的混合物,所以
X可能含有2种盐,故A正确;亚硫酸铵或亚硫酸氢铵与硫酸反应产生的气体不
可能是三氧化硫,只能是二氧化硫,故B错误;亚硫酸铵或亚硫酸氢铵与硫酸反
应除生成二氧化硫外,还有硫酸铵或硫酸氢铵生成,所以Y可能含有硫酸铵,故
C正确;S元素的最外层只有6个电子,最高价为+6价,不可能显+7价,故D正
确。
9.探究浓硫酸和铜的反应,下列装置或操作正确的是( )
A.用装置甲进行铜和浓硫酸的反应
B.用装置乙收集二氧化硫并吸收尾气
C.用装置丙稀释反应后的混合液
D.用装置丁测定余酸的浓度
答案 C
解析 铜与浓硫酸需要在加热条件下才能反应,A错误;二氧化硫的密度比
空气的大,应使用向上排空气法收集,即气体应“长进短出”,B错误;反应后的
混合液中含有过量的浓硫酸,稀释时,应将其沿烧杯内壁慢慢倒入水中,且用玻
璃棒不断搅拌,C正确;应使用碱式滴定管(带胶管)盛装氢氧化钠溶液,D错误。
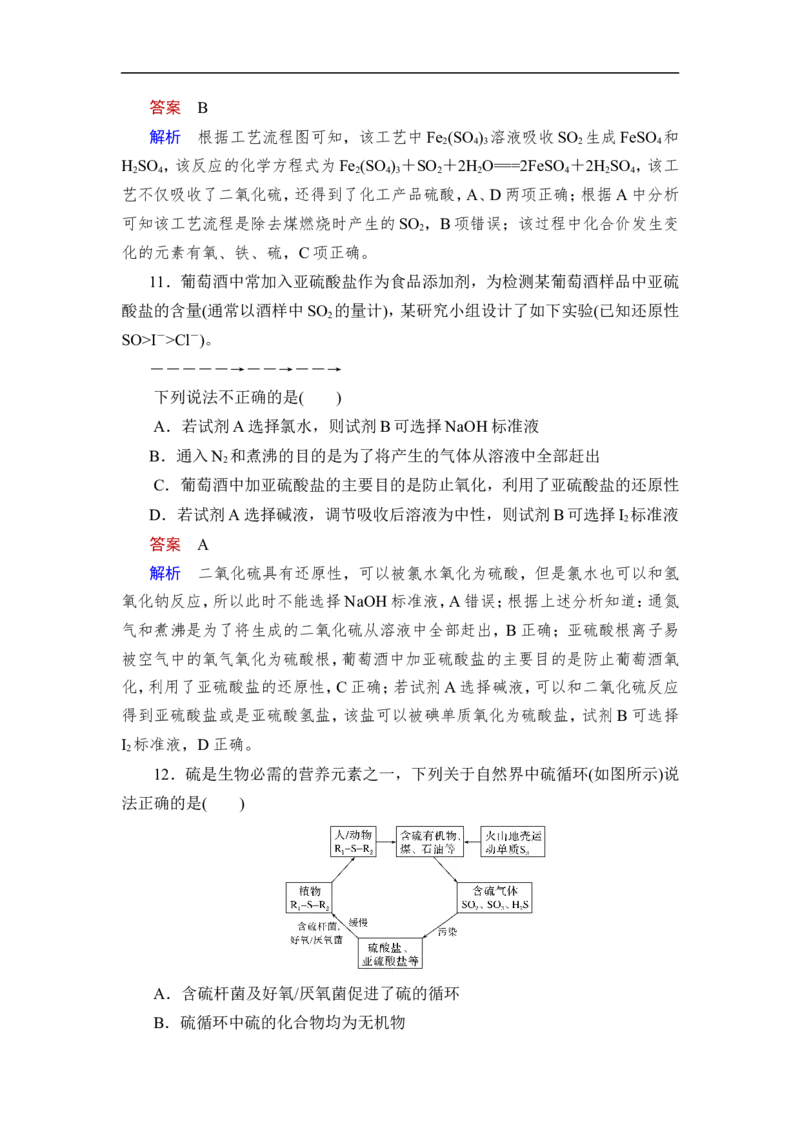
10.含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了新的治污
方法,同时可得到化工产品,该工艺流程如图所示,下列叙述不正确的是( )
A.该过程中可得到化工产品H SO
2 4
B.该工艺流程是除去煤燃烧时产生的SO
3
C.该过程中化合价发生改变的元素为O、Fe和S
D.图中涉及的反应之一为Fe (SO ) +SO +2H O===2FeSO +2H SO
2 4 3 2 2 4 2 4答案 B
解析 根据工艺流程图可知,该工艺中Fe (SO ) 溶液吸收SO 生成FeSO 和
2 4 3 2 4
H SO ,该反应的化学方程式为Fe (SO ) +SO +2H O===2FeSO +2H SO ,该工
2 4 2 4 3 2 2 4 2 4
艺不仅吸收了二氧化硫,还得到了化工产品硫酸,A、D两项正确;根据A中分析
可知该工艺流程是除去煤燃烧时产生的SO ,B项错误;该过程中化合价发生变
2
化的元素有氧、铁、硫,C项正确。
11.葡萄酒中常加入亚硫酸盐作为食品添加剂,为检测某葡萄酒样品中亚硫
酸盐的含量(通常以酒样中SO 的量计),某研究小组设计了如下实验(已知还原性
2
SO>I->Cl-)。
―――――→――→――→
下列说法不正确的是( )
A.若试剂A选择氯水,则试剂B可选择NaOH标准液
B.通入N 和煮沸的目的是为了将产生的气体从溶液中全部赶出
2
C.葡萄酒中加亚硫酸盐的主要目的是防止氧化,利用了亚硫酸盐的还原性
D.若试剂A选择碱液,调节吸收后溶液为中性,则试剂B可选择I 标准液
2
答案 A
解析 二氧化硫具有还原性,可以被氯水氧化为硫酸,但是氯水也可以和氢
氧化钠反应,所以此时不能选择NaOH标准液,A错误;根据上述分析知道:通氮
气和煮沸是为了将生成的二氧化硫从溶液中全部赶出,B正确;亚硫酸根离子易
被空气中的氧气氧化为硫酸根,葡萄酒中加亚硫酸盐的主要目的是防止葡萄酒氧
化,利用了亚硫酸盐的还原性,C正确;若试剂A选择碱液,可以和二氧化硫反应
得到亚硫酸盐或是亚硫酸氢盐,该盐可以被碘单质氧化为硫酸盐,试剂B可选择
I 标准液,D正确。
2
12.硫是生物必需的营养元素之一,下列关于自然界中硫循环(如图所示)说
法正确的是( )
A.含硫杆菌及好氧/厌氧菌促进了硫的循环
B.硫循环中硫的化合物均为无机物C.上述硫循环中硫元素均被氧化
D.燃煤时加石灰石,可减少酸雨及温室气体的排放
答案 A
解析 硫酸盐和亚硫酸盐等在硫杆菌及好氧/厌氧菌作用下缓慢转化成植物
R —S—R ,含硫杆菌及好氧/厌氧菌促进了硫的循环,故A正确;硫循环中硫的化
1 2
合物有含硫的有机物,不全是无机物,故B错误;含硫杆菌及好氧/厌氧菌将硫酸
盐、亚硫酸盐中硫还原成R —S—R ,硫循环中硫元素有时被氧化,有时被还原,
1 2
故C错误;燃煤时加石灰石,可减少酸雨,但生成二氧化碳,会增加温室气体的排
放,故D错误。
二、非选择题(本题包括3小题)
13.在下列物质转化中,A是一种正盐,D的相对分子质量比C的相对分子
质量大16,E是强酸,当X无论是强酸还是强碱时,都有如下的转化关系:
――→――→――→――→
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、
E均含另外同一种元素。请回答:
(1)A是________,Y是________,Z是________(填化学式,下同)。
(2)当 X 是强酸时,E 是________,写出 B 生成 C 的化学方程式:
__________________________________________________________________。
(3)当 X 是强碱时,E 是________,写出 B 生成 C 的化学方程式:
__________________________________________________________________。
答案 (1)(NH ) S O H O
4 2 2 2
(2)H SO 2H S+3O =====2SO +2H O
2 4 2 2 2 2
(3)HNO 4NH +5O =====4NO+6H O
3 3 2 2
解析 解推断题的两个关键点:一是找出突破口;二是要熟悉物质间的相互
转化关系。此题的突破口是D的相对分子质量比C的相对分子质量大16,可推测
多1个氧原子,则Y应为O 。连续氧化最终生成酸,则E可能为H SO 或HNO 。
2 2 4 3
(2)当X是强酸时,转化关系为
――→――→SO ――→SO ――→。
2 3
(3)当X为强碱时,转化关系为
――→――→――→――→。
14.(2020·湖北武汉部分学校高三质量检测)硫代硫酸钠(Na S O )是一种重要
2 2 3
的化工产品,将SO 通入Na CO 和Na S混合溶液中可制得Na S O 。其制备装置
2 2 3 2 2 2 3如图所示。
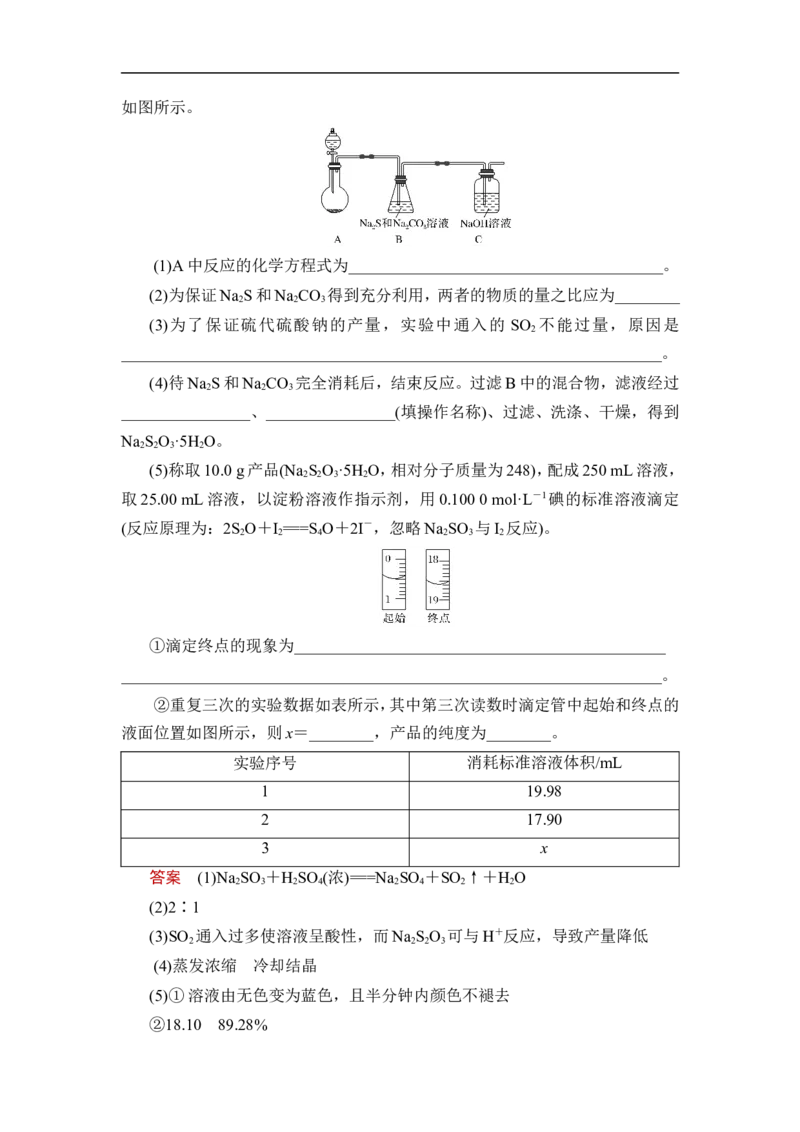
(1)A中反应的化学方程式为_______________________________________。
(2)为保证Na S和Na CO 得到充分利用,两者的物质的量之比应为________
2 2 3
(3)为了保证硫代硫酸钠的产量,实验中通入的 SO 不能过量,原因是
2
___________________________________________________________________。
(4)待Na S和Na CO 完全消耗后,结束反应。过滤B中的混合物,滤液经过
2 2 3
________________、________________(填操作名称)、过滤、洗涤、干燥,得到
Na S O ·5H O。
2 2 3 2
(5)称取10.0 g产品(Na S O ·5H O,相对分子质量为248),配成250 mL溶液,
2 2 3 2
取25.00 mL溶液,以淀粉溶液作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定
(反应原理为:2S O+I ===S O+2I-,忽略Na SO 与I 反应)。
2 2 4 2 3 2
①滴定终点的现象为______________________________________________
___________________________________________________________________。
②重复三次的实验数据如表所示,其中第三次读数时滴定管中起始和终点的
液面位置如图所示,则x=________,产品的纯度为________。
实验序号 消耗标准溶液体积/mL
1 19.98
2 17.90
3 x
答案 (1)Na SO +H SO (浓)===Na SO +SO ↑+H O
2 3 2 4 2 4 2 2
(2)2∶1
(3)SO 通入过多使溶液呈酸性,而Na S O 可与H+反应,导致产量降低
2 2 2 3
(4)蒸发浓缩 冷却结晶
(5)①溶液由无色变为蓝色,且半分钟内颜色不褪去
②18.10 89.28%解析 (1)A为二氧化硫的发生装置,实验室中常用Na SO 固体与浓H SO
2 3 2 4
反应制备 SO ,反应的化学方程式为 Na SO +H SO (浓)===Na SO +SO ↑+
2 2 3 2 4 2 4 2
H O。(2)装置B中发生的反应为2Na S+Na CO +4SO ===3Na S O +CO ,为保
2 2 2 3 2 2 2 3 2
证Na S和Na CO 得到充分利用,两者的物质的量之比应为2∶1。(3)硫代硫酸钠
2 2 3
在酸性条件下会发生歧化反应:S O+2H+===S↓+SO ↑+H O,二氧化硫过量
2 2 2
会使溶液呈酸性,导致产品产量减少,所以通入的二氧化硫不能过量。(4)过滤B
中的混合物,滤液经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到
Na S O ·5H O。(5)①滴定所用指示剂是淀粉溶液,当达到滴定终点时,碘稍过量,
2 2 3 2
淀粉遇碘变蓝色,所以溶液会由无色变为蓝色,且半分钟内颜色不褪去。②由图
可知滴定管的开始读数是0.50 mL,终点读数是18.60 mL,则所消耗溶液的体积
是18.10 mL,即x=18.10,实验1所测体积与另外两组数据相差较大,舍去,则消
耗标准液的平均体积为18.00 mL,根据碘与硫代硫酸钠反应的方程式可知硫代
硫酸钠的物质的量是0.018 0 L×0.100 0 mol·L-1×2×10=0.036 mol,所以产品
的纯度为×100%=89.28%。
15.(2020·江西名师联盟第一次模拟测试)煤燃烧排放的烟气中含有SO ,易
2
形成酸雨、污染大气。有效去除和利用SO 是环境保护的重要议题。
2
(1)双碱法洗除SO 。NaOH溶液Na SO 溶液
2 2 3
①上述过程生成Na SO 的离子方程式为
2 3
___________________________________________________________________。
②双碱法洗除SO 的优点为_______________________________________。
2
(2)NaClO 氧化法吸收SO 。向NaClO 溶液中通入含有SO 的烟气,反应温度
2 2 2 2
为323 K,反应一段时间。
①随着吸收反应的进行,吸收剂溶液的pH逐渐________(填“增大”“不
变”或“减小”)。
②如果采用NaClO替代NaClO ,也能得到较好的烟气脱硫效果。吸收等量的
2
SO ,所需NaClO的物质的量是NaClO 的________倍。
2 2
(3)SO 的利用。生产焦亚硫酸钠(Na S O ),通常是由NaHSO 过饱和溶液经结
2 2 2 5 3
晶脱水制得。利用烟道气中的SO 生产Na S O 的工艺如下:
2 2 2 5
①Ⅰ中反应的化学方程式为______________________________________。
②若Ⅲ中通入 SO 不足,结晶脱水得到的 Na S O 中混有的主要杂质是
2 2 2 5________(填化学式)。
③工艺中加入Na CO 固体,并再次充入SO 的目的是
2 3 2
_______________________________________________________________。
答案 (1)①2OH-+SO ===SO+H O
2 2
②用CaO可使NaOH再生
(2)①减小 ②2
(3)①Na CO +2SO +H O===2NaHSO +CO
2 3 2 2 3 2
②Na SO ③得到NaHSO 过饱和溶液
2 3 3
解析 (1)①SO 与NaOH反应,生成 Na SO 和H O,反应的离子方程式为
2 2 3 2
2OH-+SO ===SO+H O;②双碱法洗除SO 的优点为CaO可使NaOH再生;
2 2 2
(2)①随着吸收反应的进行,吸收剂溶液发生的反应为ClO+2SO +
2
2H O===Cl-+2SO+4H+,所以溶液的pH逐渐减小;②如果采用NaClO替代
2
NaClO ,反应的离子方程式为ClO-+SO +H O===Cl-+SO+2H+;根据ClO+
2 2 2
2SO +2H O===Cl-+2SO+4H+反应可知,吸收等量的SO ,所需NaClO的物质
2 2 2
的量是NaClO 的2倍;
2
(3)①Ⅰ中,pH=4.1,说明反应生成酸性物质,只能为NaHSO ,反应的化学方
3
程式为Na CO +2SO +H O===2NaHSO +CO ;②若Ⅲ中通入SO 不足,则溶液
2 3 2 2 3 2 2
为Na SO 和NaHSO 的混合物,结晶脱水得到的 Na S O 中混有的主要杂质是
2 3 3 2 2 5
Na SO ;③由题干信息“生产焦亚硫酸钠(Na S O ),通常是由NaHSO 过饱和溶
2 3 2 2 5 3
液经结晶脱水制得”知,工艺中加入Na CO 固体,并再次充入SO 的目的,是为
2 3 2
了最终获得NaHSO 过饱和溶液。
3
微专题 14 O 和 H O 的性质及应用
3 2 2
1.臭氧(O )
3
(1)组成:臭氧的分子式为O ,与O 互为同素异形体。
3 2
(2)化学性质
O 不稳定,容易分解,分解的化学方程式为2O ===3O ;在放电
3 3 2
不稳定性 条件下空气中的O 可以转化为O ,反应的化学方程式为
2 3
3O =====2O
2 3
O 容易使淀粉-KI溶液变蓝色,反应的化学方程式为2KI+O
3 3
强氧化性
+H O===I +2KOH+O
2 2 2
漂白性 O 具有强氧化性,能使有色物质褪色,可用作杀菌消毒剂
3(3)臭氧层可以吸收来自太阳的紫外线,是人类和其他生物的“保护伞”。
2.过氧化氢(H O )
2 2
(1)结构
电子式: ,结构式:H—O—O—H。
(2)化学性质
易分解,加热、加催化剂都能使分解速率加快:2H O =====2H O+
2 2 2
不稳定性
O ↑
2
弱酸性 相当于二元弱酸,H O H++HO,HOH++O
2 2
a.用10%的H O 溶液漂白羽毛及丝织品
2 2
b.氧化Fe2+、SO等还原性物质:H O +2Fe2++2H+===2Fe3++
2 2
强氧化性
2H O、H O +Na SO ===Na SO +H O
2 2 2 2 3 2 4 2
c.使湿润的淀粉-KI试纸变蓝:H O +2I-+2H+===I +2H O
2 2 2 2
遇强氧化剂时作还原剂:2KMnO +5H O +3H SO ===K SO +
4 2 2 2 4 2 4
弱还原性
2MnSO +5O ↑+8H O
4 2 2
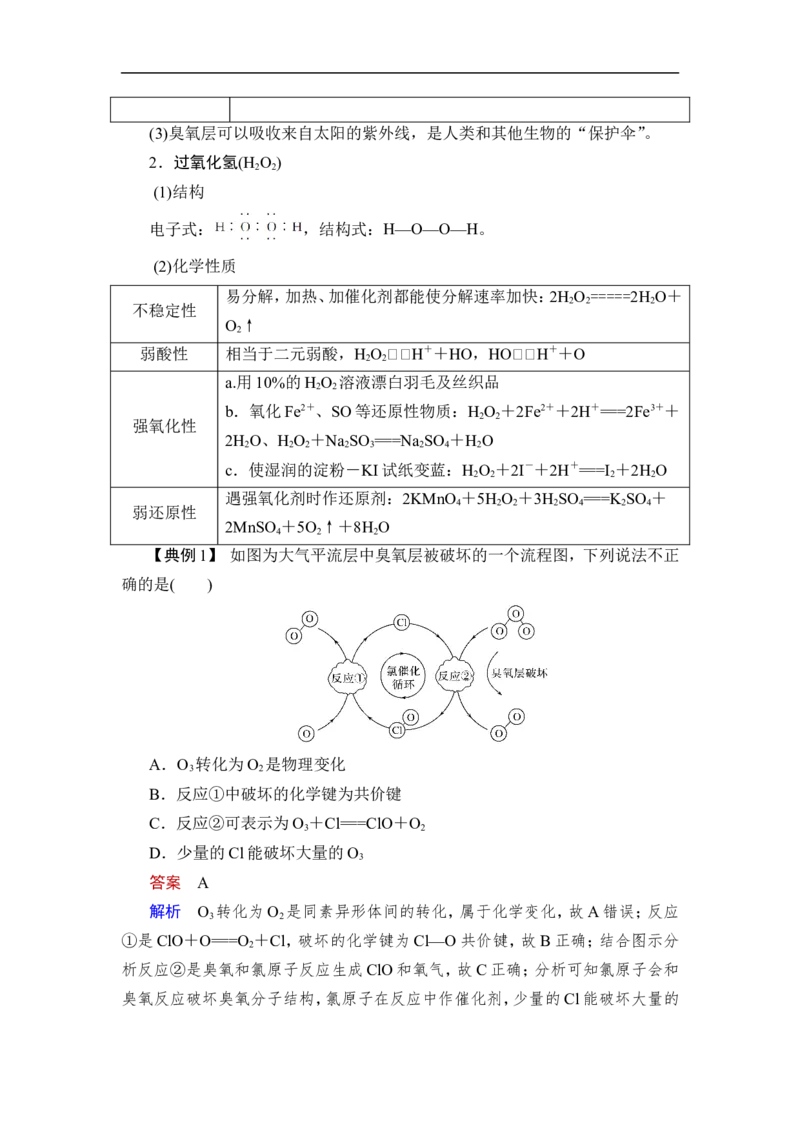
【典例1】 如图为大气平流层中臭氧层被破坏的一个流程图,下列说法不正
确的是( )
A.O 转化为O 是物理变化
3 2
B.反应①中破坏的化学键为共价键
C.反应②可表示为O +Cl===ClO+O
3 2
D.少量的Cl能破坏大量的O
3
答案 A
解析 O 转化为O 是同素异形体间的转化,属于化学变化,故A错误;反应
3 2
①是ClO+O===O +Cl,破坏的化学键为Cl—O共价键,故B正确;结合图示分
2
析反应②是臭氧和氯原子反应生成ClO和氧气,故C正确;分析可知氯原子会和
臭氧反应破坏臭氧分子结构,氯原子在反应中作催化剂,少量的Cl能破坏大量的O ,故D正确。
3
【典例2】 向CuSO 溶液中加入H O 溶液,很快有大量气体逸出,同时放热,
4 2 2
一段时间后,蓝色溶液变为红色浑浊(Cu O),继续加入H O 溶液,红色浑浊又变
2 2 2
为蓝色溶液,这个反应可以反复多次。下列关于上述过程的说法不正确的是(
)
A.Cu2+是H O 分解反应的催化剂
2 2
B.H O 只表现了氧化性
2 2
C.H O 的电子式为:
2 2
D.发生了反应Cu O+H O +4H+===2Cu2++3H O
2 2 2 2
答案 B
解析 根据“蓝色溶液变为红色浑浊(Cu O)”,说明铜离子被还原成+1价,
2
H O 表现了还原性;继续加入H O 溶液,红色浑浊又变为蓝色溶液,说明发生了
2 2 2 2
反应Cu O+H O +4H+===2Cu2++3H O,Cu O中+1价Cu被氧化成 Cu2+,
2 2 2 2 2
H O 又表现了氧化性,故B错误、D正确;H O 的电子式为 ,故C正
2 2 2 2
确。
1.下列有关双氧水的说法错误的是( )
A.H O 、Na O 属于过氧化物
2 2 2 2
B.双氧水是绿色氧化剂,可作医疗消毒剂
C.H O 在过氧化氢酶的催化下,温度越高,分解速率越快
2 2
D.H O 作漂白剂是利用其氧化性,漂白原理与HClO类似,与SO 不同
2 2 2
答案 C
解析 酶在过高的温度下会失去活性,故C项错误。
2.O 是重要的氧化剂和水处理剂,在平流层存在:2O 3O ,O O+O ,
3 3 2 3 2
粒子X能加速O 的分解:X+O ===XO+O ;XO+O===X+O (X=Cl、Br、NO
3 3 2 2
等)。已知:2O (g)3O (g) ΔH=-144.8 kJ·mol-1,t ℃时K=3×1076。下列说法
3 2
不正确的是( )
A.O 转变为O 的能量曲线可用下图表示
3 2B.O 转变为O 为氧化还原反应
3 2
C.臭氧层中氟利昂释放出的氯原子是O 分解的催化剂
3
D.t ℃时,3O (g)2O (g),K≈3.33×10-77
2 3
答案 B
解析 根据吸热反应的ΔH>0,放热反应的ΔH<0,图像中反应物的总能量
大于生成物的总能量,故该反应是放热反应,A正确;O 可以转化成O ,但元素化
3 2
合价未变,不是氧化还原反应,故B错误;X参与反应加快了O 的分解速率,X本
3
身的质量和化学性质在反应前后不变,属于催化剂,氟利昂在紫外线的照射下分
解释放出的氯原子在O 分解过程中作催化剂,故C正确;相同条件下,逆反应的
3
K值是正反应K值的倒数,故D正确。
3.H O 是重要的化学试剂,在实验室和实际生产中应用广泛。
2 2
(1)写出H O 的结构式:________,H O 在MnO 催化下分解的化学方程式:
2 2 2 2 2
_______________________________________________________________。
(2)①我们知道,稀硫酸不与铜反应,但在稀硫酸中加入H O 后,则可使铜顺
2 2
利溶解,写出该反应的离子方程式:
___________________________________________________________________。
②在“海带提碘”的实验中,利用酸性 H O 得到碘单质的离子方程式是
2 2
___________________________________________________________________。
③你认为H O 被称为绿色氧化剂的主要原因是________________________
2 2
___________________________________________________________________。
(3)H O 还有一定的还原性,能使酸性KMnO 溶液褪色。
2 2 4
①写出反应的离子方程式:_______________________________________。
②实验室常用酸性KMnO 标准液测定溶液中H O 的浓度,酸性KMnO 溶液
4 2 2 4
应盛放在________(填“酸式”或“碱式”)滴定管中,判断到达滴定终点的现象
是______________________________________________________________。
(4)H O 是一种二元弱酸,写出其第一步电离的方程式:
2 2
_______________________________________________________________;
它与过量的Ba(OH) 反应的化学方程式为
2___________________________________________________________________。
答案 (1)H—O—O—H 2H O =====2H O+O ↑
2 2 2 2
(2)①H O +Cu+2H+===Cu2++2H O ② H O +2I-+2H+===2H O+I
2 2 2 2 2 2 2
③还原产物为水,对环境无污染
(3)①5H O +2MnO+6H+===5O ↑+2Mn2++8H O
2 2 2 2
②酸式 滴入最后一滴酸性KMnO 溶液后变浅紫色;30 s内不褪色
4
(4)H O H++HO H O +Ba(OH) ===BaO +2H O
2 2 2 2 2 2 2
4.过氧化氢是一种绿色氧化剂、还原剂,工业上有多种方法制备H O 。
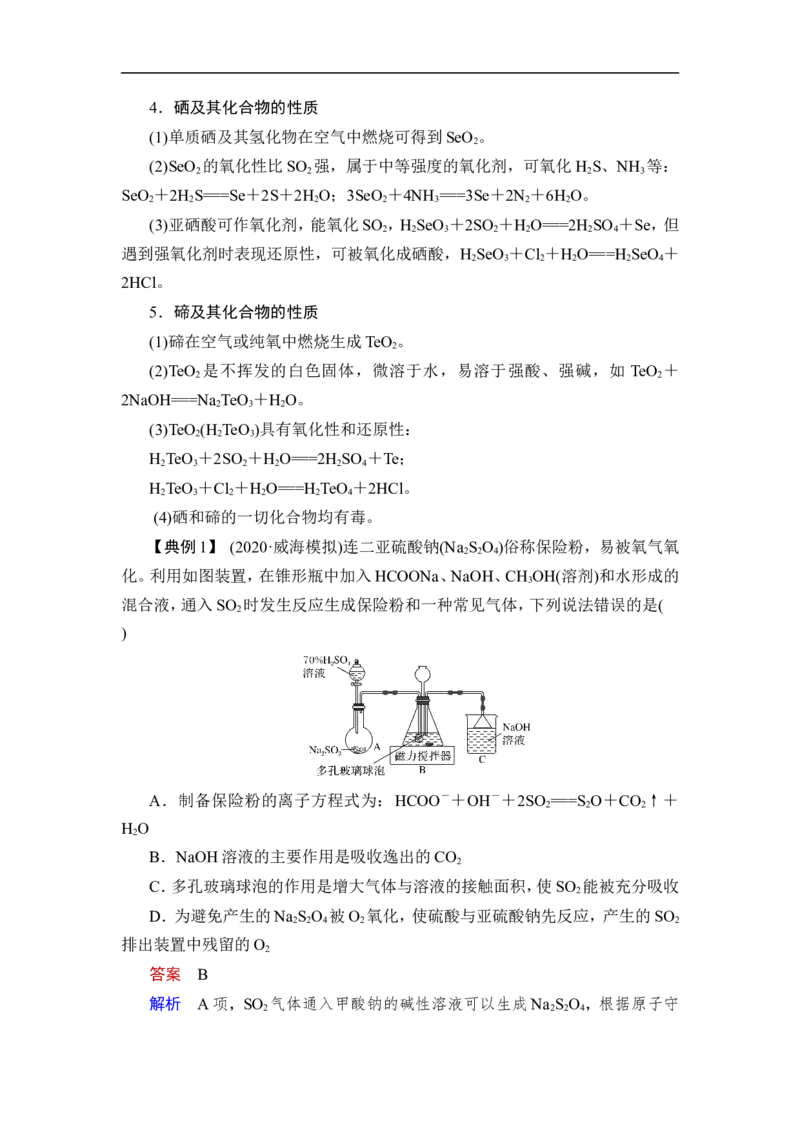
2 2
(1)①乙基蒽醌法是制备过氧化氢最常用的方法,其主要过程可以用上图表
示,写出此过程的总化学方程式:_______________________________________
___________________________________________________________________。
②空气阴极法制备H O 是一种环境友好型、节能型制备方法,电解总方程式
2 2
为3H O+3O =====3H O +O ,则阳极上电极反应式为
2 2 2 2 3
___________________________________________________________________。
(2)氧也能与钾元素形成K O、K O 、KO 、KO 等氧化物,其中KO 是一种比
2 2 2 2 3 2
Na O 效率高的供氧剂,写出它与CO 反应的化学方程式:
2 2 2
___________________________________________________________________。
(3)研究表明,H O 相当于二元弱酸,在实验中,甲同学将H O 加入含酚酞的
2 2 2 2
NaOH溶液中,发现溶液红色褪去,甲的结论为:H O 和NaOH中和,从而使溶液
2 2
褪色,而乙同学不赞同甲同学的观点,他认为是H O 的漂白性,将酚酞氧化而褪
2 2
色 , 请 设 计 实 验 证 明 , 到 底 是 甲 同 学 还 是 乙 同 学 观 点 正 确 :
_____________________________________________________________________
___________________________________________________________________。
答案 (1)①H +O =====H O
2 2 2 2
②2H O-2e-===H O +2H+
2 2 2
(2)4KO +2CO ===2K CO +3O
2 2 2 3 2
(3)取甲同学实验后褪色后的溶液少许置于试管中,用滴管再加入 NaOH溶
液,若溶液又变红色,则甲同学观点正确,若溶液不变红色,则乙同学观点正确
解析 (1)①由图可以看出,反应过程中的有机物为催化剂,总化学方程式为H +O =====H O 。②水在阳极上发生氧化反应生成H O :2H O-2e-=== H O
2 2 2 2 2 2 2 2 2
+2H+。(2)因为KO 可以作供氧剂,故与二氧化碳反应生成碳酸钾和氧气,化学
2
方程式为4KO +2CO ===2K CO +3O 。(3)溶液褪色可能是H O 和NaOH发生
2 2 2 3 2 2 2
中和反应,溶液碱性减弱而褪色,也可能是因为H O 的强氧化性,将酚酞漂白而
2 2
褪色,要证明甲、乙两同学的观点只需证明酚酞有无被氧化即可。
微专题 15 信息题中的第Ⅵ A 族元素
1.硫代硫酸钠(Na S O )
2 2 3
(1)制备
①硫化碱法,即将Na S和Na CO 以物质的量之比为2∶1配成溶液,然后通
2 2 3
入SO ,发生的反应为2Na S+Na CO +4SO ===3Na S O +CO 。
2 2 2 3 2 2 2 3 2
②亚硫酸钠法,使沸腾的Na SO 溶液同硫粉反应,其反应的方程式为Na SO
2 3 2 3
+S=====Na S O 。
2 2 3
(2)性质
①中等强度还原剂,可被碘氧化成连四硫酸钠(Na S O ),该反应常用来定量
2 4 6
测定碘的含量,反应的离子方程式为I +2S O===2I-+S O。
2 2 4
②可被氯、溴等氧化为SO,如Na S O +4Cl +5H O=== Na SO +H SO +
2 2 3 2 2 2 4 2 4
8HCl。
③可与酸反应,离子方程式为2H++S O===S↓+SO ↑+H O。
2 2 2
2.焦亚硫酸钠(Na S O )
2 2 5
(1)制备:NaHSO 过饱和溶液结晶脱水而成,2NaHSO ===Na S O +H O。
3 3 2 2 5 2
(2)性质
①与酸反应放出二氧化硫,如Na S O +2HCl===2NaCl+2SO ↑+H O。
2 2 5 2 2
②强还原性,如Na S O +2I +3H O===2NaHSO +4HI。
2 2 5 2 2 4
3.过二硫酸钠(Na S O )、连二亚硫酸钠(Na S O )
2 2 8 2 2 4
(1)过二硫酸钠中S为+6价,含有1个过氧键(—O—O—),性质与过氧化氢
相似,具有氧化性。作为氧化剂参与反应时,过氧键断裂,过氧键中的氧原子由-
1价变为-2价,硫原子化合价不变。如S O+2I-=====2SO+I 5S O+2Mn2++
2 2, 2
8H O===10SO+2MnO+16H+。过二硫酸钠不稳定,受热分解生成Na SO 、SO
2 2 4 3
和O 。
2
(2)连二亚硫酸钠中S为+3价,是强还原剂,能将I 、Cu2+、Ag+还原,能被空
2
气中的氧气氧化。在无氧条件下,用锌粉还原亚硫酸氢钠可制得连二亚硫酸钠。4.硒及其化合物的性质
(1)单质硒及其氢化物在空气中燃烧可得到SeO 。
2
(2)SeO 的氧化性比SO 强,属于中等强度的氧化剂,可氧化 H S、NH 等:
2 2 2 3
SeO +2H S===Se+2S+2H O;3SeO +4NH ===3Se+2N +6H O。
2 2 2 2 3 2 2
(3)亚硒酸可作氧化剂,能氧化SO ,H SeO +2SO +H O===2H SO +Se,但
2 2 3 2 2 2 4
遇到强氧化剂时表现还原性,可被氧化成硒酸,H SeO +Cl +H O===H SeO +
2 3 2 2 2 4
2HCl。
5.碲及其化合物的性质
(1)碲在空气或纯氧中燃烧生成TeO 。
2
(2)TeO 是不挥发的白色固体,微溶于水,易溶于强酸、强碱,如 TeO +
2 2
2NaOH===Na TeO +H O。
2 3 2
(3)TeO (H TeO )具有氧化性和还原性:
2 2 3
H TeO +2SO +H O===2H SO +Te;
2 3 2 2 2 4
H TeO +Cl +H O===H TeO +2HCl。
2 3 2 2 2 4
(4)硒和碲的一切化合物均有毒。
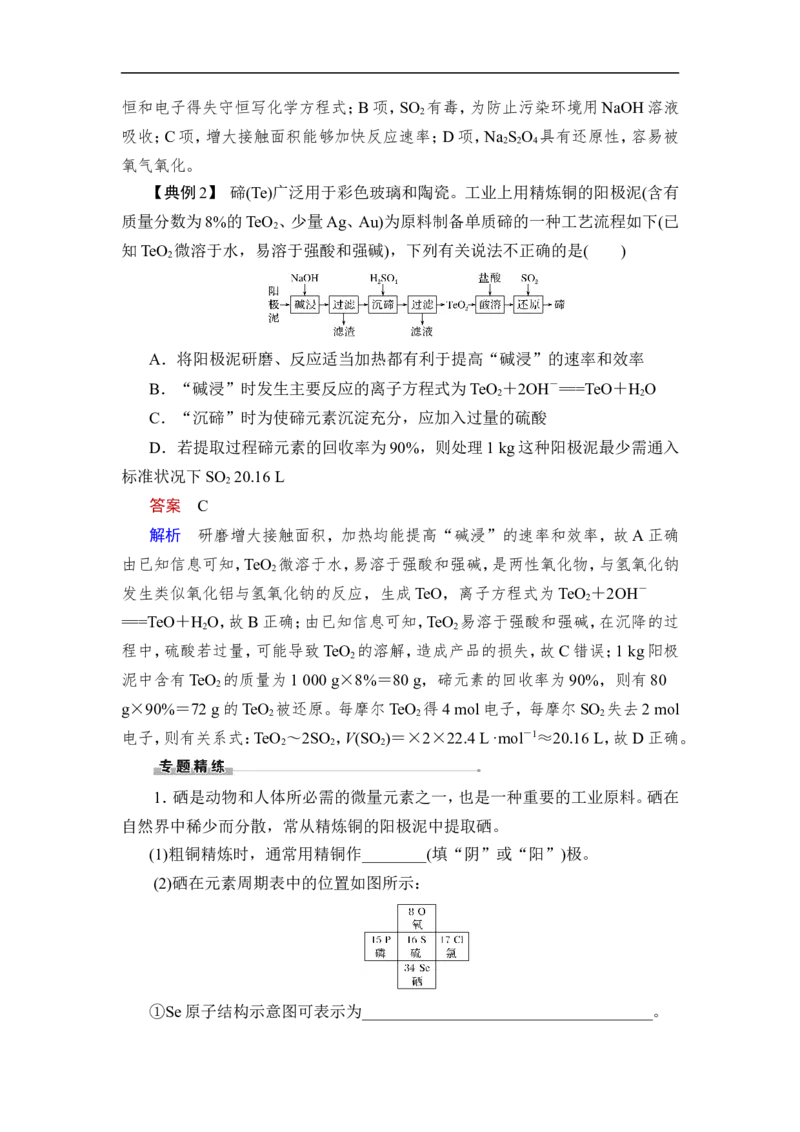
【典例1】 (2020·威海模拟)连二亚硫酸钠(Na S O )俗称保险粉,易被氧气氧
2 2 4
化。利用如图装置,在锥形瓶中加入HCOONa、NaOH、CH OH(溶剂)和水形成的
3
混合液,通入SO 时发生反应生成保险粉和一种常见气体,下列说法错误的是(
2
)
A.制备保险粉的离子方程式为:HCOO-+OH-+2SO ===S O+CO ↑+
2 2 2
H O
2
B.NaOH溶液的主要作用是吸收逸出的CO
2
C.多孔玻璃球泡的作用是增大气体与溶液的接触面积,使SO 能被充分吸收
2
D.为避免产生的Na S O 被O 氧化,使硫酸与亚硫酸钠先反应,产生的SO
2 2 4 2 2
排出装置中残留的O
2
答案 B
解析 A项,SO 气体通入甲酸钠的碱性溶液可以生成Na S O ,根据原子守
2 2 2 4恒和电子得失守恒写化学方程式;B项,SO 有毒,为防止污染环境用NaOH溶液
2
吸收;C项,增大接触面积能够加快反应速率;D项,Na S O 具有还原性,容易被
2 2 4
氧气氧化。
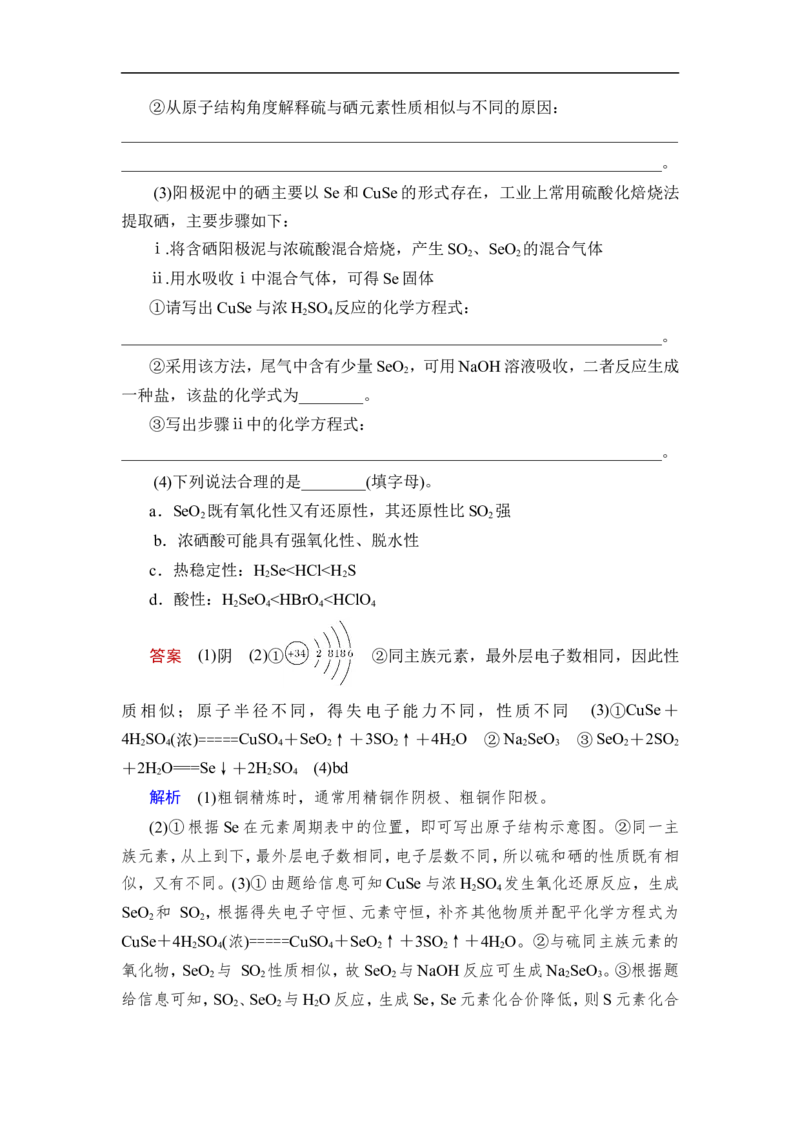
【典例2】 碲(Te)广泛用于彩色玻璃和陶瓷。工业上用精炼铜的阳极泥(含有
质量分数为8%的TeO 、少量Ag、Au)为原料制备单质碲的一种工艺流程如下(已
2
知TeO 微溶于水,易溶于强酸和强碱),下列有关说法不正确的是( )
2
A.将阳极泥研磨、反应适当加热都有利于提高“碱浸”的速率和效率
B.“碱浸”时发生主要反应的离子方程式为TeO +2OH-===TeO+H O
2 2
C.“沉碲”时为使碲元素沉淀充分,应加入过量的硫酸
D.若提取过程碲元素的回收率为90%,则处理1 kg这种阳极泥最少需通入
标准状况下SO 20.16 L
2
答案 C
解析 研磨增大接触面积,加热均能提高“碱浸”的速率和效率,故A正确
由已知信息可知,TeO 微溶于水,易溶于强酸和强碱,是两性氧化物,与氢氧化钠
2
发生类似氧化铝与氢氧化钠的反应,生成TeO,离子方程式为TeO +2OH-
2
===TeO+H O,故B正确;由已知信息可知,TeO 易溶于强酸和强碱,在沉降的过
2 2
程中,硫酸若过量,可能导致TeO 的溶解,造成产品的损失,故C错误;1 kg阳极
2
泥中含有TeO 的质量为1 000 g×8%=80 g,碲元素的回收率为90%,则有80
2
g×90%=72 g的TeO 被还原。每摩尔TeO 得4 mol电子,每摩尔SO 失去2 mol
2 2 2
电子,则有关系式:TeO ~2SO ,V(SO )=×2×22.4 L ·mol-1≈20.16 L,故D正确。
2 2 2
1.硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在
自然界中稀少而分散,常从精炼铜的阳极泥中提取硒。
(1)粗铜精炼时,通常用精铜作________(填“阴”或“阳”)极。
(2)硒在元素周期表中的位置如图所示:
①Se原子结构示意图可表示为____________________________________。②从原子结构角度解释硫与硒元素性质相似与不同的原因:
_____________________________________________________________________
___________________________________________________________________。
(3)阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法
提取硒,主要步骤如下:
ⅰ.将含硒阳极泥与浓硫酸混合焙烧,产生SO 、SeO 的混合气体
2 2
ⅱ.用水吸收ⅰ中混合气体,可得Se固体
①请写出CuSe与浓H SO 反应的化学方程式:
2 4
___________________________________________________________________。
②采用该方法,尾气中含有少量SeO ,可用NaOH溶液吸收,二者反应生成
2
一种盐,该盐的化学式为________。
③写出步骤ⅱ中的化学方程式:
___________________________________________________________________。
(4)下列说法合理的是________(填字母)。
a.SeO 既有氧化性又有还原性,其还原性比SO 强
2 2
b.浓硒酸可能具有强氧化性、脱水性
c.热稳定性:H Se