文档内容
1.下列关于钠的说法不正确的是( )
A.切开金属钠,切面会逐渐变暗
B.实验室的单质钠常常保存在石蜡油或煤油中
C.金属钠着火时用湿抹布盖灭
D.固体钠的密度比液体水的密度小
2.等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,则
下列说法正确的是( )
A.第一块钠失去电子多
B.两块钠失去电子一样多
C.第二块钠的反应产物质量大
D.两块钠的反应产物质量一样大
3.下列叙述正确的是( )
A.切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O===NaO
2 2 2
B.一定条件下,2.3 g Na完全与O 反应生成3.6 g产物,失去的电子数为0.2N
2 A
C.钠在空气中受热时,熔化为银白色的小球,产生黄色的火焰,生成白色粉末
D.钠在空气中长期放置,最终主要生成物为碳酸钠
4.观察是研究物质性质的一种基本方法。某同学将一小块金属钠露置于空气中,观察到下
列现象:银白色――→变灰暗――→变白色――→出现液滴――→白色固体,则下列说法正确的是(
)
A.①发生氧化还原反应生成了过氧化钠
B.④只发生物理变化
C.③是碳酸钠吸收空气中的水蒸气形成了溶液
D.②④是非氧化还原反应
5.某溶液含有①NO、②HCO、③SO、④CO、⑤SO五种阴离子。现向其中加入少量的
NaO 固体后,溶液中离子浓度增大的是(设溶液体积无变化)( )
2 2
A.① B.④ C.①④⑤ D.④⑤
6.过氧化钠具有强氧化性,遇木炭、铝粉等还原性物质时可燃烧。下列有关说法不正确的
是( )
A.NaO 与CO 反应时,NaO 是氧化剂,CO 是还原剂
2 2 2 2 2 2
B.熔融过氧化钠时不可使用石英坩埚
C.过氧化钠与木炭、铝粉反应时,过氧化钠均表现出强氧化性
D.过氧化钠与二氧化硫反应时可生成硫酸钠7.下列物质均为a g,将它们在氧气中完全燃烧的产物全部通入到足量的过氧化钠固体中,
则过氧化钠固体增重为 a g的是( )
①CO ②H ③CH ④HCHO ⑤CHCOOH ⑥HCOOH
2 4 3
A.①②⑤⑥ B.②③④⑤
C.①②④⑤ D.①②③⑤
8.将过氧化钠投入FeCl 溶液中,可观察到的实验现象是( )
2
A.有无色气体和白色沉淀生成
B.有无色气体和红褐色沉淀生成
C.无气体产生,有沉淀生成
D.有气体产生,无沉淀生成
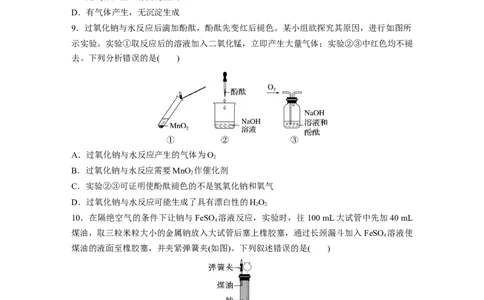
9.过氧化钠与水反应后滴加酚酞,酚酞先变红后褪色。某小组欲探究其原因,进行如图所
示实验。实验①取反应后的溶液加入二氧化锰,立即产生大量气体;实验②③中红色均不褪
去。下列分析错误的是( )
A.过氧化钠与水反应产生的气体为O
2
B.过氧化钠与水反应需要MnO 作催化剂
2
C.实验②③可证明使酚酞褪色的不是氢氧化钠和氧气
D.过氧化钠与水反应可能生成了具有漂白性的HO
2 2
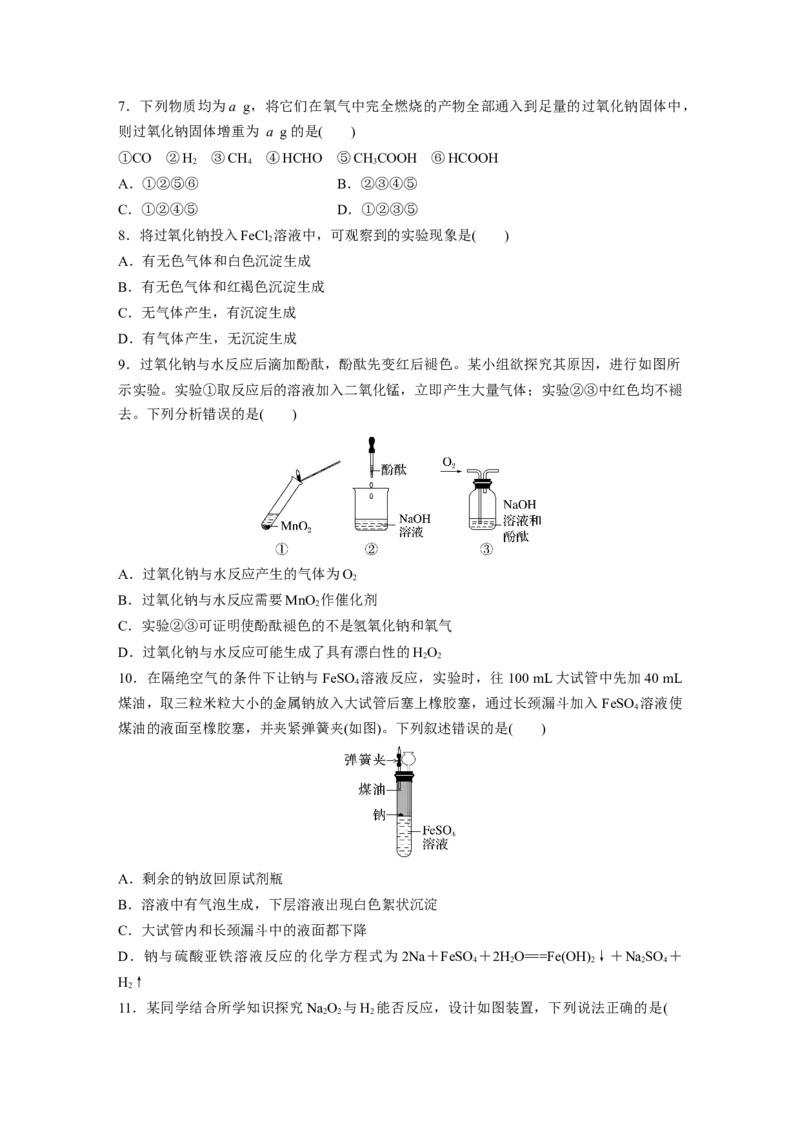
10.在隔绝空气的条件下让钠与FeSO 溶液反应,实验时,往100 mL大试管中先加40 mL
4
煤油,取三粒米粒大小的金属钠放入大试管后塞上橡胶塞,通过长颈漏斗加入 FeSO 溶液使
4
煤油的液面至橡胶塞,并夹紧弹簧夹(如图)。下列叙述错误的是( )
A.剩余的钠放回原试剂瓶
B.溶液中有气泡生成,下层溶液出现白色絮状沉淀
C.大试管内和长颈漏斗中的液面都下降
D.钠与硫酸亚铁溶液反应的化学方程式为2Na+FeSO +2HO===Fe(OH) ↓+NaSO +
4 2 2 2 4
H↑
2
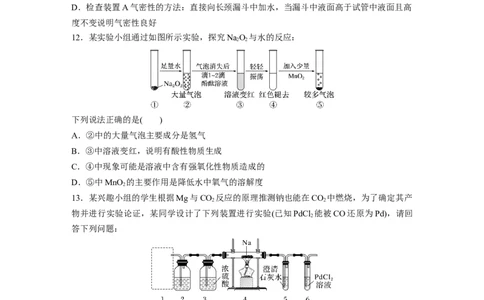
11.某同学结合所学知识探究NaO 与H 能否反应,设计如图装置,下列说法正确的是(
2 2 2)
A.装置A也可直接用于Cu与浓硫酸反应制取SO
2
B.装置B中盛放硅胶的作用只是除去A中挥发出来的少量水蒸气
C.装置C加热前,用试管在装置D管口末端处收集气体点燃,通过声音判断气体纯度
D.检查装置A气密性的方法:直接向长颈漏斗中加水,当漏斗中液面高于试管中液面且高
度不变说明气密性良好
12.某实验小组通过如图所示实验,探究NaO 与水的反应:
2 2
下列说法正确的是( )
A.②中的大量气泡主要成分是氢气
B.③中溶液变红,说明有酸性物质生成
C.④中现象可能是溶液中含有强氧化性物质造成的
D.⑤中MnO 的主要作用是降低水中氧气的溶解度
2
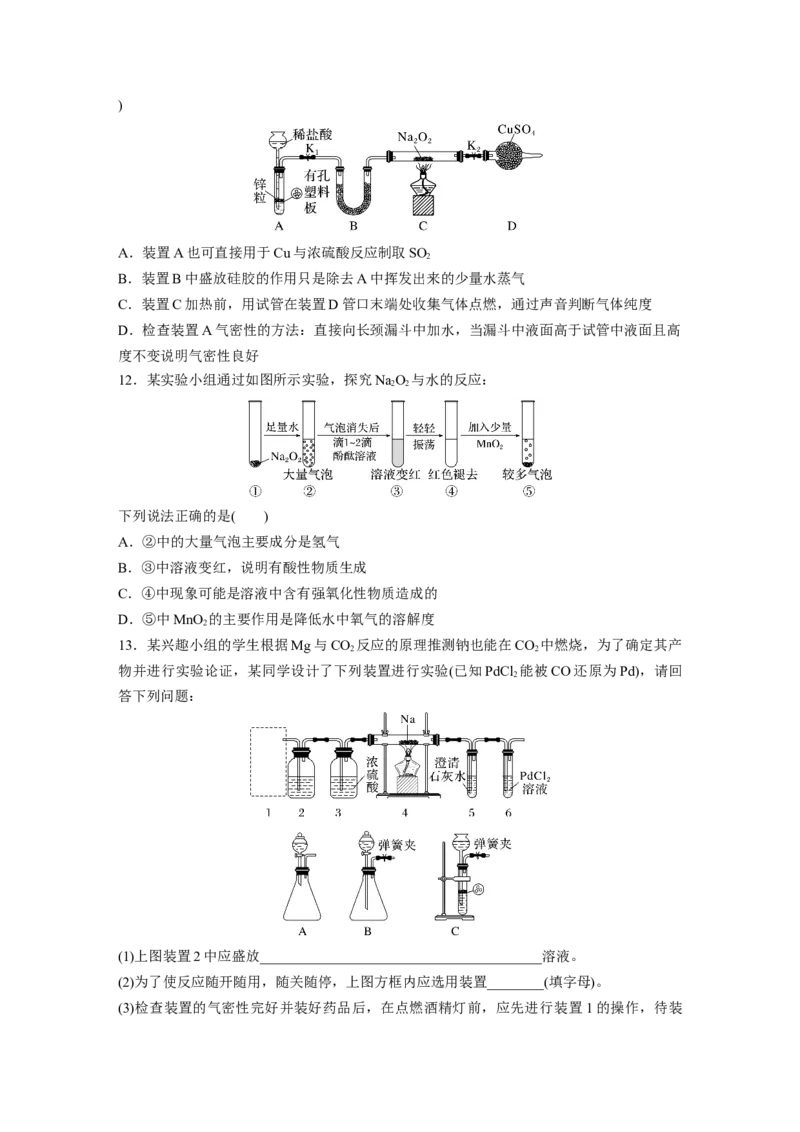
13.某兴趣小组的学生根据Mg与CO 反应的原理推测钠也能在CO 中燃烧,为了确定其产
2 2
物并进行实验论证,某同学设计了下列装置进行实验(已知PdCl 能被CO还原为Pd),请回
2
答下列问题:
(1)上图装置2中应盛放________________________________________溶液。
(2)为了使反应随开随用,随关随停,上图方框内应选用装置________(填字母)。
(3)检查装置的气密性完好并装好药品后,在点燃酒精灯前,应先进行装置1的操作,待装置______(填数字)中出现______________的现象时,再点燃酒精灯。
(4)①若装置6中有黑色沉淀(Pd)生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄
清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为_____________________。
②若装置6中无明显现象,装置4中残留固体(有两种物质)加盐酸后有能使澄清石灰水变浑
浊的气体放出,则钠与二氧化碳反应的化学方程式为_________________________________。
14.已知NaO 可用作漂白剂和呼吸面具中的供氧剂。
2 2
(1)写出NaO 作供氧剂时发生反应的化学方程式:___________________________________。
2 2
(2)Na O 具有强氧化性,H 具有还原性,有同学猜想NaO 与H 能反应。为了验证此猜想,
2 2 2 2 2 2
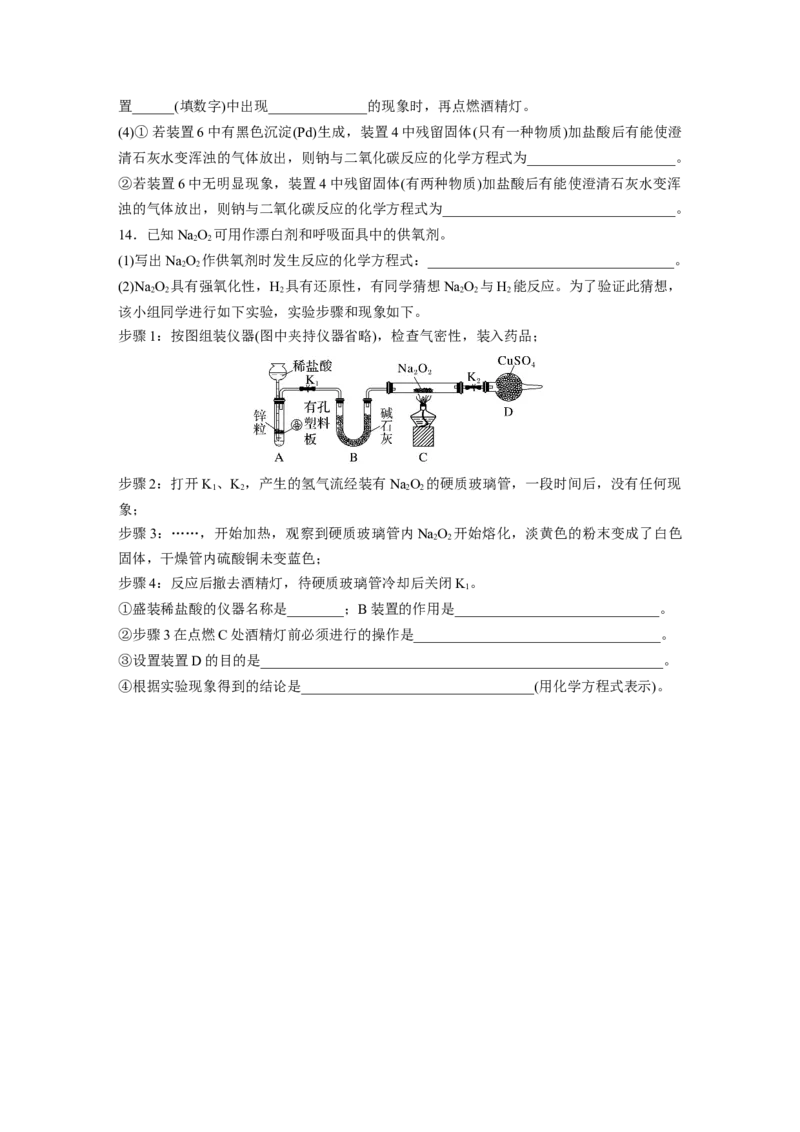
该小组同学进行如下实验,实验步骤和现象如下。
步骤1:按图组装仪器(图中夹持仪器省略),检查气密性,装入药品;
步骤2:打开K 、K ,产生的氢气流经装有NaO 的硬质玻璃管,一段时间后,没有任何现
1 2 2 2
象;
步骤3:……,开始加热,观察到硬质玻璃管内NaO 开始熔化,淡黄色的粉末变成了白色
2 2
固体,干燥管内硫酸铜未变蓝色;
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K。
1
①盛装稀盐酸的仪器名称是________;B装置的作用是_____________________________。
②步骤3在点燃C处酒精灯前必须进行的操作是___________________________________。
③设置装置D的目的是_________________________________________________________。
④根据实验现象得到的结论是_________________________________(用化学方程式表示)。