文档内容
第 12 讲 钠及其氧化物
[复习目标] 1.了解钠的单质和氧化物的性质及用途。2.掌握钠与氧气、水、酸、盐溶液反
应的特点。3.了解氧化钠与过氧化钠的区别,掌握NaO 与HO、CO 反应的规律。
2 2 2 2
考点一 钠的性质及用途
1.物理性质
______色,有金属光泽的固体,质地________,熔点低(____于100 ℃),密度比水的____,
但比煤油的____。
2.化学性质
(1)与非金属单质(如O、Cl)的反应
2 2
O
2
Cl:____________________________。
2
(2)与水、酸、盐等的反应
与水(滴有酚酞) 2Na+2HO===__________________(现象:浮、熔、游、响、红)
2
与酸
与熔融盐发
4Na+TiCl =====____________________
4
与盐 生置换反应
与盐溶液 2Na+2HO+CuSO ===_________________
2 4
2Na+2C HOH―→________________(Na沉在乙醇底部,比Na
2 5
与含羟基或
与水的反应速率____);
羧基的有机物
2CHCOOH+2Na―→_________________
3
3.钠的制取及保存
(1)制取:化学方程式为_________________________________________________。(2)保存:密封保存,通常保存在____________________中。
4.钠的用途
(1)钠钾合金(室温呈液态)可用于核反应堆的传热介质。
(2)用作电光源,制作高压钠灯。
(3)冶炼某些金属。
1.钠可以保存在四氯化碳溶液中( )
2.金属钠着火时,可用泡沫灭火器或干燥的沙土灭火( )
3.钠表面自然形成的氧化层能够保护内层金属不被空气氧化( )
4.金属钠具有强还原性,可与TiCl 溶液反应制取金属Ti( )
4
5.钠的金属性比钾强,工业上用钠制钾的原理为Na+KCl=====K↑+NaCl( )
6.实验结束后剩余的金属钠不能随意丢弃,应放回原试剂瓶中( )
一、钠的性质实验
1.(2022·长春模拟)下列关于钠的实验现象的叙述不正确的是( )
选项 实验操作 实验现象
切开一小块钠,观察切面颜色
A 钠切面颜色变暗,最后呈淡黄色
的变化
钠熔化成闪亮的小球,在液面上四处游
B 把一小块钠投入CuSO 溶液中
4
动,发出“嘶嘶”的响声,产生蓝色沉淀
钠熔化成闪亮的小球,在液面上四处游
把一小块钠投入滴有紫色石蕊
C 动,发出“嘶嘶”的响声,反应后溶液变
溶液的冷水中
蓝
把一小块钠迅速投入热坩埚 钠熔成小球,然后剧烈燃烧,发出黄色火
D
中,继续加热坩埚片刻 焰,生成淡黄色固体
二、钠与溶液反应的分析
2.钠与水溶液反应的本质是与水电离的氢离子反应,思考解答下列问题:
将一小块金属钠分别投入盛有:a.水、b.乙醇、c.稀HSO 的三个小烧杯中,反应速率由大
2 4
到 小 的 顺 序 为 ___________( 用 字 母 表 示 ) 。 解 释 反 应 速 率 不 同 的 原 因 :
________________________________________________________________________。
3.将金属钠放入盛有下列溶液的小烧杯中,既有气体又有白色沉淀产生的是
______________(填序号)。
①MgSO 溶液 ②BaCl 溶液 ③饱和澄清石灰水
4 2
④Ca(HCO ) 溶液 ⑤CuCl 溶液 ⑥饱和食盐水
3 2 2⑦浓盐酸
(1)钠与水、酸反应的本质与顺序:本质上均是与 H+的反应,反应顺序是有酸酸在前,无酸
水为先。
(2)钠与盐溶液的反应
钠与盐溶液反应时一般先考虑与水反应,生成的NaOH与盐可能发生复分解反应。
考点二 钠的氧化物
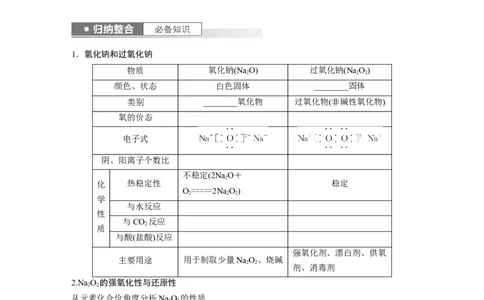
1.氧化钠和过氧化钠
物质 氧化钠(Na O) 过氧化钠(Na O)
2 2 2
颜色、状态 白色固体 ________固体
类别 ________氧化物 过氧化物(非碱性氧化物)
氧的价态
电子式
阴、阳离子个数比
不稳定(2Na O+
2
化 热稳定性 稳定
O=====2NaO)
2 2 2
学
与水反应
性
与CO 反应
2
质
与酸(盐酸)反应
强氧化剂、漂白剂、供氧
主要用途 用于制取少量NaO、烧碱
2 2
剂、消毒剂
2.Na O 的强氧化性与还原性
2 2
从元素化合价角度分析NaO 的性质
2 2
O ←――――――――― NaO――――――――――→O
2 2 2
(1)Na O 的强氧化性
2 2
试剂 反应原理(化学方程式) 现象
SO 气体 -
2
FeCl 溶液 有红褐色沉淀和气泡产生
2
NaSO 溶液 -
2 3
氢硫酸与水反应生成NaOH,NaO 的强
2 2
酚酞溶液
氧化性使之褪色
品红溶液 NaO 的强氧化性使之褪色
2 2
(2)遇KMnO 等强氧化剂时,表现出还原性,氧化产物为O。
4 2
(3)遇CO、HO、H+则发生自身的氧化还原反应。
2 2
1.氧化钠、过氧化钠均为离子化合物( )
2.1 mol Na O 固体中含离子总数为4N ( )
2 2 A
3.HO 和NaO 都属于过氧化物,含有的化学键完全相同( )
2 2 2 2
4.7.8 g过氧化钠含有的共用电子对数为0.2N ( )
A
5.NaO 在潮湿的空气中放置一段时间,最终产物是NaOH( )
2 2
6.NaO由两种单质直接反应生成,将其加入Ba(HCO ) 溶液中同时有气体和沉淀产生(
2 3 2
)
一、钠的氧化物与水、CO 反应的定量关系
2
1.(1)用单线桥分析NaO 与水的反应中电子转移的方向和数目:______________________;
2 2
其中氧化剂是__________,还原剂是__________,氧化产物是________,还原产物是
________________________________________________________________________。
(2)Na O 与CO 反应生成0.1 mol氧气时,转移的电子数为________。
2 2 2
2.在一密闭容器中有CO、H 、O 共16.5 g和足量的NaO ,用电火花引燃,使其完全反应,
2 2 2 2
NaO 增重7.5 g,则原混合气体中O 的质量分数是( )
2 2 2
A.54.5% B.40% C.36% D.33.3%
3.现有NaO和NaO 的混合物14 g,加入适量水使其充分溶解得到溶液 A和1.12 L气体
2 2 2
B(标准状况下)。
(1)混合物中NaO的物质的量为________ mol。
2
(2)在25 ℃下将溶液A加水稀释至400 mL,则该溶液的pH为________。
二、过氧化钠的性质与探究
4.NaO 是一种常见的过氧化物,具有强氧化性和漂白性。
2 2
(1)请写出NaO 的电子式:___________________________________________________,
2 2其中化学键的类型为_____________________________________________________,氧元素
的化合价为__________。
(2)用化学方程式解释使酚酞溶液变红的原因:_______________________________
________________________________________________________________________,
依据实验现象推测红色褪去的原因是________________________________________
________________________________________________________________________。
(3)用离子方程式解释加入酸性高锰酸钾溶液后溶液褪色的原因:________________
________________________________________________________________________。
(4)根据实验分析,过氧化钠与水反应除了生成氢氧化钠和氧气外,还存在另一反应,则另
一反应的化学方程式为________________________________________________________,其
反应类型为__________________。
过氧化物的结构特点与性质
无论是过氧化钠还是其他过氧化物,具有强氧化性、漂白性等特殊性质的根本原因是这些物
质中都含有过氧键。
1 . (1) 写 出 下 列 物 质 的 电 子 式 : 过 氧 化 钙 :
___________________________________________,过氧化氢:______________;从结构上
看 上 述 两 种 物 质 在 结 构 上 的 共 同 特 点 是
________________________________________________________________________。
(2)纯净的过氧化钙(CaO)是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。可以起到
2
杀菌、解酸(吸收二氧化碳)、防腐、供氧的作用。
分别写出供氧、解酸(吸收二氧化碳)的化学方程式:___________________________、
________________________________________________________________________。
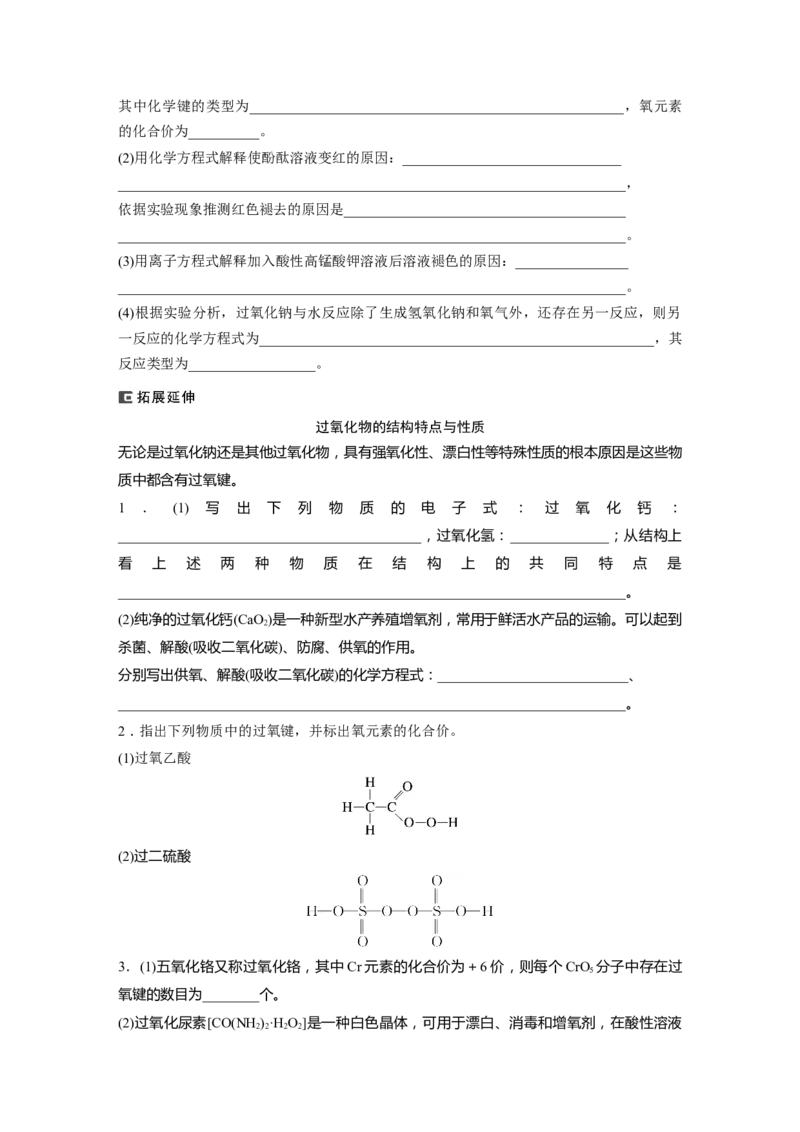
2.指出下列物质中的过氧键,并标出氧元素的化合价。
(1)过氧乙酸
(2)过二硫酸
3.(1)五氧化铬又称过氧化铬,其中Cr元素的化合价为+6价,则每个CrO 分子中存在过
5
氧键的数目为________个。
(2)过氧化尿素[CO(NH)·H O]是一种白色晶体,可用于漂白、消毒和增氧剂,在酸性溶液
2 2 2 2中过氧化尿素中的过氧化氢与重铬酸钾反应生成较稳定的蓝色过氧化铬(CrO ),重铬酸钾与
5
HO 反应的离子方程式为_______________________________________________________,
2 2
上述反应__________________________________________________________(填“是”或
“不是”)氧化还原反应。
1.正误判断,正确的打“√”,错误的打“×”。
(1)高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明(2022·浙江6月选考,8B)(
)
(2)23 g Na与足量HO反应生成的H 分子数目为N (2021·广东,11D)( )
2 2 A
(3)金属钠在空气中加热生成淡黄色固体:4Na+O===2NaO(2021·北京,7B)( )
2 2
(4)Na O在空气中加热可得固体NaO(2020·浙江7月选考,12A)( )
2 2 2
2.(2014·上海,19)下列反应与NaO +SO ―→NaSO 相比较,NaO 的作用相同的是(
2 2 2 2 4 2 2
)
A.2NaO+2CO―→2NaCO+O
2 2 2 2 3 2
B.2NaO+2SO ―→2NaSO +O
2 2 3 2 4 2
C.NaO+HSO ―→NaSO +HO
2 2 2 4 2 4 2 2
D.3NaO+Cr O―→2NaCrO+NaO
2 2 2 3 2 4 2
3.(2021·福建1月适应性考试,10)钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,
如图为钠投入液氨中的溶剂化示意图。钠沉入液氨中,快速得到深蓝色溶液,并慢慢产生气
泡。下列说法错误的是( )
A.钠的密度比液氨大
B.溶液的导电性增强
C.0.1 mol钠投入液氨中生成0.01 mol H 时,Na共失去0.02 mol电子
2
D.钠和液氨可以发生的反应为2NH +2Na===2NaNH +H↑
3 2 2