文档内容
1.(2022·潍坊模拟)《本草述钩元》中“石碱”条目下写道:“采蒿蓼之属,……晒干烧灰,
以原水淋汁,……久则凝淀如石,……浣衣发面,……亦去垢发面。”这里的“石碱”是指
( )
A.KOH B.KAl(SO )
4 2
C.KHCO D.KCO
3 2 3
2.下列说法错误的是( )
A.向碳酸钠中加入少量水后,插入温度计,显示温度上升
B.焰色试验的铂丝可用稀盐酸洗
C.可用澄清的石灰水鉴别NaCO 和NaHCO 两种溶液
2 3 3
D.NaCl可用作食品调味剂
3.除去混在碳酸钠溶液中少量的碳酸氢钠,最合理的方法是( )
A.加热 B.加适量氢氧化钠溶液
C.加盐酸 D.加CaCl 溶液
2
4.下列有关碳酸钠、碳酸氢钠的说法正确的是( )
A.25 ℃时,碳酸氢钠在水中的溶解度比碳酸钠大
B.常温下,分别向碳酸钠溶液和碳酸氢钠溶液中滴加等浓度的稀盐酸,立即产生气泡的是
NaCO
2 3
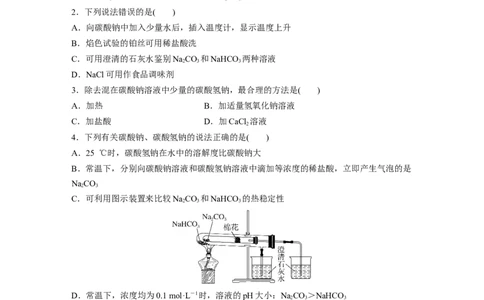
C.可利用图示装置来比较NaCO 和NaHCO 的热稳定性
2 3 3
D.常温下,浓度均为0.1 mol·L-1时,溶液的pH大小:NaCO>NaHCO
2 3 3
5.某同学用NaCO 和NaHCO 溶液进行如图所示实验。下列说法不正确的是( )
2 3 3
A.实验前pH(Na CO)>pH(NaHCO)
2 3 3
B.实验后两溶液中离子种类完全相同C.NaCO 溶液中生成的沉淀比NaHCO 溶液中生成的沉淀多
2 3 3
D.两溶液中反应的基本类型相同
6.下列各组中两种物质作用时,反应条件或反应物用量改变,对生成物没有影响的是(
)
A.NaOH溶液与CO
2
B.NaHCO 和盐酸
3
C.Na与O
2
D.NaHSO 溶液与Ba(OH) 溶液
4 2
7.(2023·厦门模拟)以不同类别物质间的转化为线索,认识钠及其化合物。
下列分析不正确的是( )
A.反应③表明CO 具有酸性氧化物的性质
2
B.反应④说明NaHCO 的热稳定性强于NaCO
3 2 3
C.反应⑤⑥可用于潜水艇中氧气的供给
D.上述转化中发生的反应有分解反应、化合反应、置换反应
8.钠元素广泛存在于自然界,中国科学技术大学的钱逸泰教授等以 CCl 和金属钠为原料,
4
在700 ℃时制造出纳米级金刚石粉末。该成果发表在世界权威杂志上,立刻被科学家们高
度评价为“稻草变黄金”。下列关于含钠元素的物质的说法错误的是( )
A.“稻草变黄金”的过程中元素种类没有改变
B.NaCl与NaCO 灼烧时火焰颜色相同
2 3
C.治疗胃酸过多可以用NaHCO ,糕点制作也可以用NaHCO
3 3
D.金属钠放置在空气中,最终会变成NaO
2 2
9.碱金属元素是金属性表现的最鲜明和最有规律的一族元素。下列说法正确的是( )
A.碱金属单质中锂的密度最小,熔点最低
B.25 ℃时碳酸钾溶液的pH<7
C.乙醇与金属钾反应生成氢气
D.用电解铯盐溶液的方法冶炼金属铯
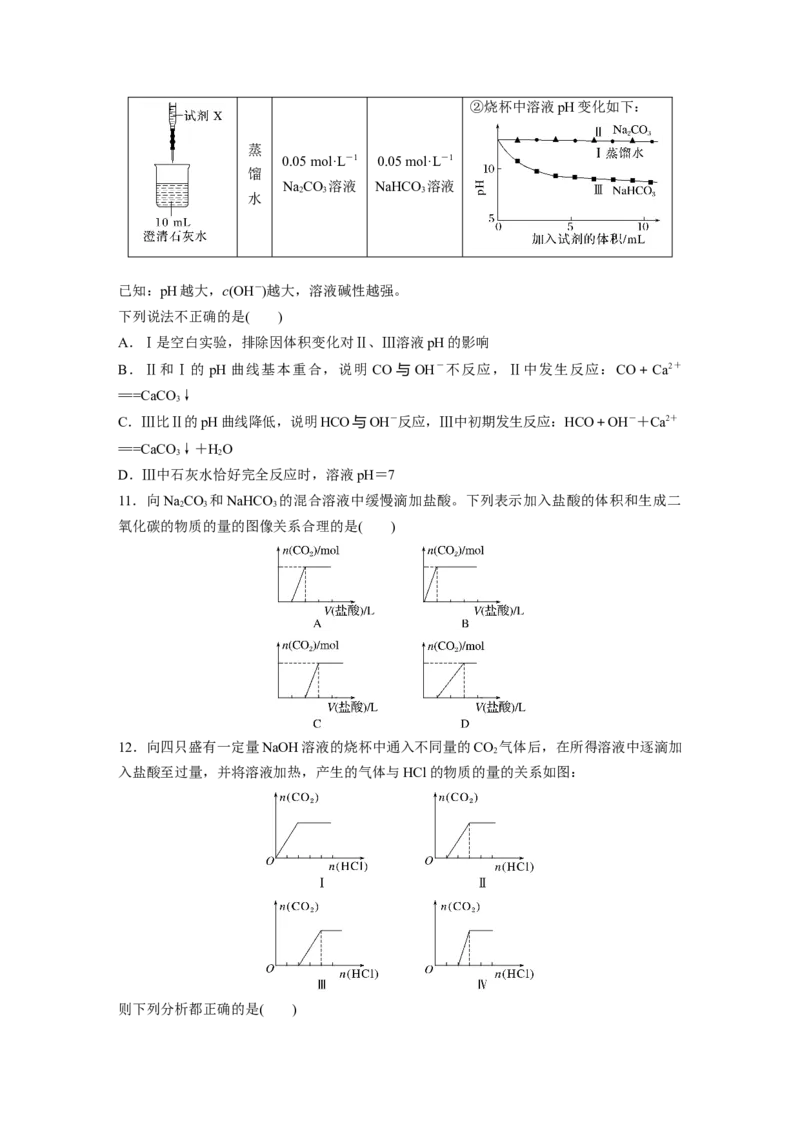
10.某化学实验小组探究NaCO 和NaHCO 与碱的反应,实验过程及结果如下。
2 3 3
实验装置 试剂X 实验结果
Ⅰ Ⅱ Ⅲ ①Ⅱ、Ⅲ均产生白色沉淀②烧杯中溶液pH变化如下:
蒸
0.05 mol·L-1 0.05 mol·L-1
馏
NaCO 溶液 NaHCO 溶液
2 3 3
水
已知:pH越大,c(OH-)越大,溶液碱性越强。
下列说法不正确的是( )
A.Ⅰ是空白实验,排除因体积变化对Ⅱ、Ⅲ溶液pH的影响
B.Ⅱ和Ⅰ的 pH 曲线基本重合,说明 CO 与 OH-不反应,Ⅱ中发生反应:CO+Ca2+
===CaCO ↓
3
C.Ⅲ比Ⅱ的pH曲线降低,说明HCO与OH-反应,Ⅲ中初期发生反应:HCO+OH-+Ca2+
===CaCO ↓+HO
3 2
D.Ⅲ中石灰水恰好完全反应时,溶液pH=7
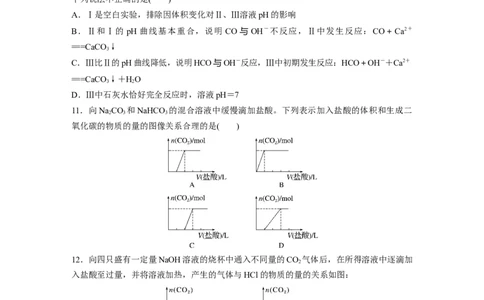
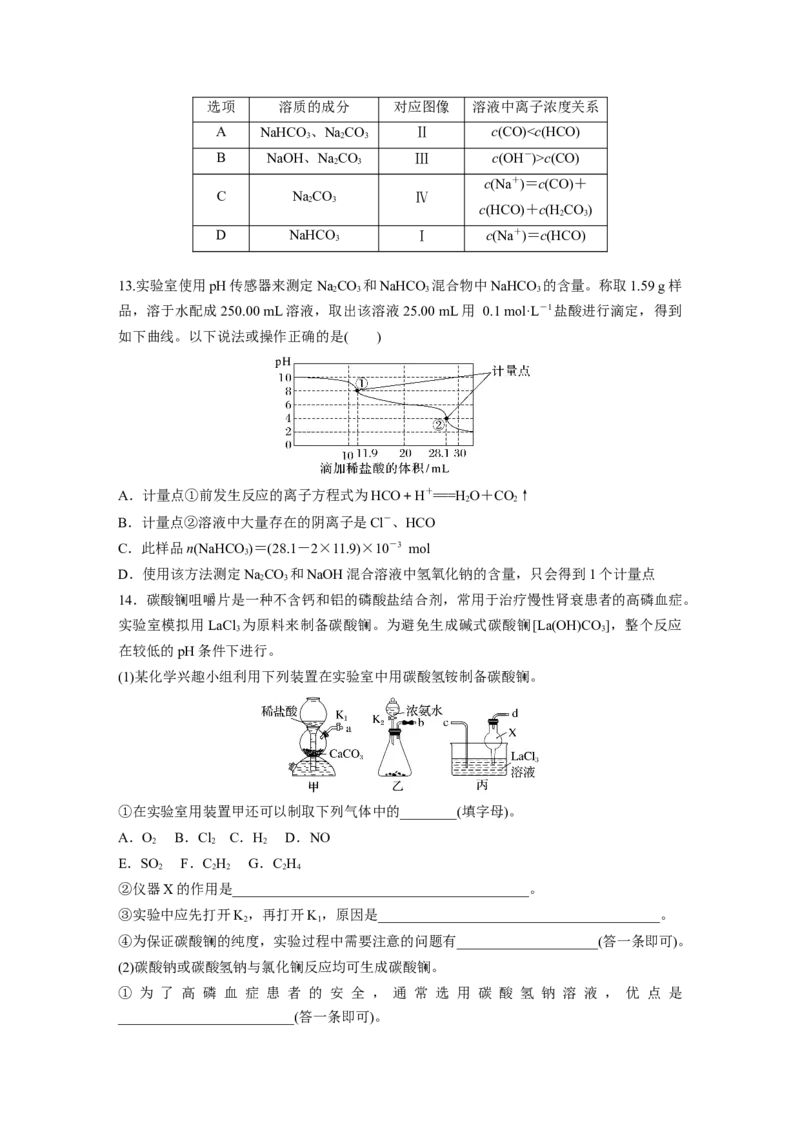
11.向NaCO 和NaHCO 的混合溶液中缓慢滴加盐酸。下列表示加入盐酸的体积和生成二
2 3 3
氧化碳的物质的量的图像关系合理的是( )
12.向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO 气体后,在所得溶液中逐滴加
2
入盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图:
则下列分析都正确的是( )选项 溶质的成分 对应图像 溶液中离子浓度关系
A NaHCO 、NaCO Ⅱ c(CO)c(CO)
2 3
c(Na+)=c(CO)+
C NaCO Ⅳ
2 3
c(HCO)+c(H CO)
2 3
D NaHCO Ⅰ c(Na+)=c(HCO)
3
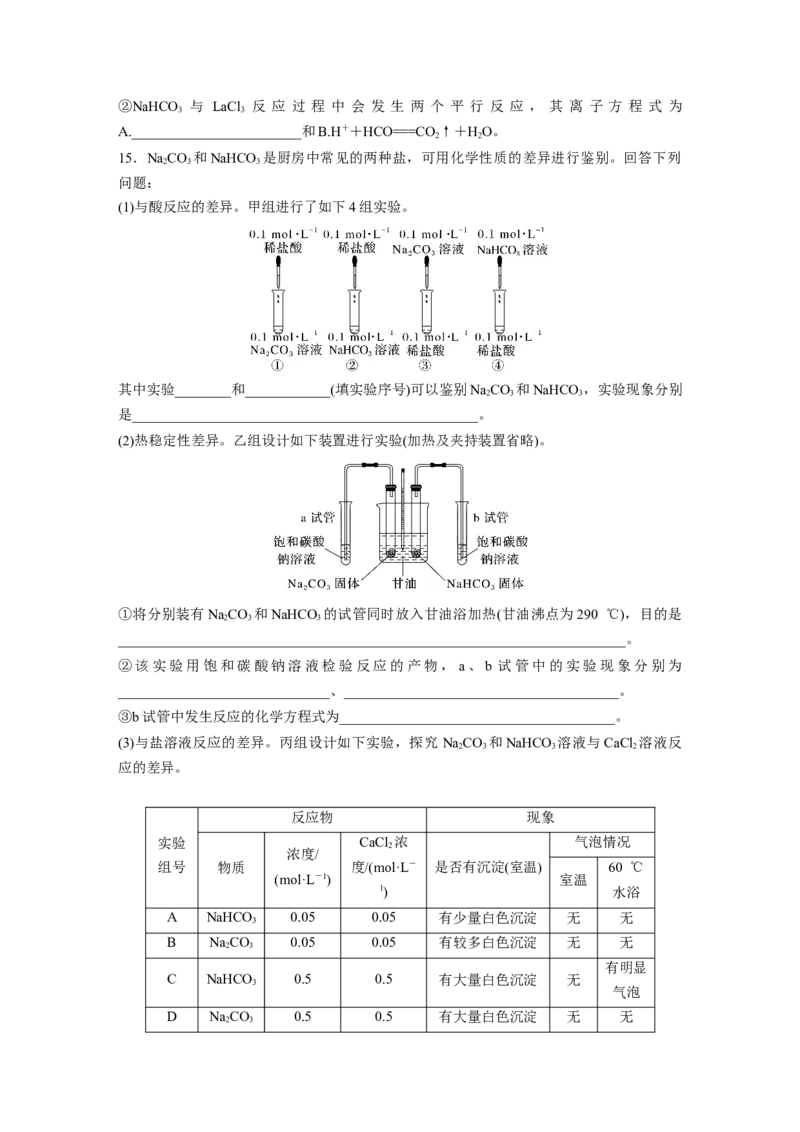
13.实验室使用pH传感器来测定NaCO 和NaHCO 混合物中NaHCO 的含量。称取1.59 g样
2 3 3 3
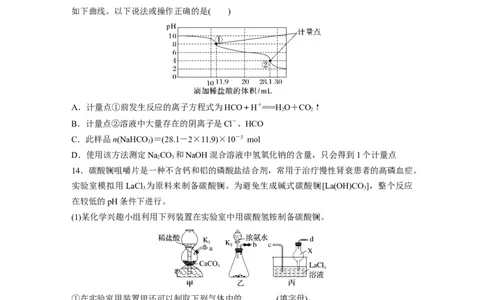
品,溶于水配成250.00 mL溶液,取出该溶液25.00 mL用 0.1 mol·L-1盐酸进行滴定,得到
如下曲线。以下说法或操作正确的是( )
A.计量点①前发生反应的离子方程式为HCO+H+===HO+CO↑
2 2
B.计量点②溶液中大量存在的阴离子是Cl-、HCO
C.此样品n(NaHCO )=(28.1-2×11.9)×10-3 mol
3
D.使用该方法测定NaCO 和NaOH混合溶液中氢氧化钠的含量,只会得到1个计量点
2 3
14.碳酸镧咀嚼片是一种不含钙和铝的磷酸盐结合剂,常用于治疗慢性肾衰患者的高磷血症。
实验室模拟用LaCl 为原料来制备碳酸镧。为避免生成碱式碳酸镧[La(OH)CO ],整个反应
3 3
在较低的pH条件下进行。
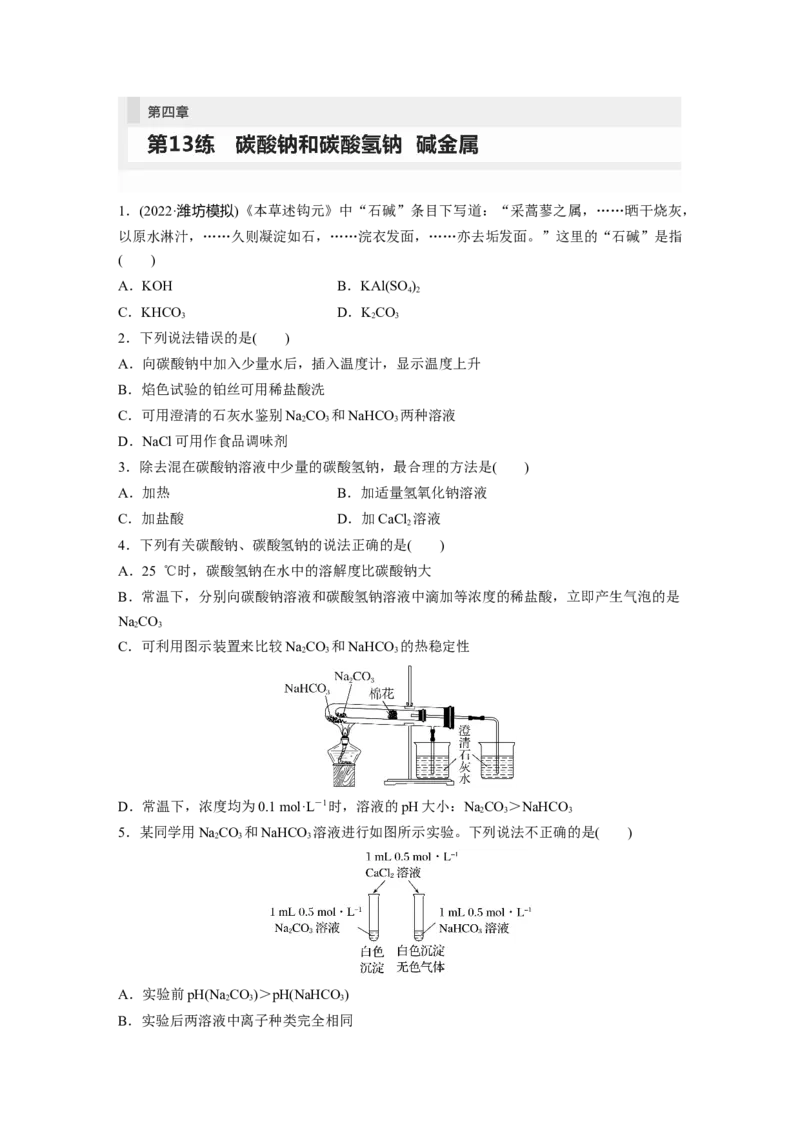
(1)某化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。
①在实验室用装置甲还可以制取下列气体中的________(填字母)。
A.O B.Cl C.H D.NO
2 2 2
E.SO F.C H G.C H
2 2 2 2 4
②仪器X的作用是__________________________________________。
③实验中应先打开K,再打开K,原因是________________________________________。
2 1
④为保证碳酸镧的纯度,实验过程中需要注意的问题有____________________(答一条即可)。
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
① 为 了 高 磷 血 症 患 者 的 安 全 , 通 常 选 用 碳 酸 氢 钠 溶 液 , 优 点 是
_________________________(答一条即可)。②NaHCO 与 LaCl 反 应 过 程 中 会 发 生 两 个 平 行 反 应 , 其 离 子 方 程 式 为
3 3
A.________________________和B.H++HCO===CO↑+HO。
2 2
15.NaCO 和NaHCO 是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列
2 3 3
问题:
(1)与酸反应的差异。甲组进行了如下4组实验。
其中实验________和____________(填实验序号)可以鉴别NaCO 和NaHCO ,实验现象分别
2 3 3
是_________________________________________________。
(2)热稳定性差异。乙组设计如下装置进行实验(加热及夹持装置省略)。
①将分别装有NaCO 和NaHCO 的试管同时放入甘油浴加热(甘油沸点为290 ℃),目的是
2 3 3
________________________________________________________________________。
②该实验用饱和碳酸钠溶液检验反应的产物,a、b 试管中的实验现象分别为
______________________________、_______________________________________。
③b试管中发生反应的化学方程式为_______________________________________。
(3)与盐溶液反应的差异。丙组设计如下实验,探究 NaCO 和NaHCO 溶液与CaCl 溶液反
2 3 3 2
应的差异。
反应物 现象
实验 CaCl 浓 气泡情况
2
浓度/
组号 物质 度/(mol·L- 是否有沉淀(室温) 60 ℃
(mol·L-1) 室温
1) 水浴
A NaHCO 0.05 0.05 有少量白色沉淀 无 无
3
B NaCO 0.05 0.05 有较多白色沉淀 无 无
2 3
有明显
C NaHCO 0.5 0.5 有大量白色沉淀 无
3
气泡
D NaCO 0.5 0.5 有大量白色沉淀 无 无
2 3①丙组由此得出“能用 CaCl 鉴别同浓度的 NaCO 和 NaHCO 溶液”的结论,理由是
2 2 3 3
________________________________________________________________________。
② 请 写 出 C 组 中 60 ℃ 时 , NaHCO 与 CaCl 溶 液 反 应 的 离 子 方 程 式 :
3 2
________________________________________________________________________。