文档内容
第 13 讲 碳酸钠和碳酸氢钠 碱金属
[复习目标] 1.掌握NaCO 、NaHCO 的基本性质及相互转化。2.掌握NaCO 、NaHCO 的
2 3 3 2 3 3
鉴别及除杂。3.了解碱金属的通性与特性及焰色试验。
考点一 碳酸钠和碳酸氢钠
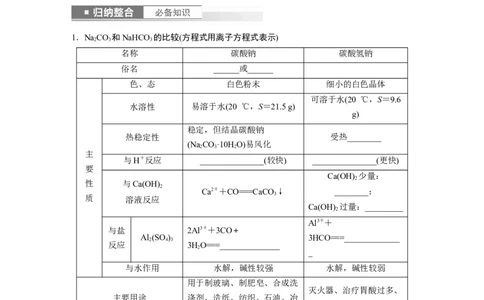
1.NaCO 和NaHCO 的比较(方程式用离子方程式表示)
2 3 3
名称 碳酸钠 碳酸氢钠
俗名 ______或______
色、态 白色粉末 细小的白色晶体
可溶于水(20 ℃,S=9.6
水溶性 易溶于水(20 ℃,S=21.5 g)
g)
稳定,但结晶碳酸钠
热稳定性 受热________
(Na CO·10H O)易风化
2 3 2
主
与H+反应 _______________(较快) _______________(更快)
要
Ca(OH) 少量:
2
性 与Ca(OH)
2
Ca2++CO===CaCO ↓ ________;
质 溶液反应 3
Ca(OH) 过量:_________
2
Al3++
与盐 2Al3++3CO+
Al (SO ) 3HCO===_____________
2 4 3
反应 3HO===______________
2
_
与水作用 水解,碱性较强 水解,碱性较弱
用于制玻璃、制肥皂、合成洗
灭火器、治疗胃酸过多、
主要用途 涤剂、造纸、纺织、石油、冶
发酵粉的主要成分之一
金等工业中
2.NaCO 和NaHCO 的相互转化
2 3 3
NaCONaHCO
2 3 3
应用举例
选择适当的试剂或方法除去杂质,并完成转化的化学方程式,“[ ]”内为杂质。
(1)Na CO(s)[NaHCO ]_______________________________,_______________________。
2 3 3
(2)NaHCO (aq)[Na CO]_____________________________,________________________。
3 2 3(3)Na CO(aq)[NaHCO ]_____________________________,________________________。
2 3 3
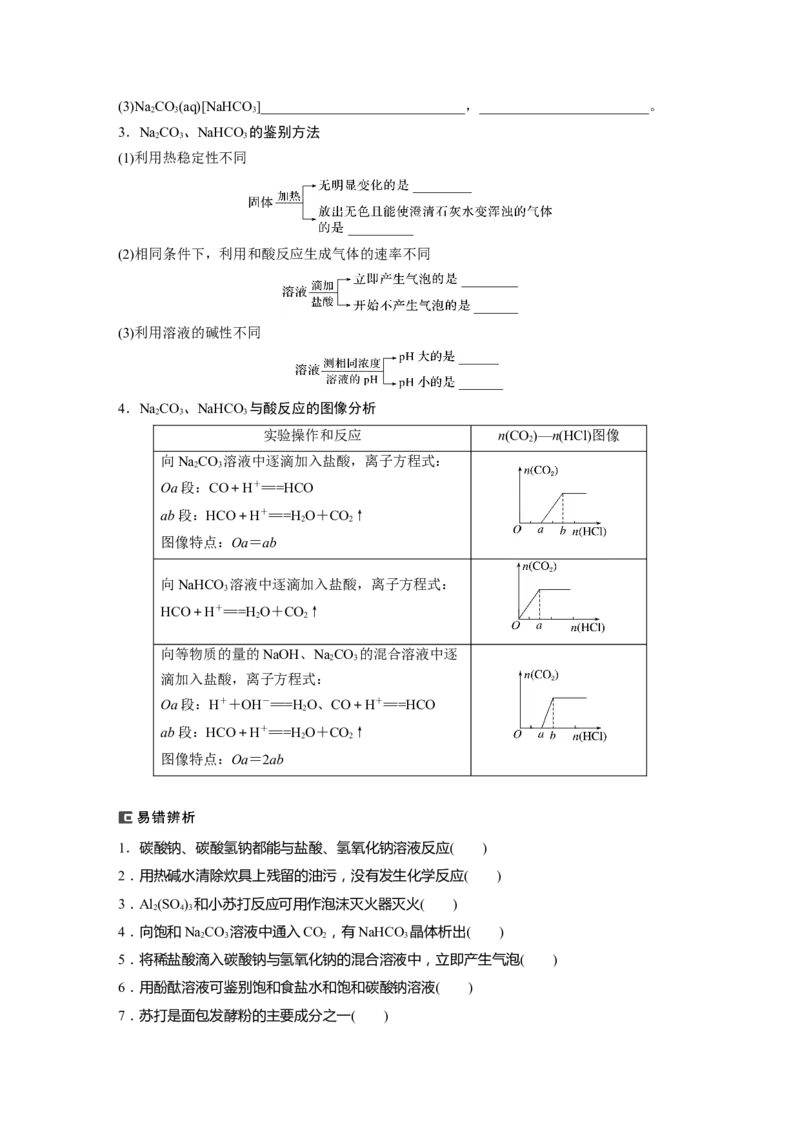
3.NaCO、NaHCO 的鉴别方法
2 3 3
(1)利用热稳定性不同
(2)相同条件下,利用和酸反应生成气体的速率不同
(3)利用溶液的碱性不同
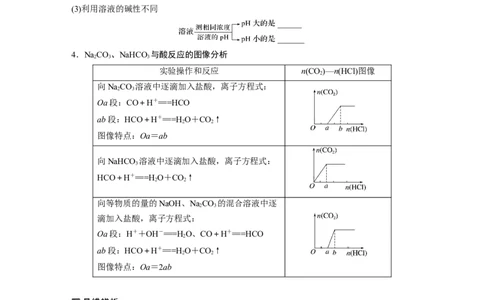
4.NaCO、NaHCO 与酸反应的图像分析
2 3 3
实验操作和反应 n(CO)—n(HCl)图像
2
向NaCO 溶液中逐滴加入盐酸,离子方程式:
2 3
Oa段:CO+H+===HCO
ab段:HCO+H+===HO+CO↑
2 2
图像特点:Oa=ab
向NaHCO 溶液中逐滴加入盐酸,离子方程式:
3
HCO+H+===HO+CO↑
2 2
向等物质的量的NaOH、NaCO 的混合溶液中逐
2 3
滴加入盐酸,离子方程式:
Oa段:H++OH-===HO、CO+H+===HCO
2
ab段:HCO+H+===HO+CO↑
2 2
图像特点:Oa=2ab
1.碳酸钠、碳酸氢钠都能与盐酸、氢氧化钠溶液反应( )
2.用热碱水清除炊具上残留的油污,没有发生化学反应( )
3.Al (SO ) 和小苏打反应可用作泡沫灭火器灭火( )
2 4 3
4.向饱和NaCO 溶液中通入CO,有NaHCO 晶体析出( )
2 3 2 3
5.将稀盐酸滴入碳酸钠与氢氧化钠的混合溶液中,立即产生气泡( )
6.用酚酞溶液可鉴别饱和食盐水和饱和碳酸钠溶液( )
7.苏打是面包发酵粉的主要成分之一( )8.相同温度下,溶解度:小苏打<苏打,热稳定性:NaCO>NaHCO( )
2 3 3
一、NaCO、NaHCO 性质比较与鉴别
2 3 3
1.(2023·佛山调研)NaCO 和NaHCO 混合溶液具有控制酸碱平衡的作用。室温下,通过下
2 3 3
列实验探究一定浓度的NaCO 和NaHCO 混合溶液的性质。
2 3 3
实验1:向混合溶液中滴几滴酚酞,溶液显红色;
实验2:向实验1所得溶液中滴加几滴稀盐酸,溶液红色变浅;
实验3:向混合溶液中通入过量的CO,无明显现象;
2
实验4:向实验3所得溶液中滴加少量Ba(OH) 溶液,产生白色沉淀。
2
下列有关说法正确的是( )
A.实验1中溶液显红色的主要原因是CO+2HOHCO+2OH-
2 2 3
B.实验2中溶液红色变浅的原因是HCO+H+HO+CO↑
2 2
C.实验3中无明显现象说明没有发生化学反应
D.实验4中产生白色沉淀的原因是2HCO+Ba2++2OH-===2HO+CO+BaCO ↓
2 3
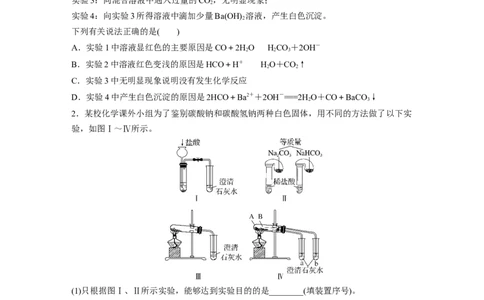
2.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实
验,如图Ⅰ~Ⅳ所示。
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是________(填装置序号)。
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为________________
___________________________________________________________________________;
与实验Ⅲ相比,实验Ⅳ的优点是____________(填字母)。
A.Ⅳ比Ⅲ复杂
B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便
D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管 B 中装入的固体最好是_____________________________________________________________________(填化学式)。
二、NaCO、NaHCO 与H+反应定量关系应用
2 3 3
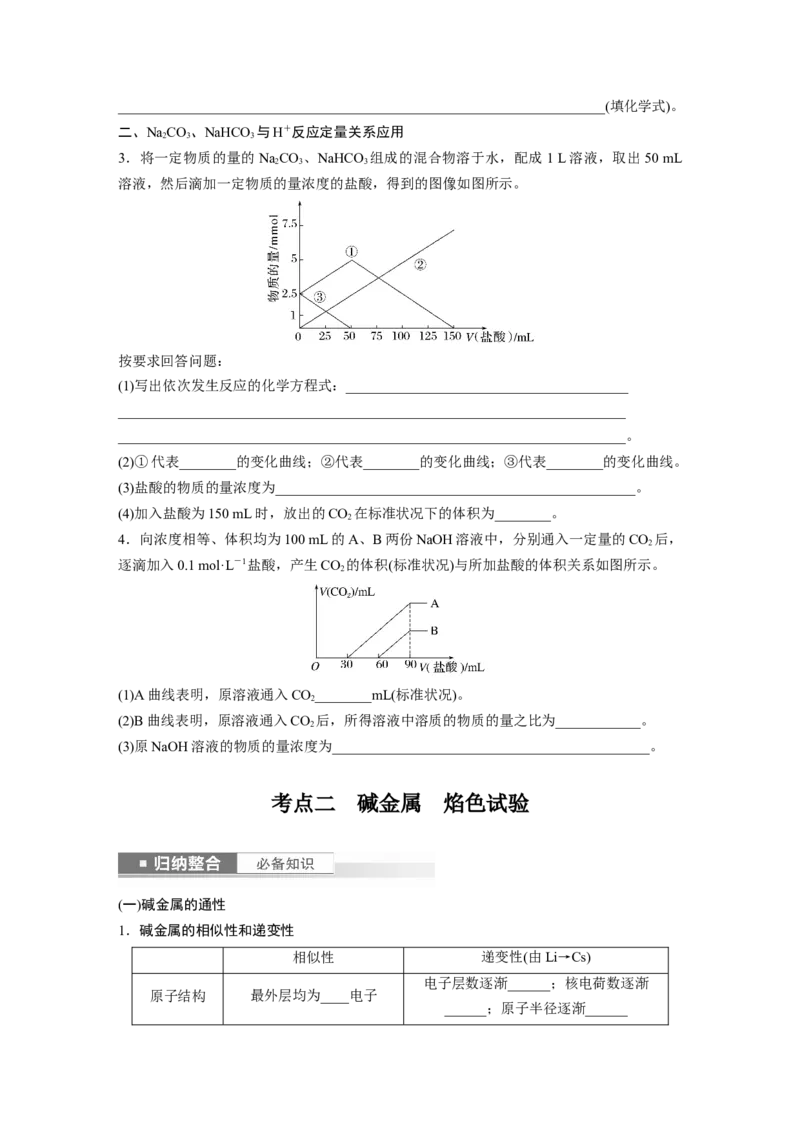
3.将一定物质的量的NaCO 、NaHCO 组成的混合物溶于水,配成1 L溶液,取出50 mL
2 3 3
溶液,然后滴加一定物质的量浓度的盐酸,得到的图像如图所示。
按要求回答问题:
(1)写出依次发生反应的化学方程式:________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)①代表________的变化曲线;②代表________的变化曲线;③代表________的变化曲线。
(3)盐酸的物质的量浓度为___________________________________________________。
(4)加入盐酸为150 mL时,放出的CO 在标准状况下的体积为________。
2
4.向浓度相等、体积均为100 mL的A、B两份NaOH溶液中,分别通入一定量的CO 后,
2
逐滴加入0.1 mol·L-1盐酸,产生CO 的体积(标准状况)与所加盐酸的体积关系如图所示。
2
(1)A曲线表明,原溶液通入CO________mL(标准状况)。
2
(2)B曲线表明,原溶液通入CO 后,所得溶液中溶质的物质的量之比为____________。
2
(3)原NaOH溶液的物质的量浓度为_____________________________________________。
考点二 碱金属 焰色试验
(一)碱金属的通性
1.碱金属的相似性和递变性
相似性 递变性(由Li→Cs)
电子层数逐渐______;核电荷数逐渐
原子结构 最外层均为____电子
______;原子半径逐渐______都具有较强的______性,
元素性质 金属性逐渐______
最高正价均为____价
物理 (除Cs外)都呈银白色,密 密度逐渐增大(钾反常),熔、沸点逐渐
单
性质 度较小,熔、沸点______ ______
质
性 化学 还原性逐渐______;与O 反应越来越剧
2
质 都具有较强的______性
性质 烈,产物越来越复杂
2.碱金属的特性
(1)碱金属的密度一般随核电荷数的增大而增大,但钾的密度比钠的小。
(2)碱金属一般都保存在______中,但由于锂的密度小于煤油的密度而将锂保存在石蜡中。
(3)试剂瓶中的药品取出后,一般不能放回原瓶,但Na、K等需放回原试剂瓶。
(4)锂与O 反应与钠不同,只生成LiO。
2 2
(二)焰色试验
1.焰色试验的概念
某些金属或它们的化合物在灼烧时都会使火焰呈现出特征颜色,属于______变化,是元素的
性质。
2.焰色试验的操作
(1)清洗铂丝:将铂丝用盐酸洗净,在外焰上灼烧至与原来的火焰颜色相同。
(2)灼烧试样:蘸取试样在外焰上灼烧,观察火焰的颜色。
(3)清洗铂丝:将铂丝再用盐酸洗净后,在外焰上灼烧至与原来的火焰颜色相同。
提醒 做钾的焰色试验时,需透过蓝色钴玻璃观察火焰的颜色。
3.熟记常见金属的焰色
钠元素:____色;钾元素:____色(透过____________观察);铜元素:____色;钡元素:
______色;钙元素:______色。
(三)碱金属氢化物的性质及应用
碱金属跟氢气反应生成的碱金属氢化物都是______________,其中氢以H-形式存在,显-1
价,碱金属氢化物是____________。
1.在酒精灯加热的条件下,NaCO、NaHCO 固体都会分解( )
2 3 3
2.KOH的碱性比NaOH的弱( )
3.常温下,Rb、Cs露置在空气中不易变质( )
4.焰色试验是金属化合物的性质( )
5.碱金属元素由Li到Cs,随着核电荷数的递增,单质密度逐渐增大,熔、沸点逐渐降低(
)一、焰色试验
1.下列有关焰色试验操作注意事项的说法正确的是( )
①钾的火焰颜色要透过蓝色钴玻璃观察 ②先将铂丝灼烧到与原来火焰的颜色相同,再蘸取
被检验的物质 ③每次实验后,要将铂丝用盐酸洗净
④实验时最好选择本身颜色较浅的火焰 ⑤没有铂丝时,也可以用光洁无锈的铁丝代替
A.仅有③不正确 B.仅有④不正确
C.仅有⑤不正确 D.全对
二、碱金属元素性质规律的应用
2.碱金属单质及其化合物有广泛应用。回答下列问题:
(1)锂是最轻的活泼金属,常用于制造高效锂电池。电解池中的电解液不能用水作溶剂,原
因是____________________________________________________________________________。
(2)金属钾是一种活泼的金属,下列有关其性质的说法正确的是________(填字母)。
A.钾在空气中燃烧时,只生成KO
2
B.钾与水反应,由于反应剧烈可能会发生爆炸
C.1 mol·L-1KOH溶液比1 mol·L-1NaOH溶液碱性强
(3)KH 是一种野外供氢剂,其电子式为________,与水反应放出氢气,化学方程式为
________________________________________________________________________。
生成1 mol氢气时,反应中转移的电子数为_______________________________________。
(4)NaH在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe O),脱锈过程中
2 3
生成两种产物,其反应的化学方程式: ________________________________________。
1.正误判断,正确的打“√”,错误的打“×”。
(1)碳酸氢钠可做食品膨松剂(2022·全国乙卷,7B)( )
(2)焰火中红色来源于钠盐灼烧(2022·全国乙卷,7D)( )
(3)面包师用小苏打作发泡剂烘焙面包,是因为NaCO 可与酸反应(2022·广东,6A)( )
2 3
(4)NaHCO 的热稳定性比NaCO 强(2020·浙江7月选考,8B)( )
3 2 3
(5)盐碱地(含较多NaCO 等)不利于作物生长,可施加熟石灰进行改良(2019·天津,3C)(
2 3
)
(6)碳酸钠可用于去除餐具的油污(2018·全国卷Ⅱ,7A)( )
(7)溶解度:NaCO