文档内容
第 16 讲 铁盐、亚铁盐及相互转化
[复习目标] 1.掌握Fe2+和Fe3+的检验方法。2.掌握铁盐、亚铁盐的性质,能实现Fe2+和Fe3
+的转化。
考点一 铁盐、亚铁盐的性质与检验
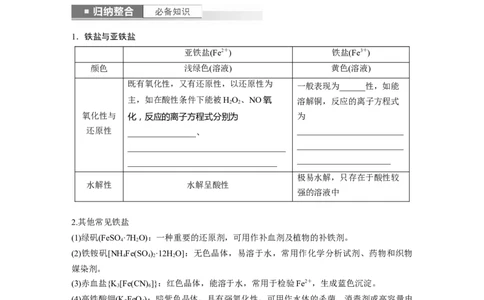
1.铁盐与亚铁盐
亚铁盐(Fe2+) 铁盐(Fe3+)
颜色 浅绿色(溶液) 黄色(溶液)
既有氧化性,又有还原性,以还原性为 一般表现为______性,如能
主,如在酸性条件下能被HO、NO氧 溶解铜,反应的离子方程式
2 2
氧化性与 化,反应的离子方程式分别为 为
还原性 ________________、 _________________________
_____________________________________ _________________________
___________________________________ ______________________
极易水解,只存在于酸性较
水解性 水解呈酸性
强的溶液中
2.其他常见铁盐
(1)绿矾(FeSO ·7H O):一种重要的还原剂,可用作补血剂及植物的补铁剂。
4 2
(2)铁铵矾[NH Fe(SO )·12H O]:无色晶体,易溶于水,常用作化学分析试剂、药物和织物
4 4 2 2
媒染剂。
(3)赤血盐{K [Fe(CN) ]}:红色晶体,能溶于水,常用于检验Fe2+,生成蓝色沉淀。
3 6
(4)高铁酸钾(K FeO):暗紫色晶体,具有强氧化性,可用作水体的杀菌、消毒剂或高容量电
2 4
池材料。
3.Fe2+和Fe3+的检验
(1)(2)
(3)含Fe2+、Fe3+的混合溶液中Fe2+、Fe3+的检验
―――――――→溶液变红色,说明含有______。
――――――→酸性KMnO 溶液紫红色褪去,说明含有______。
4
1.氢氧化铁与HI溶液仅能发生中和反应( )
2.中性溶液中可能大量存在Fe3+、Cl-、K+、SO( )
3.酸性条件下HO 氧化Fe2+的离子方程式为2Fe2++HO+2H+===2Fe3++2HO( )
2 2 2 2 2
4.将Fe(NO ) 样品溶于稀HSO 后,滴加KSCN溶液,溶液变红,则Fe(NO ) 晶体已氧化
3 2 2 4 3 2
变质( )
5.用酸性高锰酸钾溶液检验FeCl 溶液中是否含有FeCl ( )
3 2
一、铁盐、亚铁盐的性质
1.铁及其化合物是中学化学中一类重要的物质。下列关于铁元素的叙述正确的是( )
A.采用将FeCl 溶液直接蒸干的方法制备FeCl 固体
3 3
B.保存FeCl 溶液常常加一些铁粉,其目的是抑制Fe2+水解
2
C.25 ℃时,pH=0的溶液中,Al3+、NH、NO、Fe2+可以大量共存
D.FeSO 溶液中加入HO 溶液时,Fe2+表现还原性
4 2 2
2.在FeCl 、CuCl 混合溶液中,加入铁粉与铜粉的混合物。
3 2
(1)若金属无剩余,则溶液中一定存在的金属阳离子有________,可能存在的有________。
(2)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有________,一定不存在
________。
(3)若剩余固体中只有铜,则溶液中一定存在的金属阳离子有________,可能存在的有
____________,一定不存在________。
二、Fe2+和Fe3+的检验
3.下列离子的检验方法合理的是( )
A.向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+
B.向某溶液中通入Cl,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+
2
C.向某溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中
只含有Fe2+,不含有Mg2+4.以下实验能证明某溶液中不含Fe3+而含有Fe2+的是( )
A.滴入KSCN溶液,不显红色
B.滴加足量氯水,再加KSCN溶液,显红色
C.滴入KSCN溶液,不显红色,再加氯水,溶液变红
D.滴入KSCN溶液,不显红色,再加足量高锰酸钾溶液,溶液变红
检验Fe2+和Fe3+时的注意事项
(1)检验Fe2+时不能先加氯水后加KSCN溶液,也不能将加KSCN后的混合溶液加入足量的
新制氯水中(新制氯水能氧化SCN-)。
(2)Fe3+、Fe2+、Cl-同时存在时不能用酸性KMnO 溶液检验Fe2+(Cl-能还原酸性KMnO ,
4 4
有干扰)。
考点二 Fe2+、Fe3+的相互转化
Fe2+与Fe3+的相互转化
用离子方程式实现下列转化:
Fe2+Fe3+
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________;
④________________________________________________________________________;
⑤________________________________________________________________________;
⑥________________________________________________________________________;
⑦________________________________________________________________________。
某班同学用如下实验探究Fe2+与Fe3+的转化,回答下列问题:
(1)实验Ⅰ:Fe3+转化为Fe2+
实验步骤及现象:甲组同学将少量铜粉加入1 mL 0.1 mol·L-1 FeCl 溶液中,观察到铜粉消
3
失,溶液黄色变浅,加入蒸馏水后无明显现象;乙组同学将过量铜粉加入 1 mL 0.1 mol·L-1
FeCl 溶液中,观察到铜粉有剩余,溶液黄色褪去,加入蒸馏水后出现白色沉淀;丙组同学
3
将过量铜粉加入1 mL 0.05 mol·L-1 Fe 溶液中,观察到铜粉有剩余,溶液黄色褪去,变成
23蓝色,加入蒸馏水后无白色沉淀。
①分别取三组实验反应后的溶液于三支试管中,_____________________________
________________________________________________________________________
(填操作步骤及现象),证明生成了Fe2+;分析三组实验结果,实验中均发生的反应的离子方
程式为_________________________________________________________________。
②对比三组实验,说明加入蒸馏水后沉淀的产生与__________________________有关。
③向丙组实验后的溶液中加入饱和NaCl溶液可能出现的现象为______________________。
④丙组在检验反应后的溶液中是否存在 Fe3+时,取反应后的上层清液于试管中,滴加 3滴
KSCN溶液,结果出现白色沉淀,查阅资料:ⅰ.SCN-的化学性质与I-相似,CuSCN为白
色固体;ⅱ.2Cu2++4I-===2CuI↓+I ,写出该实验中出现白色沉淀的离子方程式:
2
________________________________________________________________________。
(2)实验Ⅱ:Fe2+转化为Fe3+
实验步骤及现象:向3 mL 0.1 mol·L-1 FeSO 溶液中加入稍过量稀硝酸,溶液变为棕色,放
4
置一段时间后,棕色消失,溶液变为黄色,已知Fe2++NO―→Fe(NO)2+(棕色)。
①使用的FeSO 溶液中存在少量铁屑,其目的是_______________________________。
4
②实验中产生NO的原因为____________________________________________________
________________________________________________________________________(用离子
方程式表示)。
(3)实验Ⅲ:Fe2+与Fe3+相互转化
实验步骤及现象:将SO 通入足量Fe 溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕
2 3
黄色,此时若滴入BaCl 溶液,则会产生白色沉淀。将产生的白色沉淀经过滤、洗涤、干燥
2
后称量其质量为6.99 g,则整个实验中产生的气体(假设只生成一种气体,该气体遇空气变
为红棕色)在标准状况下的体积为_______________________________________________。
1.(2019·浙江4月选考,24)聚合硫酸铁[Fe(OH)SO ] 能用作净水剂(絮凝剂),可由绿矾
4 n
(FeSO ·7H O)和KClO 在水溶液中反应得到。下列说法不正确的是( )
4 2 3
A.KClO 作氧化剂,每生成1 mol [Fe(OH)SO ] 消耗 mol KClO
3 4 n 3
B.生成聚合硫酸铁后,水溶液的pH增大
C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强
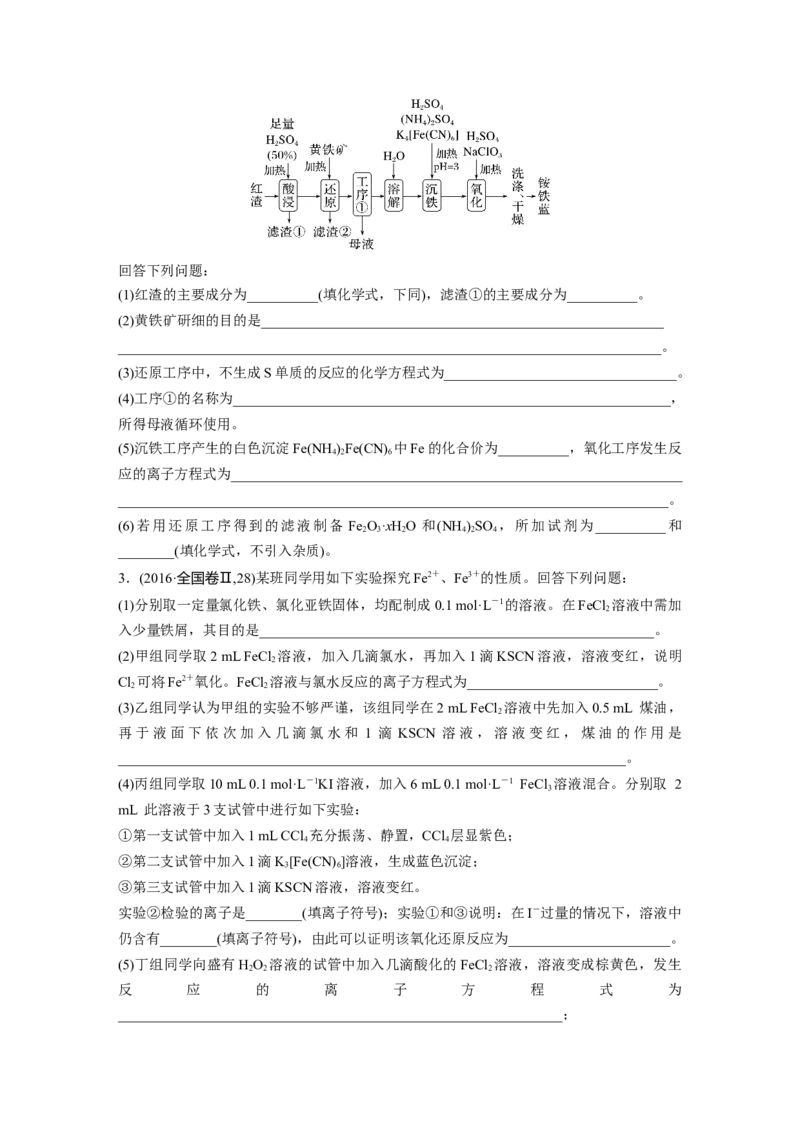
2.(2022·河北,15)以焙烧黄铁矿 FeS(杂质为石英等)产生的红渣为原料制备铵铁蓝
2
Fe(NH )Fe(CN) 颜料。工艺流程如下:
4 6回答下列问题:
(1)红渣的主要成分为__________(填化学式,下同),滤渣①的主要成分为__________。
(2)黄铁矿研细的目的是_________________________________________________________
_____________________________________________________________________________。
(3)还原工序中,不生成S单质的反应的化学方程式为_________________________________。
(4)工序①的名称为______________________________________________________________,
所得母液循环使用。
(5)沉铁工序产生的白色沉淀Fe(NH )Fe(CN) 中Fe的化合价为__________,氧化工序发生反
4 2 6
应的离子方程式为________________________________________________________________
______________________________________________________________________________。
(6)若用还原工序得到的滤液制备 Fe O·xHO 和(NH )SO ,所加试剂为__________和
2 3 2 4 2 4
________(填化学式,不引入杂质)。
3.(2016·全国卷Ⅱ,28)某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液。在FeCl 溶液中需加
2
入少量铁屑,其目的是________________________________________________________。
(2)甲组同学取2 mL FeCl 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明
2
Cl 可将Fe2+氧化。FeCl 溶液与氯水反应的离子方程式为___________________________。
2 2
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl 溶液中先加入0.5 mL 煤油,
2
再于液面下依次加入几滴氯水和 1 滴 KSCN 溶液,溶液变红,煤油的作用是
________________________________________________________________________。
(4)丙组同学取10 mL 0.1 mol·L-1KI溶液,加入6 mL 0.1 mol·L-1 FeCl 溶液混合。分别取 2
3
mL 此溶液于3支试管中进行如下实验:
①第一支试管中加入1 mL CCl 充分振荡、静置,CCl 层显紫色;
4 4
②第二支试管中加入1滴K[Fe(CN) ]溶液,生成蓝色沉淀;
3 6
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是________(填离子符号);实验①和③说明:在I-过量的情况下,溶液中
仍含有________(填离子符号),由此可以证明该氧化还原反应为_______________________。
(5)丁组同学向盛有HO 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄色,发生
2 2 2
反 应 的 离 子 方 程 式 为
_______________________________________________________________;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是
______________________________________________,生成沉淀的原因是____________(用
平衡移动原理解释)。