文档内容
1.(2022·广东茂名模拟)青矾矿石(主要成分为FeSO ·7H O)在《唐本草》中记载:“本来绿
4 2
色,新出窟未见风者,正如琉璃……烧之赤色……”。下列关于FeSO ·7H O的说法正确的
4 2
是( )
A.可用于制净水剂
B.溶于水形成无色溶液
C.在干燥空气中稳定存在
D.在空气中加热转化为Fe O
3 4
2.铁及其化合物在生产、生活中应用广泛。下列铁及其化合物的性质与用途具有对应关系
的是( )
A.Fe有导电性,可用于湿法炼铜
B.FeCl 有氧化性,可用于净水
3
C.Fe O 呈红棕色,可用于制作颜料
2 3
D.KFeO 易溶于水,可用于杀菌消毒
2 4
3.下列离子方程式书写正确的是( )
A.铁与稀盐酸反应:Fe+6H+===Fe3++3H↑
2
B.氯气与氯化亚铁溶液反应:Cl+Fe2+===Fe3++2Cl-
2
C.氯化铁溶液与铜反应:3Cu+2Fe3+===2Fe+3Cu2+
D.氯化铁溶液与硫化氢反应:2Fe3++HS===2Fe2++S↓+2H+
2
4.(2023·哈尔滨模拟)工业废水中含有的重铬酸根离子(CrO)有毒,必须处理达标后才能排
2
放。工业上常用绿矾(FeSO ·7H O)作处理剂,反应的离子方程式为 6Fe2++Cr O+14H+
4 2 2
===6Fe3++2Cr3++7HO,下列说法正确的是( )
2
A.氧化剂与还原剂的物质的量之比为6∶1
B.用绿矾作处理剂,不仅可去除毒性,还可净水
C.酸化试剂可以用盐酸或硫酸
D.不能用草酸溶液代替绿矾作处理剂
5.向含有 Cu(NO ) 、Zn(NO ) 、Fe(NO ) 、AgNO 各 0.1 mol 的混合溶液中加入 0.1 mol
3 2 3 2 3 3 3
Fe,充分搅拌后Fe溶解,溶液中不存在Fe3+,同时析出0.1 mol Ag。下列结论错误的是(
)
A.氧化性:Zn2+>Cu2+>Fe3+>Ag+
B.Fe3+的氧化性大于Cu2+C.溶液中Cu2+与Fe2+的物质的量之比为1∶2
D.1 mol Fe可还原2 mol Fe3+
6.(2022·江苏常州高三质检)铁元素的常见价态有+2、+3 价,实验室可用赤血盐
{K [Fe(CN) ]}溶液检验Fe2+,黄血盐{K [Fe(CN) ]}溶液检验Fe3+。Fe O 是重要的化工原料,
3 6 4 6 2 3
Au/Fe O 可用作反应 CO(g)+HO(g)===CO(g)+H(g)的催化剂。硫铁矿烧渣中含有大量
2 3 2 2 2
Fe O ,工业上常用于制取绿矾(FeSO ·7H O)。由硫铁矿烧渣(主要含Fe O 、Al O 、SiO)制
2 3 4 2 2 3 2 3 2
取绿矾的流程如下:
下列有关说法不正确的是( )
A.“酸溶”时先将烧渣粉碎并不断搅拌,可提高铁元素的浸出率
B.“反应”时发生的主要反应为2Fe3++Fe===3Fe2+
C.“检验”时可用K 溶液检验上一步“反应”是否进行完全
4
D.将第二次“过滤”所得滤液加热,经蒸发结晶可以制得绿矾
7.(2022·辽宁鞍山模拟)资料显示:FeCl(亮黄色)只有在Cl-浓度较大的溶液中才能稳定存在,
为了验证该事实,某实验小组取三份2 mL黄色的工业盐酸分别做了一系列实验,记录如下:
操作 现象
实验Ⅰ:直接滴加2滴KSCN溶液 无明显变化
实验Ⅱ:加10 mL蒸馏水稀释,后滴入 稀释后溶液几乎变为无色,加KSCN
2滴浓KSCN溶液 溶液显红色
实验Ⅲ:滴加2滴AgNO 饱和溶液 产生白色沉淀,溶液亮黄色消失
3
下列说法不正确的是( )
A.工业盐酸显黄色是因为其中混有FeCl
B.实验Ⅰ中,未检测到Fe3+
C.实验Ⅲ中,AgNO 溶液稀释了样品是溶液亮黄色消失的主要原因
3
D.通过上述实验,可以证明FeCl只有在Cl-浓度较大的溶液中才能稳定存在
8.为探究SO 与Fe3+是否发生氧化还原反应,按如图所示装置进行实验(夹持、加热仪器
2
略),下列说法正确的是( )
A.A中的反应仅体现了浓硫酸的氧化性
B.试剂a为饱和NaHCO 溶液
3C.C中溶液pH降低,证明Fe3+氧化了SO
2
D.检验C中的溶液含有Fe2+,证明Fe3+氧化了SO
2
9.(2022·山东淄博模拟)中药材铁华粉的主要成分是醋酸亚铁,检测的流程如图。下列说法
错误的是( )
A.气体X中含有醋酸蒸气
B.该铁华粉中可能含有铁单质
C.向滤液中滴入酸性KMnO 溶液,可用于证明Fe2+具有还原性
4
D.产生蓝色沉淀的反应为K++Fe2++[Fe(CN) ]3-===KFe[Fe(CN) ]↓
6 6
10.(2022·福建漳州模拟)高铁酸钾(K FeO)具有强氧化性,是一种环保、高效、多功能的饮
2 4
用水处理剂,可以用如下流程进行制备。下列说法正确的是( )
A.“酸溶”前,可用热的NaCO 溶液处理铁屑表面的油污
2 3
B.“氧化”过程中反应的离子方程式为2Fe2++O+4H+===2Fe3++2HO
2 2
C.“制备NaFeO”中氧化剂和还原剂的物质的量之比为2∶3
2 4
D.“转化”中析出KFeO 晶体的原因可能是相同条件下其溶解度大于NaFeO
2 4 2 4
11.黄色固体X,可能含有漂白粉、FeSO 、Fe (SO ) 、CuCl 、KI之中的几种或全部。将X
4 2 4 3 2
与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是( )
A.X中含KI,可能含有CuCl
2
B.X中含有漂白粉和FeSO
4
C.X中含有CuCl ,Y中含有Fe(OH)
2 3
D.用HSO 酸化溶液Z,若有黄绿色气体放出,说明X中含有CuCl
2 4 2
12.以高硫铝土矿(主要成分为Fe O 、Al O 、SiO ,少量FeS 和硫酸盐)为原料制备聚合硫
2 3 2 3 2 2
酸铁{[Fe (OH)(SO )]}和明矾的部分工艺流程如下,下列说法错误的是( )
2 x 4 y n
已知:赤泥液的主要成分为NaCO。
2 3A.赤泥液的作用是吸收“焙烧”阶段中产生的SO
2
B.聚合硫酸铁可用于净化自来水,与其组成中的Fe3+具有氧化性有关
C.在“聚合”阶段,若增加Fe O 的用量,会使[Fe (OH)(SO )] 中x变大
2 3 2 x 4 y n
D.从“滤液”到“明矾”的过程中还应有“除硅”步骤
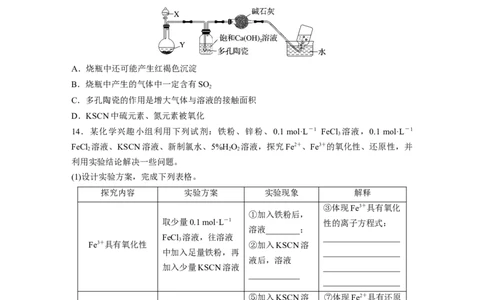
13.某化学实验小组探究Fe2+和Fe3+性质时发现:向FeCl 和KSCN的混合溶液中滴加氯水,
2
溶液变成红色,但当氯水过量时,红色会褪去。为此,他们设计如图装置进一步探究。
已知:①X为NaClO溶液,Y为FeCl 和KSCN的混合溶液。②持续缓慢滴入NaClO溶液
3
至过量的过程中,圆底烧瓶中红色变浅,有大量气泡产生;Ca(OH) 溶液变浑浊。根据实验
2
现象推测,下列说法不正确的是( )
A.烧瓶中还可能产生红褐色沉淀
B.烧瓶中产生的气体中一定含有SO
2
C.多孔陶瓷的作用是增大气体与溶液的接触面积
D.KSCN中硫元素、氮元素被氧化
14.某化学兴趣小组利用下列试剂:铁粉、锌粉、0.1 mol·L-1 FeCl 溶液,0.1 mol·L-1
3
FeCl 溶液、KSCN溶液、新制氯水、5%H O 溶液,探究Fe2+、Fe3+的氧化性、还原性,并
2 2 2
利用实验结论解决一些问题。
(1)设计实验方案,完成下列表格。
探究内容 实验方案 实验现象 解释
③体现Fe3+具有氧化
①加入铁粉后,
取少量0.1 mol·L-1 性的离子方程式:
溶液________;
FeCl 溶液,往溶液 __________________
3
Fe3+具有氧化性 ②加入KSCN溶
中加入足量铁粉,再 __________________
液后,溶液
加入少量KSCN溶液 __________________
____________
__________________
⑤加入KSCN溶 ⑦体现Fe2+具有还原
④取少量0.1 mol·L-1
液后,溶液 性的离子方程式:
FeCl 溶液,往溶液
2
________; __________________
Fe2+具有还原性 中加入少量KSCN溶
⑥加入你选的试 __________________
液,再加入
剂后,溶液 __________________
__________
__________ __________________
(2)该兴趣小组为说明“Fe2+具有氧化性”,提出了向FeCl 溶液中加入锌粉,观察实验现象
2
的方案,该反应的离子方程式为___________________________________________________________________________________________________________________。
(3)某反应中反应物与生成物有 Fe3+、Mn2+、H+、MnO、HO和一种未知离子X,已知
2
MnO在反应中得到电子,则X是________。
15.(2022·河南信阳模拟)硫酸亚铁铵晶体[(NH )Fe(SO )·6H O]是分析化学中的重要试剂,
4 2 4 2 2
是一种复盐,一般亚铁盐在空气中易被氧化,形成复盐后就比较稳定。与其他复盐一样,硫
酸亚铁铵在水中的溶解度比组成它的每一种盐的溶解度都小,利用这一性质可以用等物质的
量的(NH )SO 和FeSO 混合制备。请回答下列问题:
4 2 4 4
Ⅰ.硫酸亚铁铵晶体的制备
步骤一:称取3.0 g铁屑,加入15 mL 10%Na CO 溶液,小火加热30分钟,过滤、洗涤、干
2 3
燥、称量得固体m g。
1
步骤二:将步骤一中的m g固体转移至锥形瓶,加入15 mL 3 mol·L-1HSO ,加热至不再
1 2 4
有气体生成,趁热过滤,洗涤固体,将滤液和洗涤液合并后转移至蒸发皿中备用,准确称量
剩余固体质量得m g。
2
步骤三:计算所得FeSO 的物质的量,计算等物质的量的(NH )SO 固体的质量,准确称取
4 4 2 4
(NH )SO 。
4 2 4
步骤四:将(NH )SO 固体加入蒸发皿中,缓慢加热浓缩至表面出现结晶薄膜为止,放置冷
4 2 4
却。
步骤五:经过一系列操作,最终得到较纯净的(NH )Fe(SO )·6H O。
4 2 4 2 2
(1)碱煮30分钟的目的是__________________________________________________。
(2)步骤二中的加热,最佳加热方式为______________,理由是__________________。
(3)关于步骤五中的一系列操作的相关表述,错误的是________(填字母)。
A.过滤时可使用玻璃棒搅拌的方式来缩短时间
B.过滤和洗涤的速度都要尽可能的快,可以减少产品的氧化
C.洗涤时使用无水乙醇既可以洗去晶体表面的杂质离子,又可以起到干燥的作用
D.所得的产品可以采取电热炉烘干的方式彻底干燥
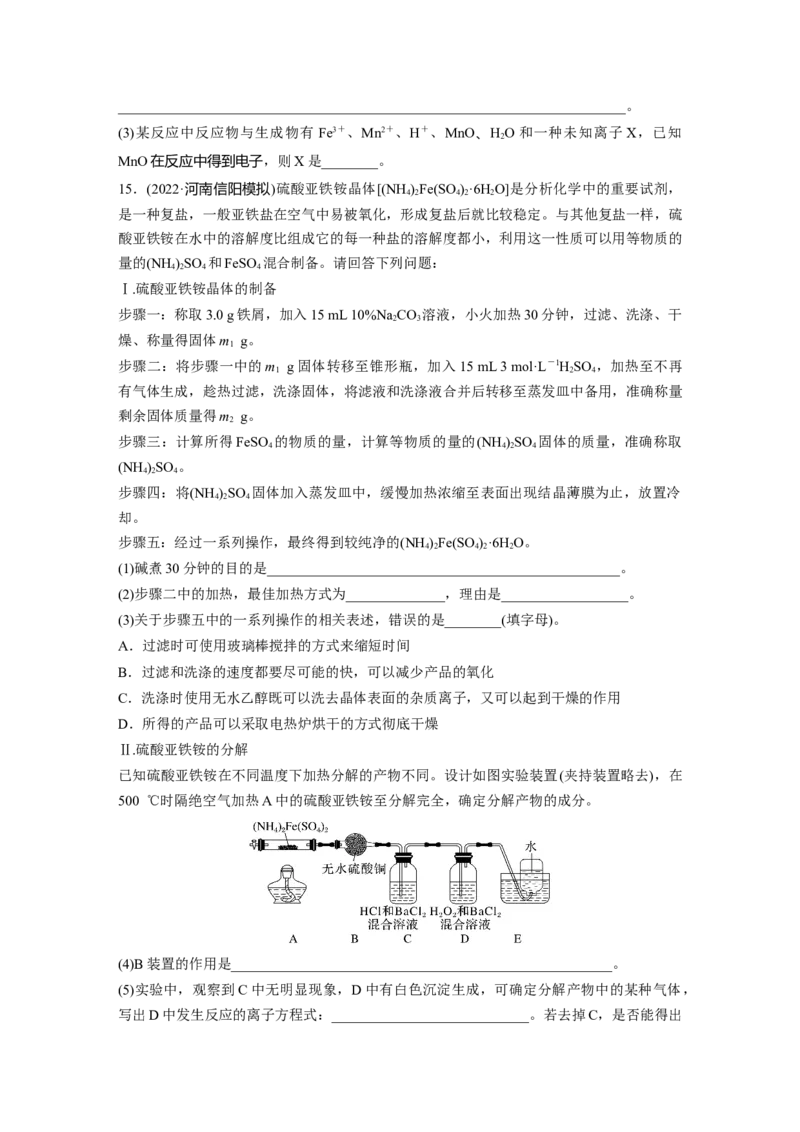
Ⅱ.硫酸亚铁铵的分解
已知硫酸亚铁铵在不同温度下加热分解的产物不同。设计如图实验装置(夹持装置略去),在
500 ℃时隔绝空气加热A中的硫酸亚铁铵至分解完全,确定分解产物的成分。
(4)B装置的作用是______________________________________________________。
(5)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定分解产物中的某种气体,
写出D中发生反应的离子方程式:____________________________。若去掉C,是否能得出同样结论,并解释其原因: _______________________________________________
________________________________________________________________________。
(6)A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为 Fe O 而不含
2 3
FeO。请填写表中的实验现象。
实验步骤 实验现象 结论
①取少量A中残留物于试管中,加入
适量稀硫酸,充分振荡使其完全溶
固体残留物仅为Fe O
2 3
解;②将溶液分成两份,分别滴加高
锰酸钾溶液、KSCN溶液