文档内容
第 15 讲 铁及其氧化物和氢氧化物
[复习目标] 1.掌握铁的主要性质及应用。2.知道不同价态的铁的氧化物的主要性质和用途。
3.掌握Fe(OH) 、Fe(OH) 的性质及Fe(OH) 的制备方法。
2 3 2
考点一 铁及其氧化物
1.铁单质
(1)铁的物理性质
______色固体,熔点较高,具有良好的导热、导电、延展性,能被______吸引。
(2)铁的原子结构
Fe的价层电子排布式为______,铁位于元素周期表的第____周期第____族,是应用最广泛
的过渡金属元素,其原子结构示意图:____________________________________________。
(3)铁的化学性质
铁比较活泼,还原性较强,失去电子后生成____价或____价的铁。重要的化学反应为
2.铁的氧化物
(1)物理性质
化学式 FeO Fe O Fe O
2 3 3 4俗名 铁红 磁性氧化铁
颜色状态 ______粉末 ______粉末 ______晶体(有磁性)
水溶性
铁的化合价
(2)化学性质
①FeO、Fe O 都属于碱性氧化物,能溶于强酸,分别写出它们溶于盐酸的离子方程式:
2 3
________________________,______________________________________。
② 铁 的 氧 化 物 还 能 被 CO 、 Al 还 原 , 以 氧 化 铁 为 例 写 出 化 学 方 程 式 :
________________________________________________________________________,
________________________________________________________________________。
③分别写出 Fe O 溶于足量稀硝酸、氢碘酸(HI)的离子方程式:______________、
3 4
___________。
1.铁的化学性质比较活泼,所以铁在自然界中全部以化合态形式存在( )
2.Fe分别与Cl 和盐酸反应所得氯化物相同( )
2
3.常温下可用铁制容器储存、运输浓硝酸、浓硫酸( )
4.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe O( )
3 4
一、铁及其氧化物的性质与应用
1.下列叙述正确的是( )
A.Fe与I 反应生成FeI
2 3
B.硫酸铜溶液中加入少量铁粉反应的离子方程式:3Cu2++2Fe===2Fe3++3Cu
C.5.6 g Fe与足量的S反应转移的电子数为0.3N
A
D.高温下水蒸气与Fe反应,固体的质量增加
2.化学让生活更美好。下列说法不正确的是( )
A.钢铁使用要尽可能减少钢铁的氧化损耗,Fe O 是一种碱性氧化物
2 3
B.常温下,铁的氧化物都不溶于水,也不与水反应
C.故宫是中国最大的古代文化艺术博物馆,氧化铁可作故宫红色外墙的涂料
D.氧化亚铁在空气中加热会被迅速氧化成三氧化二铁
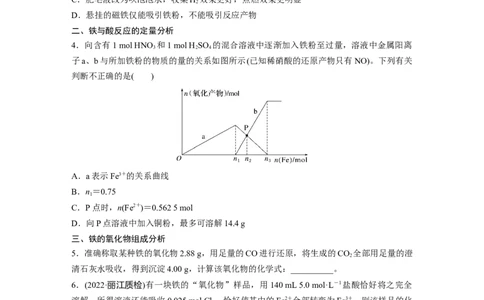
3.铁与水蒸气反应实验改进前后的装置如图所示:下列说法错误的是( )
A.将湿棉花改为浸水的尿不湿,酒精灯由单头改为双头,可提供足量的水蒸气
B.用具支试管可将试管口附近冷凝的水导出,避免冷凝水与灼热铁粉接触
C.肥皂液改为吹泡泡水,收集H 效果更好,点燃效果更明显
2
D.悬挂的磁铁仅能吸引铁粉,不能吸引反应产物
二、铁与酸反应的定量分析
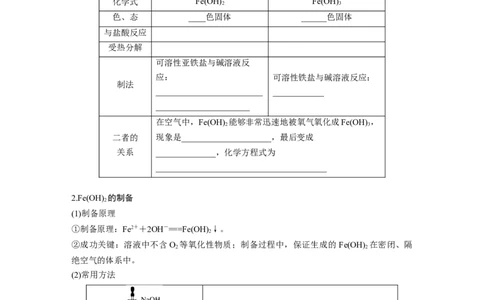
4.向含有1 mol HNO 和1 mol H SO 的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离
3 2 4
子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关
判断不正确的是( )
A.a表示Fe3+的关系曲线
B.n=0.75
1
C.P点时,n(Fe2+)=0.562 5 mol
D.向P点溶液中加入铜粉,最多可溶解14.4 g
三、铁的氧化物组成分析
5.准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO 全部用足量的澄
2
清石灰水吸收,得到沉淀4.00 g,计算该氧化物的化学式:__________。
6.(2022·丽江质检)有一块铁的“氧化物”样品,用140 mL 5.0 mol·L-1盐酸恰好将之完全
溶解,所得溶液还能吸收0.025 mol Cl ,恰好使其中的Fe2+全部转变为Fe3+,则该样品的化
2
学式可能为_________________________________________________。
确定铁的氧化物组成的基本方法
设铁的氧化物中铁元素与氧元素的质量比为m∶n,则氧化物中n(Fe)∶n(O)=∶=a∶b,
若a∶b=1∶1,则铁的氧化物为FeO;
若a∶b=2∶3,则铁的氧化物为Fe O;
2 3
若a∶b=3∶4,则铁的氧化物是Fe O 或FeO与Fe O 按物质的量之比为1∶1组成的混合物
3 4 2 3或FeO、Fe O、Fe O 的混合物(其中FeO、Fe O 的物质的量之比为1∶1,Fe O 的物质的量
2 3 3 4 2 3 3 4
为任意值)。
考点二 铁的氢氧化物
1.氢氧化铁和氢氧化亚铁的比较
化学式 Fe(OH) Fe(OH)
2 3
色、态 ____色固体 ______色固体
与盐酸反应
受热分解
可溶性亚铁盐与碱溶液反
应: 可溶性铁盐与碱溶液反应:
制法
_________________________ ____________
______________________
在空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,
2 3
二者的 现象是_____________________,最后变成
关系 ______________,化学方程式为
________________________________________
2.Fe(OH) 的制备
2
(1)制备原理
①制备原理:Fe2++2OH-===Fe(OH) ↓。
2
②成功关键:溶液中不含O 等氧化性物质;制备过程中,保证生成的 Fe(OH) 在密闭、隔
2 2
绝空气的体系中。
(2)常用方法
将吸有NaOH溶液的胶头滴管插到FeSO 溶液液
4
面以下,并在液面上覆盖一层苯或煤油(不能用
CCl ),以防止____________________发生反应
4
有机覆盖层法
先在装置Ⅰ中生成FeSO 溶液,并利用生成的H
4 2
将装置内的________排尽后,再把______溶液压
入装置Ⅱ中与________混合,这样可长时间观察
到白色沉淀还原性气体保护法
用铁作阳极,电解NaCl(或NaOH)溶液,并在液面
上覆盖苯(或煤油)
电解法
1.在空气中,白色的Fe(OH) 迅速转变成灰绿色,最终变成红褐色( )
2
2.FeCl 溶液滴入热的浓NaOH溶液中可得到Fe(OH) 胶体( )
3 3
3.Fe(OH) 与HNO 发生反应的离子方程式为Fe(OH) +2H+===Fe2++2HO( )
2 3 2 2
4.Fe(OH) 与氢碘酸反应生成FeI( )
3 3
5.Fe(OH) 呈红褐色、透明,能产生丁达尔效应( )
3
6.Fe(OH) 在空气中加热分解生成Fe O,则Fe(OH) 在空气中加热分解生成FeO( )
3 2 3 2
7.制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色
的氢氧化亚铁( )
氢氧化亚铁制备实验探究
1.用FeSO 溶液与不含O 的蒸馏水配制的NaOH溶液反应制备Fe(OH) 。
4 2 2
(1)用硫酸亚铁晶体配制上述FeSO 溶液时还需要加入________________。
4
(2)除去蒸馏水中溶解的O 常采用______的方法。
2
(3)生成Fe(OH) 白色沉淀的操作是用长滴管吸取不含O 的NaOH溶液,插入FeSO 溶液液
2 2 4
面 下 , 再 挤 出 NaOH 溶 液 , 这 样 操 作 的 理 由 是
________________________________________
_______________________________________________________________________________
。
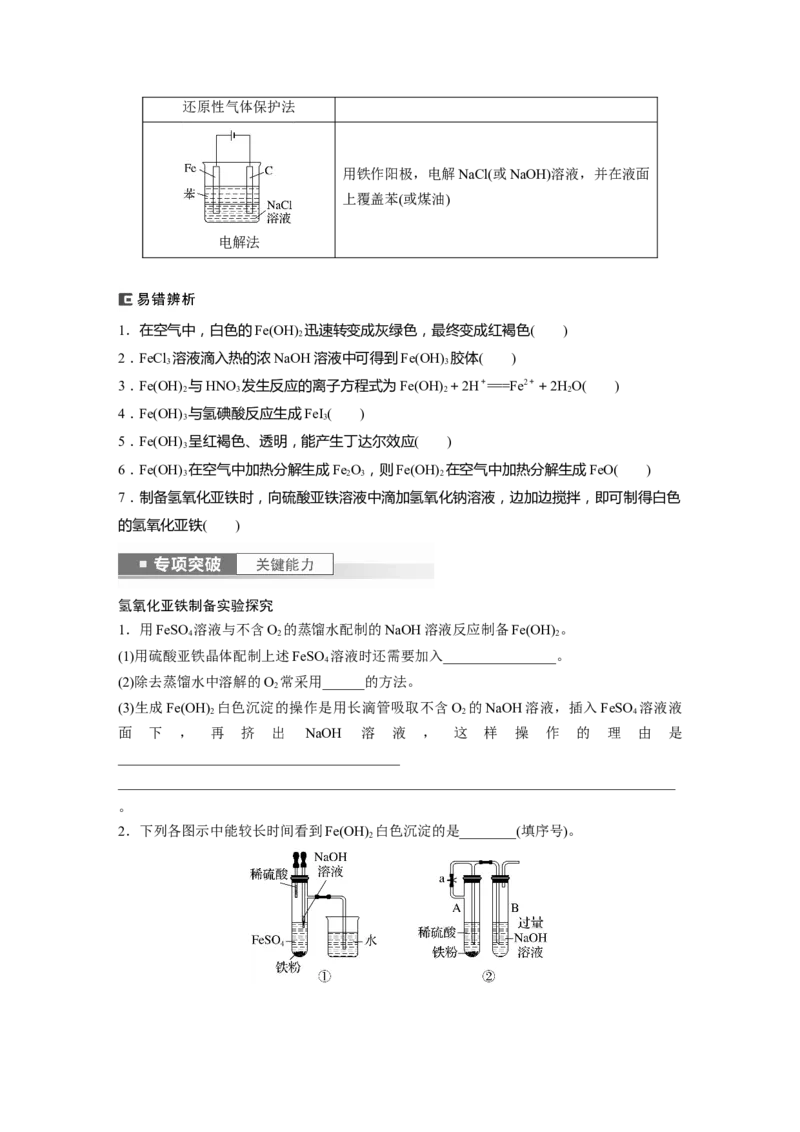
2.下列各图示中能较长时间看到Fe(OH) 白色沉淀的是________(填序号)。
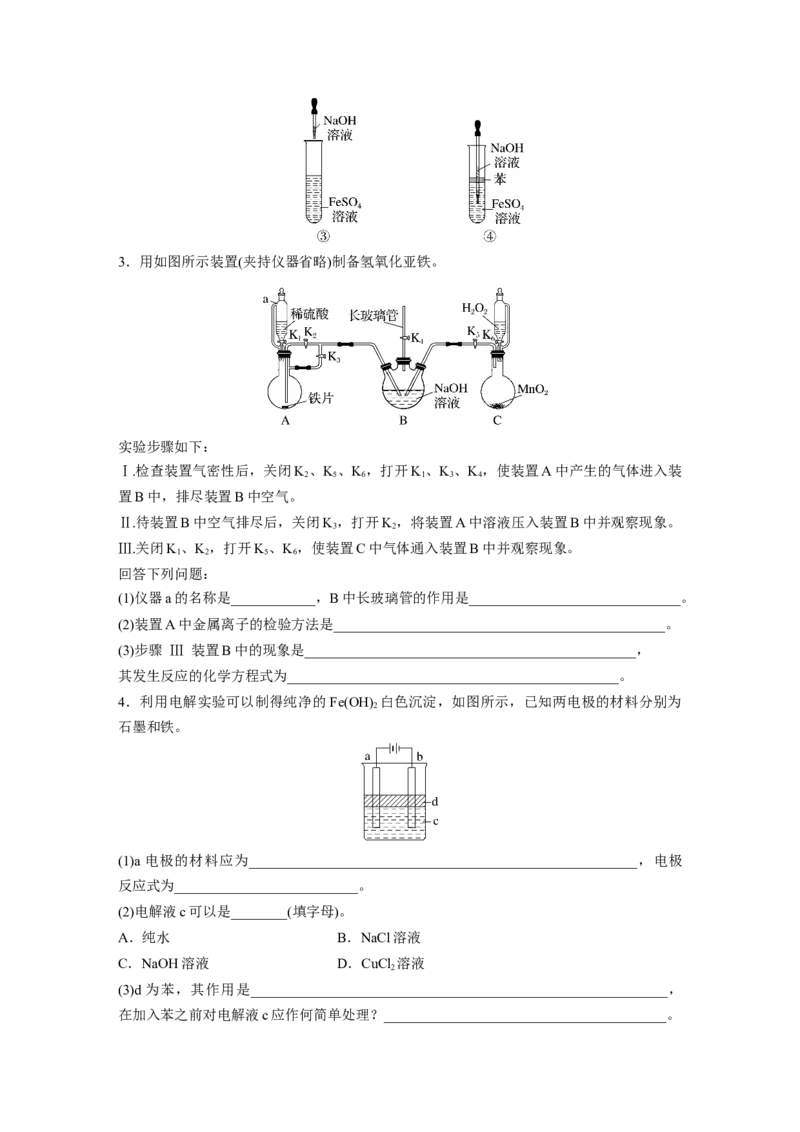
23.用如图所示装置(夹持仪器省略)制备氢氧化亚铁。
实验步骤如下:
Ⅰ.检查装置气密性后,关闭K 、K 、K ,打开K 、K 、K ,使装置A中产生的气体进入装
2 5 6 1 3 4
置B中,排尽装置B中空气。
Ⅱ.待装置B中空气排尽后,关闭K,打开K,将装置A中溶液压入装置B中并观察现象。
3 2
Ⅲ.关闭K、K,打开K、K,使装置C中气体通入装置B中并观察现象。
1 2 5 6
回答下列问题:
(1)仪器a的名称是____________,B中长玻璃管的作用是______________________________。
(2)装置A中金属离子的检验方法是_______________________________________________。
(3)步骤 Ⅲ 装置B中的现象是_______________________________________________,
其发生反应的化学方程式为_______________________________________________。
4.利用电解实验可以制得纯净的Fe(OH) 白色沉淀,如图所示,已知两电极的材料分别为
2
石墨和铁。
(1)a电极的材料应为_______________________________________________________,电极
反应式为__________________________。
(2)电解液c可以是________(填字母)。
A.纯水 B.NaCl溶液
C.NaOH溶液 D.CuCl 溶液
2
(3)d为苯,其作用是___________________________________________________________,
在加入苯之前对电解液c应作何简单处理?________________________________________。(4)若c用NaSO 溶液,当电解一段时间后看到白色Fe(OH) 沉淀,再反接电源电解,除了
2 4 2
电 极 上 看 到 气 泡 外 , 另 一 明 显 现 象 为
_________________________________________________。
1.下列叙述不正确的是( )
A.浓硝酸与铁在常温下不反应,所以可用铁质容器贮运浓硝酸(2022·浙江6月选考,9C)
B.工人将模具干燥后再注入熔融钢水,是因为铁与HO高温下会反应(2022·广东,6C)
2
C.将废铁屑加入FeCl 溶液中,可用于除去工业废气中的Cl(2019·天津,3A)
2 2
D.铁锈的主要成分可表示为Fe O·nHO(2020·浙江1月选考,9B)
2 3 2
2.下列关于铁及其化合物的说法正确的是( )
A.FeS 在沸腾炉中与O 反应主要生成SO (2020·浙江7月选考,12C)
2 2 3
B.Mg加入到过量FeCl 溶液中可得Fe(2020·浙江7月选考,12B)
3
C.钢铁在潮湿空气中生锈主要是发生了电化学腐蚀(2020·浙江7月选考,8D)
D.室温下,Fe与浓HSO 反应生成FeSO (2020·江苏,6D)
2 4 4