文档内容
1.我国清代《本草纲目拾遗》中叙述了“铁线粉”:“粤中洋行有舶上铁丝,……日久起
销,用刀刮其销,……,所刮下之销末,名铁线粉”。这里的“铁线粉”是指( )
A.Fe B.FeCl C.FeO D.Fe O
3 2 3
2.用铁制备较纯净的氧化铁,下列实验方案最好的是( )
A.使铁在潮湿的空气中缓慢氧化
B.铁在氯气中燃烧,加水溶解,加入足量NaOH溶液,过滤、洗涤,然后充分加热分解
C.使铁溶解于稀硫酸,然后加入足量NaOH溶液,过滤、洗涤,然后充分加热分解
D.使铁与足量稀硝酸反应,然后加入足量NaOH溶液,过滤、洗涤,然后充分加热分解
3.下列关于氧化铁、氧化亚铁、四氧化三铁三种氧化物的说法不正确的是( )
A.铁元素的化合价不完全相同
B.氧元素的化合价完全相同
C.氧化亚铁俗称铁红,为红棕色固体
D.铁在氧气中燃烧的产物为黑色固体
4.在100 mL 1.00 mol·L-1 HSO 溶液中加入足量铁屑,生成的气体在标准状况下的体积为(
2 4
)
A.11.2 L B.6.72 L C.4.48 L D.2.24 L
5.某同学设计的制备氯化铁溶液的方案中,分别采用下列物品,其中能实现的是( )
A.氢氧化铁和硫酸 B.铁和盐酸
C.氧化亚铁和盐酸 D.氧化铁和盐酸
6.实验过程中不可能产生 Fe(OH) 的是( )
3
A.蒸发 FeCl 溶液
3
B.FeCl 溶液中滴入氨水
3
C.将水蒸气通过灼热的铁
D.FeCl 溶液中滴入 NaOH 溶液
2
7.用饱和氯化铁溶液制取氢氧化铁胶体,正确的操作是( )
A.将饱和氯化铁溶液滴入蒸馏水中即可
B.将饱和氯化铁溶液滴入热水中,至溶液呈深黄色
C.将饱和氯化铁溶液滴入沸水中,继续煮沸至溶液呈红褐色
D.将饱和氯化铁溶液滴入沸水中,并继续加热煮沸至生成红褐色沉淀
8.下列有关铁及其化合物的说法正确的是( )
A.Fe(OH) 易被氧化成Fe(OH) ,说明稳定性:Fe(OH) <Fe(OH)
2 3 2 3
B.铁是较活泼的金属,它与卤素单质(X )反应的生成物均为FeX
2 3C.氢氧化铁与氢碘酸反应:Fe(OH) +3HI===FeI+3HO
3 3 2
D.铁与水蒸气在高温下的反应产物为Fe O 和H
2 3 2
9.混合下列各组物质使之充分反应,加热蒸干产物并在 300 ℃下灼烧至质量不变,最终残
留固体不是纯净物的是( )
A.向红褐色的Fe(OH) 固体中加入过量盐酸
3
B.等物质的量浓度、等体积的(NH )SO 与BaCl 溶液
4 2 4 2
C.等物质的量的NaHCO 与NaO 固体溶于水
3 2 2
D.向NaBr溶液中通入过量氯气
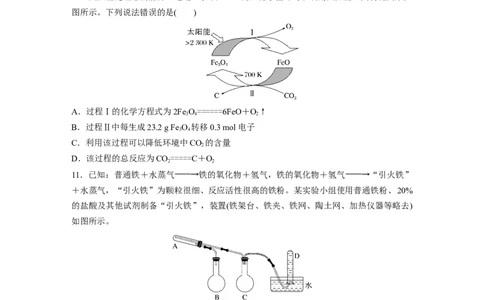
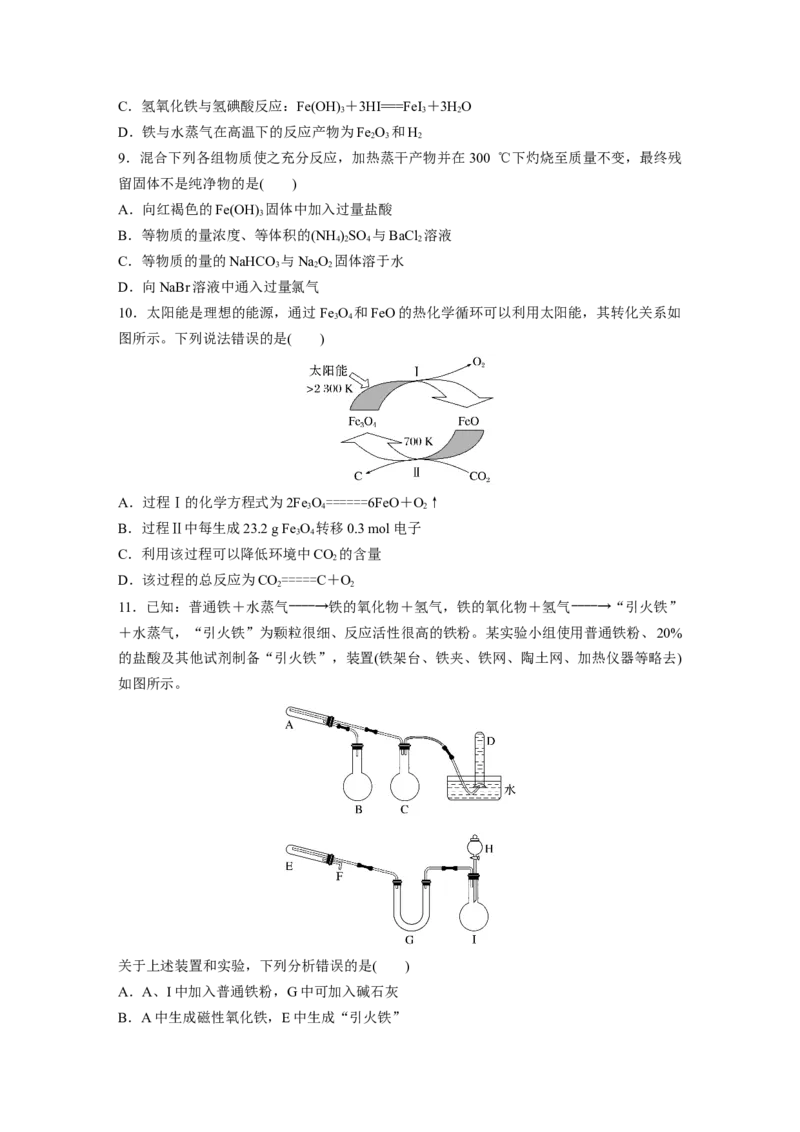
10.太阳能是理想的能源,通过Fe O 和FeO的热化学循环可以利用太阳能,其转化关系如
3 4
图所示。下列说法错误的是( )
A.过程Ⅰ的化学方程式为2Fe O======6FeO+O↑
3 4 2
B.过程Ⅱ中每生成23.2 g Fe O 转移0.3 mol电子
3 4
C.利用该过程可以降低环境中CO 的含量
2
D.该过程的总反应为CO=====C+O
2 2
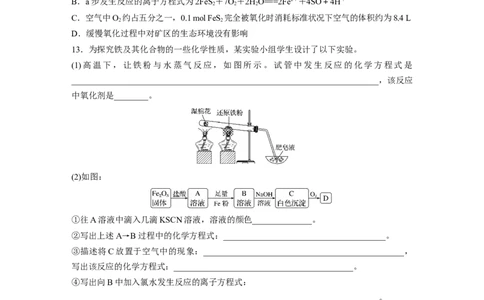
11.已知:普通铁+水蒸气――――→铁的氧化物+氢气,铁的氧化物+氢气――――→“引火铁”
+水蒸气,“引火铁”为颗粒很细、反应活性很高的铁粉。某实验小组使用普通铁粉、20%
的盐酸及其他试剂制备“引火铁”,装置(铁架台、铁夹、铁网、陶土网、加热仪器等略去)
如图所示。
关于上述装置和实验,下列分析错误的是( )
A.A、I中加入普通铁粉,G中可加入碱石灰
B.A中生成磁性氧化铁,E中生成“引火铁”C.需要加热的仪器只有A、E
D.D用于收集氢气
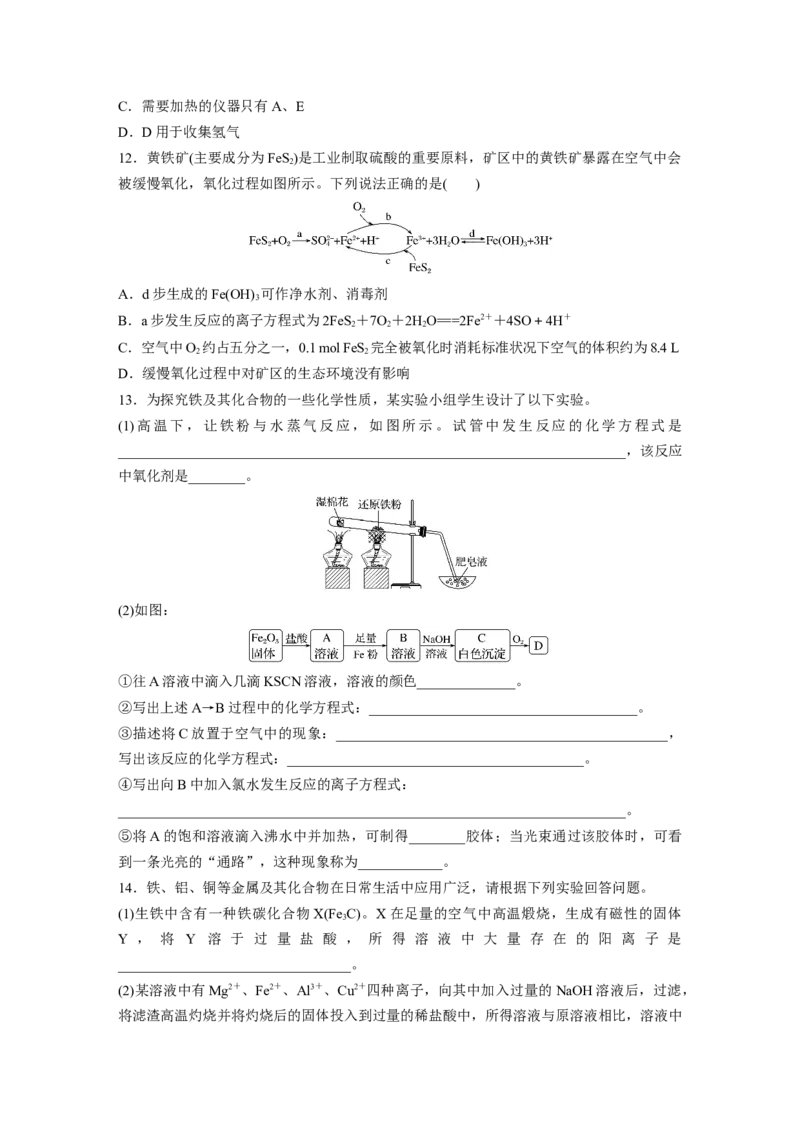
12.黄铁矿(主要成分为FeS)是工业制取硫酸的重要原料,矿区中的黄铁矿暴露在空气中会
2
被缓慢氧化,氧化过程如图所示。下列说法正确的是( )
A.d步生成的Fe(OH) 可作净水剂、消毒剂
3
B.a步发生反应的离子方程式为2FeS+7O+2HO===2Fe2++4SO+4H+
2 2 2
C.空气中O 约占五分之一,0.1 mol FeS 完全被氧化时消耗标准状况下空气的体积约为8.4 L
2 2
D.缓慢氧化过程中对矿区的生态环境没有影响
13.为探究铁及其化合物的一些化学性质,某实验小组学生设计了以下实验。
(1)高温下,让铁粉与水蒸气反应,如图所示。试管中发生反应的化学方程式是
________________________________________________________________________,该反应
中氧化剂是________。
(2)如图:
①往A溶液中滴入几滴KSCN溶液,溶液的颜色______________。
②写出上述A→B过程中的化学方程式:______________________________________。
③描述将C放置于空气中的现象:_______________________________________________,
写出该反应的化学方程式:__________________________________________。
④写出向B中加入氯水发生反应的离子方程式:
________________________________________________________________________。
⑤将A的饱和溶液滴入沸水中并加热,可制得________胶体;当光束通过该胶体时,可看
到一条光亮的“通路”,这种现象称为____________。
14.铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题。
(1)生铁中含有一种铁碳化合物X(Fe C)。X在足量的空气中高温煅烧,生成有磁性的固体
3
Y , 将 Y 溶 于 过 量 盐 酸 , 所 得 溶 液 中 大 量 存 在 的 阳 离 子 是
_________________________________。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+四种离子,向其中加入过量的NaOH溶液后,过滤,
将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是________(填字母)。
A.Mg2+ B.Fe2+
C.Al3+ D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备氧化铁的流程如图:
操作Ⅰ的名称是____________,操作Ⅱ的名称是________。
(4)有些同学认为用酸性KMnO 溶液滴定也能进行铁元素含量的测定,其反应如下:5Fe2++
4
MnO+8H+===5Fe3++Mn2++4HO。
2
a.称取2.85 g绿矾(FeSO ·7H O)产品,溶解,配制成250 mL一定物质的量浓度的溶液;
4 2
b.量取25.00 mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.010 00 mol·L-1 KMnO 溶液滴定至终点,消耗KMnO 溶液体积的平均值
4 4
为20.00 mL。
①实验前,首先要精确配制一定物质的量浓度的KMnO 溶液250 mL,配制时需要的仪器除
4
天 平 、 玻 璃 棒 、 烧 杯 、 胶 头 滴 管 外 , 还 需
______________________________________________。
②上述样品中FeSO ·7H O的质量分数为__________________________________(保留3位有
4 2
效数字)。
15.某化学兴趣小组拟用如图装置制备氢氧化亚铁并观察其颜色。提供化学药品:铁粉、稀
硫酸、氢氧化钠溶液。
(1)稀硫酸应放在________(填写仪器编号)中。
(2)本实验通过控制A、B、C三个开关,将仪器中的空气排尽后,再关闭开关________、打
开开关________,就可观察到氢氧化亚铁的颜色。试分析实验开始时排尽装置中空气的理由:
________________________________________________________________________。
(3) 实 验 时 为 防 止 仪 器 2 中 铁 粉 通 过 导 管 进 入 仪 器 3 中 , 可 采 取 的 措 施 是
________________________________________________________________________。
(4)在FeSO 溶液中加入(NH )SO 固体可制备硫酸亚铁铵晶体[(NH )Fe(SO )·6H O](式量为
4 4 2 4 4 2 4 2 2
392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。①为洗涤(NH )Fe(SO )·6H O粗产品,下列方法中最合适的是________(填字母)。
4 2 4 2 2
A.用冷水洗
B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗
D.用90%的乙醇溶液洗
②为了测定产品的纯度,称取a g产品溶于水,配制成500 mL溶液,用浓度为c mol·L-1
的酸性KMnO 溶液滴定。每次所取待测液体积均为25.00 mL,实验结果记录如下:
4
实验次数 第一次 第二次 第三次
消耗高锰酸钾溶液体积/mL 25.52 25.02 24.98
则该产品纯度为__________________。上表中第一次实验中记录数据明显大于后两次,其原
因可能是________(填字母)。
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低