文档内容
第 14 讲 侯氏制碱法与 Na CO 含量的测定
2 3
[复习目标] 1.了解侯氏制碱法的原理。2.掌握NaCO 含量的测定方法。
2 3
考点一 侯氏制碱法
1.制备原料
食盐、氨、二氧化碳——合成氨厂用水煤气制取氢气时的废气,其反应为 C+
HO(g)=====CO+H,CO+HO(g)=====CO+H。
2 2 2 2 2
2.工艺流程
3.反应原理
(1)产生NaHCO 的反应:_______________________________________________________。
3
(2)产生NaCO 的反应: _______________________________________________________。
2 3
4.绿色思想
循环使用的物质为________、________。
1. 如图是模拟“侯氏制碱法”制取NaHCO 的部分装置。
3
(1)实验时向饱和食盐水中通入CO、NH 的先后顺序是____________________________。
2 3
(2)a通入__________,然后b通入____________,简述理由:______________________
____________________________________________________________________________。
(3)c中放蘸有稀硫酸的脱脂棉,作用是_______________________________________
________________________________________________________________________。2.我国化学家侯德榜改进国外的纯碱生产工艺,生产流程可简要表示如图:
(1)分别写出沉淀池、煅烧炉中发生反应的化学方程式。
________________________________________________________________________________
________________________________________________________________________________
(2)写出上述流程中X物质的分子式。
________________________________________________________________________________
(3)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品。通氨气除了增大 NH的浓度,
使NH Cl更多地析出外,还有什么作用?循环Ⅰ的作用是什么?
4
________________________________________________________________________________
________________________________________________________________________________
(4)如何检验产品碳酸钠中是否含有碳酸氢钠?
________________________________________________________________________________
________________________________________________________________________________
考点二 Na CO 含量的测定方法
2 3
1.气体法
(1)测定原理:NaCO+HSO ===NaSO +HO+CO↑。
2 3 2 4 2 4 2 2
依据CO 的体积确定NaCO 的物质的量,进而确定纯碱中NaCO 的含量。
2 2 3 2 3
(2)实验操作:向m g纯碱样品中加入足量的稀硫酸,准确测量产生的CO 气体的体积为
2
V mL(已折算为标准状况)。
(3)数据处理:纯碱样品中NaCO 的质量为 mol×106 g·mol-1= g,则纯碱样品中NaCO
2 3 2 3
的质量分数为×100%=%。
2.沉淀法
(1)测定原理:NaCO+BaCl ===BaCO ↓+2NaCl。
2 3 2 3
依据BaCO 沉淀的质量确定NaCO 的物质的量,进而确定纯碱中NaCO 的含量。
3 2 3 2 3
(2)实验操作:先将m g纯碱样品溶于水配成溶液,向溶液中加入过量的BaCl 溶液,经过滤、
2
洗涤、干燥得BaCO 沉淀的质量为n g。
3
(3)数据处理:纯碱样品中NaCO 的质量为×106 g·mol-1= g,则纯碱样品中NaCO 的质
2 3 2 3量分数为×100%=×100%。
3.滴定法
测定原理(用酚酞作指示剂,用盐酸滴定):当指示剂变色时,发生的反应为 NaCO +
2 3
2HCl===2NaCl+HO+CO↑,根据消耗标准盐酸的体积,求出 NaCO 的物质的量,进一
2 2 2 3
步求其含量。
实验室欲测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数w(Na CO),称取此混合物5.0
2 3
g,溶于水中,配成250 mL溶液。
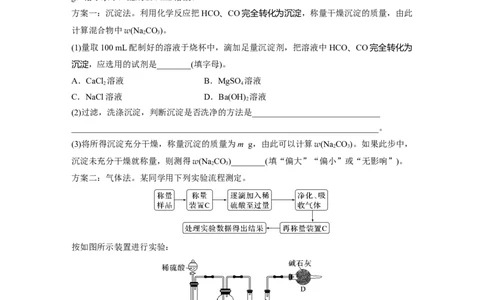
方案一:沉淀法。利用化学反应把HCO、CO完全转化为沉淀,称量干燥沉淀的质量,由此
计算混合物中w(Na CO)。
2 3
(1)量取100 mL配制好的溶液于烧杯中,滴加足量沉淀剂,把溶液中HCO、CO完全转化为
沉淀,应选用的试剂是________(填字母)。
A.CaCl 溶液 B.MgSO 溶液
2 4
C.NaCl溶液 D.Ba(OH) 溶液
2
(2)过滤,洗涤沉淀,判断沉淀是否洗净的方法是______________________________
________________________________________________________________________。
(3)将所得沉淀充分干燥,称量沉淀的质量为m g,由此可以计算w(Na CO)。如果此步中,
2 3
沉淀未充分干燥就称量,则测得w(Na CO)________(填“偏大”“偏小”或“无影响”)。
2 3
方案二:气体法。某同学用下列实验流程测定。
按如图所示装置进行实验:
(1)在装置C中装碱石灰来吸收净化后的气体,装置D的作用是_________________
________________________________________________________________________。
(2)有的同学认为,为了减小实验误差,应在反应前后都通入 N ,反应后通入N 的目的是
2 2
________________________________________________________________________
________________________________________________________________________。
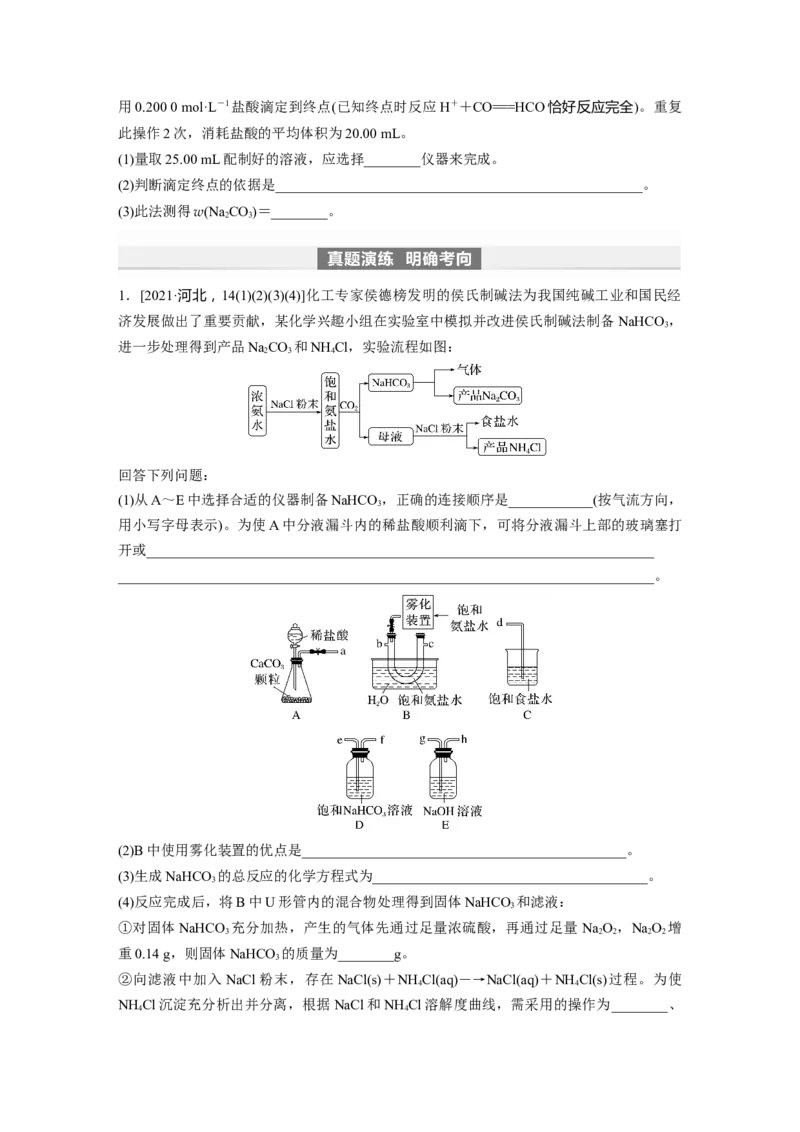
方案三:滴定法。量取25.00 mL配制好的溶液加入锥形瓶中,滴加 2滴酚酞溶液,摇匀,用0.200 0 mol·L-1盐酸滴定到终点(已知终点时反应H++CO===HCO恰好反应完全)。重复
此操作2次,消耗盐酸的平均体积为20.00 mL。
(1)量取25.00 mL配制好的溶液,应选择________仪器来完成。
(2)判断滴定终点的依据是____________________________________________________。
(3)此法测得w(Na CO)=________。
2 3
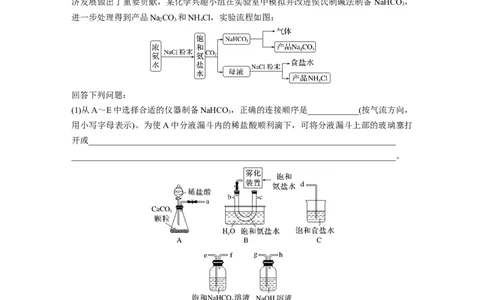
1.[2021·河北,14(1)(2)(3)(4)]化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经
济发展做出了重要贡献,某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备NaHCO ,
3
进一步处理得到产品NaCO 和NH Cl,实验流程如图:
2 3 4
回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO ,正确的连接顺序是____________(按气流方向,
3
用小写字母表示)。为使A中分液漏斗内的稀盐酸顺利滴下,可将分液漏斗上部的玻璃塞打
开或________________________________________________________________________
____________________________________________________________________________。
(2)B中使用雾化装置的优点是______________________________________________。
(3)生成NaHCO 的总反应的化学方程式为_______________________________________。
3
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO 和滤液:
3
①对固体NaHCO 充分加热,产生的气体先通过足量浓硫酸,再通过足量 NaO ,NaO 增
3 2 2 2 2
重0.14 g,则固体NaHCO 的质量为________g。
3
②向滤液中加入NaCl粉末,存在NaCl(s)+NH Cl(aq)―→NaCl(aq)+NH Cl(s)过程。为使
4 4
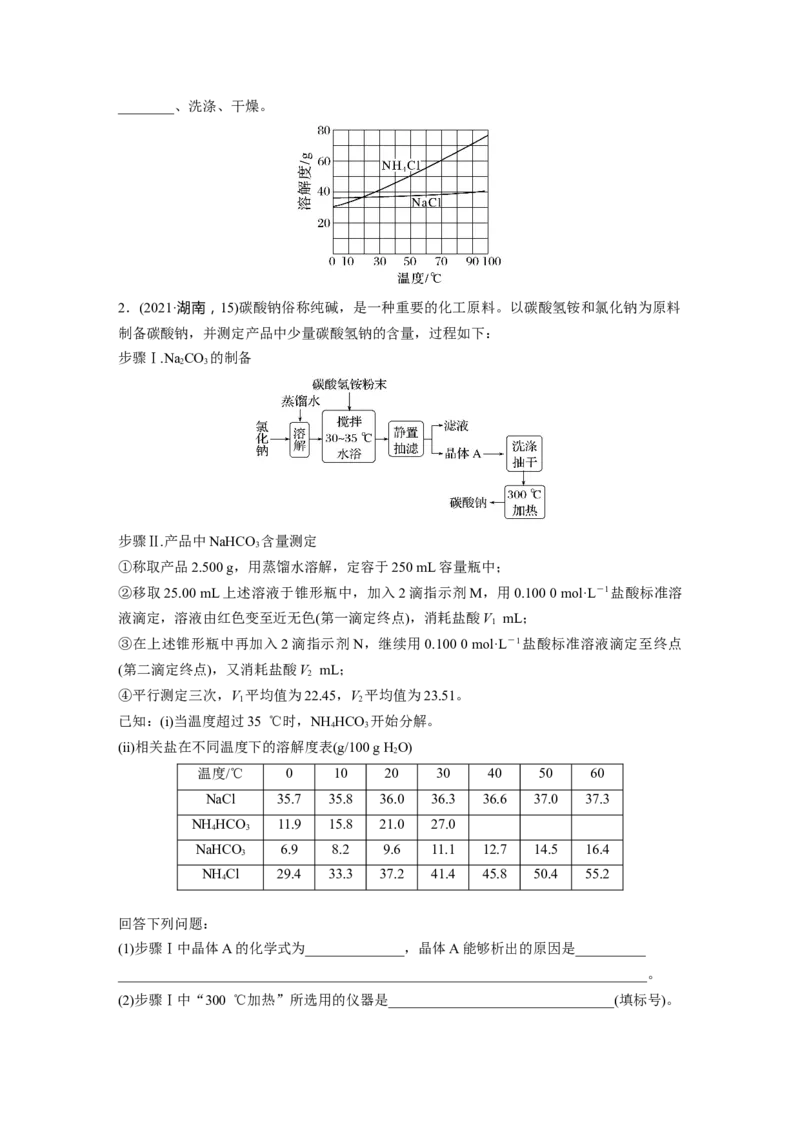
NH Cl沉淀充分析出并分离,根据NaCl和NH Cl溶解度曲线,需采用的操作为________、
4 4________、洗涤、干燥。
2.(2021·湖南,15)碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料
制备碳酸钠,并测定产品中少量碳酸氢钠的含量,过程如下:
步骤Ⅰ.Na CO 的制备
2 3
步骤Ⅱ.产品中NaHCO 含量测定
3
①称取产品2.500 g,用蒸馏水溶解,定容于250 mL容量瓶中;
②移取25.00 mL上述溶液于锥形瓶中,加入2滴指示剂M,用0.100 0 mol·L-1盐酸标准溶
液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸V mL;
1
③在上述锥形瓶中再加入2滴指示剂N,继续用0.100 0 mol·L-1盐酸标准溶液滴定至终点
(第二滴定终点),又消耗盐酸V mL;
2
④平行测定三次,V 平均值为22.45,V 平均值为23.51。
1 2
已知:(i)当温度超过35 ℃时,NH HCO 开始分解。
4 3
(ii)相关盐在不同温度下的溶解度表(g/100 g HO)
2
温度/℃ 0 10 20 30 40 50 60
NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3
NH HCO 11.9 15.8 21.0 27.0
4 3
NaHCO 6.9 8.2 9.6 11.1 12.7 14.5 16.4
3
NH Cl 29.4 33.3 37.2 41.4 45.8 50.4 55.2
4
回答下列问题:
(1)步骤Ⅰ中晶体A的化学式为______________,晶体A能够析出的原因是__________
___________________________________________________________________________。
(2)步骤Ⅰ中“300 ℃加热”所选用的仪器是________________________________(填标号)。(3) 指 示 剂 N 为 ______________ , 描 述 第 二 滴 定 终 点 前 后 颜 色 变 化 :
______________________。
(4)产品中NaHCO 的质量分数为____________(保留三位有效数字)。
3
(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则 NaHCO 质量分数的计算结果
3
________(填“偏大”“偏小”或“无影响”)。