文档内容
训练(三十七) 化学反应原理在物质制备中的调控作用
1.(2021·广西南宁二中检测)汽车尾气(含烃类、CO、NO与SO 等),是城市主要污染源之
2
一,治理的办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气
生态循环的无毒气体,反应原理:2NO(g)+2CO(g)===N (g)+2CO(g),在298 K、101 kPa下,
2 2
ΔH=-113 kJ/mol、ΔS=-145 J/(mol·K)。下列说法中错误的是( )
A.该反应中反应物的总能量高于生成物的总能量
B.该反应常温下不能自发进行,因此需要高温和催化剂
C.该反应常温下能自发进行,高温和催化剂只是加快反应的速率
D.汽车尾气中的这两种气体会与血红蛋白结合而使人中毒
B [该反应是放热反应,则反应物的总能量高于生成物的总能量,A项正确;在298 K、
101 kPa下,ΔH=-113 kJ/mol、ΔS=-145 J/(mol·K),则有ΔH-TΔS=(-113 kJ/mol)-298
K×[-0.145 kJ/(mol·K)]=-69.79 kJ/mol<0,该反应常温下能自发进行,高温和催化剂只是
加快反应的速率,B项错误,C项正确;NO、CO均会与血红蛋白结合而使人中毒,D项正确。]
2.(2021·安徽六校第一次联考)工业上可通过甲醇羰基化法制取甲酸甲酯(HCOOCH ):
3
CH
3
OH(g)+CO(g)⇌HCOOCH
3
(g)。在容积固定的密闭容器中,投入等物质的量CH
3
OH和
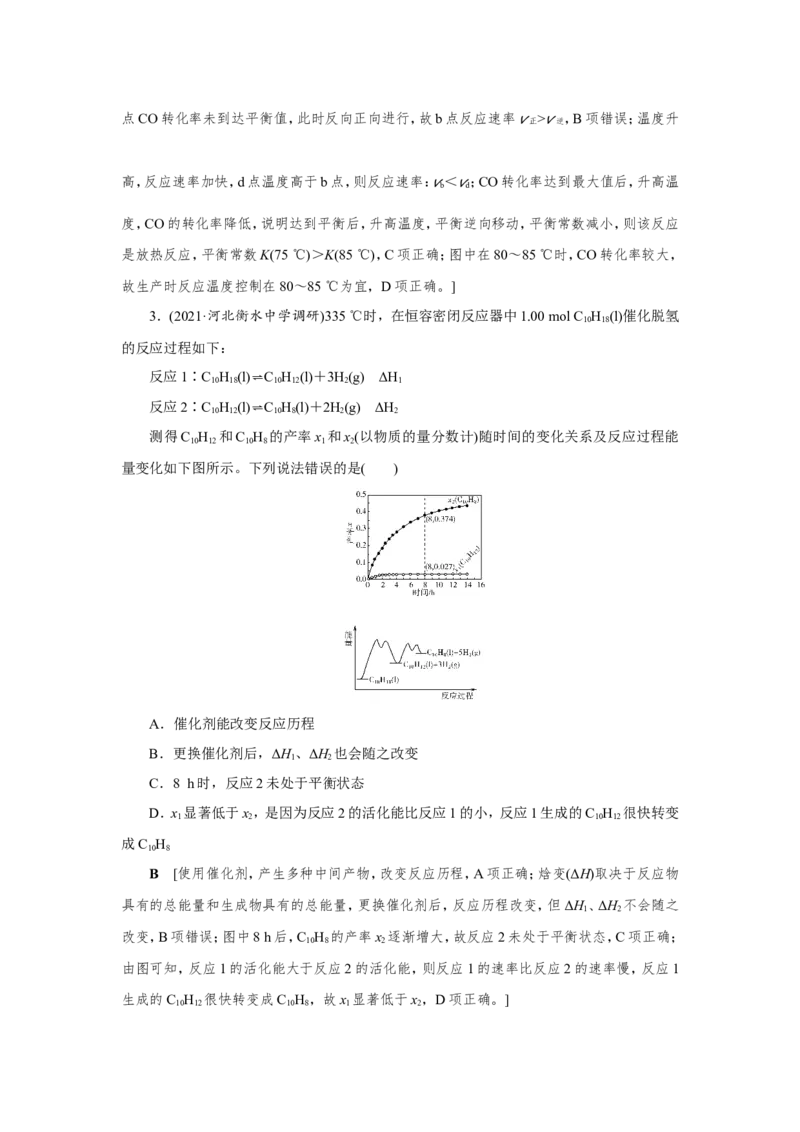
CO,测得相同时间内CO的转化率随温度变化如图所示。下列说法不正确的是( )
A.增大压强,甲醇转化率增大
B.b点反应速率
v正
=
v逆
C.平衡常数K(75 ℃)>K(85 ℃),反应速率:
vb
<
vd
D.生产时反应温度控制在80~85 ℃为宜
B [增大压强,平衡正向移动,甲醇转化率增大,A项正确;b点处于图中最高点左侧,b点CO转化率未到达平衡值,此时反向正向进行,故b点反应速率 v正 >v逆 ,B项错误;温度升
高,反应速率加快,d点温度高于b点,则反应速率:
vb
<
vd
;CO转化率达到最大值后,升高温
度,CO的转化率降低,说明达到平衡后,升高温度,平衡逆向移动,平衡常数减小,则该反应
是放热反应,平衡常数K(75 ℃)>K(85 ℃),C项正确;图中在80~85 ℃时,CO转化率较大,
故生产时反应温度控制在80~85 ℃为宜,D项正确。]
3.(2021·河北衡水中学调研)335 ℃时,在恒容密闭反应器中1.00 mol C H (l)催化脱氢
10 18
的反应过程如下:
反应1∶C
10
H
18
(l)⇌C
10
H
12
(l)+3H
2
(g) ΔH
1
反应2∶C
10
H
12
(l)⇌C
10
H
8
(l)+2H
2
(g) ΔH
2
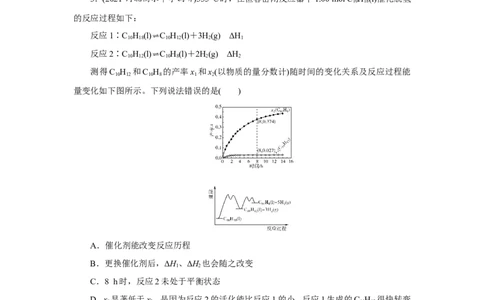
测得C H 和C H 的产率x 和x(以物质的量分数计)随时间的变化关系及反应过程能
10 12 10 8 1 2
量变化如下图所示。下列说法错误的是( )
A.催化剂能改变反应历程
B.更换催化剂后,ΔH、ΔH 也会随之改变
1 2
C.8 h时,反应2未处于平衡状态
D.x 显著低于x,是因为反应2的活化能比反应1的小,反应1生成的C H 很快转变
1 2 10 12
成C H
10 8
B [使用催化剂,产生多种中间产物,改变反应历程,A项正确;焓变(ΔH)取决于反应物
具有的总能量和生成物具有的总能量,更换催化剂后,反应历程改变,但ΔH、ΔH 不会随之
1 2
改变,B项错误;图中8 h后,C H 的产率x 逐渐增大,故反应2未处于平衡状态,C项正确;
10 8 2
由图可知,反应1的活化能大于反应2的活化能,则反应1的速率比反应2的速率慢,反应1
生成的C H 很快转变成C H,故x 显著低于x,D项正确。]
10 12 10 8 1 24.(2021·山东肥城检测)氢能作为新型能源,可利用CO制得,北京大学马丁教授等团队
向容积为V L的密闭容器中充入等物质的量的CO和HO进行反应。
2
已知:
反应Ⅰ:FeO(s)+CO(g)⇌Fe(s)+CO
2
(g) ΔH
1
反应Ⅱ:FeO(s)+H
2
(g)⇌Fe(s)+H
2
O(g) ΔH
2
反应Ⅲ:CO(g)+H
2
O(g)⇌CO
2
(g)+H
2
(g) ΔH
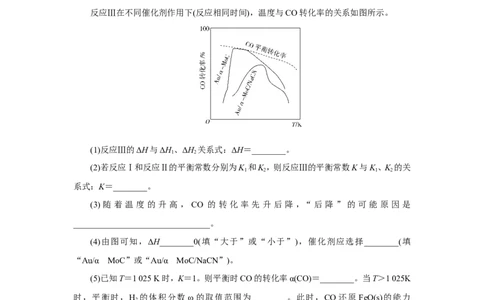
反应Ⅲ在不同催化剂作用下(反应相同时间),温度与CO转化率的关系如图所示。
(1)反应Ⅲ的ΔH与ΔH、ΔH 关系式:ΔH=________。
1 2
(2)若反应Ⅰ和反应Ⅱ的平衡常数分别为K 和K ,则反应Ⅲ的平衡常数K与K 、K 的关
1 2 1 2
系式:K=________。
(3) 随 着 温 度 的 升 高 , CO 的 转 化 率 先 升 后 降 ,“ 后 降 ” 的 可 能 原 因 是
________________________________。
(4)由图可知,ΔH________0(填“大于”或“小于”),催化剂应选择________(填
“Au/αMoC”或“Au/αMoC/NaCN”)。
(5)已知T=1 025 K时,K=1。则平衡时CO的转化率α(CO)=________。当T>1 025K
时,平衡时,H 的体积分数 ω 的取值范围为________。此时,CO 还原 FeO(s)的能力
2
________H(填“大于”或“小于”)。
2
(6)欲提高H 的体积分数,可采取的措施为________________________________。
2
解析 (1)由反应Ⅰ-Ⅱ可得反应Ⅲ,根据盖斯定律,则反应Ⅲ的ΔH=ΔH-ΔH 。
1 2
(2)由于反应Ⅰ-Ⅱ=Ⅲ,反应I和II的平衡常数分别为K 和K ,则反应Ⅲ的平衡常数为
1 2
K=。
(3)由图可知,催化剂的催化活性随温度先增大后减小,温度过高,催化剂的催化活性下
降,会引起CO的转化率降低。(4)由图可知,随着温度的升高,CO平衡转化率逐渐减小,说明升高温度,平衡逆向移动,
则该反应的ΔH<0。由图可知,催化剂Au/αMoC在较低温度时具有较高的催化活性,故催化
剂应选择Au/αMoC。
(5)起始时 CO 和 HO(g)的物质的量相等,假设均为 1 mol,由于反应 CO(g)+
2
H
2
O(g)⇌CO
2
(g)+H
2
(g)前后气体总分子数不变,平衡常数K=1,则平衡时四种物质的物质的
量均为0.5 mol,故CO的平衡转化率为×100%=50%。1 025 K时,H 的体积分数为25%;升
2
高温度,平衡向逆反应方向移动,平衡时H 的体积分数减小,但肯定大于0,故H 的体积分
2 2
数取值范围为0<ω<25%。
(6)欲提高H 的体积分数,可采取的措施有及时分离出CO,或降低温度等。
2 2
答案 (1)ΔH-ΔH (2)
1 2
(3)温度过高,催化剂的催化活性下降
(4)小于 Au/αMoC
(5)50% 0<ω<25% 小于
(6)及时分离出CO(或降低温度)
2
5.(2021·河北石家庄二中检测)苯乙烯 是生产各种塑料的重要单
体 , 可 通 过 乙 苯 催 化 脱 氢 制 得 :
ΔH=+123.5 kJ·mol-1。工业上,通常在乙苯(EB)蒸气中掺混N(原料气中乙苯和N 的物质
2 2
的量之比为1∶10,N 不参与反应),控制反应温度为600 ℃,并保持体系总压为0.1 MPa不
2
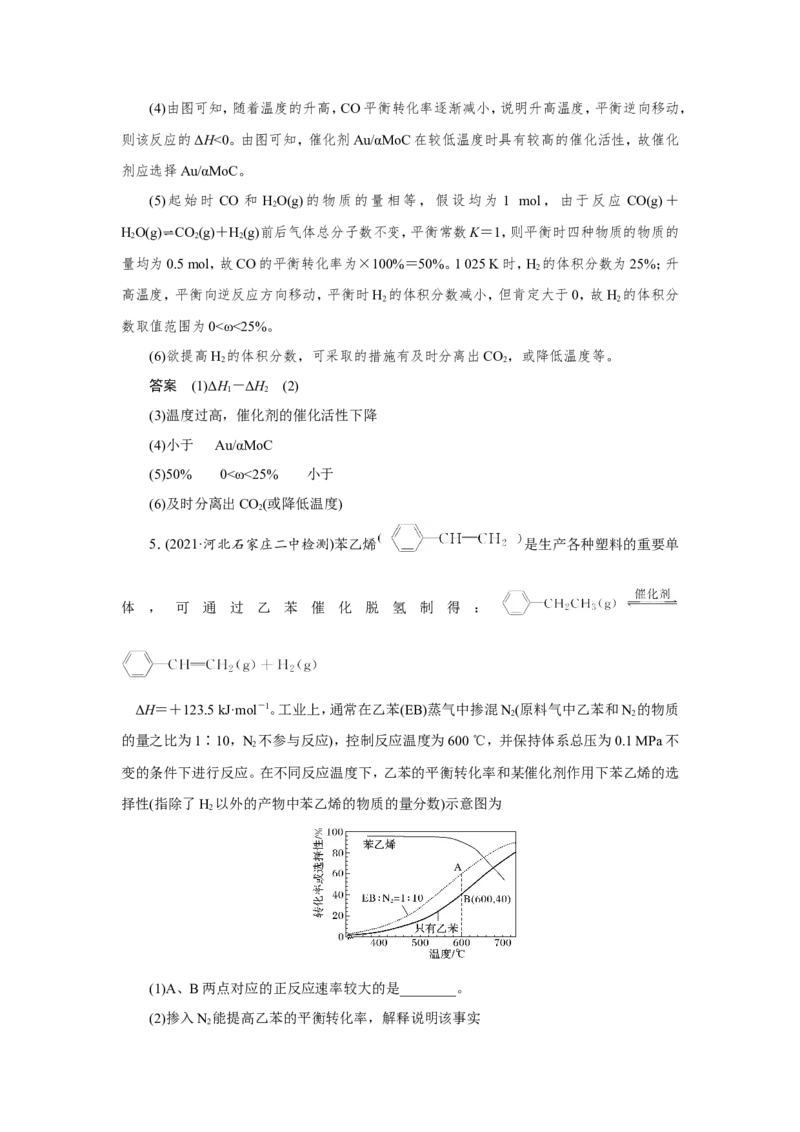
变的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选
择性(指除了H 以外的产物中苯乙烯的物质的量分数)示意图为
2
(1)A、B两点对应的正反应速率较大的是________。
(2)掺入N 能提高乙苯的平衡转化率,解释说明该事实
2________________________________________________________________________。
(3)用平衡分压代替平衡浓度计算600 ℃时的平衡常数K =________。(保留两位有效数
p
字,分压=总压×物质的量分数)
(4)控制反应温度为600 ℃的理由是____________________________________________
___________________________________________________________________________
。
解析 (1)由图可知,A、B两点对应的温度和压强都相同,A点是乙苯和氮气的混合气体,
B点是纯乙苯,则B点乙苯浓度大于A点,浓度越大反应速率越大,则正反应速率B点大于
A点。(2)该反应正反应气体分子数增加,加入氮气稀释,相当于减压,减小压强,化学平衡正
向移动,乙苯的转化率增大。(3)由图可知,反应温度为600 ℃,并保持体系总压为0.1 MPa时,
乙苯转化率为40%,设乙苯起始物质的量为1 mol,则依据题意可建立如下三段式:
1 0 0
0.4 0.4 0.4
0.6 0.4 0.4
平衡时总物质的量为1.4 mol,乙苯的平衡分压为×0.1 MPa,苯乙烯和氢气的平衡分压
为×0.1 MPa,则600 ℃时的平衡常数K =≈0.019。
p
答案 (1)B (2)正反应方向气体分子数增加,加入氮气稀释,相当于减压,平衡正向移
动 (3)0.019 (4)600 ℃时,乙苯的转化率和苯乙烯的选择性均较高。温度过低,反应速率慢,
转化率低;温度过高,选择性下降。高温还可能使催化剂失活,且能耗大