文档内容
1.下列关于硫的说法不正确的是( )
A.游离态的硫存在于火山口附近或地壳的岩层里
B.单质硫既有氧化性,又有还原性
C.试管内壁附着的硫可用二硫化碳溶解除去
D.硫与铁、铜反应,生成FeS、CuS
2.下列关于硫的叙述正确的是( )
A.硫的非金属性较强,在自然界中只以化合态存在
B.可用水溶解过滤分离硝酸钾和硫黄的混合物
C.硫与金属或非金属反应时都做氧化剂
D.硫的氧化性比氯气强
3.下列关于硫及其化合物的叙述正确的是( )
A.硫黄是一种易溶于水的黄色晶体
B.二氧化硫的水溶液显酸性
C.二氧化硫是黄色易溶于水的有毒气体
D.二氧化硫不稳定,极易转化为三氧化硫
4.下列说法错误的是( )
A.残留在试管内壁上的硫可用热的NaOH溶液除去
B.硫单质与变价金属反应时一般生成低价态的金属硫化物
C.汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理
D.单质硫或含硫物质燃烧时,氧气少量时生成SO ,氧气足量时生成SO
2 3
5.我国晋代《抱朴子》中描述了“丹砂(HgS)烧之成水银,积变又还成丹砂”。下列有关叙
述正确的是( )
A.“丹砂”和“水银”都是化合物
B.该描述中的反应是可逆反应
C.水银有恒定的体积膨胀系数,被用于制作温度计
D.“积变又还成丹砂”中的“还”可理解为“被还原”
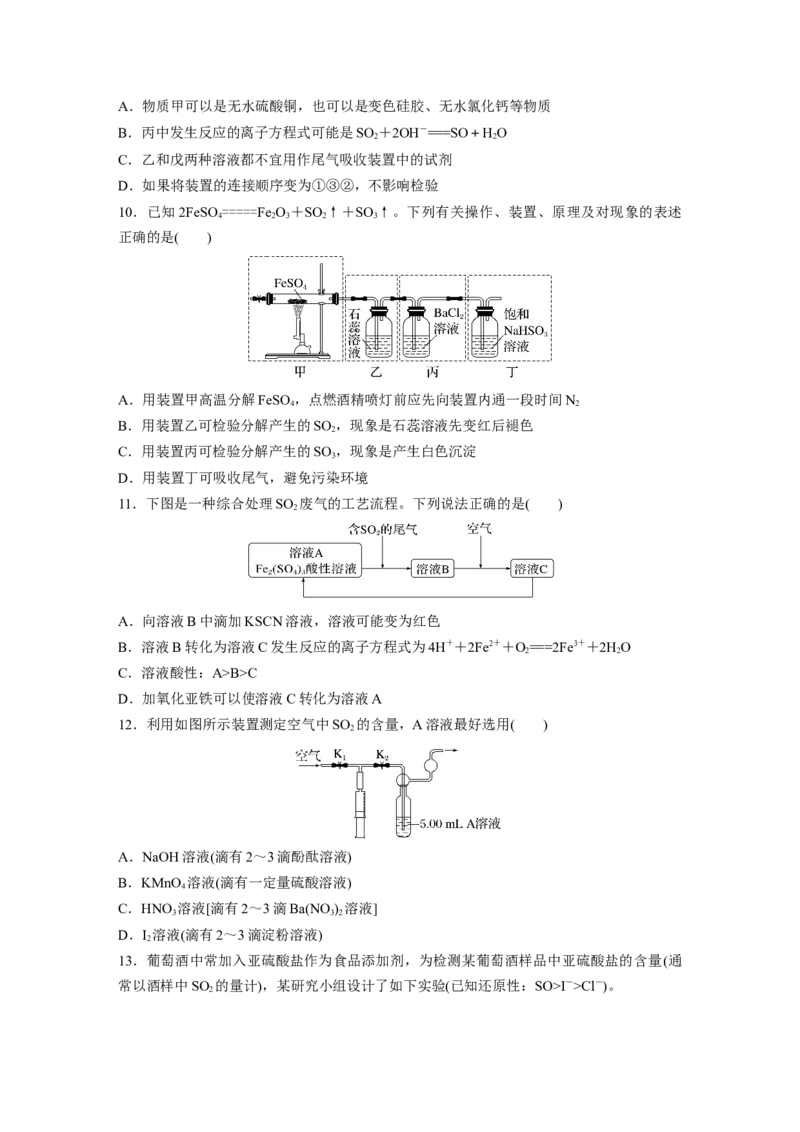
6.如图是硫元素在自然界中的循环示意图,下列说法不正确的是( )A.海水中的硫元素主要以S2-形式存在
B.煤中含有硫元素,燃煤中加入生石灰可脱硫
C.硫具有弱氧化性,和变价金属反应,通常将金属氧化成低价态
D.硫化氢溶于水得到氢硫酸,氢硫酸是弱酸,能与碱、碱性氧化物反应
7.食品、大气、工业尾气中的SO 均需严格检测或转化吸收,下列有关SO 的检测或吸收
2 2
方法正确的是( )
A.滴定法:用酸性KMnO 溶液滴定葡萄酒试样以测定葡萄酒中SO 的浓度
4 2
B.沉淀法:用Ba(OH) 溶液沉淀SO ,然后将沉淀在空气中洗涤、过滤、干燥、称重以测
2 2
定大气中SO 的浓度
2
C.氨酸法:用氨水吸收尾气中的SO 后再将吸收液与硫酸反应,将富集后的SO 循环使用
2 2
D.石灰石—石膏法:常温下用石灰石吸收尾气中的SO 得到CaSO ,再经氧化可用于生产
2 3
石膏
8.SO 属于大气污染物,可用H 与SO 在加热条件下反应消除SO 的污染,其反应原理可
2 2 2 2
分为两步,过程如图所示。
下列说法正确的是( )
A.SO 排放到空气中会形成pH≈5.6的酸雨
2
B.可用CuSO 溶液检验是否有气体X生成
4
C.在100~200 ℃时发生的是置换反应
D.工业上可用浓硝酸处理尾气中的SO
2
9.下图虚线框中的装置(试剂均足量)可用来检验浓硫酸与木炭粉在加热条件下反应所产生
的所有气体产物,其中供选择的试剂有无水硫酸铜、品红溶液、酸性高锰酸钾溶液、澄清石
灰水四种试剂,下列说法正确的是( )A.物质甲可以是无水硫酸铜,也可以是变色硅胶、无水氯化钙等物质
B.丙中发生反应的离子方程式可能是SO +2OH-===SO+HO
2 2
C.乙和戊两种溶液都不宜用作尾气吸收装置中的试剂
D.如果将装置的连接顺序变为①③②,不影响检验
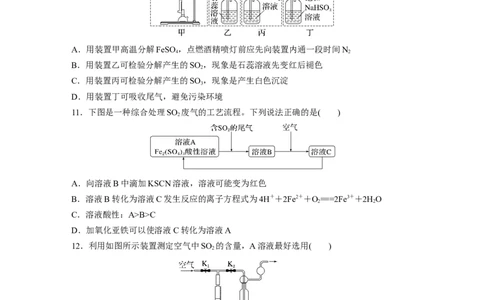
10.已知2FeSO =====Fe O +SO ↑+SO ↑。下列有关操作、装置、原理及对现象的表述
4 2 3 2 3
正确的是( )
A.用装置甲高温分解FeSO ,点燃酒精喷灯前应先向装置内通一段时间N
4 2
B.用装置乙可检验分解产生的SO ,现象是石蕊溶液先变红后褪色
2
C.用装置丙可检验分解产生的SO ,现象是产生白色沉淀
3
D.用装置丁可吸收尾气,避免污染环境
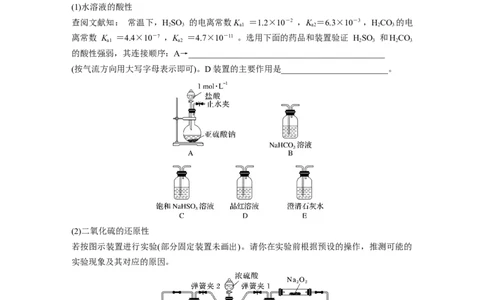
11.下图是一种综合处理SO 废气的工艺流程。下列说法正确的是( )
2
A.向溶液B中滴加KSCN溶液,溶液可能变为红色
B.溶液B转化为溶液C发生反应的离子方程式为4H++2Fe2++O===2Fe3++2HO
2 2
C.溶液酸性:A>B>C
D.加氧化亚铁可以使溶液C转化为溶液A
12.利用如图所示装置测定空气中SO 的含量,A溶液最好选用( )
2
A.NaOH溶液(滴有2~3滴酚酞溶液)
B.KMnO 溶液(滴有一定量硫酸溶液)
4
C.HNO 溶液[滴有2~3滴Ba(NO ) 溶液]
3 3 2
D.I 溶液(滴有2~3滴淀粉溶液)
2
13.葡萄酒中常加入亚硫酸盐作为食品添加剂,为检测某葡萄酒样品中亚硫酸盐的含量(通
常以酒样中SO 的量计),某研究小组设计了如下实验(已知还原性:SO>I->Cl-)。
2下列说法不正确的是( )
A.若试剂A选择氯水,则试剂B可选择NaOH标准液
B.通入N 和煮沸的目的是将产生的气体从溶液中全部赶出
2
C.葡萄酒中加亚硫酸盐的主要目的是防止葡萄酒氧化,利用了亚硫酸盐的还原性
D.若试剂A选择碱液,调节吸收后溶液为中性,则试剂B可选择I 标准液
2
14.某研究性学习小组在学习SO 的性质时,通过查阅文献、理性分析、实验验证与 CO
2 2
的性质进行了比较。试根据研究主题和过程,回答下列问题。
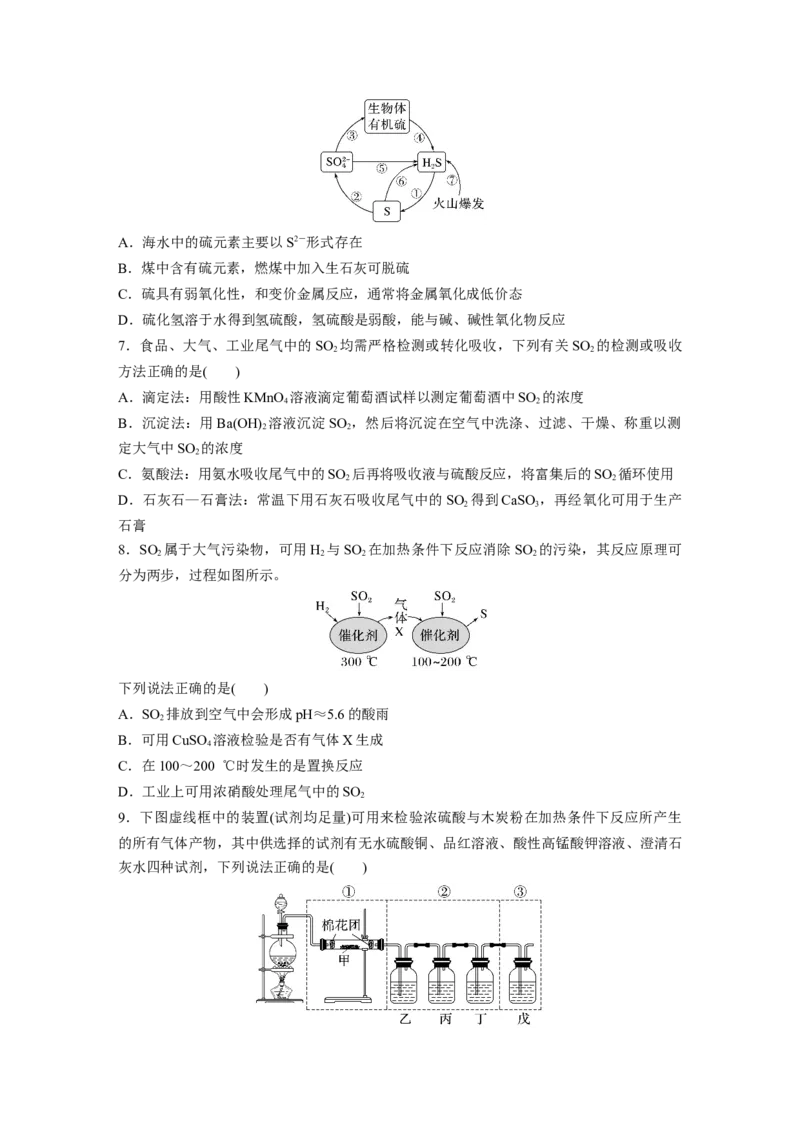
(1)水溶液的酸性
查阅文献知: 常温下,HSO 的电离常数K =1.2×10-2 ,K =6.3×10-3 ,HCO 的电
2 3 a1 a2 2 3
离常数 K =4.4×10-7 ,K =4.7×10-11 。选用下面的药品和装置验证 HSO 和HCO
a1 a2 2 3 2 3
的酸性强弱,其连接顺序:A→______________________________________________
(按气流方向用大写字母表示即可)。D装置的主要作用是_________________________。
(2)二氧化硫的还原性
若按图示装置进行实验(部分固定装置未画出)。请你在实验前根据预设的操作,推测可能的
实验现象及其对应的原因。
预设的操作步骤 预期的实验现象 推测可能的原因
关闭弹簧夹2, SO 与NaO 反应无O 生成,可能发
若将带火星的木条放在D试管 2 2 2 2
打开弹簧夹1, 生反应的化学方程式为
口处,木条不复燃
将浓硫酸注入三 ①________________________________________________________________
颈烧瓶至浸没固 ________
体 若将带火星的木条放在D试管 SO 与NaO 反应有O 生成,发生的
2 2 2 2
口处,木条复燃 反应:2SO +2NaO===2NaSO +O
2 2 2 2 3 2
E中反应的离子方程式
关闭弹簧夹1, ③_______________________________
E中②________________
打开弹簧夹2, _________________________________
残余气体进入 ________
E、F中 F中反应为2OH- + SO ===SO+
2
F中④________________
HO
2
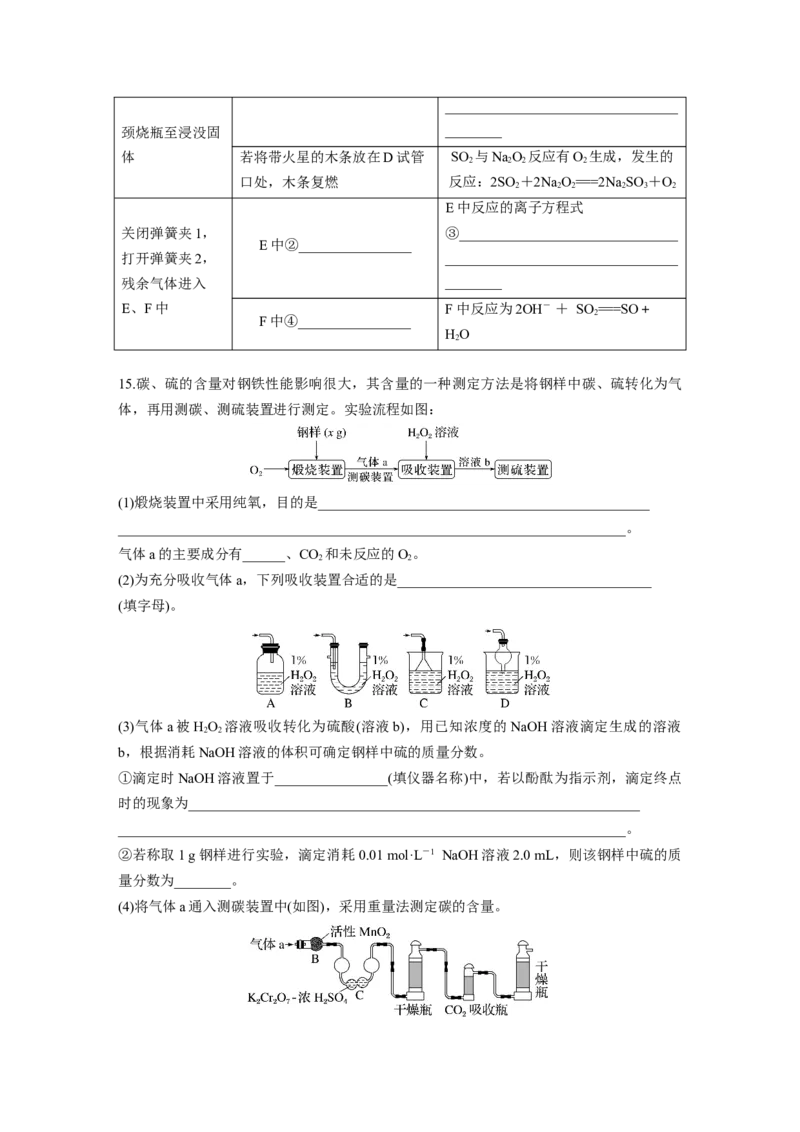
15.碳、硫的含量对钢铁性能影响很大,其含量的一种测定方法是将钢样中碳、硫转化为气
体,再用测碳、测硫装置进行测定。实验流程如图:
(1)煅烧装置中采用纯氧,目的是_______________________________________________
________________________________________________________________________。
气体a的主要成分有______、CO 和未反应的O。
2 2
(2)为充分吸收气体a,下列吸收装置合适的是____________________________________
(填字母)。
(3)气体a被HO 溶液吸收转化为硫酸(溶液b),用已知浓度的NaOH溶液滴定生成的溶液
2 2
b,根据消耗NaOH溶液的体积可确定钢样中硫的质量分数。
①滴定时NaOH溶液置于________________(填仪器名称)中,若以酚酞为指示剂,滴定终点
时的现象为________________________________________________________________
________________________________________________________________________。
②若称取1 g钢样进行实验,滴定消耗0.01 mol·L-1 NaOH溶液2.0 mL,则该钢样中硫的质
量分数为________。
(4)将气体a通入测碳装置中(如图),采用重量法测定碳的含量。①气体a通过B和C的目的是除去SO ,通过所用试剂判断该法所利用的 SO 的性质是
2 2
________________________________________________________________________。
②计算钢样中碳的质量分数,应测量的数据是________________________________________
________________________________________________________________________。