文档内容
第 21 讲 卤族元素 溴、碘单质的提取
[复习目标] 1.掌握卤素单质的性质及卤素离子的检验。2.掌握卤素单质的提取。
考点一 卤素单质的性质及 X-的检验
1.卤族元素
卤族元素又称卤素,位于元素周期表的第ⅦA族,价电子排布为ns2np5。
2.溴、碘单质物理性质比较
性质 Br I
2 2
颜色 ________色 ______色
状态 液体
①在水中溶解度不大;
溶解性
②易溶于有机溶剂
①易______;
特性 易______、有毒
②使淀粉溶液______
3.氯、溴、碘单质化学性质比较
X+HO______________
2 2
与水反应
氯、溴、碘与水反应由____到____
与碱反应(NaOH) 2NaOH+X===________________
2
①Cl____Br ____I,还原性:Cl-____Br-____I-;
2 2 2
氧化性 ②氯、溴、碘与氢气化合由____到____;
③I 与Fe反应只生成FeI,其他卤素单质可将Fe氧化为+3价
2 2
4.氟的特殊性
(1)氟无正化合价。
(2)F 能与水反应放出O,化学方程式:__________________________________________
2 2
____________________________________________________________________________。
(3)在HX中,HF的熔、沸点最高,氢氟酸是弱酸,能腐蚀玻璃。
5.卤素离子的检验方法
(1)AgNO 溶液——沉淀法
3
未知液―――――→生成(2)置换——萃取法
未知液――――――――→
―――――――――――――――→
有机层呈
(3)氧化——淀粉法检验
未知液――――――――――――――――→ ――――→____色溶液,表明有I-
应用举例
鉴别NaCl溶液、NaBr溶液、NaI溶液可以选用的试剂是________(填序号)。
①碘水、淀粉溶液 ②氯水、CCl ③溴水、苯 ④硝酸、AgNO 溶液 ⑤氯水、苯
4 3
⑥CCl 、淀粉溶液
4
1.卤素气态氢化物的水溶液都是强酸溶液( )
2.浓HSO 能干燥HCl,所以浓硫酸也能干燥HBr( )
2 4
3.加碘盐能使淀粉变蓝( )
4.清洗碘升华实验所用试管的操作是先用酒精清洗,再用水清洗( )
5.液溴易挥发,在存放液溴的试剂瓶中应加水封( )
6.用加热的方法可将NaHCO 中混有的少量碘除去( )
3
7.可用F 与NaCl溶液反应产生Cl,检证F 的氧化性大于Cl( )
2 2 2 2
一、Cl、Br 、I 氧化性强弱的实验探究
2 2 2
1.某小组用如图所示装置比较氯、溴、碘单质的氧化性强弱(夹持仪器已略去,气密性已检
查)。
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是_______________________________________。
(2)验证氯气的氧化性强于碘的实验现象是___________________________________________________________________________________________________________。
(3)B中溶液发生反应的离子方程式是________________________________________
________________________________________________________________________。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是__________________________
________________________________________________________________________。
(5)过程Ⅲ实验的目的是__________________________________________________
________________________________________________________________________。
(6) 氯 、 溴 、 碘 单 质 的 氧 化 性 逐 渐 减 弱 的 原 因 : 同 主 族 元 素 从 上 到 下 ,
________________________________________________________________________,
得电子能力逐渐减弱。
二、拟卤素和卤素互化物的结构与性质
2.氰[(CN) ]的结构简式为N≡C—C≡N,其化学性质与卤素(X )很相似,化学上称之为拟
2 2
卤素,其氧化性介于Br 和I 之间。
2 2
(1)写出(CN) 的电子式: __________________________________________________。
2
(2)写出(CN) 在常温下与烧碱溶液反应的化学方程式: _________________________。
2
(3)在 KBr、KI、KCN 的混合溶液中通入少量氯气,发生反应的离子方程式为
________________________________________________________________________。
3.一氯化碘(ICl)、三氯化碘(ICl )是卤素互化物,它们的性质与卤素单质相似。
3
(1)ICl 与水反应的产物可能为__________________________________________
3
(填化学式)。
(2)ICl在常温下与烧碱溶液反应的离子方程式为______________________________,该反应
是否是氧化还原反应?__________(填“是”或“否”)。
考点二 从海水资源中提取卤素单质
1.氯的提取——氯碱工业
(1)工艺流程
海水―→粗盐――→饱和食盐水――→
(2)发生反应的化学方程式为____________________________________________________
________________________________________________________________________。
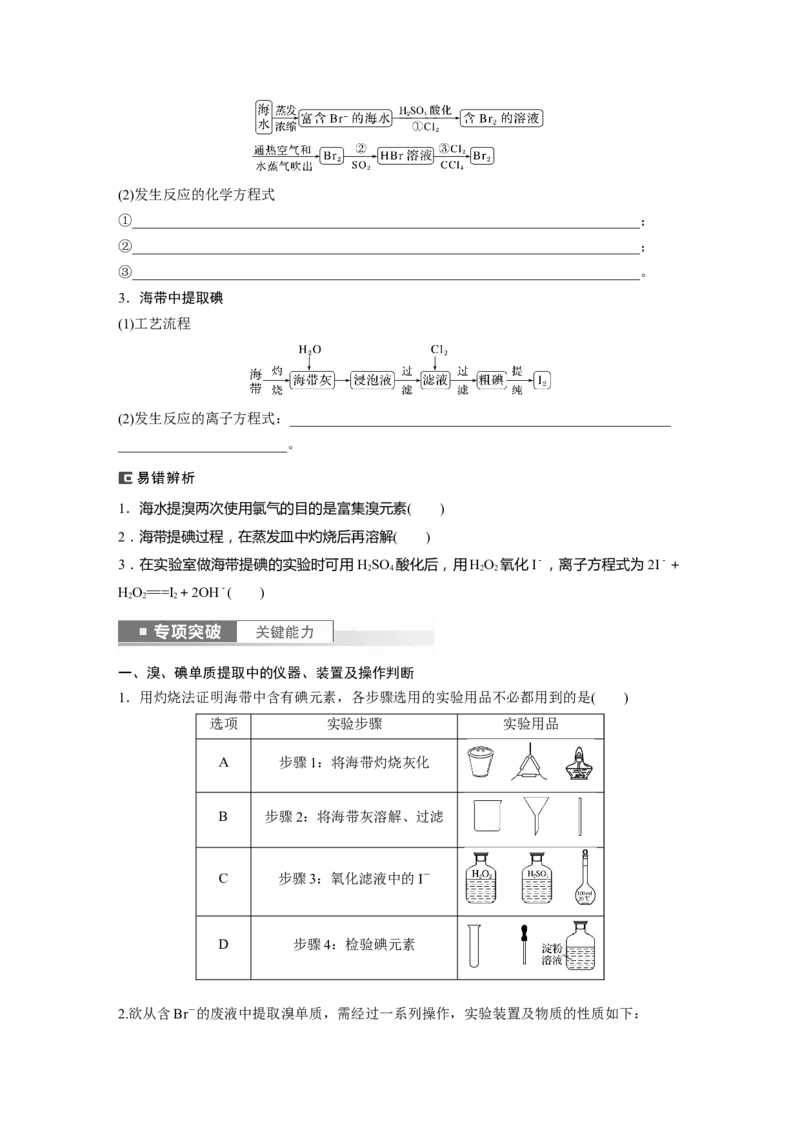
2.海水中提取溴
(1)工艺流程(2)发生反应的化学方程式
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________。
3.海带中提取碘
(1)工艺流程
(2)发生反应的离子方程式:______________________________________________________
________________________。
1.海水提溴两次使用氯气的目的是富集溴元素( )
2.海带提碘过程,在蒸发皿中灼烧后再溶解( )
3.在实验室做海带提碘的实验时可用HSO 酸化后,用HO 氧化I-,离子方程式为2I-+
2 4 2 2
HO===I+2OH-( )
2 2 2
一、溴、碘单质提取中的仪器、装置及操作判断
1.用灼烧法证明海带中含有碘元素,各步骤选用的实验用品不必都用到的是( )
选项 实验步骤 实验用品
A 步骤1:将海带灼烧灰化
B 步骤2:将海带灰溶解、过滤
C 步骤3:氧化滤液中的I-
D 步骤4:检验碘元素
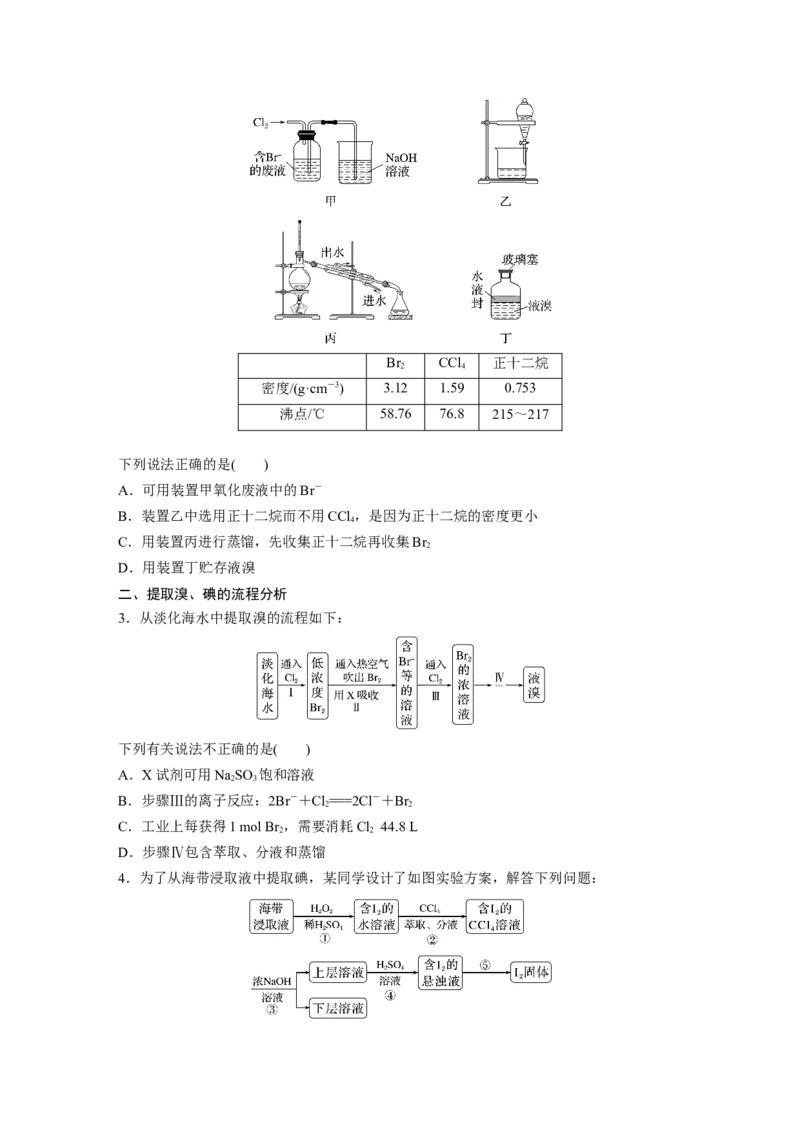
2.欲从含Br-的废液中提取溴单质,需经过一系列操作,实验装置及物质的性质如下:Br CCl 正十二烷
2 4
密度/(g·cm-3) 3.12 1.59 0.753
沸点/℃ 58.76 76.8 215~217
下列说法正确的是( )
A.可用装置甲氧化废液中的Br-
B.装置乙中选用正十二烷而不用CCl ,是因为正十二烷的密度更小
4
C.用装置丙进行蒸馏,先收集正十二烷再收集Br
2
D.用装置丁贮存液溴
二、提取溴、碘的流程分析
3.从淡化海水中提取溴的流程如下:
下列有关说法不正确的是( )
A.X试剂可用NaSO 饱和溶液
2 3
B.步骤Ⅲ的离子反应:2Br-+Cl===2Cl-+Br
2 2
C.工业上每获得1 mol Br ,需要消耗Cl 44.8 L
2 2
D.步骤Ⅳ包含萃取、分液和蒸馏
4.为了从海带浸取液中提取碘,某同学设计了如图实验方案,解答下列问题:(1)①中反应的离子方程式: ________________________________________________
________________________________________________________________________。
(2)②中分液时含I 的CCl 溶液从分液漏斗________(填“上口倒出”或“下口放出”)。
2 4
(3)③是将富集在CCl 中的碘单质利用化学转化重新富集在水中,称为反萃取,写出该反应
4
的化学方程式: __________________________________________________________。
(4)④中反应的离子方程式: ________________________________________________
________________________________________________________________________。
(5)操作⑤的名称为________。
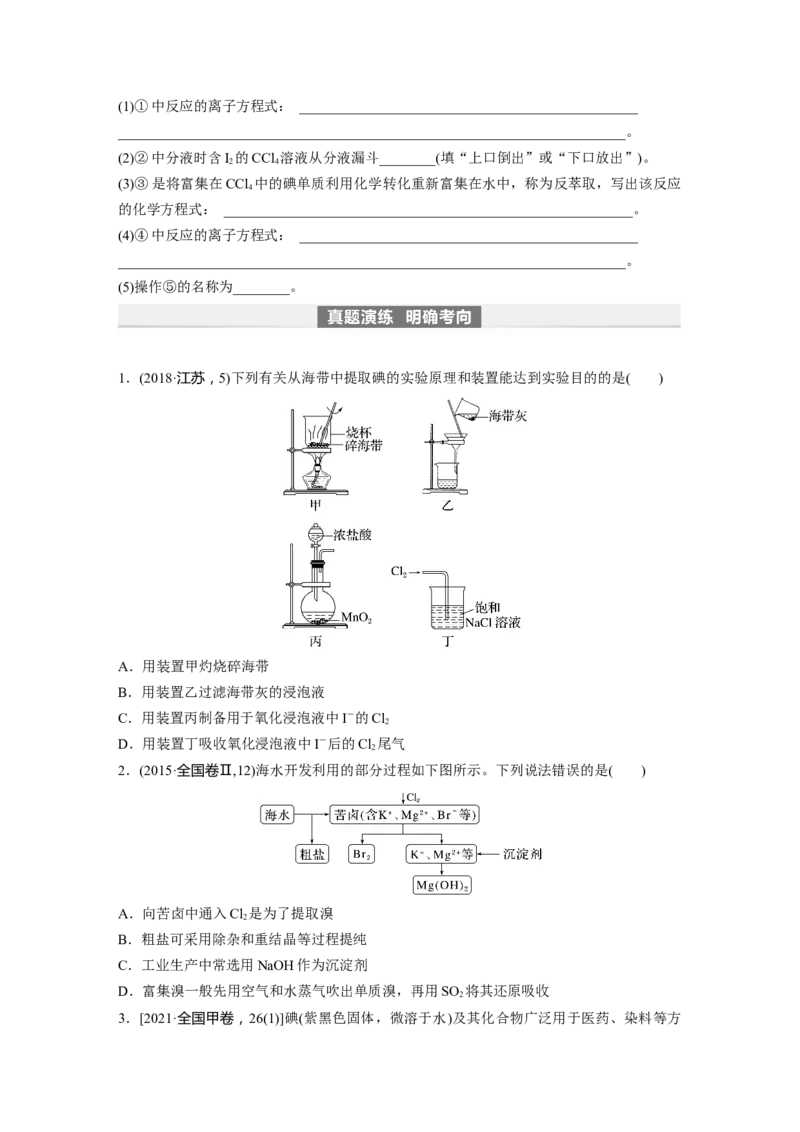
1.(2018·江苏,5)下列有关从海带中提取碘的实验原理和装置能达到实验目的的是( )
A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中I-的Cl
2
D.用装置丁吸收氧化浸泡液中I-后的Cl 尾气
2
2.(2015·全国卷Ⅱ,12)海水开发利用的部分过程如下图所示。下列说法错误的是( )
A.向苦卤中通入Cl 是为了提取溴
2
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产中常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO 将其还原吸收
2
3.[2021·全国甲卷,26(1)]碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
I 的一种制备方法如图所示:
2
①加入Fe粉进行转化反应的离子方程式为______________________________________,生
成的沉淀与硝酸反应,生成____________后可循环使用。
②通入Cl 的过程中,若氧化产物只有一种,反应的化学方程式为___________________;
2
若反应物用量比=1.5时,氧化产物为______________;当>1.5后,单质碘的收率会降低,
原因是____________________________________________________________。