文档内容
1.下列关于卤素的叙述正确的是( )
①卤素的钾盐中,最易被氧化的是氟化钾 ②溴中溶有少量氯气,可以用加入溴化钠再用汽
油萃取的方法提纯 ③溴化银具有感光性,碘化银不具有感光性 ④某溶液与淀粉-KI溶液
反应出现蓝色,则证明该溶液是氯水或溴水 ⑤氟气跟氯化钠水溶液反应,一定有氟化氢和
氧气生成 ⑥氯气跟水反应时,水既不是氧化剂也不是还原剂
A.①③⑤ B.②③⑥
C.②⑤⑥ D.①③④
2.下列有关卤素的说法错误的是( )
A.从HF、HCl、HBr、HI酸性递增的事实,可推出F、Cl、Br、I的非金属性递增的规律
B.HF、HCl、HBr、HI的热稳定性依次减弱,还原性依次增强
C.淀粉碘化钾溶液在空气中变蓝:4I-+O+2HO===2I+4OH-
2 2 2
D.碘在碘化钾溶液中的溶解度大于在纯水中的溶解度
3.下列能够检验出KI中是否含有Br-的实验是( )
A.加入足量的新制氯水,溶液变色则有Br-
B.加入酸性KMnO 溶液,观察溶液颜色是否褪去
4
C.加入少量的碘水,再加入CCl 振荡,有机层有色,则有Br-
4
D.加入足量FeCl 溶液,用CCl 萃取后,取无色的水层并加入AgNO 溶液,有浅黄色沉淀
3 4 3
生成,则含有Br-
4.下列说法正确的是( )
A.卤素单质(X )跟水反应的通式是X+HO===HX+HXO
2 2 2
B.液溴保存在煤油中
C.漂白粉的有效成分是次氯酸钙
D.光照氯水有气泡逸出,该气体是Cl
2
5.如图是盛放液溴的试剂瓶剖面图,仔细观察发现其分成了明显的气相、溴溶液相和液溴
相三相,下列说法错误的是( )
A.气相呈现红棕色,因为其中含有Br 的蒸气
2B.溴溶液相中显酸性,主要因为HBr电离出了H+
C.液溴保存时加水形成水封的目的是减少Br 的挥发
2
D.液溴保存时不可敞口放置,应保存在细口瓶中并塞上橡胶塞
6.实验室中的碘水一般是将碘单质溶于KI溶液配制而成,发生反应:I-+II(主要溶质
2
为KI 或KI·I )。下列说法不正确的是( )
3 2
A.淀粉遇该溶液显蓝色
B.该溶液见光易变质,应用棕色试剂瓶密封保存
C.采用此法配制碘水的目的是为了提高碘水的浓度
D.该溶液中通入SO 后,溶液由中性变为强酸性
2
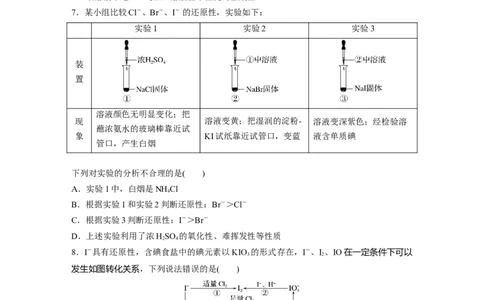
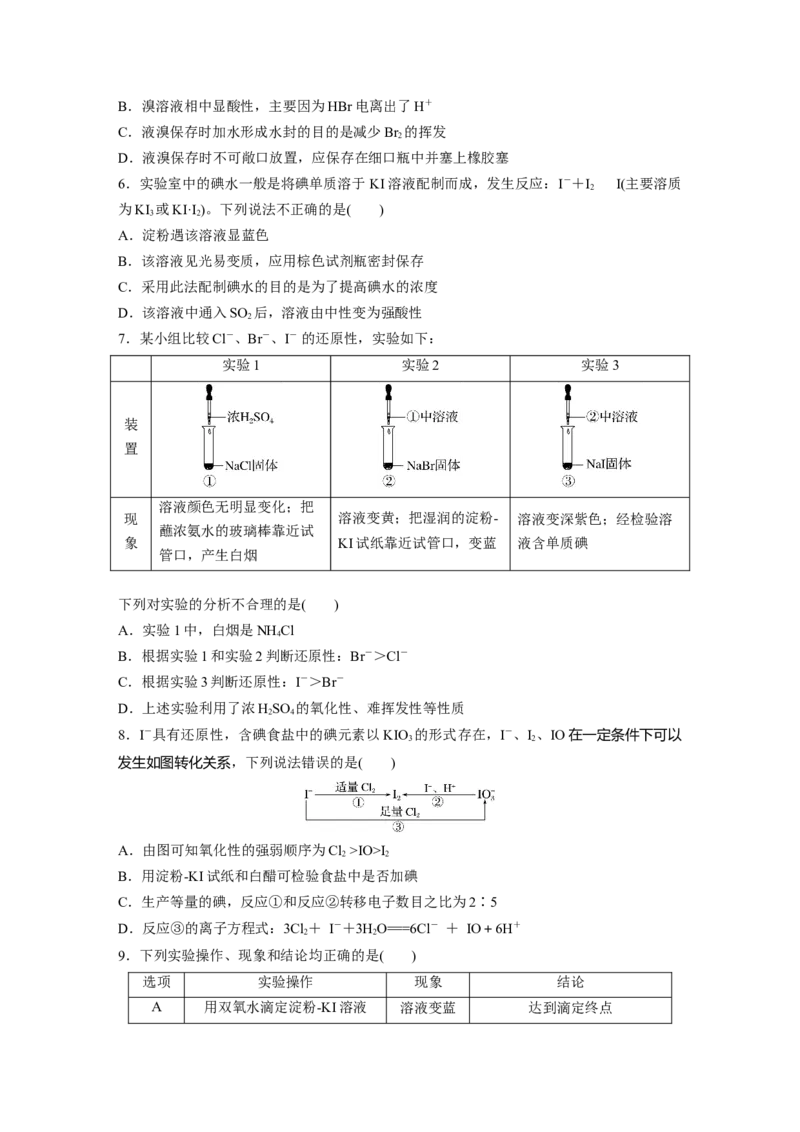
7.某小组比较Cl-、Br-、I- 的还原性,实验如下:
实验1 实验2 实验3
装
置
溶液颜色无明显变化;把
现 溶液变黄;把湿润的淀粉- 溶液变深紫色;经检验溶
蘸浓氨水的玻璃棒靠近试
象 KI试纸靠近试管口,变蓝 液含单质碘
管口,产生白烟
下列对实验的分析不合理的是( )
A.实验1中,白烟是NH Cl
4
B.根据实验1和实验2判断还原性:Br->Cl-
C.根据实验3判断还原性:I->Br-
D.上述实验利用了浓HSO 的氧化性、难挥发性等性质
2 4
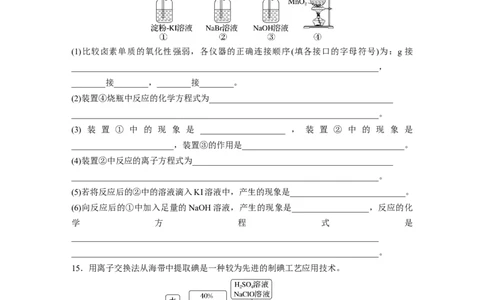
8.I-具有还原性,含碘食盐中的碘元素以KIO 的形式存在,I-、I 、IO在一定条件下可以
3 2
发生如图转化关系,下列说法错误的是( )
A.由图可知氧化性的强弱顺序为Cl >IO>I
2 2
B.用淀粉-KI试纸和白醋可检验食盐中是否加碘
C.生产等量的碘,反应①和反应②转移电子数目之比为2∶5
D.反应③的离子方程式:3Cl+ I-+3HO===6Cl- + IO+6H+
2 2
9.下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
A 用双氧水滴定淀粉-KI溶液 溶液变蓝 达到滴定终点向食用加碘盐中加入食醋和KI 下层呈紫
B 该食用加碘盐中含有KIO
3
溶液,再加入CCl 振荡,静置 红色
4
用湿润的淀粉-KI试纸鉴别
C 试纸变蓝 该气体为溴蒸气
NO 、溴蒸气
2
最后试管
D 有浅黄色 有机物中含有溴原子
沉淀
10.“吹出法”是工业上常用的一种海水提溴技术,该技术主要流程如下:
下列有关说法不正确的是( )
A.氧化1所用的氯气可通过电解饱和NaCl溶液制得
B.吹出后剩余溶液中可能大量存在的离子有Na+、Mg2+、Cl-、Br-
C.吸收过程发生反应的离子方程式为SO +Br +2HO===4H++2Br-+SO
2 2 2
D.氧化2所得溶液可通过萃取分离出溴
11.(2023·烟台模拟)工业上用活性炭吸附海带提碘后废水中的I-制取I,其流程如图:
2
下列说法错误的是( )
A.NaNO 氧化I-时使溶液pH变大
2
B.活性炭吸附是为了净化水溶液
C.I 与NaOH(浓、热)反应的化学方程式:3I +6NaOH(浓、热)===5NaI+NaIO +3HO
2 2 3 2
D.热空气能吹出I,是因为I 在水中溶解度小、易升华
2 2
12.溴化碘(IBr)的化学性质类似卤素单质,它同水反应的化学方程式为 IBr+HO===HBr+
2
HIO。下列有关IBr的叙述不正确的是( )
A.在与水的反应中,IBr既不是氧化剂也不是还原剂
B.在与水的反应中,IBr既是氧化剂又是还原剂
C.在很多反应中,IBr是强氧化剂
D.IBr跟NaOH稀溶液反应生成NaBr、NaIO和HO
2
13.“XY ”表示不同卤素之间靠共用电子对形成的卤素互化物(非金属性:X