文档内容
绝密★启用前
2024 年中考押题预测卷 01【南京卷】
化 学
(考试时间:60分钟 试卷满分:80分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Si-28 S-32 Cl-35.5 Cu-64 Ba-137
一、选择题(本题15小题,每小题只有一个选项符合题意。每小题2分,共30分)
1.书法艺术是我国的文化瑰宝。手工制墨历史悠久,下列制墨环节涉及化学变化的是
A. 点灯炼制黑烟 B. 搅拌研磨黑烟
C. 按压墨条成形 D. 天然晾干墨条
2.规范的实验操作是完成实验的基本保障。下列基本实验操作正确的是
A.铁丝与氧气反应 B.组装发生装置
C.测定溶液的pH D.倾倒液体3. 化学用语是学习化学的重要工具。下列化学用语表示正确的是
A. 尿素:CO(NH) B. 氧化铁:FeO
2 2
C. 钙离子:Ca+2 D. 两个氧原子:O
2
4.化学与人体健康息息相关。下列有关人体健康和营养的说法中正确的是
A. 水果、蔬菜中不含维生素 B. 缺钙元素,易引起骨质疏松
C. 糖类不能为人体提供能量 D. 用已经霉变大米淘洗来煮饭
5.唐代诗人韦应物的《观田家》中有诗句“微雨众卉新,一雷惊蛰始”。雷电时,N 与O 反应是自然界
2 2
氮循环的重要反应之一。下列氮循环中的物质属于氧化物的是
A. N B. NO C. HNO D. NH NO
2 3 4 3
6.下列物质性质属于化学性质,且与其用途具有对应关系的是
A. 焊锡熔点低,可用用于焊接金属
B. 活性炭具有吸附性,可用于净化水
C. 一氧化碳具有可燃性,可用于冶炼铜
D. 小苏打能与盐酸反应,可用于治疗胃酸过多
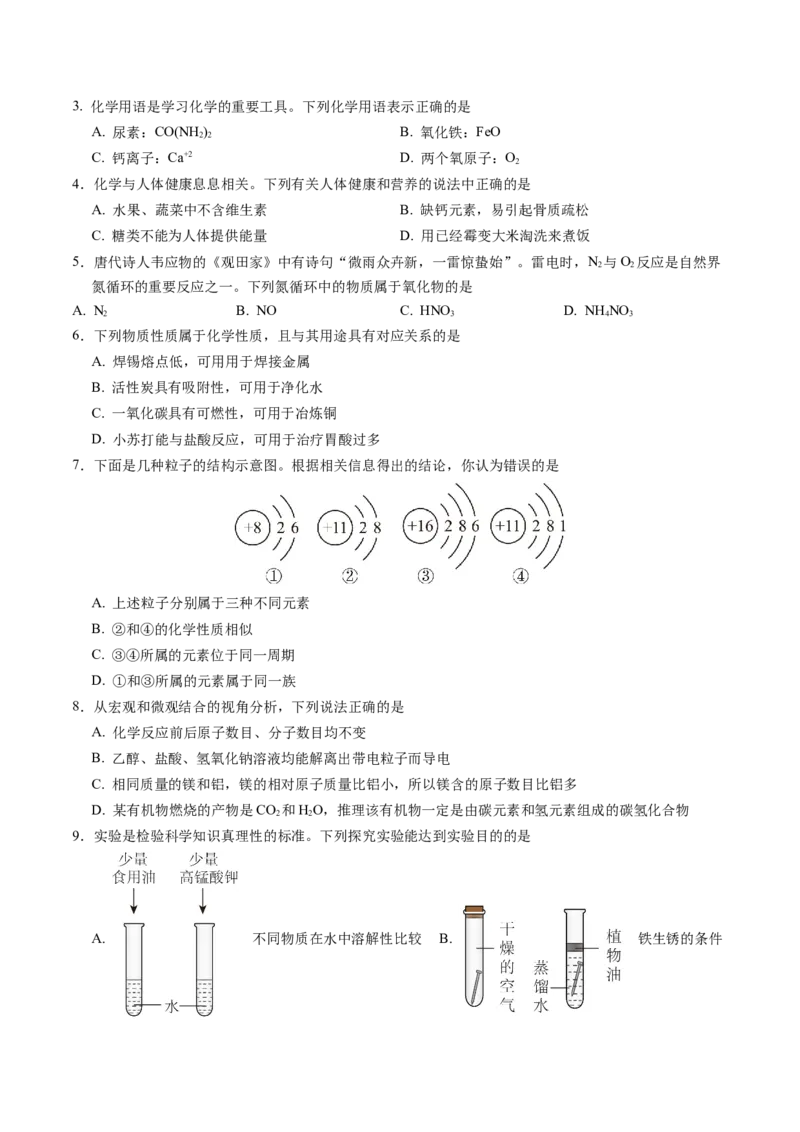
7.下面是几种粒子的结构示意图。根据相关信息得出的结论,你认为错误的是
A. 上述粒子分别属于三种不同元素
B. ②和④的化学性质相似
C. ③④所属的元素位于同一周期
D. ①和③所属的元素属于同一族
8.从宏观和微观结合的视角分析,下列说法正确的是
A. 化学反应前后原子数目、分子数目均不变
B. 乙醇、盐酸、氢氧化钠溶液均能解离出带电粒子而导电
C. 相同质量的镁和铝,镁的相对原子质量比铝小,所以镁含的原子数目比铝多
D. 某有机物燃烧的产物是CO 和HO,推理该有机物一定是由碳元素和氢元素组成的碳氢化合物
2 2
9.实验是检验科学知识真理性的标准。下列探究实验能达到实验目的的是
A. 不同物质在水中溶解性比较 B. 铁生锈的条件C. 燃烧的条件 D. CO 能与水反应
2
10.分析推理是化学学习中最常用的思维方法,下列说法正确的是
A. 离子是带电荷的粒子,则带电荷的粒子一定是离子
B. 氧化物中一定含有氧元素,则含有氧元素 的化合物一定是氧化物
C. 燃烧有发光放热现象出现,则有发光放热现象的变化一定是燃烧
D. 碱性溶液能使酚酞溶液变红,则能使酚酞溶液变红的溶液一定呈碱性
11.茶叶中含茶氨酸(化学式为C H ON)、锌等多种成分,茶树适宜在pH为5-6的土壤中生长。下列说法
2 14 3 2
错误的是
A. 茶氨酸属于有机物 B. 茶氨酸中碳、氢元素的质量比为12:7
C. 1个茶氨酸分子中含有1个氮分子 D. 茶树不宜在碱性土壤中生长
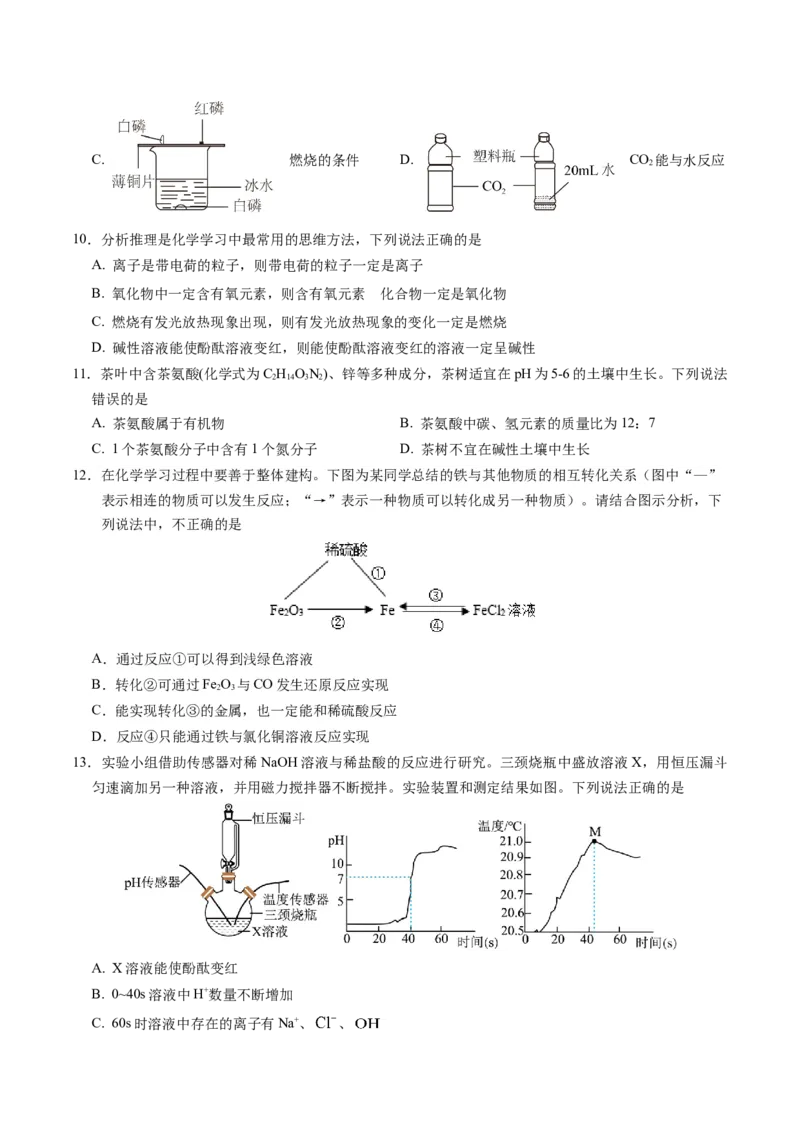
12.在化学学习过程中要善于整体建构。下图为某同学总结的铁与其他物质的相互转化关系(图中“—”
表示相连的物质可以发生反应;“→”表示一种物质可以转化成另一种物质)。请结合图示分析,下
列说法中,不正确的是
A.通过反应①可以得到浅绿色溶液
B.转化②可通过Fe O 与CO发生还原反应实现
2 3
C.能实现转化③的金属,也一定能和稀硫酸反应
D.反应④只能通过铁与氯化铜溶液反应实现
13.实验小组借助传感器对稀NaOH溶液与稀盐酸的反应进行研究。三颈烧瓶中盛放溶液X,用恒压漏斗
匀速滴加另一种溶液,并用磁力搅拌器不断搅拌。实验装置和测定结果如图。下列说法正确的是
A. X溶液能使酚酞变红
B. 0~40s溶液中H+数量不断增加
C. 60s时溶液中存在的离子有Na+、 、D. 可以用硝酸银验证M点时氢氧化钠和盐酸是否恰好完全反应
14.下列除去杂质的方法正确的是
选项 物质 杂质 除去杂质的方法
A NaCl NaCO 加入过量的稀盐酸
2 3
B FeCl 溶液 CuCl 溶液 加入过量的Fe粉,过滤
2 2
C NaCl溶液 NaCO 溶液 加入过量的CaCl 溶液,过滤
2 3 2
D Fe Fe O 加入过量的稀盐酸,过滤
2 3
A. A B. B C. C D. D
15.某化工厂废水中含有HCl和FeCl ,现采集该废水样品80.7g,向其中滴加20%的NaOH溶液至溶液沉
3
淀完成时消耗该NaOH溶液80g,待溶液冷至常温,测得其pH=7。过滤,将生成的沉淀滤出,经水洗,
干燥后称重为10.7g。下列说法不正确的是
A. 过滤后,滤液中溶质只有NaCl
B. 废水样品中含有16.25 g FeCl
3
C. 与HCl发生中和反应的NaOH为4g
D. 若pH>7,则溶液中NaCl质量分数大于15.6%
二、填空题(本大题共4小题,每空1分,共31分。)
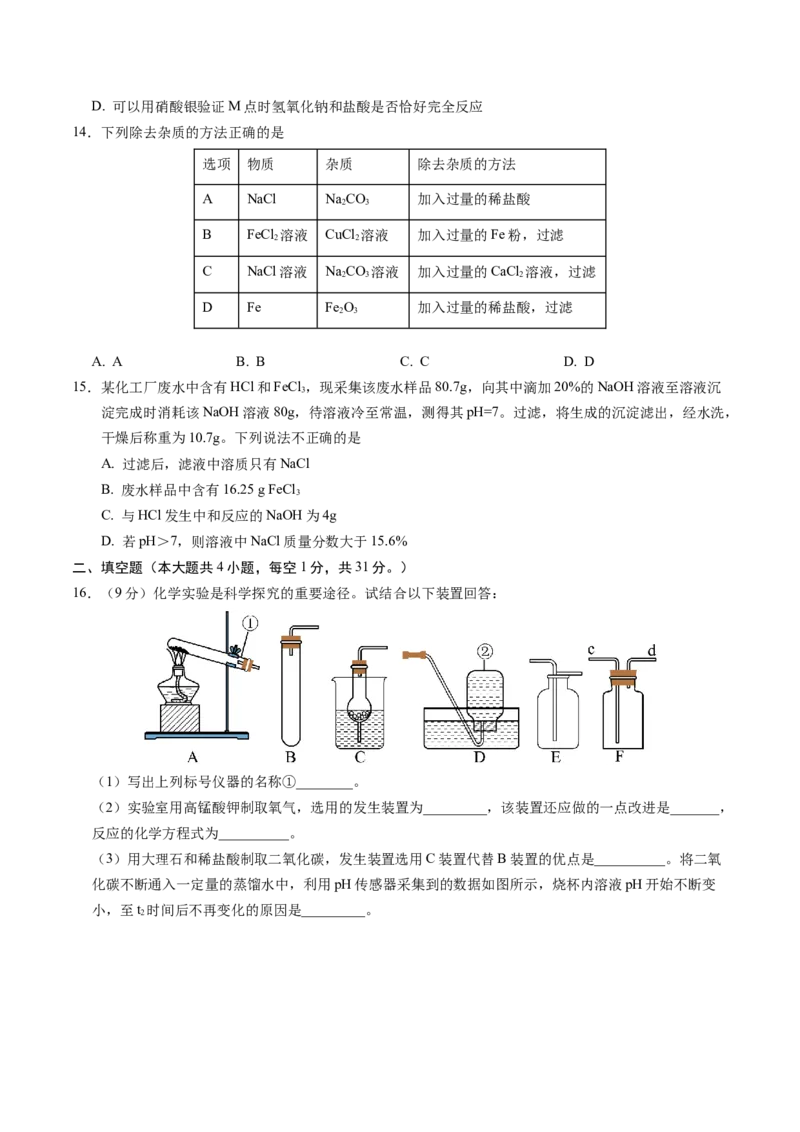
16.(9分)化学实验是科学探究的重要途径。试结合以下装置回答:
(1)写出上列标号仪器的名称①________。
(2)实验室用高锰酸钾制取氧气,选用的发生装置为_________,该装置还应做的一点改进是_______,
反应的化学方程式为__________。
(3)用大理石和稀盐酸制取二氧化碳,发生装置选用C装置代替B装置的优点是__________。将二氧
化碳不断通入一定量的蒸馏水中,利用pH传感器采集到的数据如图所示,烧杯内溶液pH开始不断变
小,至t 时间后不再变化的原因是_________。
2(4)通常状况下,二氧化硫密度比空气大,易溶于水,能与水反应生成亚硫酸(HSO )。实验室常用
2 3
亚硫酸钠(NaSO )固体与浓硫酸在常温下反应制取二氧化硫。
2 3
①若用F装置收集SO ,气体从_________(填“c”或“d”)端进入。
2
②上图中“防倒吸装置”应选择_________(填“甲”或“乙”) 。
③上图中NaOH溶液的作用是_________。
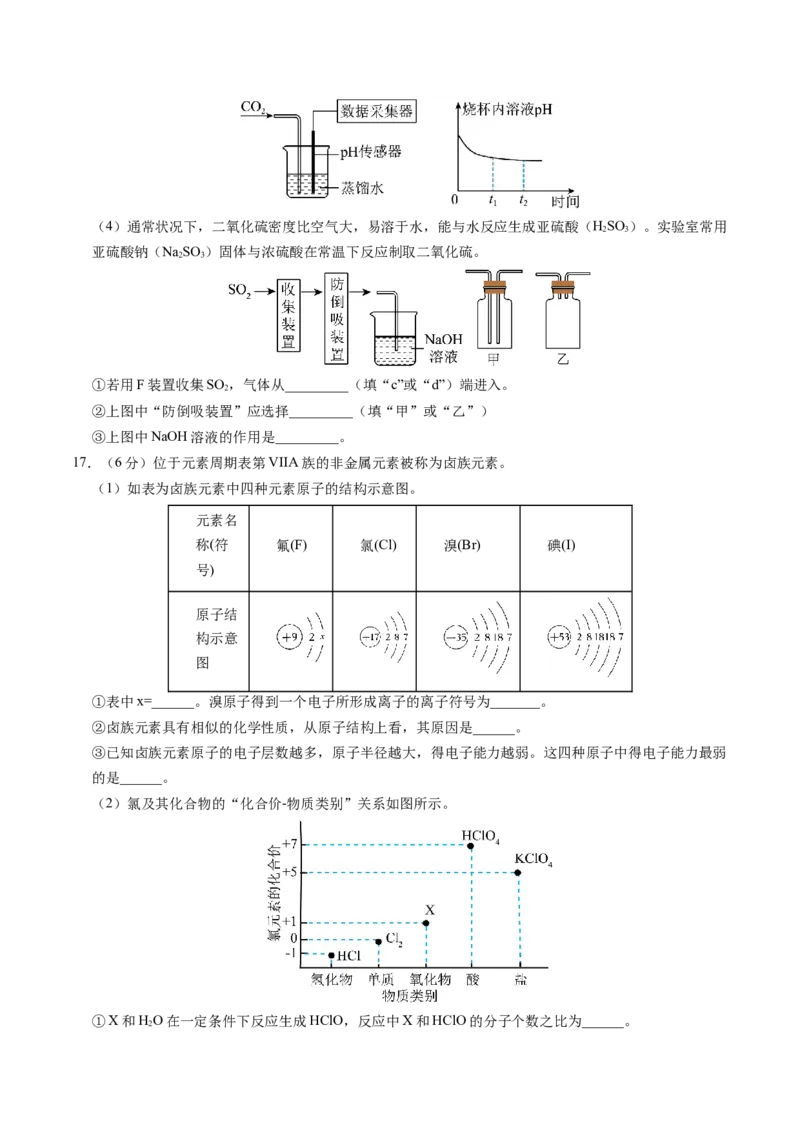
17.(6分)位于元素周期表第VIIA族的非金属元素被称为卤族元素。
(1)如表为卤族元素中四种元素原子的结构示意图。
元素名
称(符 氟(F) 氯(Cl) 溴(Br) 碘(I)
号)
原子结
构示意
图
①表中x=______。溴原子得到一个电子所形成离子的离子符号为_______。
②卤族元素具有相似的化学性质,从原子结构上看,其原因是______。
③已知卤族元素原子的电子层数越多,原子半径越大,得电子能力越弱。这四种原子中得电子能力最弱
的是______。
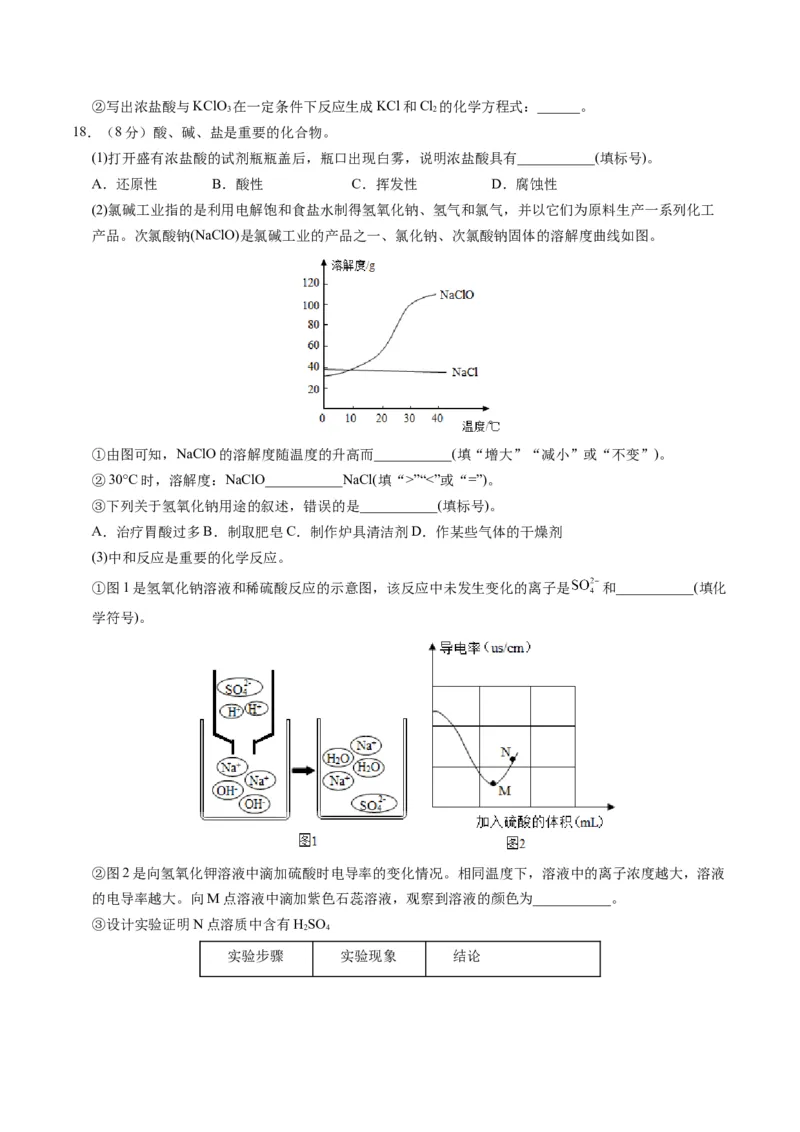
(2)氯及其化合物的“化合价-物质类别”关系如图所示。
①X和HO在一定条件下反应生成HClO,反应中X和HClO的分子个数之比为______。
2②写出浓盐酸与KClO 在一定条件下反应生成KCl和Cl 的化学方程式:______。
3 2
18.(8分)酸、碱、盐是重要的化合物。
(1)打开盛有浓盐酸的试剂瓶瓶盖后,瓶口出现白雾,说明浓盐酸具有___________(填标号)。
A.还原性 B.酸性 C.挥发性 D.腐蚀性
(2)氯碱工业指的是利用电解饱和食盐水制得氢氧化钠、氢气和氯气,并以它们为原料生产一系列化工
产品。次氯酸钠(NaClO)是氯碱工业的产品之一、氯化钠、次氯酸钠固体的溶解度曲线如图。
①由图可知,NaClO的溶解度随温度的升高而___________(填“增大”“减小”或“不变”)。
②30°C时,溶解度:NaClO___________NaCl(填“>”“<”或“=”)。
③下列关于氢氧化钠用途的叙述,错误的是___________(填标号)。
A.治疗胃酸过多B.制取肥皂C.制作炉具清洁剂D.作某些气体的干燥剂
(3)中和反应是重要的化学反应。
①图1是氢氧化钠溶液和稀硫酸反应的示意图,该反应中未发生变化的离子是 和___________(填化
学符号)。
②图2是向氢氧化钾溶液中滴加硫酸时电导率的变化情况。相同温度下,溶液中的离子浓度越大,溶液
的电导率越大。向M点溶液中滴加紫色石蕊溶液,观察到溶液的颜色为___________。
③设计实验证明N点溶质中含有HSO
2 4
实验步骤 实验现象 结论__________
___________ N点溶质中含有HSO
2 4
_
实验现
实验步骤 结论
象
N点溶质中含有HSO
2 4
19.(8分)金属与合金无论是古代还是当今,在生产生活中应用都很广泛。
(1)司母戊鼎是商周时期青铜文化的代表作,现藏于中国国家博物馆。青铜是重要的铜合金,其硬度
_______(填“大于”或“小于”)纯铜。
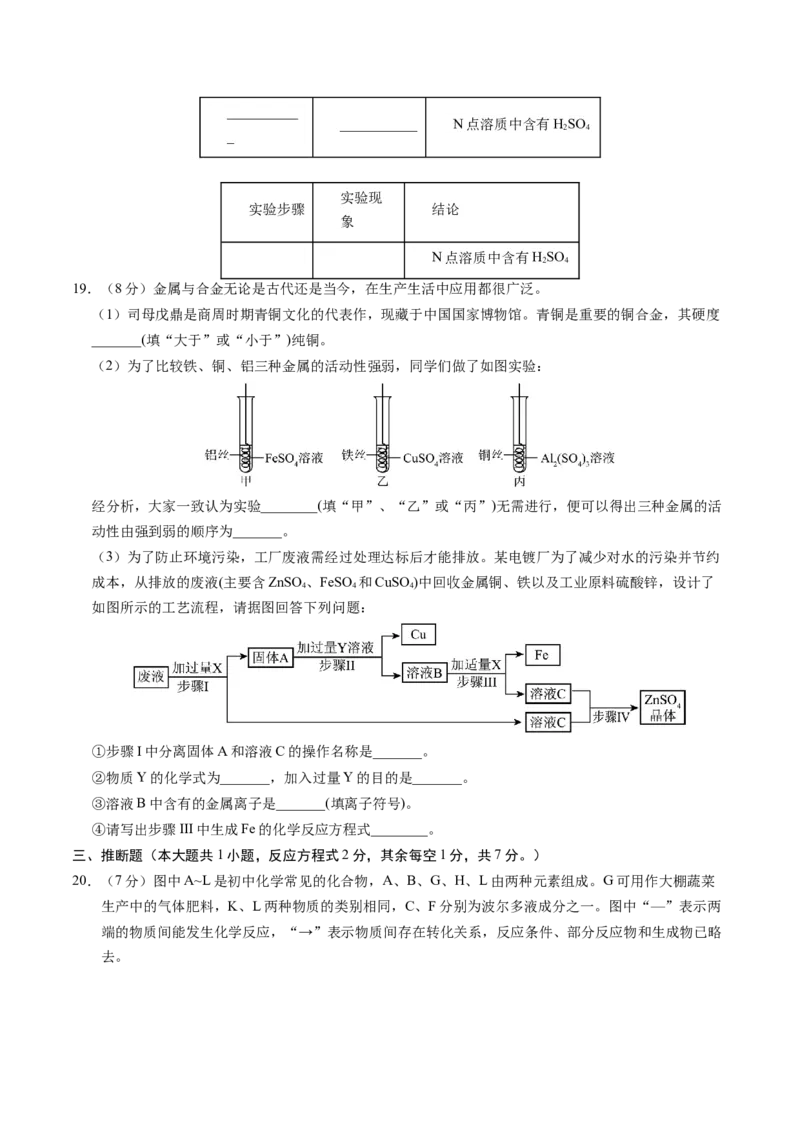
(2)为了比较铁、铜、铝三种金属的活动性强弱,同学们做了如图实验:
经分析,大家一致认为实验________(填“甲”、“乙”或“丙”)无需进行,便可以得出三种金属的活
动性由强到弱的顺序为_______。
(3)为了防止环境污染,工厂废液需经过处理达标后才能排放。某电镀厂为了减少对水的污染并节约
成本,从排放的废液(主要含ZnSO、FeSO 和CuSO )中回收金属铜、铁以及工业原料硫酸锌,设计了
4 4 4
如图所示的工艺流程,请据图回答下列问题:
①步骤I中分离固体A和溶液C的操作名称是_______。
②物质Y的化学式为_______,加入过量Y的目的是_______。
③溶液B中含有的金属离子是_______(填离子符号)。
④请写出步骤III中生成Fe的化学反应方程式________。
三、推断题(本大题共1小题,反应方程式2分,其余每空1分,共7分。)
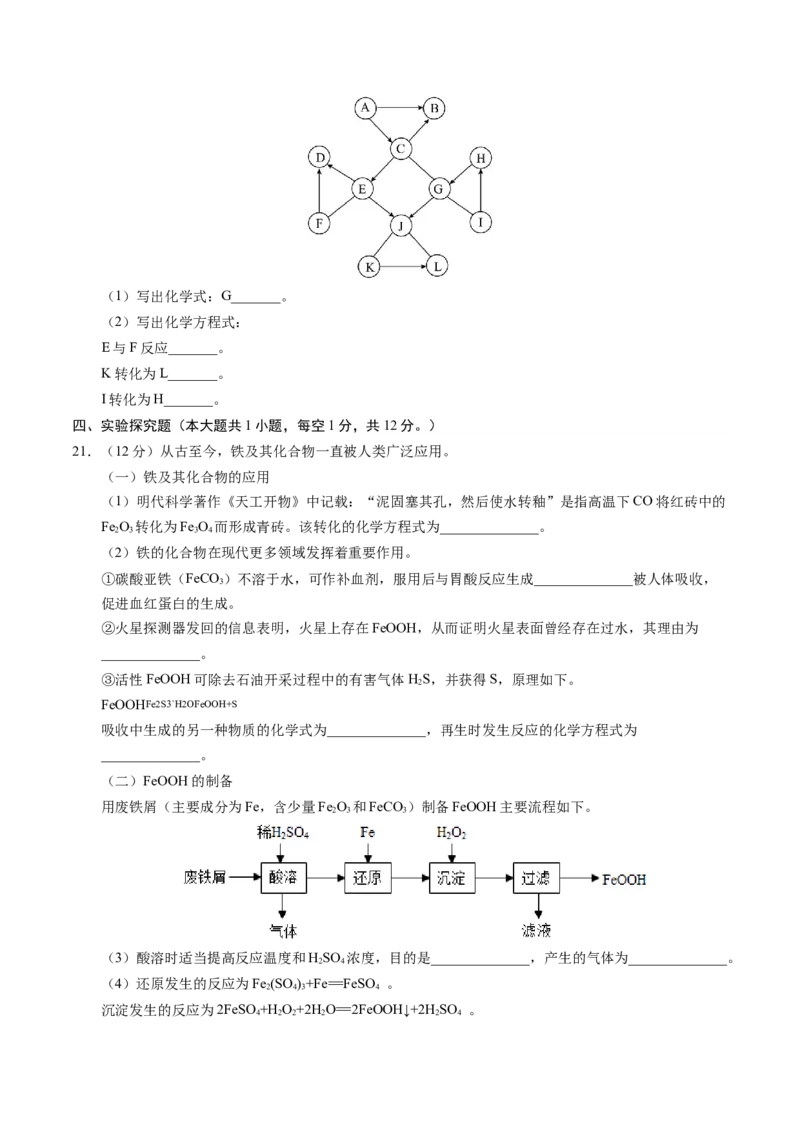
20.(7分)图中A~L是初中化学常见的化合物,A、B、G、H、L由两种元素组成。G可用作大棚蔬菜
生产中的气体肥料,K、L两种物质的类别相同,C、F分别为波尔多液成分之一。图中“—”表示两
端的物质间能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略
去。(1)写出化学式:G_______。
(2)写出化学方程式:
E与F反应_______。
K转化为L_______。
I转化为H_______。
四、实验探究题(本大题共1小题,每空1分,共12分。)
21.(12分)从古至今,铁及其化合物一直被人类广泛应用。
(一)铁及其化合物的应用
(1)明代科学著作《天工开物》中记载:“泥固塞其孔,然后使水转釉”是指高温下CO将红砖中的
Fe O 转化为Fe O 而形成青砖。该转化的化学方程式为______________。
2 3 3 4
(2)铁的化合物在现代更多领域发挥着重要作用。
①碳酸亚铁(FeCO)不溶于水,可作补血剂,服用后与胃酸反应生成______________被人体吸收,
3
促进血红蛋白的生成。
②火星探测器发回的信息表明,火星上存在FeOOH,从而证明火星表面曾经存在过水,其理由为
______________。
③活性FeOOH可除去石油开采过程中的有害气体HS,并获得S,原理如下。
2
FeOOHFe2S3`H2OFeOOH+S
吸收中生成的另一种物质的化学式为______________,再生时发生反应的化学方程式为
______________。
(二)FeOOH的制备
用废铁屑(主要成分为Fe,含少量Fe O 和FeCO)制备FeOOH主要流程如下。
2 3 3
(3)酸溶时适当提高反应温度和HSO 浓度,目的是______________,产生的气体为______________。
2 4
(4)还原发生的反应为Fe (SO )+Fe=FeSO 。
2 4 3 4
沉淀发生的反应为2FeSO +H O+2H O=2FeOOH↓+2H SO 。
4 2 2 2 2 4沉淀时反应温度不宜太高,原因是______________。
(三)FeOOH的含量测定
已知:FOOH及铁的氧化物加热分解的温度如下。
FeOOHFe O Fe OFeO
2 3 3 4
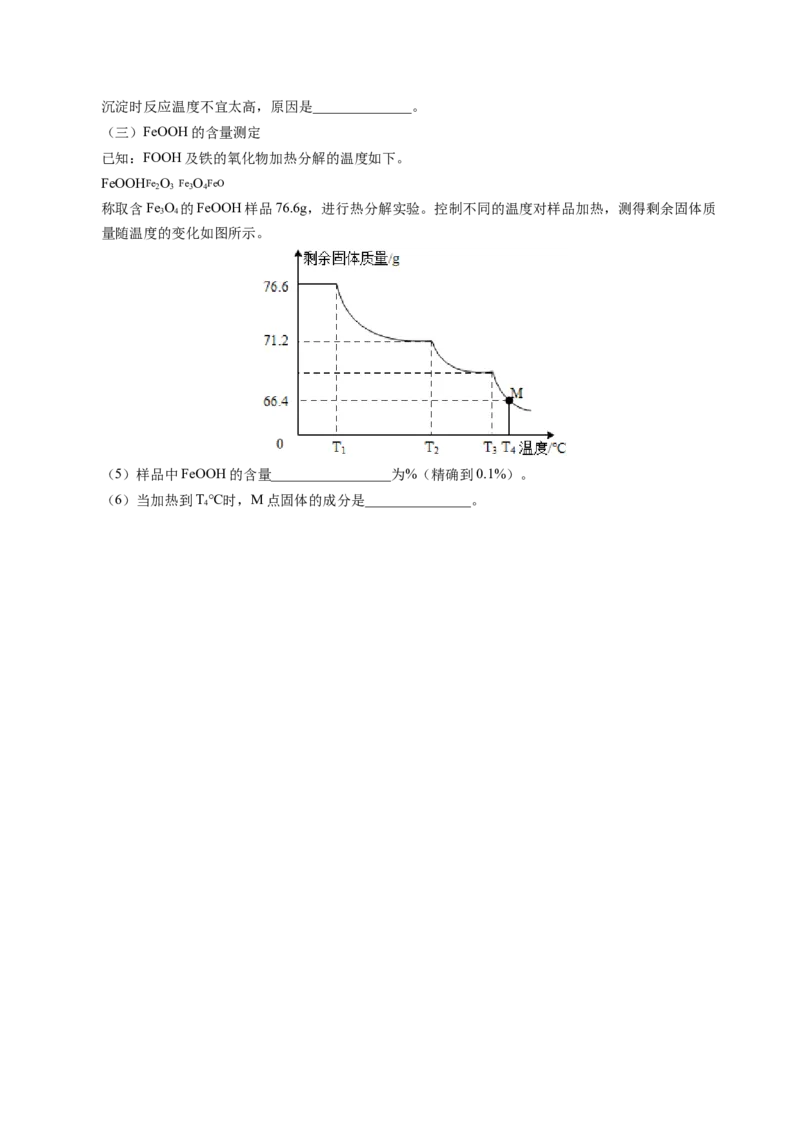
称取含Fe O 的FeOOH样品76.6g,进行热分解实验。控制不同的温度对样品加热,测得剩余固体质
3 4
量随温度的变化如图所示。
(5)样品中FeOOH的含量_________________为%(精确到0.1%)。
(6)当加热到T℃时,M点固体的成分是_______________。
4