文档内容
第 20 讲 氯气的实验室制法及应用
[复习目标] 掌握实验室制取氯气的原理、装置和操作注意事项。增强设计物质制备实验方
案的绿色环保意识。
1.制取原理
HCl (浓)――――――――――――――――――→Cl2
完成下列有关反应的离子方程式:
(1)MnO 和浓盐酸: ______________________________________________________
2
________________________________________________________________________。
(2)Ca(ClO) 与浓盐酸: ___________________________________________________。
2
(3)KClO 与浓盐酸: ______________________________________________________。
3
(4)KMnO 与浓盐酸: _____________________________________________________
4
________________________________________________________________________。
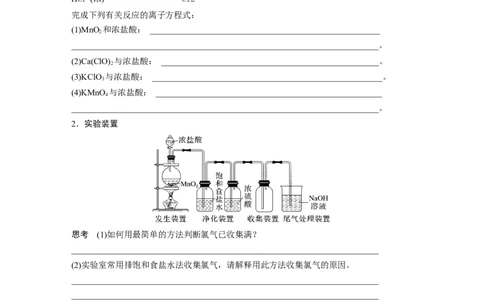
2.实验装置
思考 (1)如何用最简单的方法判断氯气已收集满?
________________________________________________________________________
(2)实验室常用排饱和食盐水法收集氯气,请解释用此方法收集氯气的原因。
________________________________________________________________________
________________________________________________________________________
3.注意事项
(1)反应物的选择:必须用浓盐酸,稀盐酸与MnO 不反应,且随着反应的进行,浓盐酸变为
2
稀盐酸时,反应停止,故盐酸中的HCl不可能全部参加反应。
(2)加热温度:不宜过高,以减少HCl挥发。
(3)实验结束后,先使反应停止并排出残留的Cl 后,再拆卸装置,避免污染空气。
2
(4)尾气处理时,用 NaOH溶液吸收Cl ,不能用澄清石灰水吸收,因为澄清石灰水中含
2
Ca(OH) 的量少,吸收不完全。
21.含0.4 mol HCl的浓盐酸与足量的MnO 共热,能得到0.1 mol Cl ( )
2 2
2.用饱和NaHCO 溶液除去Cl 中混有的HCl( )
3 2
3.常用饱和石灰水吸收尾气中的Cl( )
2
4.用干燥的淀粉碘化钾试纸检验Cl 是否收集满( )
2
1.实验室用MnO 和浓盐酸制Cl 时,有如下操作:①连好装置,检查装置气密性;②缓缓
2 2
加热;③加入MnO 粉末;④从装有浓盐酸的分液漏斗中加入浓盐酸;⑤将多余氯气用
2
NaOH溶液吸收;⑥用向上排空气法收集氯气。顺序排列正确的是( )
A.①②③④⑥⑤ B.③④②①⑥⑤
C.①④③②⑥⑤ D.①③④②⑥⑤
2.下列方法中,可制得Cl 的正确组合是( )
2
①MnO 和浓盐酸混合共热;②MnO 、NaCl和浓硫酸混合共热;③NaClO和浓盐酸混合;
2 2
④KCr O 和浓盐酸混合;⑤KClO 和浓盐酸混合;⑥KMnO 和浓盐酸混合
2 2 7 3 4
A.①②⑥ B.②④⑥
C.①④⑥ D.①②③④⑤⑥
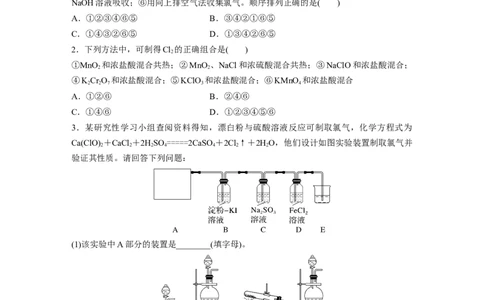
3.某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为
Ca(ClO) +CaCl +2HSO =====2CaSO +2Cl↑+2HO,他们设计如图实验装置制取氯气并
2 2 2 4 4 2 2
验证其性质。请回答下列问题:
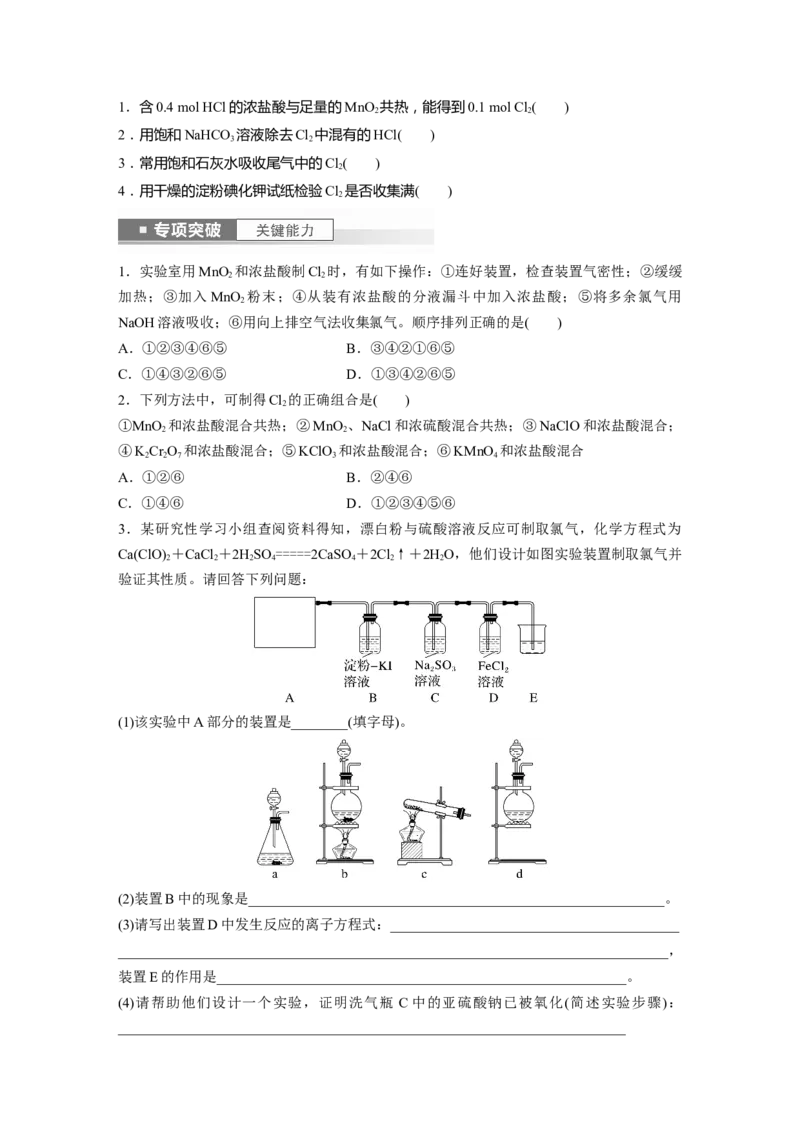
(1)该实验中A部分的装置是________(填字母)。
(2)装置B中的现象是___________________________________________________________。
(3)请写出装置D中发生反应的离子方程式:_________________________________________
______________________________________________________________________________,
装置E的作用是__________________________________________________________。
(4)请帮助他们设计一个实验,证明洗气瓶 C中的亚硫酸钠已被氧化(简述实验步骤):
________________________________________________________________________________________________________________________________________________
________________________________________________________________________。
(5)制取 Cl 的方法有多种,若 A 部分的装置是 a,请再写出一种制备方法:
2
________________________________________________________________________
________________________________________________________________________
(用化学方程式表示)。