文档内容
1.实验室既可用浓盐酸与MnO 在加热条件下反应制备Cl ,也可用KMnO 与浓盐酸在常
2 2 4
温下反应制备Cl,下列有关说法不正确的是( )
2
A.KMnO 的氧化性比MnO 的强
4 2
B.制备Cl 的整个实验过程中,只需要使用氧化剂与还原剂
2
C.用排气法收集Cl 时,不需要利用其他试剂就能确定集气瓶中已收集满
2
D.制备等质量的Cl,消耗MnO 与KMnO 的物质的量之比为5∶2
2 2 4
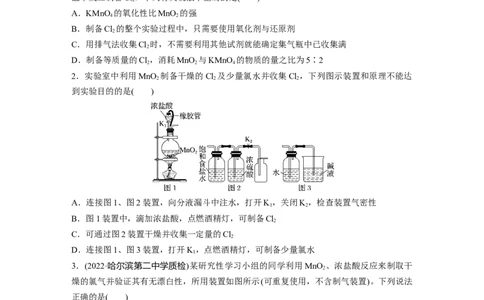
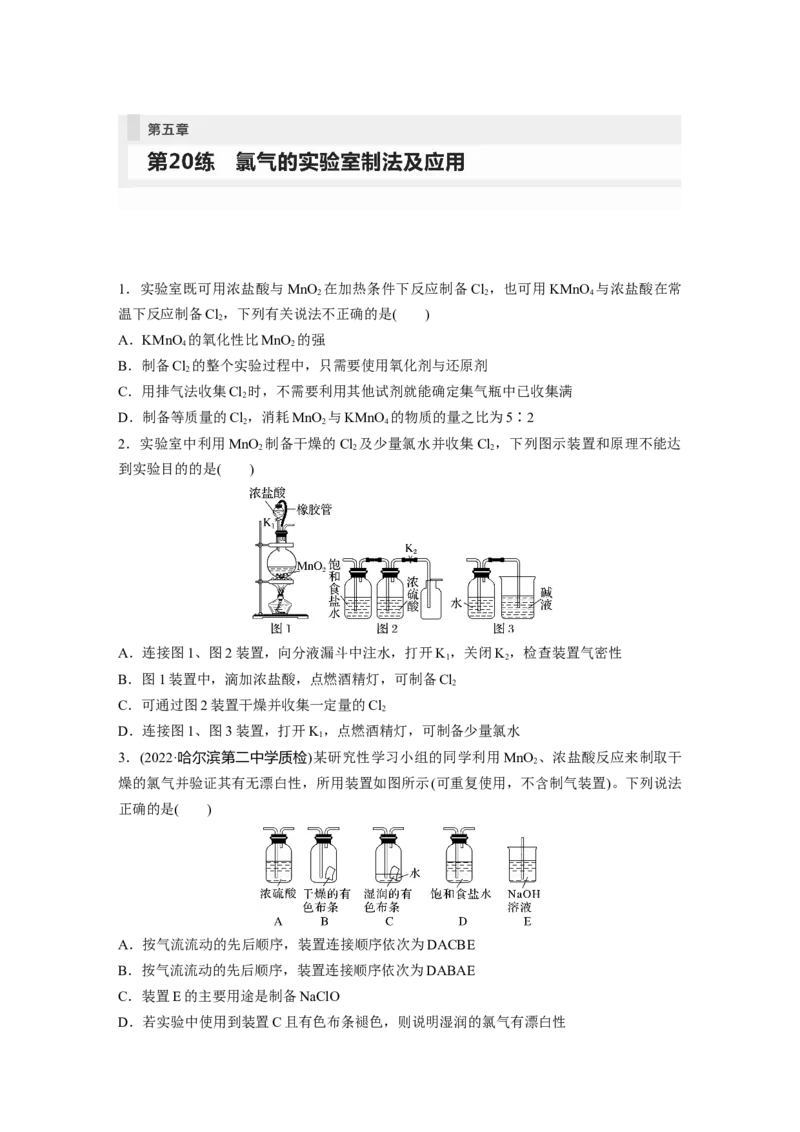
2.实验室中利用MnO 制备干燥的Cl 及少量氯水并收集Cl ,下列图示装置和原理不能达
2 2 2
到实验目的的是( )
A.连接图1、图2装置,向分液漏斗中注水,打开K,关闭K,检查装置气密性
1 2
B.图1装置中,滴加浓盐酸,点燃酒精灯,可制备Cl
2
C.可通过图2装置干燥并收集一定量的Cl
2
D.连接图1、图3装置,打开K,点燃酒精灯,可制备少量氯水
1
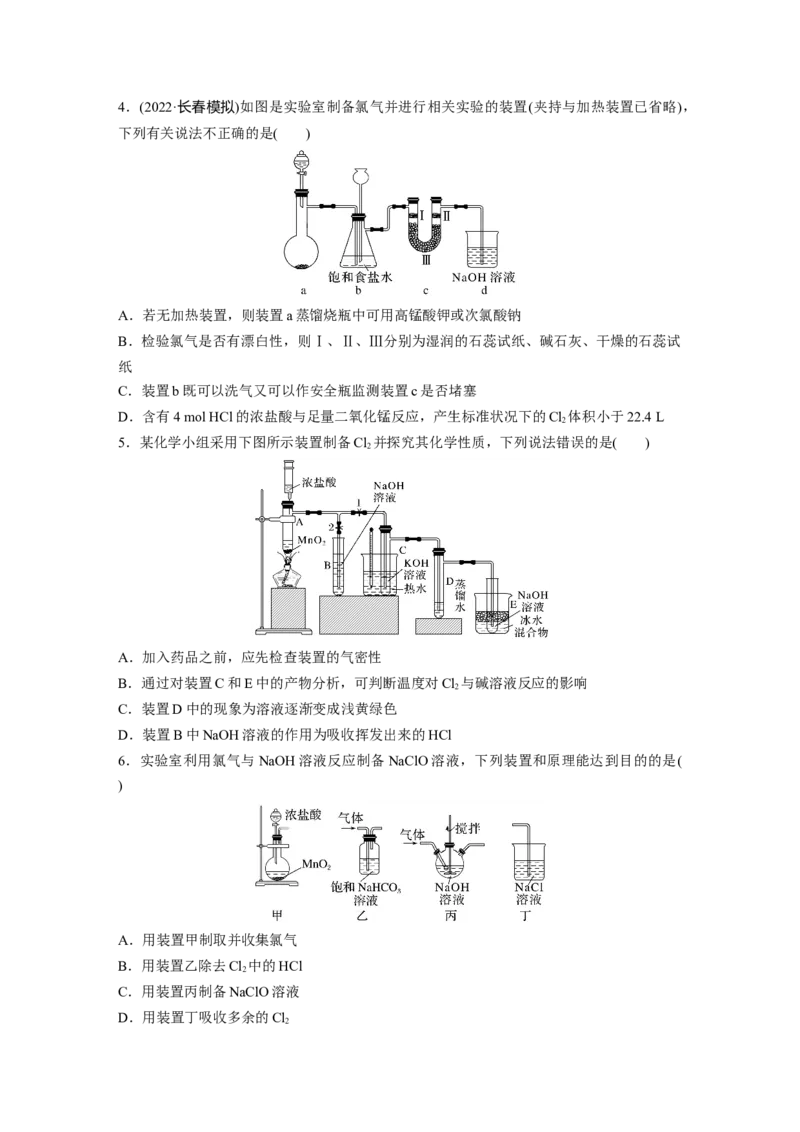
3.(2022·哈尔滨第二中学质检)某研究性学习小组的同学利用MnO 、浓盐酸反应来制取干
2
燥的氯气并验证其有无漂白性,所用装置如图所示(可重复使用,不含制气装置)。下列说法
正确的是( )
A.按气流流动的先后顺序,装置连接顺序依次为DACBE
B.按气流流动的先后顺序,装置连接顺序依次为DABAE
C.装置E的主要用途是制备NaClO
D.若实验中使用到装置C且有色布条褪色,则说明湿润的氯气有漂白性4.(2022·长春模拟)如图是实验室制备氯气并进行相关实验的装置(夹持与加热装置已省略),
下列有关说法不正确的是( )
A.若无加热装置,则装置a蒸馏烧瓶中可用高锰酸钾或次氯酸钠
B.检验氯气是否有漂白性,则Ⅰ、Ⅱ、Ⅲ分别为湿润的石蕊试纸、碱石灰、干燥的石蕊试
纸
C.装置b既可以洗气又可以作安全瓶监测装置c是否堵塞
D.含有4 mol HCl的浓盐酸与足量二氧化锰反应,产生标准状况下的Cl 体积小于22.4 L
2
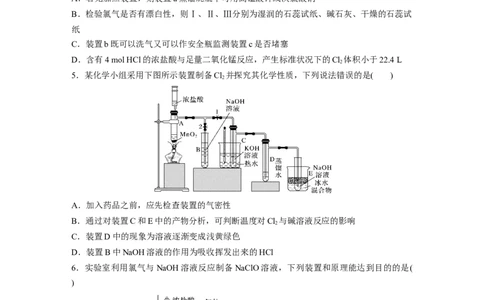
5.某化学小组采用下图所示装置制备Cl 并探究其化学性质,下列说法错误的是( )
2
A.加入药品之前,应先检查装置的气密性
B.通过对装置C和E中的产物分析,可判断温度对Cl 与碱溶液反应的影响
2
C.装置D中的现象为溶液逐渐变成浅黄绿色
D.装置B中NaOH溶液的作用为吸收挥发出来的HCl
6.实验室利用氯气与NaOH溶液反应制备NaClO溶液,下列装置和原理能达到目的的是(
)
A.用装置甲制取并收集氯气
B.用装置乙除去Cl 中的HCl
2
C.用装置丙制备NaClO溶液
D.用装置丁吸收多余的Cl
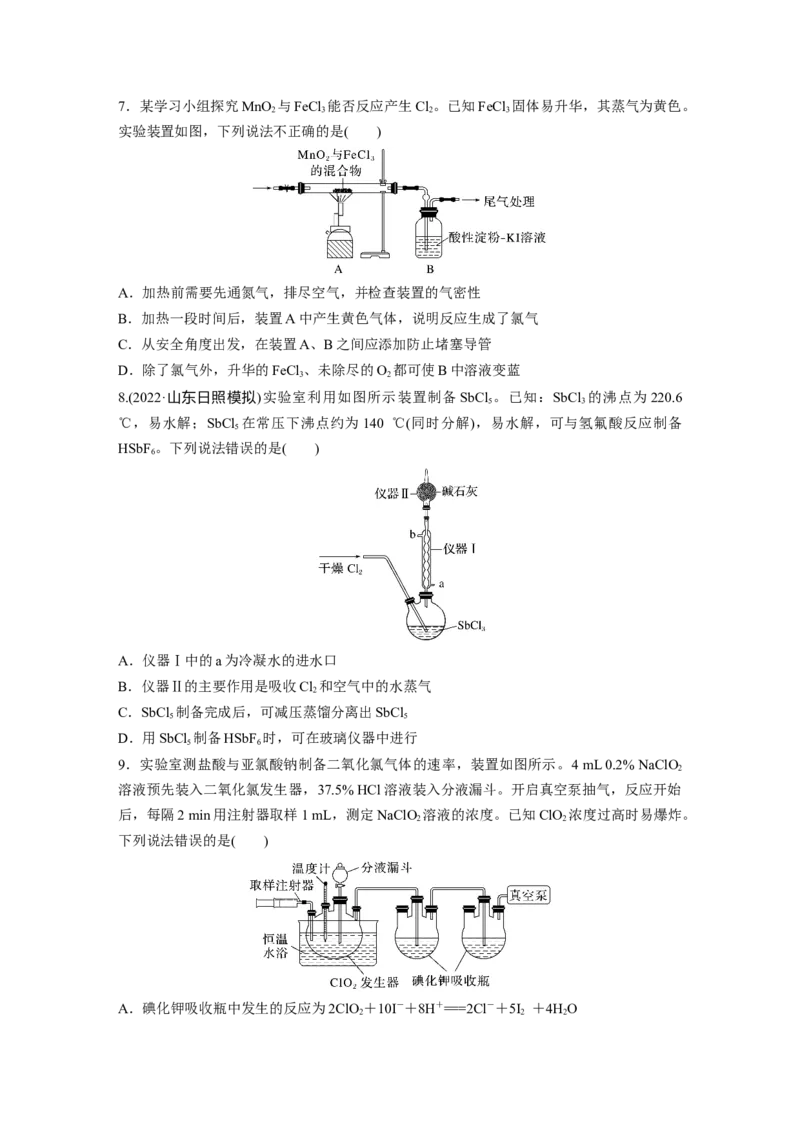
27.某学习小组探究MnO 与FeCl 能否反应产生Cl 。已知FeCl 固体易升华,其蒸气为黄色。
2 3 2 3
实验装置如图,下列说法不正确的是( )
A.加热前需要先通氮气,排尽空气,并检查装置的气密性
B.加热一段时间后,装置A中产生黄色气体,说明反应生成了氯气
C.从安全角度出发,在装置A、B之间应添加防止堵塞导管
D.除了氯气外,升华的FeCl 、未除尽的O 都可使B中溶液变蓝
3 2
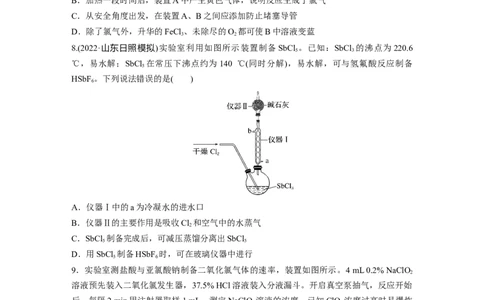
8.(2022·山东日照模拟)实验室利用如图所示装置制备SbCl 。已知:SbCl 的沸点为220.6
5 3
℃,易水解;SbCl 在常压下沸点约为140 ℃(同时分解),易水解,可与氢氟酸反应制备
5
HSbF 。下列说法错误的是( )
6
A.仪器Ⅰ中的a为冷凝水的进水口
B.仪器Ⅱ的主要作用是吸收Cl 和空气中的水蒸气
2
C.SbCl 制备完成后,可减压蒸馏分离出SbCl
5 5
D.用SbCl 制备HSbF 时,可在玻璃仪器中进行
5 6
9.实验室测盐酸与亚氯酸钠制备二氧化氯气体的速率,装置如图所示。4 mL 0.2% NaClO
2
溶液预先装入二氧化氯发生器,37.5% HCl溶液装入分液漏斗。开启真空泵抽气,反应开始
后,每隔2 min用注射器取样1 mL,测定NaClO 溶液的浓度。已知ClO 浓度过高时易爆炸。
2 2
下列说法错误的是( )
A.碘化钾吸收瓶中发生的反应为2ClO +10I-+8H+===2Cl-+5I +4HO
2 2 2B.做实验时整套装置要先抽真空,再加入37.5%HCl溶液,防止ClO 聚集
2
C.分液漏斗作为空气入口,起到搅拌作用
D.实验过程中分液漏斗活塞保持关闭,防止ClO 逸出
2
10.NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,下列说法错误的是( )
2
A.NaClO 的名称是亚氯酸钠
2
B.“尾气吸收”是吸收“电解”过程排出的少量ClO ,此反应的离子方程式为2OH-+
2
HO+2ClO ===2ClO+O↑+2HO
2 2 2 2 2
C.“电解”中阴极反应的主要产物是Cl
2
D.“一系列操作”为蒸发浓缩、趁热过滤、洗涤、干燥
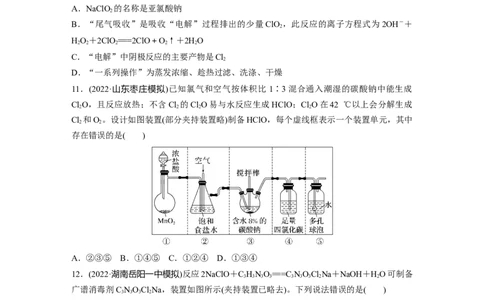
11.(2022·山东枣庄模拟)已知氯气和空气按体积比 1∶3混合通入潮湿的碳酸钠中能生成
ClO,且反应放热;不含Cl 的ClO易与水反应生成HClO;ClO在42 ℃以上会分解生成
2 2 2 2
Cl 和O 。设计如图装置(部分夹持装置略)制备HClO,每个虚线框表示一个装置单元,其中
2 2
存在错误的是( )
A.②③⑤ B.①④⑤ C.①②④ D.①③④
12.(2022·湖南岳阳一中模拟)反应2NaClO+C HNO===C NOClNa+NaOH+HO可制备
3 3 3 3 3 3 3 2 2
广谱消毒剂C NOClNa,装置如图所示(夹持装置已略去)。下列说法错误的是( )
3 3 3 2
A.按气流从左至右,装置中导管连接顺序为f→c→d→a→b→e
B.升高温度有利于装置A中产品的生成
C.当加入4 mol NaOH时,消耗氰尿酸(C HNO)的量大于1 mol
3 3 3 3
D.装置D中橡胶管可平衡气压,便于浓盐酸顺利流下13.(2022·山西临汾模拟)亚硝酰氯(NOCl)是重要的有机合成试剂,可由NO与Cl 在常温下
2
合成。某学习小组在实验室利用如图装置制备亚硝酰氯。
已知:①亚硝酰氯易水解,能与O 反应;
2
②沸点:NOCl为-5.5 ℃,Cl 为-34 ℃,NO为-152 ℃;
2
③常温下,2NO + Cl===2NOCl、2NO +Cl===2NO Cl。
2 2 2 2
请回答下列问题:
(1)NOCl中N元素的化合价为________;NOCl水解生成两种酸,其化学方程式为
________________________________________________________________________
________________________________________________________________________。
(2)实验所需的NO在A装置中制得,反应的离子方程式为_____________________。
(3)装置B中所盛试剂为________,其作用是_________________________________
________________________________________________________________________。
(4)实验开始时,先关闭 K ,打开 K 、K ,从 a 处通一段时间氩气,其目的是
3 2 4
________________________________________________________________________
________________________________________________________________________。
然后在a处接废气处理装置,关闭K 、K ,打开K ,再打开分液漏斗的活塞,滴加酸性
1 4 3
FeSO 溶 液 , 当 观 察 到 D 中
4
____________________________________________________________时,
关闭K,打开K、K ,通干燥纯净的Cl。
2 1 4 2
(5)为收集产物和分离未反应的两种原料, E、F装置采用不同温度的低温浴槽,其中装置E
的温度(T)区间应控制在_______________________________________________________,
装置F 的U形管中收集到的是________。
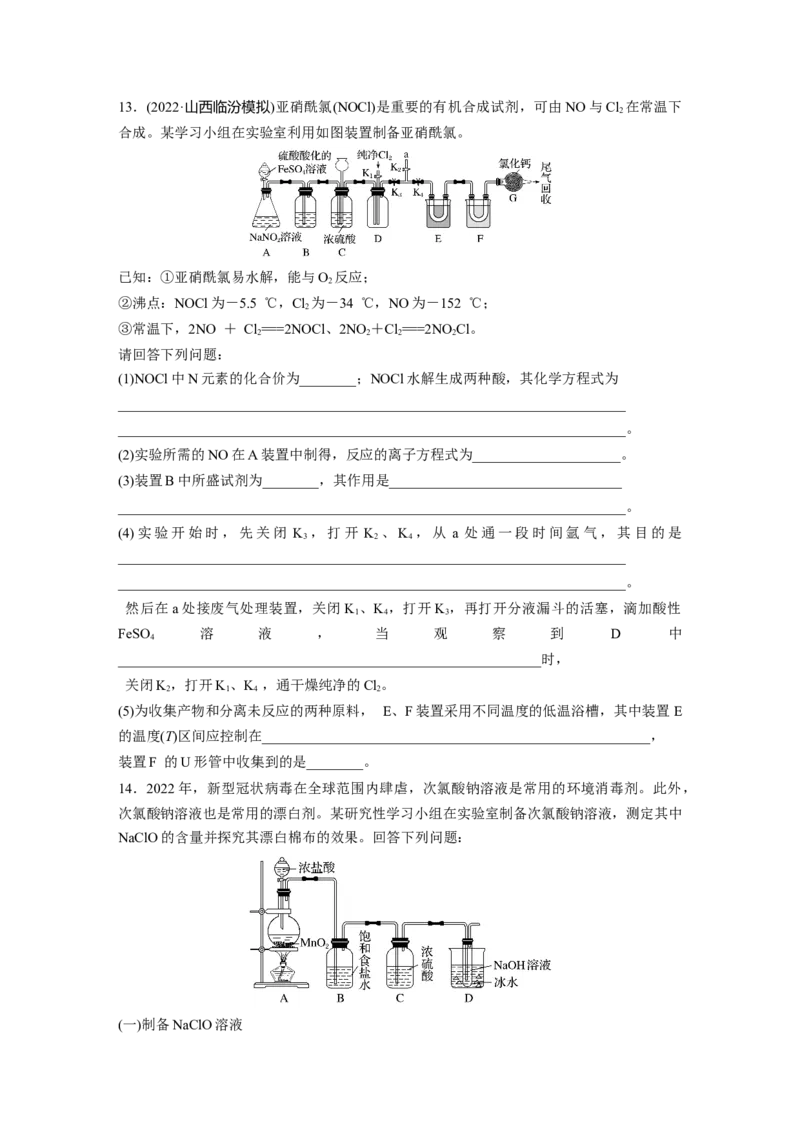
14.2022年,新型冠状病毒在全球范围内肆虐,次氯酸钠溶液是常用的环境消毒剂。此外,
次氯酸钠溶液也是常用的漂白剂。某研究性学习小组在实验室制备次氯酸钠溶液,测定其中
NaClO的含量并探究其漂白棉布的效果。回答下列问题:
(一)制备NaClO溶液(1)装置B的作用是________________;若没有装置B,且D中氢氧化钠不足量,对次氯酸
钠产率的影响是__________(填“增大”“减小”或“无影响”)。
(2)装置D中反应的离子方程式为________________________________________________
________________________________________________________________________。
(3)有同学提出三点意见:①装置A中不需要酒精灯;②装置C没有必要;③在装置D后再
连接一个盛有NaOH溶液的尾气处理装置,以降低氯气逸出污染空气的可能性。合理的是
______(填序号)。
(二)测定消毒液中NaClO的含量
步骤①:取制得的消毒液20 mL于锥形瓶中,加足量盐酸酸化,迅速加入过量 KI溶液,盖
紧瓶塞并在暗处充分反应。
步骤②:加入淀粉做指示剂,用NaSO 标准溶液滴定至终点,重复滴定操作3次。
2 2 3
(4)步骤①中在暗处反应的原因是___________________________________________。
(5)步骤②中判断滴定终点的现象是________________________________________
________________________________________________________________________,
已知I +2SO===2I-+SO。平均用去25.00 mL 0.100 0 mol·L-1 Na SO 标准溶液,测得
2 2 4 2 2 3
NaClO的含量为________ g·L-1(结果保留2位小数)。
(三)探究次氯酸钠漂白棉布的效果
已知:棉布用次氯酸钠漂白液漂白会受到一定损伤。织物断裂强度是指织物在被拉断时,所
能承受的最大荷重,单位为kg。
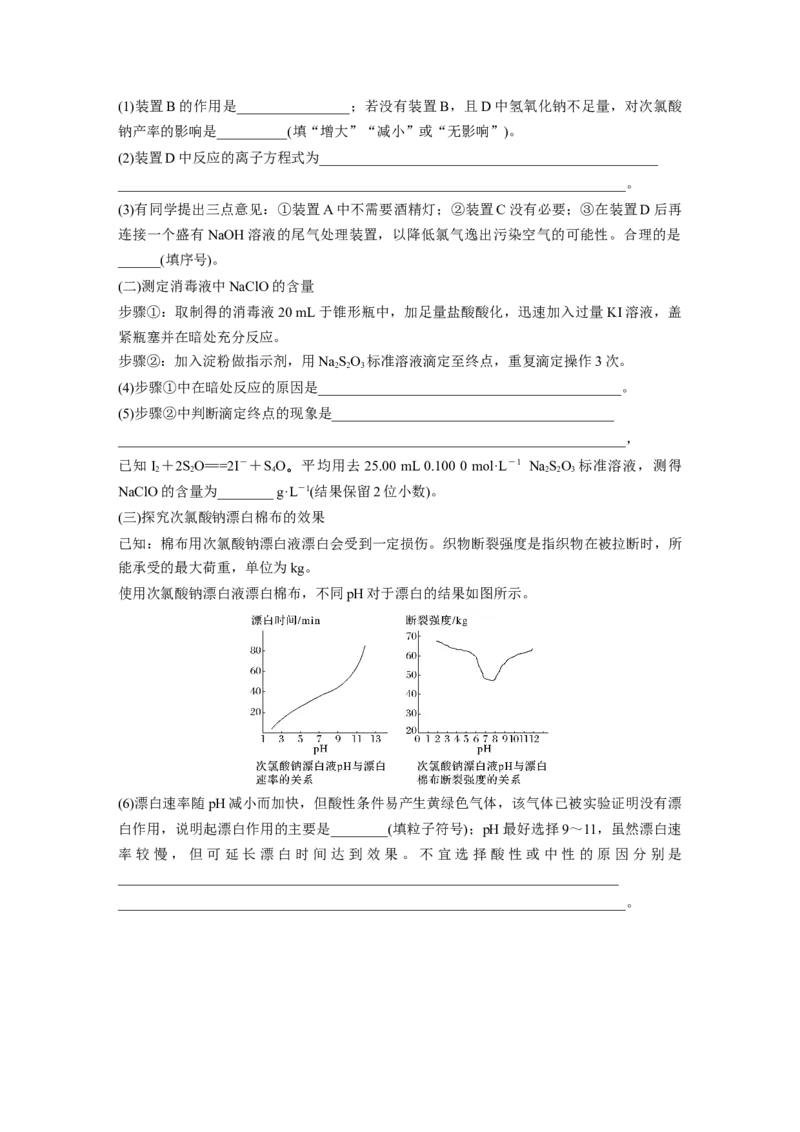
使用次氯酸钠漂白液漂白棉布,不同pH对于漂白的结果如图所示。
(6)漂白速率随pH减小而加快,但酸性条件易产生黄绿色气体,该气体已被实验证明没有漂
白作用,说明起漂白作用的主要是________(填粒子符号);pH最好选择9~11,虽然漂白速
率较慢,但可延长漂白时间达到效果。不宜选择酸性或中性的原因分别是
_______________________________________________________________________
________________________________________________________________________。