文档内容
第 22 讲 硫及其氧化物
[复习目标] 1.了解硫的存在及其单质的性质和用途。2.掌握硫的氧化物的主要性质及应用。
考点一 硫单质的性质
1.硫元素的存在形态
2.硫单质的物理性质
溶解性
俗称 颜色状态
水 酒精 CS
2
硫黄 ______晶体 微溶
思考 (1)硫有S 、S 、S 、S 等多种单质,它们的关系是什么?加热时,S 转化为S 、S 、
2 4 6 8 8 6 4
S 属于什么变化?
2
________________________________________________________________________
________________________________________________________________________
(2)硫单质难溶于水,易溶于CS,其原因是什么?
2
________________________________________________________________________
________________________________________________________________________
3.从化合价的角度认识硫单质的化学性质
S ←―― ――→S
1.硫在空气中燃烧的产物是SO ,在纯氧中燃烧的产物是SO ( )
2 32.硫与铁粉和铜粉分别反应,都可生成二价金属硫化物( )
3.等质量的S 和S 分子分别与足量的KOH反应,消耗KOH的物质的量相同( )
6 8
1.在下列反应中硫元素只表现氧化性的是( )
A.2Al+3S=====Al S
2 3
B.S+2HSO (浓)=====2HO+3SO ↑
2 4 2 2
C.HS=====H+S
2 2
D.3S+6NaOH=====2NaS+NaSO +3HO
2 2 3 2
2.加热装有硫粉的试管,硫粉很快熔化为液体,继而有淡黄色气体产生。将光亮细铜丝伸
入气体中,铜丝发光发热且有黑色物质生成。由上述现象不能得出的结论是( )
A.硫的熔、沸点较低
B.硫晶体属于分子晶体
C.铜丝能在硫蒸气中燃烧
D.黑色固体是Cu S
2
考点二 二氧化硫和三氧化硫
1.二氧化硫
(1)物理性质
色、味、态 密度 溶解性
____溶于水,通常状况下,1
____色、____________气味
比空气的____ 体积的水溶解约____体积的
的____________
SO
2
(2)化学性质
按要求完成下列化学方程式:SO
2
(3)实验室制法
①固体NaSO 与较浓HSO 反应,化学方程式为____________________________。
2 3 2 4
②铜与浓HSO 混合加热,化学方程式为___________________________________
2 4
________________________________________________________________________。
三类漂白剂的区别
类型 原理 举例 特点 备注
HClO、NaClO、
将有机色质内部
氧化型 Ca(ClO) 、NaO、 不可逆、持久 无选择性
2 2 2
“生色团”破坏掉
HO、O 等
2 2 3
与有机色质内部
加合型 “生色团”“化 SO 可逆、不持久 有选择性
2
合”成无色物质
将有色物质吸附而
吸附型 活性炭 物理变化 吸附色素
褪色
2.三氧化硫
(1)物理性质
熔点:16.8 ℃,沸点:44.8 ℃,常温下为____态,标准状况下为____态。
(2)化学性质
三氧化硫具有酸性氧化物的通性,主要反应如下:
1.标准状况下,2.24 L SO 中含有硫原子数为N ( )
3 A
2.将SO 通入紫色石蕊溶液中,紫色石蕊溶液先变红后褪色( )
2
3.SO 使滴有酚酞的NaOH溶液褪色,体现了SO 的漂白性( )
2 2
4.SO 和Cl 等物质的量混合后通入装有湿润的有色布条的集气瓶中,漂白效果更好( )
2 2
5.SO 、漂白粉、活性炭、NaO 都能使红墨水褪色,其原理相同( )
2 2 2
一、SO 化学性质的多重性
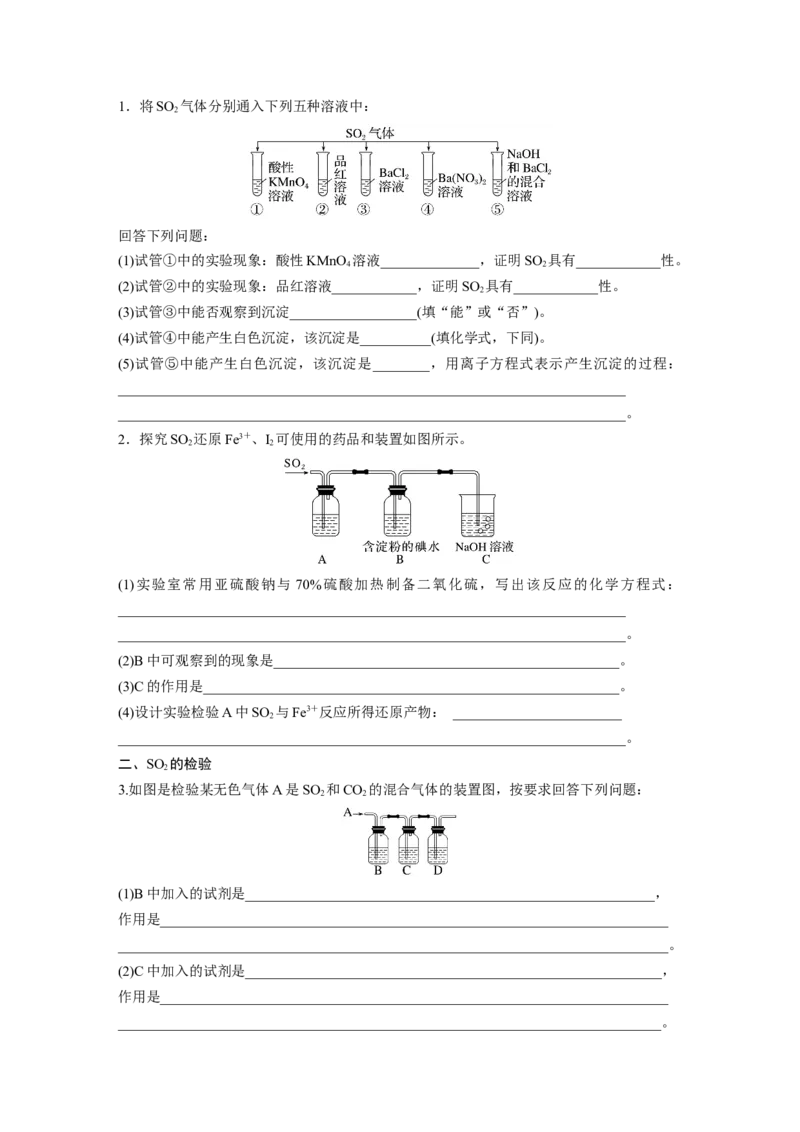
21.将SO 气体分别通入下列五种溶液中:
2
回答下列问题:
(1)试管①中的实验现象:酸性KMnO 溶液______________,证明SO 具有____________性。
4 2
(2)试管②中的实验现象:品红溶液____________,证明SO 具有____________性。
2
(3)试管③中能否观察到沉淀__________________(填“能”或“否”)。
(4)试管④中能产生白色沉淀,该沉淀是__________(填化学式,下同)。
(5)试管⑤中能产生白色沉淀,该沉淀是________,用离子方程式表示产生沉淀的过程:
________________________________________________________________________
________________________________________________________________________。
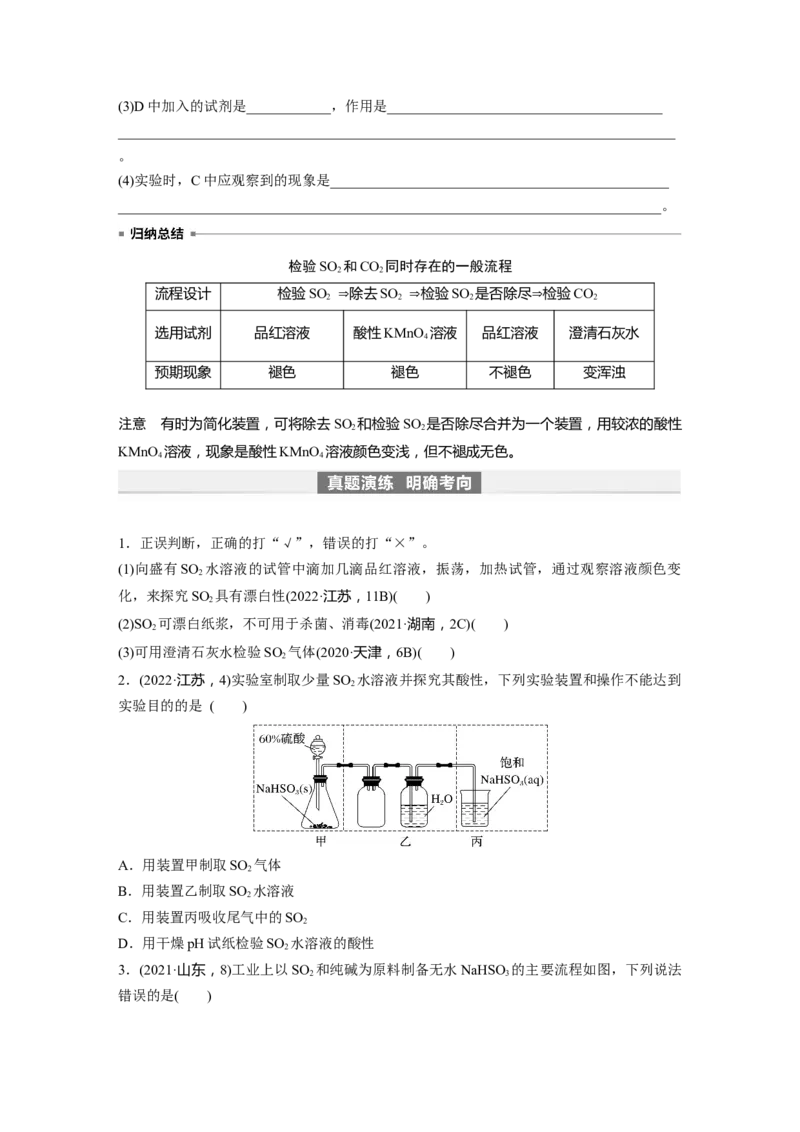
2.探究SO 还原Fe3+、I 可使用的药品和装置如图所示。
2 2
(1)实验室常用亚硫酸钠与 70%硫酸加热制备二氧化硫,写出该反应的化学方程式:
________________________________________________________________________
________________________________________________________________________。
(2)B中可观察到的现象是_________________________________________________。
(3)C的作用是___________________________________________________________。
(4)设计实验检验A中SO 与Fe3+反应所得还原产物: ________________________
2
________________________________________________________________________。
二、SO 的检验
2
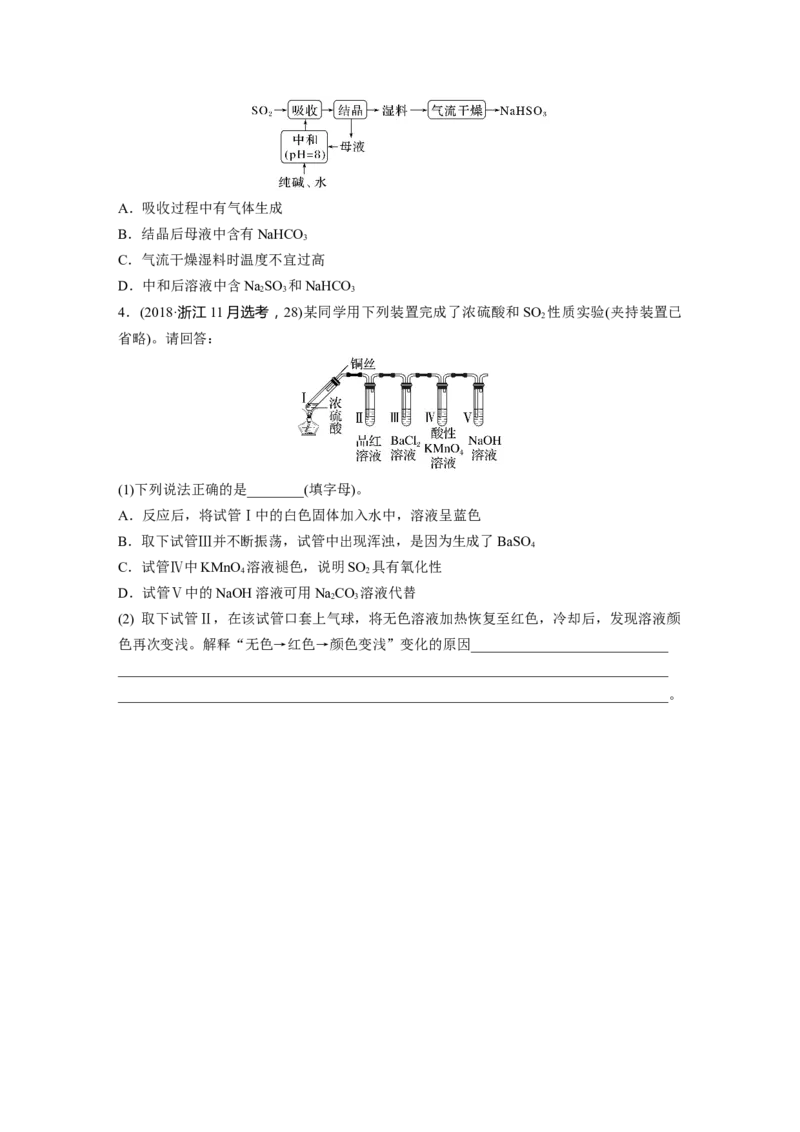
3.如图是检验某无色气体A是SO 和CO 的混合气体的装置图,按要求回答下列问题:
2 2
(1)B中加入的试剂是__________________________________________________________,
作用是________________________________________________________________________
______________________________________________________________________________。
(2)C中加入的试剂是___________________________________________________________,
作用是________________________________________________________________________
_____________________________________________________________________________。(3)D中加入的试剂是____________,作用是_______________________________________
_______________________________________________________________________________
。
(4)实验时,C中应观察到的现象是________________________________________________
_____________________________________________________________________________。
检验SO 和CO 同时存在的一般流程
2 2
流程设计 检验SO ⇒除去SO ⇒检验SO 是否除尽⇒检验CO
2 2 2 2
选用试剂 品红溶液 酸性KMnO 溶液 品红溶液 澄清石灰水
4
预期现象 褪色 褪色 不褪色 变浑浊
注意 有时为简化装置,可将除去SO 和检验SO 是否除尽合并为一个装置,用较浓的酸性
2 2
KMnO 溶液,现象是酸性KMnO 溶液颜色变浅,但不褪成无色。
4 4
1.正误判断,正确的打“√”,错误的打“×”。
(1)向盛有SO 水溶液的试管中滴加几滴品红溶液,振荡,加热试管,通过观察溶液颜色变
2
化,来探究SO 具有漂白性(2022·江苏,11B)( )
2
(2)SO 可漂白纸浆,不可用于杀菌、消毒(2021·湖南,2C)( )
2
(3)可用澄清石灰水检验SO 气体(2020·天津,6B)( )
2
2.(2022·江苏,4)实验室制取少量SO 水溶液并探究其酸性,下列实验装置和操作不能达到
2
实验目的的是 ( )
A.用装置甲制取SO 气体
2
B.用装置乙制取SO 水溶液
2
C.用装置丙吸收尾气中的SO
2
D.用干燥pH试纸检验SO 水溶液的酸性
2
3.(2021·山东,8)工业上以SO 和纯碱为原料制备无水NaHSO 的主要流程如图,下列说法
2 3
错误的是( )A.吸收过程中有气体生成
B.结晶后母液中含有NaHCO
3
C.气流干燥湿料时温度不宜过高
D.中和后溶液中含NaSO 和NaHCO
2 3 3
4.(2018·浙江11月选考,28)某同学用下列装置完成了浓硫酸和SO 性质实验(夹持装置已
2
省略)。请回答:
(1)下列说法正确的是________(填字母)。
A.反应后,将试管Ⅰ中的白色固体加入水中,溶液呈蓝色
B.取下试管Ⅲ并不断振荡,试管中出现浑浊,是因为生成了BaSO
4
C.试管Ⅳ中KMnO 溶液褪色,说明SO 具有氧化性
4 2
D.试管Ⅴ中的NaOH溶液可用NaCO 溶液代替
2 3
(2) 取下试管Ⅱ,在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜
色再次变浅。解释“无色→红色→颜色变浅”变化的原因____________________________
______________________________________________________________________________
______________________________________________________________________________。